INHIBIDORES MIF.
Un derivado 3-sustituido de un 3,4-dihidro-benzo[e][1,3]oxazin-2-ona,
siendo dicho derivado seleccionado del grupo que consiste de
i) 3-((fenil sustituido)-3,4-dihidro-benzo[e][1,3]oxazin-2-onas, 3-((naftil)-3,4-dihidro-benzo[e][1,3]oxazin-2-onas,
ii) 3-(cicloalquil(C3-8))-3,4-dihidro-benzo[e][1,3]oxazin-2-onas,
iii) 3-(aril(C6-12)alquil(C1-4))-3,4-dihidro-benzo[e][1,3]oxazin-2-onas, y
iv) 3-(cicloalquil(C3-8)alquil(C1-4))-3,4-dihidro-benzo[e][1,3]oxazin-2-onas
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/EP2005/011233.
Solicitante: NOVARTIS AG
NOVARTIS PHARMA GMBH.
Nacionalidad solicitante: Suiza.
Dirección: LICHTSTRASSE 35,4056 BASEL.
Inventor/es: BILLICH, ANDREAS, LEHR,PHILIPP, GSTACH,HUBERT.
Fecha de Publicación: .
Fecha Concesión Europea: 14 de Abril de 2010.
Clasificación Internacional de Patentes:
- C07D265/18 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07D COMPUESTOS HETEROCICLICOS (Compuestos macromoleculares C08). › C07D 265/00 Compuestos heterocíclicos que contienen ciclos de seis miembros que tienen un átomo de nitrógeno y un átomo de oxígeno como únicos heteroátomos del ciclo. › con heteroátomos unidos directamente en la posición 2.
- C07D413/04 C07D […] › C07D 413/00 Compuestos heterocíclicos que contienen dos o más heterociclos, teniendo al menos un ciclo átomos de nitrógeno y oxígeno como únicos heteroátomos del ciclo. › unidos directamente por un enlace entre dos miembros cíclicos.
Clasificación PCT:
- A61K31/535 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › que tienen ciclos con seis eslabones con al menos un nitrógeno y al menos un oxígeno como heteroátomos de un ciclo, p. ej. 1,2-oxazinas.
- A61P29/00 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › Agentes analgésicos, antipiréticos o antiinflamatorios que no actúan sobre el sistema nervioso central, p. ej. agentes antirreumáticos; Antiinflamatorios no esteroideos (AINEs).
- C07D265/18 C07D 265/00 […] › con heteroátomos unidos directamente en la posición 2.
- C07D413/04 C07D 413/00 […] › unidos directamente por un enlace entre dos miembros cíclicos.
Fragmento de la descripción:
Inhibidores MIF.
La presente invención se relaciona con inhibidores-MIF, tales como compuestos que son farmacéuticamente activos, por ejemplo inhibidores de la actividad tautomerasa del factor inhibidor de migración (MIF) del macrófago humano, tal como 3,4-dihidrobenzo[e][1,3]oxazin-2-onas que son sustituidas en el átomo de nitrógeno por cicloalquil(C3-8), cicloalquil(C3-8)alquil(C1-4), aril(C6-18), o aril(C6-18)alquil(C1-4) no sustituido o sustituido.
MIF es una citoquina con una amplia variedad de actividades celular y biológica (para revisión ver: Calandra et al., Nat. Rev. Immunol.3:791-800. 2003; Orita et al., Curr. Pharm. Design 8:1297-1317, 2002; Nishihira, J Interferon Cytokine Res 20:751-762, 2000; Swope & Lolis, Rev. Physiol. Biochem. Pharmacol. 139:1-32, 1999; Metz & Bucala, Adv. Immunol. 66:197-223, 1997). Se encontró que MIF inhibe la migración aleatoria de macrófagos, y que se asocia con reacciones de hipersensibilidad de tipo retardada (George & Vaughan, Proc. Soc. Exp. Biol. Med. 111:514-521, 1962; Weiser et al., J. Immunol. 126:1958-1962, 1981; Bloom & Bennett, Science, 153:80-82, 1966; David, Proc. Natl. Acad. Sci. USA 56: 72-77, 1966). También se encontró que MIF mejora la adherencia del macrófago, actividad de fagocitosis y tumoricidad (Nathan et al., J. Exp. Med. 137:275-288, 1973; Nathan et al., J. Exp. Med. 133:1356-1376, 1971; Churchill, et al., J. Immunol. 115:781-785, 1975).
MIF humano recombinante se clonó originalmente a partir de una biblioteca de célula T humana (Weiser et al., Proc. Natl. Acad. Sci. USA 86: 7522-7526, 1989), y se demostró que activan los macrófagos derivados de la sangre para matar parásitos intracelulares y células tumorales in vitro, para estimular la expresión de IL-1ß y TNFa, y para inducir la síntesis de óxido nítrico (Weiser et al., J. Immunol. 147:2006-2011, 1991; Pozzi et al., Cellular Immunol. 145:372-379, 1992; Weiser et al., Proc. Natl. Acad. Sci. USA 89: 8049-8052, 1992; Cunha et al., J. Immunol. 150:1908-1912, 1993). Más recientemente se ha encontrado que MIF no es solo un producto de citoquina del sistema inmune, pero también es un producto similar a una hormona del sistema endocrino, particularmente la glándula pituitaria. Este trabajo ha subrayado la potente actividad de MIF como un regulador de recuento de los efectos anti-inflamatorios de los glucocorticoides (tanto aquellos de liberación endógena como aquellos administrados terapéuticamente), con el efecto que las actividades normales de glucocorticoides para limitar y suprimir la severidad de respuestas inflamatorias se inhiben por MIF y por lo tanto se puede considerar la respuesta de MIF endógena como una causa o un factor exacerbante en una variedad de enfermedades y condiciones inflamatorias (revisado en Donnelly and Bucala, Molecular Medicine Today 3:502-507, 1997).
Las actividades biológicas adicionales incluyen la regulación de células T estimuladas (Bacher et al., Proc. Natl. Acad. Sci. USA 93:7849-7854, 1996), el control de la síntesis de IgE (Mikayama et al., Proc. Natl. Acad. Sci. USA 90:10056-60, 1993), la inactivación funcional de la proteína supresora del tumor p53 (Hudson et al., J. Exp. Med. 190:1375-1382, 1999), la regulación de glucosa y metabolismo de carbohidratos (Sakaue et al., Mol. Med. 5:361-371, 1999), y la regulación de crecimiento de tumor celular y de angiogenesis (Chesney et al., Mol Med. 5:181-191, 1999; Shimizu et al., Biochem. Biophys. Res. Commun. 264:751-758, 1999; Mitchell & Bucala, Cancer Biol. 10:359-366, 2000). Un papel de MIF en aterogenesis (Lin et al., Circulation Res. 8:1202-1208, 2000), en asma (Yamaguchi et al., Clin. Exp. Allergy 30:1244-1249, 2000), y en malaria (Martiney et al., Infection Immunity 68:2259-2267, 2000) también ha sido implicado.
Se ha demostrado que los anticuerpos anti-MF son activos en una variedad de modelos: choque tóxico inducido por la endotoxina- y exotoxina (Bemhagen et al., Nature, 365:756-759, 1993; Kobayashi et al., Hepatology, 29:1752-1759, 1999; Calandra et al., Proc. Natl. Acad. Sci. USA., 95:11383-11388, 1998; Makita et al., Am. J. Respir. Crit. Care Med. 158:573-579, 1998, Calandra et al., Nat. Med. 6:164-170, 2000), Activación de la célula T (Bacher et al., Proc. Natl. Acad. Sci. USA. 93:7849-7854, 1996), enfermedades autoinmunes, incluyendo artritis reumatoide (Leech et al., Arthritis Rheum., 42:1601-1608, 1999), uveoretinitis (Kitaichi et al., Curr. Eye Res., 20:109-114, 2000), glomerulonefritis (Yang et al., Mol. Med. 4: 413-424, 1998), encefalomielitis aguda experimental (Denkinger et al., J. Immunol. 170: 1274-1282, 2003) colitis (de Jong et al., Nat. Immunol. 2:1061-1066, 2001; Ohkawara et al., Gastroenterol. 123: 256-270, 2002), y destrucción de injerto de piel (Hou et al., Transplantation 72: 1890-1897, 2001), y aterosclerosis (Chen et al. Arterioscler. Thromb. Vasc. Biol. 24:709-714, 2004; Schober et al., Circulation 109:380-385, 2004). Adicionalmente, se ha demostrado que los anticuerpos anti-MIF inhiben el crecimiento del tumor y la angiogenesis (Chesney et al., Mol. Med. 5:181-191, 1999; Ogawa et al., Cytokine 12:309-314, 2000; Mitchell & Bucala, Cancer Biol. 10:359-366, 2000). Basándose en la actividad de los anticuerpos anti-MIF, el potencial terapéutico de inhibidores-MIF de bajo peso molecular es alto.
MIF comparte homología significante de secuencia (36% de identidad) con D-dopacromo tautomerasa, y tiene actividad enzimática para catalizar la tautomerización de los sustratos no-fisiológicos D-dopacromo (Rosengren et al., Mol. Med. 2: 143-149, 1996) y L-dopacromo metil éster (Bendrat et al., Biochemistry, 36:15356-15362, 1997) (Fig: 1A). Adicionalmente, el ácido fenilpirúvico y el ácido p-hidroxifenilpirúvico (Rosengren et al., FEBS Letter, 417:85-88, 1997), y 3,4-dihidroxifenilaminacromo y norepinefrinacromo (Matsunaga et al., J. Biol. Chem., 274:3268-3271, 1999) son sustratos MIF. La estructura de cristal tri-dimensional de MIF humano revela que la proteína existe como un homotrimero (Lolis et al., Proc. Ass. Am. Phys. 108:415-419, 1996). Varios inhibidores de la actividad tautomerasa de MIF han sido descritos (por ejemplo, Orita et al. J. Med. Chem. 44:540-547, 2001; Senter et al., Proc. Natl. Acad. Sci (USA) 99:144-149, 2002; Dios et al., J. Med. Chem. 45: 2410-2416, 2002; Lubetsky et al. J. Biol. Chem. 277:24976-24982, 2002). Mindl et al. (Collect. Czech. Chem. Comm, 1262-1267, 2000) revela un proceso para la fabricación de 4H-1,3-Benzoxazin-2(3H)-onas.
Ahora hemos encontrado sorprendentemente una nueva clase de compuestos que actúan como inhibidores de MIF.
En un aspecto la presente invención proporciona compuestos seleccionados del grupo que consiste de 3-(aril(C6-12))-3,4-dihidro-benzo[e][1,3]oxazin-2-onas,
por ejemplo 3-(fenil)-3,4-dihidro-benzo[e][1,3]oxazin-2-onas,
3-(naftil)-3,4-dihidro-benzo[e][1,3]oxazin-2-onas,
3-(cicloalquil(C3-8))-3,4-dihidro-benzo[e][1,3]oxazin-2-onas, por ejemplo 3-(ciclohexil)-3,4-dihidro-benzo[e][1,3]oxazin-2-onas,
3-(aril(C6-12)alquil(C1-4))-3,4-dihidro-benzo[e][1,3]oxazin-2-onas, por ejemplo 3-(benzil-3,4-dihidro-benzo[e] [1,3]oxazin-2-onas, y
3-(fenil)-3,4-dihidro-benzo[e][1,3]oxazin-2-onas,
3-(naftil)-3,4-dihidro-benzo[e][1,3]oxazin-2-onas,
3-(ciclohexil)-3,4-dihidro-benzo[e][1,3]oxazin-2-onas, y
3-(benzil)-3,4-dihidro-benzo[e][1,3]oxazin-2-onas,
3-(fenil)-7-hidroxi-3,4-dihidro-benzo[e][1,3]oxazin-2-onas,
3-(naftil)-7-hidroxi-3,4-dihidro-benzo[e][1,3]oxazin-2-onas,
3-(ciclohexil)-7-hidroxi-3,4-dihidro-benzo[e][1,3]oxazin-2-onas, y
3-(benzil)-7-hidroxi-3,4-dihidro-benzo[e][1,3]oxazin-2-onas,
3-(fenil)-7-aminosulfoniloxi-3,4-dihidro-benzo[e][1,3]oxazin-2-onas,
3-(naftil)-7-aminosulfoniloxi-3,4-dihidro-benzo[e][1,3]oxazin-2-onas,
3-(ciclohexil)-7-aminosulfoniloxi-3,4-dihidro-benzo[e][1,3]oxazin-2-onas, y
3-(benzil)-7-aminosulfoniloxi-3,4-dihidro-benzo[e][1,3]oxazin-2-onas.
En otro aspecto la presente...
Reivindicaciones:
1. Un derivado 3-sustituido de un 3,4-dihidro-benzo[e][1,3]oxazin-2-ona, siendo dicho derivado seleccionado del grupo que consiste de
i) 3-((fenil sustituido)-3,4-dihidro-benzo[e][1,3]oxazin-2-onas, 3-((naftil)-3,4-dihidro-benzo[e][1,3]oxazin-2-onas,
ii) 3-(cicloalquil(C3-8))-3,4-dihidro-benzo[e][1,3]oxazin-2-onas,
iii) 3-(aril(C6-12)alquil(C1-4))-3,4-dihidro-benzo[e][1,3]oxazin-2-onas, y
iv) 3-(cicloalquil(C3-8)alquil(C1-4))-3,4-dihidro-benzo[e][1,3]oxazin-2-onas.
2. Un compuesto de acuerdo con la reivindicación 1 de fórmula
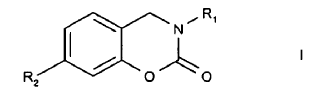
en donde
R1 es un fenil sustituido, o
R1 es no sustituido o sustituido
- cicloalquil(C3-8)alquil(C1-4),
- aril(C6-18)alquil(C1-4),
- cicloalquil(C3-8),
- naftil,
- fenil anillado con otro sistema de anillo
en donde los sustituyentes incluyen un aril(C6-18), halógeno, hidroxi, aminosulfoniloxi, alcoxi(C1-4), trialquil(C1-6)sililoxi, haloalquil(C1-4) o haloalcoxi(C1-4);
R2 es un hidrógeno, hidroxi, aminosulfoniloxi, alcoxi(C1-4), trialquil(C1-6)sililoxi o haloalcoxi (C1-4).
3. Un compuesto de acuerdo con la reivindicación 2, en donde
R1 es
- ciclohexil,
- hidroxiciclohexil,
- bifenilil,
- naftil,
- hidroxifenil,
- metoxifenil,
- triflorometoxifenil,
- bromofenil,
- aminosulfoniloxifenil,
- (ter-butil)(dimetil)sililoxifenil, o
- fenil anillado con una 18-corona-6, y
R2 es como se define en la reivindicación 2.
4. Un compuesto de acuerdo con cualquiera de las reivindicaciones 2 o 3, en donde
R1 es como se define en cualquiera de las reivindicaciones 2 o 3, y
R2 es un hidrógeno, hidroxi o aminosulfoniloxi.
5. Un compuesto de fórmula

en donde
R1 es no sustituido o sustituido
- cicloalquil(C3-8)alquil(C1-4),
- aril(C6-18)alquil(C1-4),
- cicloalquil(C3-8),
- aril(C6-18) opcionalmente anillado con otro anillo (sistema),
en donde los sustituyentes incluyen aril(C6-18), halógeno, hidroxi, aminosulfoniloxi, alcoxi(C1-4), trialquil(C1-6)sililoxi, haloalquil(C1-4) o halo alcoxi (C1-4); R2 es hidroxi, aminosulfoniloxi, alcoxi(C1-4), trialquil(C1-6)sililoxi o halo alcoxi(C1-4).
6. Un compuesto de acuerdo con la reivindicación 5
en donde
R1 es
- ciclohexil,
- hidroxiciclohexil,
- fenil,
- bifenilil,
- naftil,
- hidroxifenil,
- metoxifenil,
- triflorometoxifenil,
- bromofenil,
- aminosulfoniloxifenil,
- (ter-butil)(dimetil)sililoxifenil,
- fenilmetil, o
- fenil anillado con una 18-corona-6, y
R2 es como se define en la reivindicación 5.
7. Un compuesto de acuerdo con la reivindicación 5 en donde, R2 es hidroxi o aminosulfoniloxi.
8. Un compuesto de acuerdo con la reivindicación 1 de fórmula

9. Un compuesto de cualquiera de las reivindicaciones 1 o 8 en la forma de una sal.
10. Un compuesto de cualquiera de las reivindicaciones 1 a 9 para utilizar como un producto farmacéutico.
11. El uso de un compuesto de cualquiera de las reivindicaciones 1 a 9 para la fabricación de un medicamento para el tratamiento o prevención de enfermedades mediadas por MIF.
12. Una composición farmacéutica que comprende un compuesto de cualquiera de las reivindicaciones 1 a 9 en asociación con al menos un excipiente farmacéutico.
13. Una composición farmacéutica de acuerdo con la reivindicación 12, que además comprende uno o más agentes farmacéuticamente activos.
Patentes similares o relacionadas:
Derivados de bencimidazol como inhibidores Nav 1.7 (subunidad alfa del canal de sodio, dependiente del voltaje, tipo IX (SCN9A)) para tratar el dolor, la disuria y la esclerosis múltiple, del 22 de Julio de 2020, de Sumitomo Dainippon Pharma Co., Ltd: Un compuesto de fórmula (I): **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, donde R1a, R1b, R1c, y R1d son independientemente hidrógeno, […]
Composiciones y métodos anti-HCMV, del 22 de Julio de 2020, de Evrys Bio, LLC: Una composición que comprende un compuesto de la Fórmula I: **(Ver fórmula)** en donde: Ar es **(Ver fórmula)** en donde cada anillo cíclico de 5 o 6 miembros […]
Proceso para la producción a gran escala de oxalato de 1isopropil3{5[1(3metoxipropil) piperidin4il] [1,3,4]oxadiazol2il}1Hindazol, del 8 de Julio de 2020, de SUVEN LIFE SCIENCES LIMITED: Un proceso para la producción a gran escala del oxalato de 1-isopropil-3-{5-[1-(3-metoxipropil) piperidin- 4-il] -[1,3,4]oxadiazol-2-il}-1H-indazol […]
Derivados de tetrahidroisoquinolina, del 1 de Julio de 2020, de UCB Biopharma SRL: Un compuesto representado por la fórmula (I-A), o una sal farmacéuticamente aceptable de este, **(Ver fórmula)** En donde R1 es hidrógeno, halógeno, ciano o hidroxi; […]
Compuestos de 6-heterociclil-4-morfolin-4-ilpiridin-2-ona útiles para el tratamiento del cáncer y la diabetes, del 1 de Julio de 2020, de Sprint Bioscience AB: Un compuesto de la Fórmula (I) **(Ver fórmula)** en donde R1, R2 y R3 se seleccionan independientemente de hidrógeno, haloalquiloC1-C3 […]
Compuestos de 6-aril-4-(morfolin-4-il)-1H-piridin-2-ona útiles para el tratamiento del cáncer y la diabetes, del 1 de Julio de 2020, de Sprint Bioscience AB: Un compuesto de la fórmula (I) **(Ver fórmula)** en donde R1 es arilo o heteroarilo, dicho arilo y dicho heteroarilo son mono o bicíclicos […]
1-Ciclohexilo-2-fenilaminobenzimidazoles como inhibidores de MIDH1 para el tratamiento de tumores, del 17 de Junio de 2020, de DEUTSCHES KREBSFORSCHUNGSZENTRUM STIFTUNG DES OFFENTLICHEN RECHTS: Un compuesto de fórmula (I) **(Ver fórmula)** en donde: R1 representa un átomo de halógeno o un grupo seleccionado de: C1-C6-alquilo, C1-C6-alcoxi, C1-C6-haloalquilo, […]
Proceso para la síntesis de un inhibidor de indoleamina 2,3-dioxigenasa, del 13 de Mayo de 2020, de Incyte Holdings Corporation: Un proceso que comprende hacer reaccionar un compuesto de Fórmula F5: **(Ver fórmula)** con un aldehído de Fórmula F6: **(Ver fórmula)** en donde Pg1 es un grupo […]