MOLÉCULAS DE ADHESIÓN VASCULAR Y MODULACIÓN DE SU FUNCIÓN.
Un polipéptido que pertenece a una subfamilia de la Superfamilia de Inmunoglobulinas humanas,
seleccionado entre el grupo que consiste en: a) un polipéptido que posee la secuencia de aminoácidos de las Moléculas de Adhesión Reguladas en Confluencia-1 (CRAM-1), murinas, según se representa en la Fig. 3, fila superior: b) la forma madura del polipéptido según (a), en la que dicha forma madura comienza en el aminoácido de la posición 32; c) un polipéptido que pone de manifiesto, al menos, 70% de homología de secuencia con la secuencia de aminoácidos de las Moléculas de Adhesión Reguladas en Confluencia-1 (CRAM-1), murinas, según se representa en la Fig. 3, fila superior, cuyo polipéptido estimula la emigración de linfocitos o hace disminuir la permeabilidad paracelular de monocapas celulares; d) un polipéptido que comprende la secuencia de aminoácidos de la CRAM-1 humana, según se representa en la Fig. 6, grupo medio; e) la forma madura del polipéptido según (d), en la que dicha forma madura comienza en el aminoácido de la posición 32; y f) un polipéptido con un aminoácido que es, al menos, 70% homólogo con el polipéptido según (d), cuyo polipéptido estimula la emigración de linfocitos o hace disminuir la permeabilidad paracelular de monocapas celulares para usar como un medicamento
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/EP2000/002219.
Solicitante: MERCK SERONO SA.
Nacionalidad solicitante: Suiza.
Dirección: CENTRE INDUSTRIEL 1267 COINSINS, VADUZ SUIZA.
Inventor/es: AURRAND-LIONS,Michel, IMHOF,Beat,Albert.
Fecha de Publicación: .
Fecha Solicitud PCT: 13 de Marzo de 2000.
Clasificación Internacional de Patentes:
- C07K14/705B
Clasificación PCT:
- A61P9/00 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › Medicamentos para el tratamiento de trastornos en el aparato cardiovascular.
- C07K14/705 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 14/00 Péptidos con más de 20 aminoácidos; Gastrinas; Somatostatinas; Melanotropinas; Sus derivados. › Receptores; Antígenos celulares de superficie; Determinantes celulares de superficie.
- C07K16/28 C07K […] › C07K 16/00 Inmunoglobulinas, p. ej. anticuerpos mono o policlonales. › contra receptores, antígenos celulares de superficie o determinantes celulares de superficie.
- C12N15/12 C […] › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › C12N 15/00 Técnicas de mutación o de ingeniería genética; ADN o ARN relacionado con la ingeniería genética, vectores, p. ej. plásmidos, o su aislamiento, su preparación o su purificación; Utilización de huéspedes para ello (mutantes o microorganismos modificados por ingeniería genética C12N 1/00, C12N 5/00, C12N 7/00; nuevas plantas en sí A01H; reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00; nuevas razas animales en sí A01K 67/00; utilización de preparaciones medicinales que contienen material genético que es introducido en células del cuerpo humano para tratar enfermedades genéticas, terapia génica A61K 48/00; péptidos en general C07K). › Genes que codifican proteínas animales.
- C12Q1/68 C12 […] › C12Q PROCESOS DE MEDIDA, INVESTIGACION O ANALISIS EN LOS QUE INTERVIENEN ENZIMAS, ÁCIDOS NUCLEICOS O MICROORGANISMOS (ensayos inmunológicos G01N 33/53 ); COMPOSICIONES O PAPELES REACTIVOS PARA ESTE FIN; PROCESOS PARA PREPARAR ESTAS COMPOSICIONES; PROCESOS DE CONTROL SENSIBLES A LAS CONDICIONES DEL MEDIO EN LOS PROCESOS MICROBIOLOGICOS O ENZIMOLOGICOS. › C12Q 1/00 Procesos de medida, investigación o análisis en los que intervienen enzimas, ácidos nucleicos o microorganismos (aparatos de medida, investigación o análisis con medios de medida o detección de las condiciones del medio, p. ej. contadores de colonias, C12M 1/34 ); Composiciones para este fin; Procesos para preparar estas composiciones. › en los que intervienen ácidos nucleicos.
Clasificación antigua:
- A61P9/00 A61P […] › Medicamentos para el tratamiento de trastornos en el aparato cardiovascular.
- C07K14/705 C07K 14/00 […] › Receptores; Antígenos celulares de superficie; Determinantes celulares de superficie.
- C07K16/28 C07K 16/00 […] › contra receptores, antígenos celulares de superficie o determinantes celulares de superficie.
- C12N15/12 C12N 15/00 […] › Genes que codifican proteínas animales.
- C12Q1/68 C12Q 1/00 […] › en los que intervienen ácidos nucleicos.
Países PCT: Austria, Bélgica, Suiza, Alemania, Dinamarca, España, Francia, Reino Unido, Grecia, Italia, Liechtensein, Luxemburgo, Países Bajos, Suecia, Mónaco, Portugal, Irlanda, Eslovenia, Finlandia, Rumania, Chipre, Lituania, Letonia, Ex República Yugoslava de Macedonia, Albania.
PDF original: ES-2361905_T3.pdf
Fragmento de la descripción:
La presente invención se refiere a la identificación de una subfamilia de moléculas de adhesión vascular, a la identificación de su actividad biológica y a la modulación de la función de estas moléculas para el tratamiento de diversas enfermedades.
Durante todo el desarrollo embriónico y el desarrollo posnatal precoz, las células endoteliales proliferan y se diferencian formando nuevos vasos sanguíneos mediante vasculogénesis y angiogénesis. En los organismos adultos el endotelio define la barrera hematotisular y consiste en células quiescentes que no ciclan. Estas células polarizadas están enlazadas unas con otras mediante uniones herméticas y uniones adherentes formando una capa continua de células. Las funciones de la capa endotelial consisten en el mantenimiento de la homeostasia tisular, fibrinólisis, coagulación, tono vascular y transmigración leucocitaria. Todas estas propiedades están reguladas por una sintonía fina de la expresión y por la función de moléculas de adhesión.
Las situaciones patológicas tales como la inflamación, el crecimiento tumoral, la formación de heridas o la angiogénesis, conducen a un cambio temporal del número y función las moléculas de adhesión sobre el endotelio vascular y este hecho da por resultado una homeostasia alterada del vaso. Como ejemplo, los tumores aumentan la concentración local de factores angiogénicos lo que induce a una desviación desde las células endoteliales quiescentes que no cicla a endotelio en proliferación. La desviación angiogénica es inducida por varios factores que incluyen la IL-8, el factor de crecimiento epidérmico (EGF), el factor de crecimiento endotelial vascular (VEGF), la VCAM-1 soluble, el factor básico de crecimiento de los fibroblastos (bGFG), y el factor de la necrosis tumoral (TNF). Como resultado, las células endoteliales de los vasos existentes degradan la matriz extracelular (ECM) e invaden el tejido circundante, lo que lleva a la vascularización de tumores.
Durante la desviación angiogénica se modifica el tipo de expresión génica endotelial. Por ejemplo, el tratamiento de las células endoteliales con bFGF o TNF- da por resultado un aumento cuádruple de la expresión de la integrina V3, una molécula de adhesión implicada en la emigración de células endoteliales. Además, la desviación angiogénica modifica la respuesta inflamatoria del endotelio conduciendo a una emigración anormal de leucocitos hacia los tumores. Normalmente, los leucocitos se extravasan desde la sangre por adherencia al endotelio y emigran a través de él. Estos mecanismos ocurren en un proceso de varias etapas que implica selectinas, integrinas y moléculas de adhesión de la Superfamilia de las Inmunoglobulinas.
Se ha indicado que en el endotelio asociado a tumores la VCAM, la ICAM y las selectinas están reguladas a la baja. La regulación a la baja de estas moléculas de adhesión puede representar un mecanismo por el que los tumores evitan la invasión por células citotóxicas del sistema inmunitario. La solicitud de patente PCT, documento WO 98/24897, se refiere a moléculas de adhesión de la unión (JAM) de origen humano y murino, y describe también anticuerpos y expresión de JAM solubles. La solicitud de patente PCT, documento WO 00/36102, describe las secuencias de polinucleótidos y de polipéptidos de una proteína denominada PRO1868, pero no describe una actividad biológica concreta.
Es el objeto de la presente invención investigar nuevas proteínas de adhesión de la Superfamilia de las Inmunoglobulinas (Ig Sf), que están reguladas en el endotelio bajo la influencia de tumores en cuanto a la transcripción.
Es otro objeto de la invención definir moléculas derivadas desde las nuevas proteínas de adhesión para emplear en el tratamiento de diversas indicaciones, tales como, por ejemplo, tumores e inflamación.
En la investigación que condujo a la presente invención, se utilizó un modelo murino experimental para identificar transcritos regulados durante el cultivo conjunto de una línea de células endoteliales con células de melanoma. Para restringir la estrategia de selección a moléculas de adhesión de la Ig Sf, se desarrolló un nuevo enfoque de exposición del RNA denominado “Exposición Diferencial Dirigida” (Targeted Differential Display). La novedad de ea técnica de exposición modificada reside en el uso de solo un conjunto de cebadores degenerados. Como se demuestra en los ejemplos, se encontró, sorprendentemente, que esto lleva a una especificidad suficiente.
Más específicamente, los cebadores parcialmente degenerados (en el caso presente el nivel de degeneración está entre 2048 y 4096 formas diferentes de cebadores dentro de un conjunto), designados para dirigir la secuencia conservada encontrada en los dominios C2 de miembros de la Ig Sf, fueron utilizados para conducir la Técnica de Exposición Diferencial Dirigida basada en la Reacción en Cadena de la Polimerasa (PCR) (Samaridis and Colonna (1997) Eur. J. Immunol. 27, 660-665).
Basándose en este descubrimiento la invención proporciona un método para la identificación específica de secuencias de DNA expresadas diferencialmente, que comprende el uso de PCR de Transcripción Inversa de Exposición Diferencial, en la que se utiliza un conjunto de cebadores parcial o totalmente degenerados, específicos del gen diana. Una limitación importante de la estrategia convencional de exposición de RNA es la falta de especificidad del método. Con la pretensión de aumentar esta especificidad, los inventores, en su búsqueda de otras moléculas de adhesión, han utilizado cebadores degenerados que tienen como objetivo las secuencias que codifican moléculas con dominios C2. Esto se consiguió mediante la alineación de los dominios C2 de diversas moléculas de adhesión de la Ig Sf, y la identificación de un consenso lineal de aminoácidos, que rodean al resto de cisteína que participa en la estructura de los dominios C2: Y-(RQYS)-C-x-A-S-N-x2-G. En un sentido más general, este enfoque puede ser usado también para la búsqueda de otras secuencias en que se usa la traducción inversa de una o más de las secuencias de consenso más frecuentes, para diseñar los cebadores degenerados utilizados en la exposición diferencial.
El método ha permitido la identificación de un transcrito, regulado a la baja en las células endoteliales por confluencia en presencia de células de melanoma o de carcinomas. El cDNA codificaba una molécula de la Ig Sf con características estructurales inusuales, y se denominó CRAM-1 por “Molécula de Adhesión Regulada en Confluencia”.(Confluency Regulated Adhesion Molecule) Las secuencias de polinucleótidos y polipéptidos de CRAM-1 son idénticas a las de la proteína PRO1868 descritas en el documento WO 00/36102, pero aquí, por primera vez, su actividad biológica ha sido identificada. La descripción reciente de una molécula estructuralmente afín, JAM, implicada en la transmigración leucocitaria, sugirió la existencia de una nueva familia de moléculas de adhesión de la que las moléculas JAM y CRAM-1 eran los prototipos. La comparación de las secuencias con las bases de datos EST permitió, además, la clonación de CRAM-2, un tercer miembro de esta familia molecular. La Fig. 1 muestra las secuencias de cDNA murinas que codifican las proteínas de CRAM-1 y CRAM-2. En esta solicitud de patente los nombres JAM y JAM-1, CRAM-1 y JAM-2, así como CRAM-2 y JAM-1, se usan indistintamente.
La distribución tisular comparativa de los transcritos que codifican JAM, CRAM-1 y CRAM-2 puso de manifiesto una expresión preferente de esas moléculas en los compartimentos endotelial y epitelial, lo que sugiere un papel importante desempeñado en el mantenimiento de los contactos de célula-célula. Estas interacciones de célula-célula de células endoteliales quiescentes regulan la permeabilidad vascular, el ciclo celular y la transmigración leucocitaria a través de la pared endotelial.
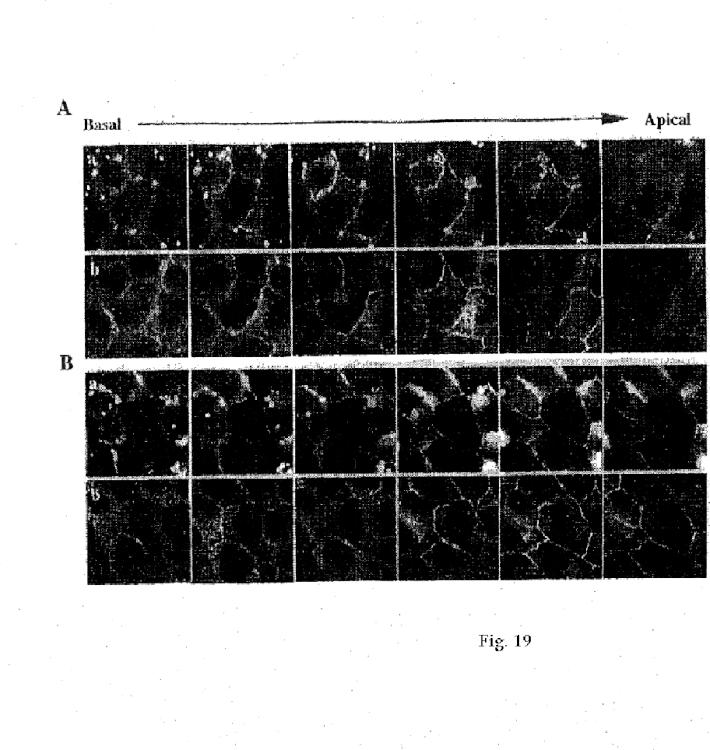
Para esclarecer adicionalmente la función y la interacción de las tres moléculas, se usó un enfoque molecular. A este fin, fueron construidas moléculas quiméricas que consistían en las secuencias “Flag-tag” y Proteína Fluorescente Verde Intensificada (Enhanced Green Fluorescent Protein) (EGFP) fusionadas a una forma soluble o una forma unida a la membrana, de CRAM-1, CRAM-2 o JAM) (resumido en la Fig. 2). Cuando fueron transfectados en líneas celulares, los productos de fusión de EGFP de CRAM-1 y JAM se localizaron en los contactos de célula-célula, confirmando el papel que desempeñan... [Seguir leyendo]
Reivindicaciones:
1. Un polipéptido que pertenece a una subfamilia de la Superfamilia de Inmunoglobulinas humanas, seleccionado entre el grupo que consiste en: a) un polipéptido que posee la secuencia de aminoácidos de las Moléculas de Adhesión Reguladas en Confluencia-1 (CRAM-1), murinas, según se representa en la Fig. 3, fila superior: b) la forma madura del polipéptido según (a), en la que dicha forma madura comienza en el aminoácido de la posición 32;
c) un polipéptido que pone de manifiesto, al menos, 70% de homología de secuencia con la secuencia de aminoácidos de las Moléculas de Adhesión Reguladas en Confluencia-1 (CRAM-1), murinas, según se representa en la Fig. 3, fila superior, cuyo polipéptido estimula la emigración de linfocitos o hace disminuir la permeabilidad paracelular de monocapas celulares;
d) un polipéptido que comprende la secuencia de aminoácidos de la CRAM-1 humana, según se representa en la Fig. 6, grupo medio; e) la forma madura del polipéptido según (d), en la que dicha forma madura comienza en el aminoácido de la posición 32; y
f) un polipéptido con un aminoácido que es, al menos, 70% homólogo con el polipéptido según (d), cuyo polipéptido estimula la emigración de linfocitos o hace disminuir la permeabilidad paracelular de monocapas celulares
para usar como un medicamento.
2. Un polipéptido soluble de CRAM-1 que comprende el dominio V de CRAM-1 según se representa en la Fig. 2-2, capaz de bloquear la emigración transendotelial de leucocitos. 3. El polipéptido soluble según la reivindicación 2, que comprende:
a) el dominio V de la CRAM-1 murina, según se representa en la Fig. 2-2 ó en la Fig. 8; b) el dominio V y el dominio C2 de la CRAM-1 murina, según se representa en la Fig. 2-2 o en la Fig. 8; c) los aminoácidos 1 a 159 de la CRAM-1 murina, según se representa en la Fig. 8; o d) los aminoácidos 1 a 238 de la CRAM-1 murina, según se representa en la Fig. 8.
4. Un polipéptido soluble según la reivindicación 2 ó 3, para usar como un medicamento.
5. Un polipéptido soluble según la reivindicación 4, para usar en el tratamiento de reacciones de inflamación.
6. Un polipéptido seleccionado entre el grupo que consiste en: a) un polinucleótido que posee una secuencia de nucleótidos idéntica a la secuencia de nucleótidos de la CRAM-1 murina, según se representa en la Fig. 1 ó en la Fig. 8; b) un polinucleótido que posee una secuencia de nucleótidos que codifica un polipéptido completo o una de sus partes, cuyo polipéptido posee una secuencia de aminoácidos que es, al menos, 70% homóloga con la secuencia de aminoácidos de la CRAM-1, según se representa en la fila superior de la Fig. 3, y cuyo polipéptido estimula la emigración de linfocitos o hace disminuir la permeabilidad paracelular de monocapas celulares;
c) un polinucleótido que posee una secuencia de nucleótidos idéntica a la secuencia de nucleótidos de la CRAM-1 humana, según se representa en la Fig. 6; y d) un polinucleótido que posee una secuencia de nucleótidos que codifica un polipéptido completo o una de sus partes, cuyo polipéptido posee una secuencia de aminoácidos que es, al menos, 70% homóloga con la
secuencia de aminoácidos de la CRAM-1 humana, según se representa en la Fig. 6, y cuyo polipéptido estimula la emigración de linfocitos o hace disminuir la permeabilidad paracelular de monocapas celulares,
para usar como un medicamento. 7. Un anticuerpo dirigido contra el polipéptido según la reivindicación 1, en el que dicho anticuerpo es capaz de inhibir la emigración transendotelial de leucocitos.
8. Un anticuerpo según la reivindicación 7, en el que el anticuerpo está acoplado a una toxina, un marcador radiactivo o un fármaco. 9. Un anticuerpo según la reivindicación 7 u 8, para usar como un medicamento.
Patentes similares o relacionadas:
COMPOSICIONES Y PROCEDIMIENTOS PARA EL TRATAMIENTO Y DIAGNÓSTICO DE TRASTORNOS INMUNITARIOS, del 15 de Diciembre de 2011, de MILLENNIUM PHARMACEUTICALS, INC.: Un anticuerpo que se une específicamente a un péptido codificado por la secuencia de nucleótidos de la SEC ID N.º: 2 o un péptido codificado por el gen […]
MUTEÍNAS GP130 SOLUBLES CON ACTIVIDAD DE UNIÓN MEJORADA, del 9 de Diciembre de 2011, de CONARIS RESEARCH INSTITUTE AG: Un polipéptido que comprende (a) la parte extracelular completa de la glucoproteína gp130 o (b) variantes o fragmentos de dicha parte extracelular, siendo dicho […]
PÉPTIDOS TERAPÉUTICOS QUE COMPRENDEN SECUENCIAS DERIVADAS DE CDR2 O CDR3 DE TREM-1 Y EL USO DE LOS MISMOS PARA INHIBIR SEPSIS, del 1 de Junio de 2011, de NOVO NORDISK A/S UNIVERSITE HENRI POINCARÉ - NANCY 1: Polipéptido o derivado, que es capaz de actuar como antagonista de la proteína TREM-1 tal y como se define en SEC ID Nº. 1, que comprende la secuencia de aminoácidos […]
MOLÉCULAS DENOMINADAS LDCAM, del 3 de Marzo de 2011, de IMMUNEX CORPORATION: Una composición que incluye una proteína que comprende los aminoácidos 39374 de SEQ ID NO: 2 y un diluyente o vehículo farmacéuticamente aceptable, en la que dicha proteína […]
SITIO DE ENLAZAMIENTO DEL LIGANDO DE RAGE Y USOS DEL MISMO, del 11 de Febrero de 2011, de THE TRUSTEES OF COLUMBIA UNIVERSITY IN THE CITY OF NEW YORK: Un péptido enlazado a un anticuerpo o a una porción de un anticuerpo, en donde el péptido es un fragmento de sRAGE que comprende los aminoácidos […]
 NUEVAS SECUENCIAS DE POLINUCLEÓTIDOS Y POLIPÉPTIDOS Y SUS USOS, del 27 de Enero de 2011, de IMCLONE LLC: Un oligonucleótido antisentido aislado, en el que dicho oligonucleótido inhibe la expresión del polinucleótido de la SEQ ID NO:1 o SEQ ID […]
NUEVAS SECUENCIAS DE POLINUCLEÓTIDOS Y POLIPÉPTIDOS Y SUS USOS, del 27 de Enero de 2011, de IMCLONE LLC: Un oligonucleótido antisentido aislado, en el que dicho oligonucleótido inhibe la expresión del polinucleótido de la SEQ ID NO:1 o SEQ ID […]
COMPOSICION FARMACEUTICA PARA EL TRATAMIENTO DE CANCER, del 24 de Enero de 2011, de PROYECTO DE BIOMEDICINA CIMA, S.L. INSTITUT NATIONAL DE LA SANTE ET DE LA RECHERCHE MEDICALE: La invención se relaciona con composiciones terapéuticas para el tratamiento del cáncer y, más concretamente, con composiciones que comprenden un ligando agonista […]
 CD52 soluble para su uso en el tratamiento o la prevención de la esclerosis múltiple o de la artritis reumatoide, del 29 de Julio de 2020, de THE WALTER AND ELIZA HALL INSTITUTE OF MEDICAL RESEARCH: Uno cualquiera o más de:
i) glucoproteína CD52 soluble, ii) una proteína de fusión que comprende la glucoproteína CD52 soluble como una primera proteína, y una segunda proteína;
[…]
CD52 soluble para su uso en el tratamiento o la prevención de la esclerosis múltiple o de la artritis reumatoide, del 29 de Julio de 2020, de THE WALTER AND ELIZA HALL INSTITUTE OF MEDICAL RESEARCH: Uno cualquiera o más de:
i) glucoproteína CD52 soluble, ii) una proteína de fusión que comprende la glucoproteína CD52 soluble como una primera proteína, y una segunda proteína;
[…]