METODO PARA LA PREPARACION DE HEXAHIDROFURO(2,3-B)FURAN-3-OL.
Un método para la síntesis de hexahidro-furo[2,3-b]furan-3-ol de fórmula (7) a partir de un compuesto intermedio de fórmula (1) en donde P1 y P2 representan cada uno independientemente un hidrógeno,
un grupo protector de hidroxi o pueden formar juntos un grupo protector de diol vecinal,
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/EP02/10062.
Solicitante: TIBOTEC PHARMACEUTICALS.
Nacionalidad solicitante: Irlanda.
Dirección: EASTGATE VILLAGE EASTGATE LITTLE ISLAND,CO CORK.
Inventor/es: SURLERAUX, DOMINIQUE, LOUIS, NESTOR, GHISLAIN, KESTELEYN,BART,RUDOLF,ROMANIE, QUAEDFLIEG,PETER.J.L.M.
Fecha de Publicación: .
Fecha Concesión Europea: 30 de Diciembre de 2009.
Clasificación Internacional de Patentes:
- C07D307/20 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07D COMPUESTOS HETEROCICLICOS (Compuestos macromoleculares C08). › C07D 307/00 Compuestos heterocíclicos que contienen ciclos de cinco miembros que tienen un átomo de oxígeno como único heteroátomo del ciclo. › Atomos de oxígeno.
- C07D493/04 C07D […] › C07D 493/00 Compuestos heterocíclicos que contienen átomos de oxígeno como únicos heteroátomos del ciclo en el sistema condensado. › Sistemas orto-condensados.
Clasificación PCT:
- C07D493/04 C07D 493/00 […] › Sistemas orto-condensados.
Clasificación antigua:
- C07D307/00 C07D […] › Compuestos heterocíclicos que contienen ciclos de cinco miembros que tienen un átomo de oxígeno como único heteroátomo del ciclo.
- C07D493/04 C07D 493/00 […] › Sistemas orto-condensados.
Fragmento de la descripción:
Método para la preparación de hexahidrofuro[2,3-b]furan-3-ol.
La presente invención se refiere a un método para preparación de hexahidro-furo[2,3-b]furan-3-ol y nuevos compuestos intermedios para uso en dicho método. De modo más particular, la invención se refiere a un método estereoselectivo para la preparación de hexahidro-furo[2,3-b]furan-3-ol, y a un método apto para aumento a escala industrial.
El hexahidro-furo[2,3-b]furan-3-ol es un resto farmacológico importante presente en la estructura de los inhibidores de la proteasa retroviral tales como los descritos por Ghosh et al. en J. Med. Chem. 1996, 39(17), 3278-3290, EP0715718, WO 99/67417, y WO 99/65870.
Se conocen varios métodos para la preparación de hexahidro-furo[2,3-b]furan-3-ol (fórmula 7)).
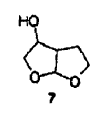
Ghosh et al. en J. Med. Chem. 1996, 39(17), 3278-3290, describen una síntesis enantioselectiva para obtener a la vez (3R,3aS,6aR) y (3S,3aR,6aS)hexahidrofuro[2,3-b]furan-3-ol en forma ópticamente pura a partir de malato de 3-(R)-dietilo y malato de 3(S)-dietilo, respectivamente. Este proceso comprende varios pasos tales como un paso de alilación utilizando diisopropil-amiduro de litio, seguido por un paso de reducción y ulteriormente un paso de oxidación de Swern seguido por una escisión ozonolítica y un paso de hidroboración utilizando 9-borabiciclo[3.3.1]nonano(9-BBN). Ghosh et al. describen también una síntesis racémica de ambos enantiómeros (3R,3aS,6aR) y (3S,3aR,6aS) de hexahidrofuro[2,3-]furan-3-ol seguida por una resolución enzimática del producto final. Esta última síntesis parte de 2,3-dihidrofurano y comprende el paso de tratar dicho compuesto intermedio con N-yodosuccinimida y alcohol alílico seguido por una ciclación radical en presencia de un catalizador, a saber cobaloxima. Una escisión ozonolítica seguida por un paso de reducción proporciona el hexahidro-furo[2,3-b]furan-3-ol racémico. El compuesto ópticamente activo (3R,3aS,6aR)hexahidrofuro[2,3-b]furan-3-ol se obtiene después de resolución enzimática seguida por cromatografía con gel de sílice. Pezeck et al. Tetrahedron Lett. 1986, 27, 3715-3718 describen también una ruta para la síntesis de hexahidro-furo[2,3-b]furan-3-ol utilizando ozonólisis. El hexahidro-furo[2,3-b]furan-3-ol se describe también como un compuesto intermedio en la síntesis de derivados ópticamente activos de perhidrofuro[2,3-b]furano (Uchiyama et al., Tetrahedron Lett. 2001, 42, 4653-4656). El paso clave en este procedimiento es la oxiselenenilación (sic) de 2,3-di- hidrofurano. Este procedimiento es adecuado para uso al nivel de laboratorio, pero no es apto para aumento de escala.
Aunque las dos rutas de síntesis descritas por Ghosh et al. proporcionan (3R,3aS,6aR)- y (3S,3aR,6aS)-hexahidro-furo[2,3-b]furan-3-ol con rendimientos razonables y exceso enantiomérico elevado, los mismos son únicamente factibles a escala de laboratorio pero, por varias razones, no son aptos para aumento a la escala industrial. Por ejemplo, estas rutas conocidas adolecen de la desventaja de utilizar materiales caros, metales pesados y compuestos escasos, tales como la N-yodosuccinimida, el catalizador cobaloxima, diisopropil-amiduro de litio y 9-BBN. El paso necesario de ozonólisis presenta la desventaja de producir ozónidos y peróxidos altamente reactivos y sensibles al impacto, que hacen este paso demasiado peligroso para ser aplicado en escala industrial. Adicionalmente, la ozonólisis y la oxidación de Swern son fuertemente exotérmicas y, como consecuencia, tienen que realizarse a temperaturas muy bajas. La ruta racémica precisa una resolución enzimática en el paso final de la síntesis, seguido por purificación con gel de sílice. Adicionalmente, la ruta racémica adolece de la desventaja de un bajo balance de materias global, originado por el hecho de que el paso de resolución, que conduce al compuesto final enantioméricamente puro, tiene lugar en el último paso de la síntesis, con lo cual solamente puede obtenerse un rendimiento de 50% como máximo del enantiómero deseado. Ambas rutas conocidas por la técnica anterior producen también una gran cantidad de residuos tales como disolventes y sales en las operaciones de lavado. Por tanto, estos métodos conocidos no son adecuados para la producción de estereoisómeros ópticamente puros de hexahidro-furo[2,3-b]furan-3-ol en escala industrial.
El objeto principal de la presente invención es proporcionar un método mejorado para producir hexahidro-furo[2,3-b]furan-3-ol, cuando se compara con los métodos conocidos en la técnica y sus inconvenientes. Es otro objeto proporcionar un método para la síntesis de hexahidro-furo[2,3-b]furan-3-ol, que es adecuado para aumento a escala industrial. Un objeto adicional de la presente invención es proporcionar un método estereoselectivo que comprende pasos en los cuales la estereoquímica de los compuestos intermedios o los compuestos finales está controlada, que permite la síntesis de los estereoisómeros de hexahidro-furo[2,3-b]furan-3-ol. Otro objeto adicional es proporcionar un método que permite la producción de hexahidro-furo[2,3-b]furan-3-ol con un rendimiento global igual o mayor que para los métodos arriba descritos y con un exceso enantiomérico mayor que 50%. Otro objeto de la presente invención es proporcionar un proceso para fabricación de hexahidro-furo[2,3-b]furan-3-ol que se produce a partir de materias primas y reactivos fácilmente disponibles. Otro objeto de la presente invención es proporcionar nuevos compuestos intermedios, que son útiles como precursores en la síntesis de hexahidro-furo[2,3-]furan-3-ol.
Los autores de la presente invención han encontrado sorprendentemente un método nuevo e inventivo para la síntesis de mezclas estereoisómeras o formas estereoisómeramente puras de hexahidro-furo[2,3-b]furan-3-ol.
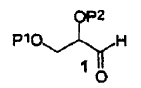
Así, el presente método implica la síntesis de hexahidro-furo[2,3-b]furan-3-ol a partir de un compuesto intermedio de fórmula (1) en la cual P2 y P2 representan cada uno independientemente hidrógeno, un grupo protector de hidroxi o pueden formar juntos un grupo protector de diol vecinal, transformar dicho compuesto intermedio de fórmula (1) en un derivado de nitrometano
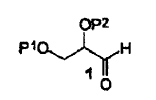
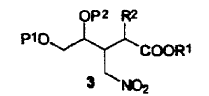
de fórmula (3) en la cual R1 representa alquilo, arilo o aralquilo, R2 representa hidrógeno o C(=O)OR3, R3 representa un alquilo, arilo o aralquilo, o R3, si está presente, y R1 considerados junto con los átomos a los cuales están unidos, pueden formar un grupo cíclico de 6 a 8 miembros que puede estar sustituido opcionalmente con arilo, aralquilo, o arilo,
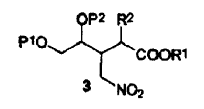
transformar subsiguientemente dicho derivado de nitrometano en un derivado de tetrahidrofurano de fórmula (6) en la cual OR4 representa un alcoholato tal como un grupo alquiloxi, haciendo uso por ejemplo de una reacción de Nef,
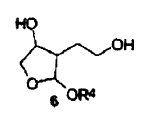
y transformar finalmente el compuesto intermedio de fórmula (6) en hexahidro-furo[2,3-b]furan-3-ol de fórmula (7) por la vía de una reacción intramolecular de ciclación.

El método anterior presenta la ventaja adicional de utilizar materiales de partida fácilmente disponibles, tales como un gliceraldehído protegido en O. Los reactivos utilizados adicionalmente en dicho método son seguros y están disponibles en gran cantidad. Adicionalmente, cada paso de dicho método proporciona el compuesto deseado con rendimiento satisfactorio. Además, cada paso de dicho método puede realizarse de modo estereoselectivo, lo que permite la síntesis de formas estereoisómeras puras de dichos compuestos cuando se utilizan, en caso apropiado, materiales de partida y reactivos ópticamente puros. Así, el método de acuerdo con la presente invención es adecuado para aumento a escala industrial.
En una realización preferida, la presente invención se refiere a un método para la síntesis de hexahidro-furo[2,3-b]furan-3-ol de fórmula (7), que comprende los pasos de:
Reivindicaciones:
1. Un método para la síntesis de hexahidro-furo[2,3-b]furan-3-ol de fórmula (7) a partir de un compuesto intermedio de fórmula (1) en donde P1 y P2 representan cada uno independientemente un hidrógeno, un grupo protector de hidroxi o pueden formar juntos un grupo protector de diol vecinal,
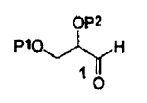
transformación de dicho compuesto intermedio de fórmula (1) en un derivado de nitrometano de fórmula (3) en donde R1 representa alquilo, arilo o aralquilo, R2 representa hidrógeno o C(=O)OR3, R3 representa alquilo, arilo o aralquilo, o R3, en caso de estar presente, y R1 considerados junto con los átomos a los cuales están unidos, pueden formar un grupo cíclico de 6 a 8 miembros que puede estar sustituido opcionalmente con alquilo, aralquilo o arilo,
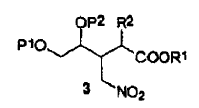
transformación subsiguientemente de dicho derivado de nitrometano en un derivado de tetrahidrofurano de fórmula (6) en donde OR4 representa un alcoholato,

y finalmente, transformación del compuesto intermedio de fórmula (6) en hexahidro-furo[2,3-b]furan-3-ol de fórmula (7) por una reacción intramolecular de ciclación:

2. Un método de acuerdo con la reivindicación 1, en el cual el compuesto intermedio de fórmula (3) se transforma en un compuesto intermedio de fórmula (6) haciendo uso de una reacción de Nef.
3. Un método de acuerdo con las reivindicaciones 1 ó 2 para la síntesis de hexahidro-furo[2,3-b]furan-3-ol de fórmula (7), que comprende los pasos de:
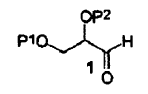

4. Un método de acuerdo con una cualquiera de las reivindicaciones 1 a 3 para la síntesis de hexahidro-furo[2,3-b]furan-3-ol de fórmula (7), que comprende los pasos de:
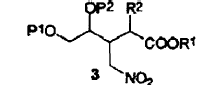
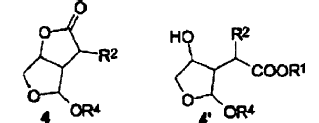


5. Un método de acuerdo con la reivindicación 1 para la síntesis de hexahidro-furo[2,3-b]furan-3-ol de fórmula (7.1) a partir de un compuesto intermedio de fórmula (1), en donde P1 y P2 considerados juntos forman un isopropilideno,

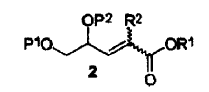
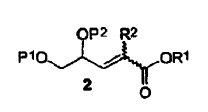
por condensación de dicho compuesto intermedio de fórmula (1) dando como resultado un compuesto intermedio de fórmula (2), en donde P1 y P2 considerados juntos forman un isopropilideno, R2 representa -C(=O)OR3, donde R3 es metilo y R1 es metilo,

reacción de dicho éster de fórmula (2) en un derivado de nitrometano de fórmula (3) en donde P1 y P2 considerados juntos forman un isopropilideno, R2 representa -C(=O)OR3, en donde R3 es metilo, y R1 es metilo,
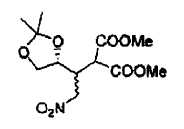
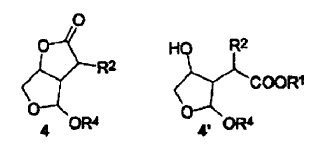
Transformación de dicho compuesto intermedio de fórmula (3) utilizando una base y subsiguientemente un ácido para producir compuestos intermedios de fórmula (4) y (4'), en donde R2 representa -C(=O)OR3, en donde R3 es metilo, R1 es metilo y R4 es metilo,
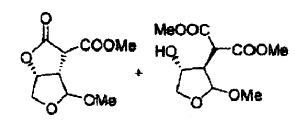
descarboxilación de los compuestos intermedios de fórmula (4) conduciendo a un compuesto intermedio de fórmula (5), en donde R4 es metilo,
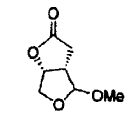
reducción de dicho compuesto intermedio de fórmula (5) con un agente reductor adecuado dando como resultado un compuesto intermedio de fórmula (6), en donde R4 es metilo,
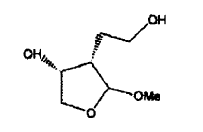
y transformación del compuesto intermedio de fórmula (6) en el compuesto 7.1 por la vía una reacción intramolecular de ciclación:

6. Un método de acuerdo con una cualquiera de las reivindicaciones 3 a 5 en el cual el compuesto intermedio de fórmula (3) se somete a una reacción de Nef utilizando extinción con ácido mientras se mantiene la temperatura por debajo de 10ºC durante dicha extinción.
7. Un método de acuerdo con la reivindicación 4 ó 5 en el cual la descarboxilación de los compuestos intermedios de fórmula (4) y (4') se realiza en una solución acuosa tamponada.
8. Un método de acuerdo con una cualquiera de las reivindicaciones 3 a 5 en el cual el compuesto intermedio (6) se prepara por reducción de compuestos intermedios de fórmula (4) y (4') o compuestos intermedios de fórmula (5) y (5') utilizando borohidruro de litio en tetrahidrofurano o NaBH4 en presencia de LiCl.
9. Un método de acuerdo con una cualquiera de las reivindicaciones 3 a 5 en el cual la ciclación del compuesto intermedio de fórmula (6) para dar el compuesto de fórmula (7) se realiza por adición de un ácido fuerte a la mezcla de reacción que contiene el compuesto intermedio de fórmula (6).
10. Un método de acuerdo con la reivindicación 9 en el cual la reacción de ciclación se realiza a una temperatura inferior a 5ºC.
11. Un método de acuerdo con una cualquiera de las reivindicaciones 1 a 3 en el cual un compuesto intermedio de fórmula (3) se prepara por un proceso que comprende los pasos de condensar primeramente un compuesto intermedio de fórmula (1) con nitrometano, dando como resultado un compuesto intermedio de fórmula (8) y, en segundo lugar, hacer reaccionar dicho compuesto intermedio de fórmula (8) con CHR2R8-C(=O)-OR1 en donde R8 es hidrógeno o un éster carboxílico:

12. Un método de acuerdo con la reivindicación H, en el cual el éster carboxílico se define como C(=O)-OR1.
13. Un método de acuerdo con una cualquiera de las reivindicaciones 1 a 5 en el cual se prepara un compuesto intermedio de fórmula (6) por un proceso que comprende los pasos de reducir primeramente el compuesto intermedio de fórmula (3) en la cual R2 es hidrógeno con un agente reductor adecuado, dando como resultado un compuesto intermedio de fórmula (9) y, en segundo lugar, someter el compuesto intermedio de fórmula (9) obtenido a una reacción de Nef por tratamiento con una base y a continuación con un ácido fuerte:
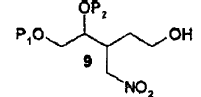
14. Un método de acuerdo con una cualquiera de las reivindicaciones 1 a 13, en el cual se aísla hexahidro-furo[2,3-b]furan-3-ol de fórmula (7) por adición de un pequeño exceso de una amina terciaria, seguido por la separación de agua y eliminación de las sales formadas.
15. Un método de acuerdo con una cualquiera de las reivindicaciones 1 a 14, en el cual R1 y R3 son cada uno independientemente alquilo C1-6, arilo o aril-alquilo C1-6, o junto con los átomos a los cuales están unidos R1 y R3, forman un grupo cíclico de 6 a 8 miembros sustituido opcionalmente con alquilo C1-6, arilo o aril-alquilo C1-6, y en donde R4 es alquilo C1-6.
16. Un método de acuerdo con una cualquiera de las reivindicaciones 1 a 15, en el cual R1, R3 y R4 son cada uno independientemente metilo, propilo, isopropilo, n-butilo, isobutilo, sec-butilo, terc-butilo o pentilo.
17. Un método de acuerdo con una cualquiera de las reivindicaciones 1 a 16 en el cual P1 y P2 forman juntos un grupo protector de diol vecinal lábil en medio ácido.
18. Un método de acuerdo con una cualquiera de las reivindicaciones 1 a 17, en el cual P1 y P2 es un radical dialquil-metileno.
19. Un método de acuerdo con una cualquiera de las reivindicaciones 4 y 6 a 10 en el cual R5 es hidrógeno, R1O-C(=O)-, (R6)3P=, en donde R6 es alquilo, arilo o aralquilo, o (R7O)2P(=O)- en donde R7 es alquilo, arilo o aralquilo.
20. Un compuesto intermedio que tiene la fórmula (3),

en la cual P1 y P2 representan cada uno independientemente un hidrógeno, un grupo protector de hidroxi, o pueden formar juntos un grupo protector de diol vecinal, R1 representa alquilo, arilo o aralquilo, R2 representa hidrógeno o C(=O)OR3, R3 representa alquilo, arilo o aralquilo, o R3, en caso de estar presente, y R1 considerados junto con los átomos a los cuales están unidos, pueden formar un grupo cíclico de 6 a 8 miembros que puede estar sustituido opcionalmente con alquilo, aralquilo, o arilo;
con la condición de que, cuando R2 es hidrógeno y P1 y P2 considerados juntos forman un isopropilideno, entonces R1 es distinto de metilo o etilo.
21. Un compuesto intermedio que tiene la fórmula (4) o (4'),
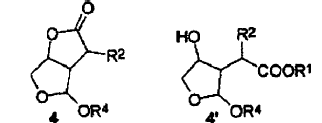
en donde R1 representa alquilo, arilo o aralquilo; R2 representa hidrógeno o C(=O)OR3; R3 representa alquilo, arilo o aralquilo, o R3, en caso de estar presente, y R1 considerados junto con los átomos a los cuales están unidos, pueden formar un grupo cíclico de 6 a 8 miembros que puede estar sustituido opcionalmente con alquilo, aralquilo, o arilo; OR4 representa un alcoholato.
22. Un compuesto intermedio que tiene la fórmula (5) o (5'),
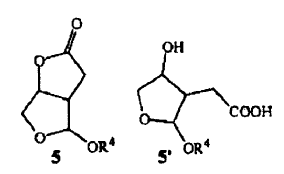
en donde OR4 representa un alcoholato.
23. Un compuesto intermedio de acuerdo con la reivindicación 22, en el cual el compuesto intermedio tiene la fórmula (5a)
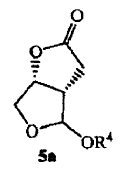
24. Un compuesto intermedio de acuerdo con la reivindicación 23 en forma cristalina.
25. Un método para la síntesis de un inhibidor de la proteasa de HIV, en el cual dicho método comprende el uso de un compuesto de fórmula (7) que se ha preparado de acuerdo con un método descrito en una cualquiera de las reivindicaciones 1 a 19.
26. Un método de acuerdo con la reivindicación 25, en el cual el compuesto de fórmula (7) es un compuesto de fórmula (7.1):
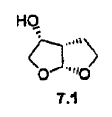
27. Un método de acuerdo con la reivindicación 25 ó 26 en el cual el inhibidor de la proteasa de HIV es
ácido [(1S,2R)-3-[[(4-aminofenil)sulfonil](2-metil-propil)amino]-2-hidroxi-1-(fenilmetil)propil]-carbámico, (3R, 3aS,6aR)-hexahidrofuro[2,3-b]furan-3-il-éster; o
ácido [(1S,2R)-2-hidroxi-3-[[(4-metoxifenil)sulfonil](2-metilpropil)-amino]-1-(fenilmetil)propil]-carbámico, (3R, 3aS,6aR)-hexahidrofuro[2,3-b]furan-3-il-éster; o
ácido [(1S,2R)-3-[(1,3-benzodioxol-5-ilsulfonil)(2-metil-propil)amino]-2-hidroxi-1-(fenilmetil)propil)-carbámico, (3R,3aS,6aR)-hexahidrofuro[2,3-b]furan-3-il-éster; o
cualquier sal de adición farmacéuticamente aceptable de cualquiera de dichos compuestos.
28. Un método de acuerdo con la reivindicación 27, en el cual el inhibidor de la proteasa de HIV es ácido [(1S,2R)-3-[[(4-aminofenil)sulfonil](2-metilpropil)ami-no]-2-hidroxi-1-(fenilmetil)propil]-carbámico, (3R,3aS,6aR)-hexahidrofuro[2,3-b]furan-3-il-éster, o cualquier sal de adición farmacéuticamente aceptable del mismo.
Patentes similares o relacionadas:
Moduladores heteroaromáticos del receptor NMDA y usos de los mismos, del 24 de Junio de 2020, de Cadent Therapeutics, Inc: Un compuesto representado por la Fórmula I **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, en el que: los anillos A y B son un sistema heteroaromático […]
Compuestos de tienopirrol y usos de los mismos como inhibidores de luciferasas procedentes de Oplophorus, del 6 de Mayo de 2020, de PROMEGA CORPORATION: Un compuesto de fórmula (I), o una sal del mismo: **(Ver fórmula)** en la que: la línea discontinua representa la presencia o ausencia de un enlace; X es […]
Nuevos compuestos antibacterianos, del 1 de Abril de 2020, de AZIENDE CHIMICHE RIUNITE ANGELINI FRANCESCO A.C.R.A.F. S.P.A.: Compuesto de fórmula: : A-L1-Y-L2-R-B en el que: A es un grupo cíclico que presenta la fórmula (II) siguiente: **(Ver fórmula)** […]
Ester de ibuprofeno de filigenina, su procedimiento de preparación y aplicaciones del mismo, del 3 de Enero de 2020, de Fu, Li: Un compuesto de éster de ibuprofeno de filigenina con fórmula estructural general representada por la fórmula (I):**Fórmula**
Compuestos de biarilamida como inhibidores de cinasas, del 25 de Diciembre de 2019, de NOVARTIS AG: Un compuesto de formula (I): **(Ver fórmula)** o una sal farmaceuticamente aceptable de este, donde: Z1 es O, S, S(=O) o SO2; […]
Tricíclicos sustituidos y métodos de uso, del 18 de Diciembre de 2019, de AbbVie Overseas S.à r.l: Un compuesto de fórmula (I) o una sal farmacéuticamente aceptable del mismo, **(Ver fórmula)** en donde R1 es H o alquilo C1-C3; X es la fórmula (a) […]
Modulación de receptores quimiosensoriales y ligandos asociados con los mismos, del 26 de Noviembre de 2019, de SENOMYX INC.: Un compuesto que tiene la fórmula estructural (IIIb1)**Fórmula** o una sal, tautómero, solvato o éster del mismo, en donde A es acilo, acilo sustituido, heteroalquilo, […]
Derivados de pirazol tricíclicos condensados útiles para modular los receptores farnesoide x, del 20 de Noviembre de 2019, de Recordati AG: Un compuesto de acuerdo con la Fórmula (II), **(Ver fórmula)** o una sal farmacéutica aceptable de esta, donde R0 es alquilo C1-6; haloalquilo C1-6; […]