ANTICUERPOS ESPECIFICOS DE CD22 HUMANA Y SUS USOS TERAPEUTICOS Y DIAGNOSTICOS.
Una molécula de anticuerpo que tiene especificidad para el CD22 humano,
que comprende una cadena pesada en la que el dominio variable comprende la SEQ ID NO: 1 para CDR-H1, la secuencia GINPGNNYATYRRKFQG de gH7 de la Figura 6 o la SEQ ID NO: 2 o la SEQ ID NO: 13 o la SEQ ID NO: 15 o la SEQ ID NO: 16 para CDR-H2, y la SEQ ID NO: 3 para CDR-H3, y una cadena ligera en la que el dominio variable comprende la SEQ ID NO: 4 para CDR-L1, la SEQ ID NO: 5 para CDR-L2 y la SEQ ID NO: 6 para CDR-L3
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/GB03/01934.
Solicitante: UCB PHARMA, S.A..
Nacionalidad solicitante: Bélgica.
Dirección: ALLEE DE LA RECHERCHE 60,1070 BRUSSELS.
Inventor/es: POPPLEWELL,ANDREW GEORGE, TICKLE,SIMON PETER, LADYMAN,HEATHER MARGARET.
Fecha de Publicación: .
Fecha Concesión Europea: 31 de Marzo de 2010.
Clasificación Internacional de Patentes:
- C07K16/28A
Clasificación PCT:
- A61K31/7088 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › Compuestos que tienen al menos tres nucleósidos o nucleótidos.
- A61K39/395 A61K […] › A61K 39/00 Preparaciones medicinales que contienen antígenos o anticuerpos (materiales para ensayos inmunológicos G01N 33/53). › Anticuerpos (aglutininas A61K 38/36 ); Inmunoglobulinas; Inmunosuero, p. ej. suero antilinfocitario.
- A61P35/00 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › Agentes antineoplásicos.
- C07K16/28 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 16/00 Inmunoglobulinas, p. ej. anticuerpos mono o policlonales. › contra receptores, antígenos celulares de superficie o determinantes celulares de superficie.
- C12N15/13 C […] › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › C12N 15/00 Técnicas de mutación o de ingeniería genética; ADN o ARN relacionado con la ingeniería genética, vectores, p. ej. plásmidos, o su aislamiento, su preparación o su purificación; Utilización de huéspedes para ello (mutantes o microorganismos modificados por ingeniería genética C12N 1/00, C12N 5/00, C12N 7/00; nuevas plantas en sí A01H; reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00; nuevas razas animales en sí A01K 67/00; utilización de preparaciones medicinales que contienen material genético que es introducido en células del cuerpo humano para tratar enfermedades genéticas, terapia génica A61K 48/00; péptidos en general C07K). › Inmunoglobulinas.
- C12N15/85 C12N 15/00 […] › para células animales.
- C12N5/10 C12N […] › C12N 5/00 Células no diferenciadas humanas, animales o vegetales, p. ej. líneas celulares; Tejidos; Su cultivo o conservación; Medios de cultivo para este fin (reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00). › Células modificadas por introducción de material genético extraño, p. ej. células transformadas por virus.
Clasificación antigua:
- A61K31/7088 A61K 31/00 […] › Compuestos que tienen al menos tres nucleósidos o nucleótidos.
- A61K39/395 A61K 39/00 […] › Anticuerpos (aglutininas A61K 38/36 ); Inmunoglobulinas; Inmunosuero, p. ej. suero antilinfocitario.
- A61P35/00 A61P […] › Agentes antineoplásicos.
- C07K16/28 C07K 16/00 […] › contra receptores, antígenos celulares de superficie o determinantes celulares de superficie.
- C12N15/13 C12N 15/00 […] › Inmunoglobulinas.
- C12N15/85 C12N 15/00 […] › para células animales.
- C12N5/10 C12N 5/00 […] › Células modificadas por introducción de material genético extraño, p. ej. células transformadas por virus.
Fragmento de la descripción:
Anticuerpos específicos de CD22 humana y sus usos terapéuticos y diagnósticos.
La presente invención se refiere a una molécula de anticuerpo que tiene especificidad para los determinantes antigénicos del antígeno de los linfocitos B, CD22. La presente invención se refiere también a los usos terapéuticos de la molécula de anticuerpo y a métodos para producir la molécula de anticuerpo.
En una molécula de un anticuerpo natural, hay dos cadenas pesadas y dos cadenas ligeras. Cada cadena pesada y cada cadena ligera tienen en su extremo N-terminal un dominio variable. Cada dominio variable se compone de cuatro regiones marco (FR) que alternan con tres regiones determinantes de la complementariedad (CDR). Los residuos de los dominios variables se numeran convencionalmente según un sistema creado por Kabat et al. Este sistema está descrito por Kabat et al., 1987, en Sequences of proteins of Immunological Interest, US Department of Health and Human Services, NIH, USA (de aquí en adelante "Kabat et al. (cita anterior)"). Este sistema de numeración se usa en la presente memoria descriptiva excepto cuando se indica otra cosa.
Las designaciones de los residuos de Kabat no siempre se corresponden directamente con la numeración lineal de los residuos de aminoácidos. La secuencia lineal real de aminoácidos puede contener menos aminoácidos o aminoácidos adicionales que los de la numeración estricta de Kabat que corresponde a un acortamiento de un componente estructural o a una inserción en un componente estructural, ya sea marco o CDR, de la estructura del dominio variable básico. La numeración correcta de Kabat de los residuos se puede determinar para un anticuerpo dado por alineamiento de los residuos de homología en la secuencia del anticuerpo con una secuencia "estándar" numerada según Kabat.
Las CDR del dominio variable de cadena pesada están localizadas en los residuos 31-35 (CDR-H1), residuos 50-65 (CDR-H2) y residuos 95-102 (CDR-H3) según la numeración de Kabat.
Las CDR del dominio variable de cadena ligera están localizadas en los residuos 24-34 (CDR-L1), residuos 50-56 (CDR-L2) y residuos 89-97 (CDR-L3) según la numeración de Kabat.
La construcción de anticuerpos injertados con CDR se describe en la solicitud de patente europea EP-A-0239400, que describe un procedimiento en el que las CDR de un anticuerpo monoclonal de ratón se injertan en las regiones marco de los dominios variables de una inmunoglobulina humana mediante mutagénesis dirigida al sitio utilizando oligonucleótidos largos. Las CDR determinan la especificidad de unión al antígeno de los anticuerpos y son secuencias peptídicas relativamente cortas mantenidas sobre las regiones marco de los dominios variables.
El primer trabajo sobre anticuerpos monoclonales humanizados por injertos de CDR se llevó a cabo sobre anticuerpos monoclonales que reconocen antígenos sintéticos, tales como NP. Sin embargo, ejemplos en los que un anticuerpo monoclonal de ratón que reconoce la lisozima y un anticuerpo monoclonal de rata que reconoce un antígeno sobre las células T humanas fueron humanizados por injertos de CDR, han sido descritos por Verhoeyen et al. (Science, 239, 1534-1536, 1988) y Riechmann et al. (Nature, 332, 323-324, 1988), respectivamente.
Riechmann et al., encontraron que la transferencia de las CDR solas (como han sido definidas por Kabat (Kabat et al. (cita anterior) y Wu et al., J. Exp. Med., 132, 211-250, 1970)) no fue suficiente para proporcionar una actividad satisfactoria de unión al antígeno en el producto injertado con CDR. Se encontró que muchos residuos marco tenían que ser alterados para que se correspondieran con los de la región marco del donante. Los criterios propuestos para seleccionar qué residuos marco necesitan ser alterados están descritos en la solicitud de patente internacional No. WO 90/07861.
Se han publicado una serie de reseñas que exponen los anticuerpos injertados con CDR, incluyendo Vaughan et al. (Nature Biotechnology, 16, 535-539, 1998).
Los linfomas malignos son un grupo diverso de neoplasmas. La mayoría de los casos aparecen en personas ancianas. El linfoma no Hodgkin (NHL) es una enfermedad que normalmente afecta de 200.000 a 250.000 pacientes en los Estados Unidos. Es el segundo cáncer que aumenta más rápidamente en los Estados Unidos, aumentando a una tasa de aproximadamente 55.000 nuevos casos por año. La incidencia aumenta a una velocidad que es mayor que la que se puede atribuir simplemente al aumento de la edad de la población y a la exposición a factores de riesgo conocidos.
La clasificación del linfoma es compleja, y ha evolucionado en las recientes décadas. En 1994 se introdujo la clasificación revisada de linfomas europeo-americanos (REAL). Esta clasificación organiza los linfomas de células B (el identificado más frecuentemente), de células T y de origen inclasificable en subtipos acordados. En la práctica diaria, el agrupamiento de los NHL en categorías de grado bajo, intermedio y grado alto basándose en su apariencia histológica general, refleja en líneas generales su comportamiento clínico.
El NHL afecta predominantemente a los nódulos linfáticos pero, en pacientes individuales, el tumor puede implicar otros sitios anatómicos tales como el hígado, bazo, médula ósea, pulmones, intestino y piel. La enfermedad comúnmente se presenta como un alargamiento indoloro de los nódulos linfáticos. El linfoma extranodural afecta con la mayor frecuencia al intestino, aunque ha sido documentado el linfoma primario virtualmente de cada órgano. Los síntomas sistémicos incluyen fiebre, sudores, cansancio y pérdida de peso.
Hasta recientemente, el sistema de clasificación de Ann Arbor, basado enteramente en la extensión anatómica de la enfermedad, ha sido el principal determinante de la terapia en el NHL. Esta información puede ser mejorada incorporando indicadores adicionales de pronóstico, incluyendo la edad, los niveles de lactato-deshidrogenasa sérica y el estado general. Aún así, el conocimiento del sistema de clasificación de Ann Arbor, junto con el subtipo histológico e inmunológico del tumor, es todavía el principal determinante del tratamiento.
El NHL de grado bajo tiene un curso poco activo, con una supervivencia media del paciente de 8 a 10 años. La supervivencia se ve poco impactada por la terapia actualmente disponible, aunque la irradiación de la enfermedad local y la quimioterapia para los síntomas sistémicos mejoran la calidad de vida de los pacientes. La quimioterapia de combinación se puede reservar para la enfermedad recurrente. La enfermedad intermedia y, especialmente, la enfermedad de grado alto es extremadamente agresiva y tiende a diseminarse. La enfermedad de este grado requiere tratamiento urgente. La radioterapia puede ser un componente útil de tratamiento en pacientes con una enfermedad muy masiva. Se han empleado muchos regímenes diferentes de quimioterapia, y se puede obtener una supervivencia a largo plazo libre de la enfermedad en más de la mitad de los pacientes. La terapia de dosis altas con soporte de células madre se introdujo inicialmente para los pacientes con enfermedad recurrente o refractaria, pero ahora está encontrando, cada vez más, un lugar en la terapia de primera línea para los pacientes con enfermedad de poco riesgo. La tendencia en los últimos años hacia una estrategia terapéutica cada vez más agresiva debe ser sopesada frente a la edad generalmente elevada y la debilidad relativa de muchos pacientes con NHL, y por la necesidad de combinar la toxicidad del tratamiento con el diagnóstico individual de la enfermedad de cada paciente.
Se necesitan mejores tratamientos, que sean más eficaces y mejor tolerados. Los agentes recientemente introducidos incluyen nuevos fármacos citotóxicos, incorporados progresivamente en combinaciones, y la introducción de terapias basadas en anticuerpos.
El linfoma no Hodgkin engloba un conjunto de linfomas de células B. Los antígenos de las células B representan por tanto dianas adecuadas para la terapia con anticuerpos.
El CD22 es una glicoproteína de membrana de 135 kDa que pertenece a una familia de proteínas de unión al ácido siálico llamadas sialoadhesinas. Se detecta en el citoplasma de modo temprano en el desarrollo de las células B, aparece en la superficie celular simultáneamente con la IgD y se encuentra en la mayor parte de las células B maduras. La expresión aumenta después de la activación de las células B. El CD22 se pierde con la diferenciación terminal...
Reivindicaciones:
1. Una molécula de anticuerpo que tiene especificidad para el CD22 humano, que comprende una cadena pesada en la que el dominio variable comprende la SEQ ID NO: 1 para CDR-H1, la secuencia GINPGNNYATYRRKFQG de gH7 de la Figura 6 o la SEQ ID NO: 2 o la SEQ ID NO: 13 o la SEQ ID NO: 15 o la SEQ ID NO: 16 para CDR-H2, y la SEQ ID NO: 3 para CDR-H3, y una cadena ligera en la que el dominio variable comprende la SEQ ID NO: 4 para CDR-L1, la SEQ ID NO: 5 para CDR-L2 y la SEQ ID NO: 6 para CDR-L3.
2. La molécula de anticuerpo según la reivindicación 1, que comprende la secuencia GINPGNNYATYRRKFQG de gH7 de la Figura 6 para CDR-H2.
3. La molécula de anticuerpo de una cualquiera de las reivindicaciones 1 a 2, que es una molécula de anticuerpo injertada con CDR.
4. La molécula de anticuerpo de la reivindicación 3, en la que el dominio variable comprende regiones marco del aceptor humano y las CDR del donante no humano.
5. La molécula de anticuerpo de la reivindicación 4, en la que las regiones marco del aceptor humano del dominio variable de la cadena pesada se basan en las SEQ ID NOs: 21 y 22 y comprenden residuos del donante en las posiciones 1, 28, 48, 71 y 93, numeradas según Kabat, que corresponden a los residuos 1, 28, 48, 72 y 97, respectivamente, en la SEQ ID NO: 8.
6. La molécula de anticuerpo de la reivindicación 5, que comprende adicionalmente residuos del donante en las posiciones 67 y 69, numeradas según Kabat, que corresponden a los residuos 68 y 70, respectivamente, en la SEQ ID NO: 8.
7. La molécula de anticuerpo de una cualquiera de las reivindicaciones 4 a 6, en la que las regiones marco del aceptor humano del dominio variable de la cadena ligera se basan en las SEQ ID NOs: 17 y 18 y comprenden residuos del donante en las posiciones 2, 4, 37, 38, 45 y 60, numeradas según Kabat, que corresponden a los residuos 2, 4, 42, 43, 50 y 65, respectivamente, en la SEQ ID NO: 7.
8. La molécula de anticuerpo de la reivindicación 7, que comprende adicionalmente un residuo del donante en la posición 3, numerada según Kabat, que corresponde al residuo en dicha posición en la SEQ ID NO: 7.
9. Una molécula de anticuerpo que tiene especificidad para el CD22 humano, que comprende una cadena pesada según la reivindicación 5 o la reivindicación 6, y una cadena ligera según la reivindicación 7 o la reivindicación 8.
10. La molécula de anticuerpo de una cualquiera de las reivindicaciones 1 a 9, que comprende la SEQ ID NO: 19 (la región variable de cadena ligera 5/44-gL1) y la SEQ ID NO: 27 (la región variable de cadena pesada 5/44-gH7).
11. Una molécula de anticuerpo que tiene especificidad para el CD22 humano, que tiene una cadena ligera que comprende la secuencia dada en la SEQ ID NO: 28 y una cadena pesada que comprende la secuencia dada en la SEQ ID NO: 30.
12. Una molécula de anticuerpo que tiene especificidad para el CD22 humano, que tiene una cadena ligera que consiste en la secuencia dada en la SEQ ID NO:28 y una cadena pesada que consiste en la secuencia dada en la SEQ ID NO: 30.
13. El anticuerpo de la reivindicación 1, que es un anticuerpo monoclonal anti-CD22 murino 5/44, en el que el dominio variable de la cadena ligera tiene la secuencia dada en la SEQ ID NO: 7 y el dominio variable de la cadena pesada tiene la secuencia dada en la SEQ ID NO: 8.
14. La molécula de anticuerpo de la reivindicación 1, que es una molécula de anticuerpo quimérico que comprende las secuencias de los dominios variables de la cadena ligera y de la cadena pesada del anticuerpo monoclonal de la reivindicación 18, citados en la SEQ ID NO: 7 y en la SEQ ID NO: 8 respectivamente.
15. Una secuencia de ADN que codifica la cadena pesada de una molécula de anticuerpo según una cualquiera de las reivindicaciones 1 a 14.
16. Una secuencia de ADN que codifica la cadena ligera de una molécula de anticuerpo según una cualquiera de las reivindicaciones 1 a 14.
17. Una secuencia de ADN que codifica la cadena pesada y la cadena ligera de una molécula de anticuerpo según una cualquiera de las reivindicaciones 1 a 14.
18. Un vector de clonación o de expresión que comprende una secuencia de ADN según una cualquiera de las reivindicaciones 15 a 17.
19. Una célula hospedante que comprende un vector de clonación o de expresión según la reivindicación 18.
20. La molécula de anticuerpo de una cualquiera de las reivindicaciones 1 a 14, o una secuencia de ADN según una cualquiera de las reivindicaciones 15 a 17, para uso en terapia.
21. La molécula de anticuerpo de una cualquiera de las reivindicaciones 1 a 14 o 20, que tiene especificidad para el CD22 humano, o una secuencia de ADN según una cualquiera de las reivindicaciones 15 a 17 o 20, para uso en el tratamiento de una patología mediada por células que expresan CD22.
22. La molécula de anticuerpo de una cualquiera de las reivindicaciones 1 a 14, 20 o 21, o una secuencia de ADN según una cualquiera de las reivindicaciones 15 a 17, 20 o 21, para uso en el tratamiento de un linfoma maligno.
23. La molécula de anticuerpo o la secuencia de ADN de la reivindicación 22, en la que el linfoma maligno es linfoma no Hodgkin.
24. El uso de la molécula de anticuerpo de una cualquiera de las reivindicaciones 1 a 14, que tiene especificidad para el CD22 humano, o el uso de una secuencia de ADN según una cualquiera de las reivindicaciones 15 a 17, en la fabricación de un medicamento para el tratamiento de una patología mediada por células que expresan CD22.
25. El uso de la reivindicación 24, en el que la patología es un linfoma maligno.
26. El uso de la reivindicación 25, en el que el linfoma maligno es un linfoma no Hodgkin.
27. Una composición terapéutica o para diagnóstico, que comprende la molécula de anticuerpo de una cualquiera de las reivindicaciones 1 a 14, o la secuencia de ADN de una cualquiera de las reivindicaciones 15 a 17.
28. Una composición terapéutica o para diagnóstico según la reivindicación 27, que comprende un excipiente, diluyente o vehículo farmacéuticamente aceptable.
29. Una composición terapéutica o para diagnóstico según la reivindicación 27 o la reivindicación 28, que comprende adicionalmente anticuerpos anti-células T, anti-IFN? o anti-LPS, o ingredientes no anticuerpos tales como las xantinas.
30. Un procedimiento para la producción de una molécula de anticuerpo según una cualquiera de las reivindicaciones 1 a 14, que comprende el cultivo de una célula hospedante según la reivindicación 19, en condiciones adecuadas para llevar a la expresión de una proteína a partir de ADN que codifica dicha molécula de anticuerpo y al aislamiento de dicha molécula de anticuerpo.
31. Un procedimiento para la preparación de una composición terapéutica o para diagnóstico según una cualquiera de las reivindicaciones 27 a 29, que comprende la mezcla de una molécula de anticuerpo según una cualquiera de las reivindicaciones 1 a 14, junto con un excipiente, diluyente o vehículo farmacéuticamente aceptable.
Patentes similares o relacionadas:
UTILIZACIÓN DE ANTÍGENOS A33 Y JAM-IT, del 10 de Febrero de 2012, de GENENTECH, INC.: Polipéptido para utilizar en el tratamiento de una enfermedad inflamatoria asociada con la sobreexpresión de STlgMA, en el que el polipéptido comprende […]
ANTICUERPOS CONTRA PD-1 Y SUS USOS, del 3 de Noviembre de 2011, de WYETH LLC MEDIMMUNE LIMITED: Un anticuerpo aislado o uno de sus fragmentos de unión al antígeno que comprende: Un dominio VH que comprende 3 CDRs; y un dominio VL que comprende 3 CDRs; […]
ANTICUERPOS ANTI-CD19 CON INMUNOGENICIDAD REDUCIDA, del 21 de Septiembre de 2011, de MERCK PATENT GMBH: Anticuerpo anti-CD19 diseñado y modificado derivado de anticuerpo B4 murino anti-CD19 caracterizado por la región variable de cadena pesada de […]
MOLÉCULAS DE ENLACE DE LINGO Y EL USO FARMACÉUTICO DE ESTAS, del 10 de Agosto de 2011, de NOVARTIS AG: Una molécula de enlace que es capaz de unirse a la proteína de acuerdo con la SEQ ID NO:1, SEQ ID NO: 2, o SEQ ID NO: 3, con una constante de disociación <1000nM, […]
ANTICUERPOS FRENTE A MAdCAM, del 11 de Julio de 2011, de PFIZER INC. AMGEN FREMONT INC: Una línea celular de hibridoma que produce un anticuerpo monoclonal humano que se une específicamente a la molécula de adhesión de Célula Mucosa […]
 ANTICUERPOS QUE SE UNEN A RECEPTORES KIR2DL1, -2, -3 PERO NO A KIR2DS4 Y SU USO TERAPÉUTICO, del 6 de Junio de 2011, de NOVO NORDISK A/S Innate Pharma University of Genoa: Un anticuerpo humano o humanizado aislado, que se une a cada uno de receptores asesinos similares a Ig (KIR) 2DL1, KIR2DL2 y KIR2DL3, pero que no se une a KIR2DS4, […]
ANTICUERPOS QUE SE UNEN A RECEPTORES KIR2DL1, -2, -3 PERO NO A KIR2DS4 Y SU USO TERAPÉUTICO, del 6 de Junio de 2011, de NOVO NORDISK A/S Innate Pharma University of Genoa: Un anticuerpo humano o humanizado aislado, que se une a cada uno de receptores asesinos similares a Ig (KIR) 2DL1, KIR2DL2 y KIR2DL3, pero que no se une a KIR2DS4, […]
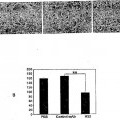 MOLÉCULAS INHIBIDORAS DE LA ANGIOGÉNESIS Y SU USO EN EL TRATAMIENTO Y DIAGNÓSTICO DEL CÁNCER, del 16 de Mayo de 2011, de MERCK SERONO SA: Una molécula que inhibe la angiogénesis, que se selecciona del grupo que consiste en el anticuerpo H33, producido por el hibridoma 13H33 según está depositado en el Deutsche […]
MOLÉCULAS INHIBIDORAS DE LA ANGIOGÉNESIS Y SU USO EN EL TRATAMIENTO Y DIAGNÓSTICO DEL CÁNCER, del 16 de Mayo de 2011, de MERCK SERONO SA: Una molécula que inhibe la angiogénesis, que se selecciona del grupo que consiste en el anticuerpo H33, producido por el hibridoma 13H33 según está depositado en el Deutsche […]
 ELEMENTOS DE UNIÓN A CD-3 DESINMUNIZADOS MULTIESPECÍFICOS, del 10 de Mayo de 2011, de MICROMET AG: Una construcción de unión específica a CD3 citotóxicamente activa que comprende un primer dominio que se une específicamente a CD3 humano […]
ELEMENTOS DE UNIÓN A CD-3 DESINMUNIZADOS MULTIESPECÍFICOS, del 10 de Mayo de 2011, de MICROMET AG: Una construcción de unión específica a CD3 citotóxicamente activa que comprende un primer dominio que se une específicamente a CD3 humano […]