ANIMAL TRANSGENICO QUE EXPRESA UNA FORMA MULTI-MUTADA DE LA PRESENILINA 1.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/FR00/02623.
Solicitante: AVENTIS PHARMA S.A..
Nacionalidad solicitante: Francia.
Dirección: 20, AVENUE RAYMOND ARON,92160 ANTONY.
Inventor/es: MULLER, WALTER, ECKERT,ANNE, CZECH,CHRISTIAN, PRADIER,LAURENT, TREMP,GUNTER.
Fecha de Publicación: .
Fecha Concesión Europea: 14 de Abril de 2010.
Clasificación Internacional de Patentes:
- A01K67/027M
- A01K67/027M4
- C07K14/47A3
Clasificación PCT:
- A01K67/027 NECESIDADES CORRIENTES DE LA VIDA. › A01 AGRICULTURA; SILVICULTURA; CRIA; CAZA; CAPTURA; PESCA. › A01K CRÍA DE ANIMALES; AVICULTURA; APICULTURA; PISCICULTURA; PESCA; ANIMALES PARA CRIA O REPRODUCCIÓN, NO PREVISTOS EN OTRO LUGAR; NUEVAS VARIEDADES DE ANIMALES. › A01K 67/00 Cría u obtención de animales, no prevista en otro lugar; Nuevas razas de animales. › Nuevas razas de vertebrados.
- A61K49/00 A […] › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › Preparaciones para examen in vivo.
- C07K14/47 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 14/00 Péptidos con más de 20 aminoácidos; Gastrinas; Somatostatinas; Melanotropinas; Sus derivados. › de mamíferos.
- C12N5/10 C […] › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › C12N 5/00 Células no diferenciadas humanas, animales o vegetales, p. ej. líneas celulares; Tejidos; Su cultivo o conservación; Medios de cultivo para este fin (reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00). › Células modificadas por introducción de material genético extraño, p. ej. células transformadas por virus.
- G01N33/50 FISICA. › G01 METROLOGIA; ENSAYOS. › G01N INVESTIGACION O ANALISIS DE MATERIALES POR DETERMINACION DE SUS PROPIEDADES QUIMICAS O FISICAS (procedimientos de medida, de investigación o de análisis diferentes de los ensayos inmunológicos, en los que intervienen enzimas o microorganismos C12M, C12Q). › G01N 33/00 Investigación o análisis de materiales por métodos específicos no cubiertos por los grupos G01N 1/00 - G01N 31/00. › Análisis químico de material biológico, p. ej. de sangre o de orina; Ensayos mediante métodos en los que interviene la formación de uniones bioespecíficas con grupos coordinadores; Ensayos inmunológicos (procedimientos de medida o ensayos diferentes de los procedimientos inmunológicos en los que intervienen enzimas o microorganismos, composiciones o papeles reactivos a este efecto, procedimientos para preparar estas composiciones, procedimientos de control sensibles a las condiciones del medio en los procedimientos microbiológicos o enzimáticos C12Q).
Clasificación antigua:
- A01K67/027 A01K 67/00 […] › Nuevas razas de vertebrados.
- A61K49/00 A61K […] › Preparaciones para examen in vivo.
- C07K14/47 C07K 14/00 […] › de mamíferos.
- C12N5/10 C12N 5/00 […] › Células modificadas por introducción de material genético extraño, p. ej. células transformadas por virus.
- G01N33/50 G01N 33/00 […] › Análisis químico de material biológico, p. ej. de sangre o de orina; Ensayos mediante métodos en los que interviene la formación de uniones bioespecíficas con grupos coordinadores; Ensayos inmunológicos (procedimientos de medida o ensayos diferentes de los procedimientos inmunológicos en los que intervienen enzimas o microorganismos, composiciones o papeles reactivos a este efecto, procedimientos para preparar estas composiciones, procedimientos de control sensibles a las condiciones del medio en los procedimientos microbiológicos o enzimáticos C12Q).
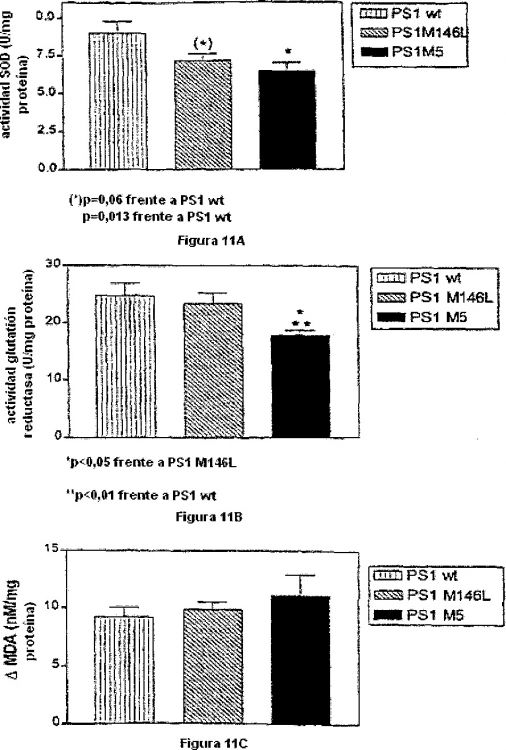
Fragmento de la descripción:
Animal transgénico que expresa una forma multi-mutada de la presenilina 1.
La presente invención se refiere al campo de los modelos animales transgénicos y más particularmente, a los modelos animales de la enfermedad de Alzheimer. La invención se refiere a un animal transgénico no humano que expresa una forma de la presenilina 1 que porta al menos cinco mutaciones entre las mutaciones de la presenilina 1 identificadas en las formas familiares de la enfermedad de Alzheimer y que presenta una susceptibilidad incrementada a la apoptosis. Dicho animal permite detectar un fenómeno apoptótico en un tejido periférico renovable.
La enfermedad de Alzheimer (AD) es una enfermedad neurodegenerativa progresiva que afecta a una gran proporción de la población de edad avanzada. Esta enfermedad se caracteriza en el plano clínico por una pérdida de la memoria y un declive de las funciones cognitivas, y en el plano neuropatológico por la presencia en el cerebro de depósitos neurofibrilares intracelulares y depósitos extracelulares del péptido ß-amiloide (Aß) que forma las placas amiloides (Yanker et al., 1996) así como una pérdida neuronal pronunciada. A estos signos se añade un número importante de otros cambios anormales que incluyen una alteración de los mecanismos de protección contra los radicales libres.
Las placas amiloides están compuestas mayoritariamente por los péptidos Aß con 40 ó 42 restos que se generan durante el proceso proteolítico de la proteína precursora del péptido ß-amiloide (APP). Los depósitos extracelulares de Aß son muy específicos de AD y de los trastornos asociados. Representan la característica precoz e invariable de todas las formas de AD, que incluyen las formas familiares (FAD). Las FAD aparecen de manera relativamente precoz (entre 40 y 60 años) y se deben a mutaciones en el gen de APP en el 5% de los casos de FAD con seis mutaciones con errores de interpretación, simples o dobles identificadas; en el gen de la presenilina 1 (PS 1) en el 50 a 70% de los casos de FAD con más de 40 mutaciones diferentes identificadas hasta este momento; y en el gen de la presenilina 2 (PS 2) en los casos más raros de FAD con 2 mutaciones con errores de interpretación descritas (para revisión véase Price y Sisodia, 1998). Las mutaciones en estos tres genes se han demostrado como inductoras de cambios en la proteolisis de APP, que conducen a una superproducción de Aß, especialmente de la forma larga Aß42, y a la aparición precoz de la patología y de los síntomas similares a los de las formas esporádicas de AD.
En los modelos animales transgénicos descritos hasta este momento la sintomatología de la pérdida neuronal comparable a AD se expresa únicamente a nivel de las neuronas o en su entorno directo y en particular el fenómeno de apoptosis (Chiu et al., 1999). Sin embargo, estos modelos presentan varios inconvenientes como principalmente la necesidad de criar un gran número de animales generalmente durante periodos de tiempo largos, que pueden ir hasta 24 meses, con el fin de seguir la aparición de los síntomas de AD, el sacrificio sistemático de los animales para el estudio de la patología y así los protocolos experimentales son particularmente laboriosos y costosos.
La solicitud de patente WO98/51781 describe animales cuya PS1 sólo porta una mutación (véase el ejemplo 8).
Otra solicitud de patente - WO98/17782- describe un ratón que expresa una PS1 que sólo porta una mutación M146L y que expresa una APP que porta la mutación Swedish.
El resumen publicado por ZAMAN et al (SOCIETY FOR NEUROSCIENCE ABSTRACTS, vol. 24, no. 1-2, 1998, página 471) se refiere a la creación de ratones que sobreexpresan una PS1 que porta la mutación A246E o una deleción del exón 9.
Los resúmenes publicados en nombre de ECKERT et al (SOCIETY FOR NEUROSCIENCE ABSTRACTS, vol. 25, no. 1-2, 1999, página 1846) y de LEUTNER S ET AL (SOCIETY FOR NEUROSCIENCE ABSTRACTS, vol. 25, no. 1-2, 1999, página 1857) no identifican las mutaciones en PS1 y no es posible por lo tanto deducir el número de mutaciones.
El artículo de CZECH et al (NEUROSCIENCE, vol. 87, no. 2, noviembre 1998 (1998-11), páginas 325-336) describe ratas transgénicas. Pero estas ratas portan la PS no mutada. En efecto, parece claramente con la lectura de este documento, en particular página 327, que la proteína expresada es la PS1 salvaje y no un mutante de esta proteína.
El artículo de LAMB et al (NAT. NEUROSCI., vol. 2, no. 8, agosto 1999 (1999-08), páginas 695-697) describe animales doble mutantes H163R y M146L.
La presente invención resulta por lo tanto de la investigación de un nuevo modelo animal representativo de la neuropatología que permite medir los síntomas asociados a AD y en particular la apoptosis, en los tejidos periféricos.
Un primer objeto de la invención se refiere por lo tanto a un animal transgénico no humano que expresa una forma de la presenilina 1 que porta al menos cinco mutaciones entre las mutaciones de la presenilina 1 identificadas en las formas familiares de la enfermedad de Alzheimer y que presenta una susceptibilidad incrementada a la apoptosis.
Dicho animal puede servir de modelo de animal transgénico de la enfermedad de alzheimer.
Se entiende por animal transgénico cualquier animal no humano que presenta una modificación de su genoma. La modificación del genoma puede resultar de una alteración o una modificación de uno o varios genes por "knock-in" o por "knock-out". Esta modificación puede deberse a la acción de agentes alterantes o mutágenos clásicos o bien se efectúa por mutagénesis dirigida, como la descrita en Materiales y Métodos.
La modificación del genoma puede resultar igualmente de una inserción de un gen o genes o del reemplazamiento de un gen o genes en su forma salvaje o mutada.
Las modificaciones del genoma se efectúan ventajosamente sobre las células madre reproductoras y preferentemente sobre los pronúcleos.
En el marco de la presente invención, el modelo animal es ventajosamente un mamífero no humano. En particular puede tratarse de un ratón, de una rata o de un conejo obtenido según las técnicas clásicas de la transgénesis. A título de ejemplo que ilustra uno de los procedimientos de transgénesis, se puede citar el método de microinyección de un casete de expresión que comprende los genes modificados en los dos pronúcleos fecundados, tal como el descrito en Materiales y Métodos.
A este respecto, el modelo animal de la invención se obtiene por inyección de un casete de expresión que comprende un ácido nucleico. De manera preferente, este ácido nucleico es un ADN que puede ser un ADN genómico (ADNg) o un ADN complementario (ADNc).
En el marco del modelo de la invención, el ADN codifica cualquier gen de la PS1 de manera que las células del modelo animal que expresa la proteína multi-mutada, portan al menos cinco mutaciones entre las mutaciones de la PS1 identificadas en las formas familiares de la enfermedad de alzheimer. La secuencia de la proteína PS1 humana no mutada ha sido descrita por Sherrington et al en 1995. Se entiende por proteína multi-mutada, la proteína PS1 que comprende al menos cinco mutaciones combinadas o asociadas entre sí, es decir, presentes al mismo tiempo en dicha proteína. Según un modo preferido de la invención, el ADN codifica el gen de la PS1 que contiene 5 mutaciones (PS1M5).
Las mutaciones en el gen de PS1 pueden ser una de las 40 mutaciones descritas hasta este momento en la bibliografía. De manera preferente, las mutaciones en el gen de PS1 son M146L, H163R, A246E, L286V, C410Y, I143T, L235P, P264L, P267S, E317G, G384A, L392V, A426P y/o P436S. Están combinadas parcialmente entre sí.
Para la realización de un modelo según la invención, se prefieren las mutaciones M146L, H163R, A246E, L286V, C410Y, combinadas entre sí.
En el marco del modelo de la invención, el ADN se pone bajo el control de secuencias que permiten su expresión y en particular de secuencias promotoras de la transcripción.
A título de secuencias promotoras, se pueden citar muy particularmente el promotor HMG (Gautier et al., 1989), así como el promotor PDGF (Sasahara et al., 1991), el promotor Thy-1 (Lüthi et al., 199) y el promotor del gel del Prión (Scott et al., 1992).
Según una aplicación particularmente interesante de la invención, el modelo animal comprende el gen de la PS1 que tiene las mutaciones M146L, H163R,...
Reivindicaciones:
1. Animal transgénico no humano que expresa una forma de la presenilina 1 que porta al menos cinco mutaciones entre las mutaciones de la presenilina 1 identificadas en las formas familiares de la enfermedad de alzheimer y que presenta una sensibilidad incrementada a la apoptosis.
2. Animal según la reivindicación 1, caracterizado porque las mutaciones en el gen de la PS1 son las mutaciones M146L, H163R, A246E, L286V, C410Y, 1143T, L235P, P264L, P267S, E317G, G384A, L392V, A426P y/o P436S.
3. Animal según una de las reivindicaciones 1 y 2, caracterizado porque las mutaciones en el gen de la PS1 son las mutaciones M146L, H163R, A246E, L286V y C410Y combinadas entre sí.
4. Animal según una de las reivindicaciones 1 a 3, caracterizado porque la expresión de la PS1 se pone bajo el control de un promotor ubicuo.
5. Utilización de un animal según una de las reivindicaciones 1 a 4 para la identificación de compuestos destinados al tratamiento de las enfermedades neurodegenerativas.
6. Utilización de un animal según una de las reivindicaciones 1 a 4 para la identificación de compuestos destinados al tratamiento de la enfermedad de Alzheimer.
7. Célula extraída de un animal según una de las reivindicaciones 1 a 4, expresando dicha célula una forma de la presenilina 1 que porta al menos cinco mutaciones entre las mutaciones de la presenilina 1 identificadas en las formas familiares de la enfermedad de alzheimer y que presenta una sensibilidad incrementada a la apoptosis.
8. Utilización de una célula según la reivindicación 7, para la identificación de compuestos destinados al tratamiento de las enfermedades neurodegenerativas.
9. Utilización de una célula según la reivindicación 7, para la identificación de compuestos destinados al tratamiento de la enfermedad de Alzheimer.
Patentes similares o relacionadas:
PROCEDIMIENTOS Y COMPOSICIONES INMUNOLÓGICAS PARA EL TRATAMIENTO DE LA ENFERMEDAD DE ALZHEIMER, del 23 de Noviembre de 2011, de THE GOVERNING COUNCIL OF THE UNIVERSITY OF TORONTO: Un péptido representado por la fórmula (A)n -- (Th)m -- (B)o -- Abeta -- (C)p en la que cada A, B y C son un resto de aminoácido o una secuencia de restos […]
MÉTODO DE DIAGNÓSTICO IN VITRO DE LA ENFERMEDAD DE ALZHEIMER MEDIANTE UN ANTICUERPO MONOCLONAL, del 8 de Noviembre de 2011, de CONSEJO SUPERIOR DE INVESTIGACIONES CIENTIFICAS: Método de diagnóstico in vitro de la enfermedad de Alzheimer medante un anticuerpo monoclonal. Dicho anticuerpo es capaz de unire al menos a los aminoácidos 12-16 del […]
MODELO TRANSGÉNICO DE LA ENFERMEDAD DE ALZHEIMER, del 2 de Noviembre de 2011, de BioArctic Neuroscience AB: Un ratón transgénico que expresa un transgén que comprende una secuencia de ADN que codifica una Proteína Precursora Amiloide (APP) heteróloga que comprende la mutación […]
COMPOSICIÓN DE PÉPTIDO INMUNOGÉNICO PARA LA PREVENCIÓN Y EL TRATAMIENTO DE LA ENFERMEDAD DE ALZHEIMER, del 6 de Junio de 2011, de UNITED BIOMEDICAL, INC.: Un inmnunógeno del péptido representado por una de las siguientes fórmulas: (A)n-(fragmento N-terminal del péptido Aß1-42)-(B)o-(Th)m-X; o […]
POLIPÉPTIDOS DERIVADOS DE PROTEÍNA PRECURSORA AMILOIDE (APP) Y SUS USOS, del 31 de Marzo de 2011, de THE OPEN UNIVERSITY: Una composición farmacéutica que comprende: (a) un compuesto con la fórmula: X1 es un grupo acilo representado por la fórmula: X2 es H o un grupo acilo representado […]
COMPOSICION DE PÈPTIDO INMUNOGENO PARA LA PREVENCION Y TRATAMIENTO DE LA ENFERMEDAD DE ALZEHIMER, del 20 de Diciembre de 2010, de UNITED BIOMEDICAL, INC.: Un péptido inmunógeno representado por una de las siguientes fórmulas: en donde cada A es independientemente un aminoácido; (A)n-(fragmento N-terminal […]
 ANIMALES TRANSGENICOS QUE PRESENTAN TRANSTORNOS SERIOS ASOCIADOS A LA ENFERMEDAD DE ALZHEIMER, del 26 de Noviembre de 2010, de AVENTIS PHARMA S.A.: Animal no humano que presenta una secuencia de ácidos nucleicos que codifica una proteína presenilina 1 que lleva en el estado homocigoto […]
ANIMALES TRANSGENICOS QUE PRESENTAN TRANSTORNOS SERIOS ASOCIADOS A LA ENFERMEDAD DE ALZHEIMER, del 26 de Noviembre de 2010, de AVENTIS PHARMA S.A.: Animal no humano que presenta una secuencia de ácidos nucleicos que codifica una proteína presenilina 1 que lleva en el estado homocigoto […]
 METODOS PARA LA IDENTIFICACION DE LOS COMPUESTOS INHIBIDORES DE LA LIBERACION DEL PEPTIDO BETA-AMILOIDE (BETAAP), del 21 de Octubre de 2010, de ELAN PHARMACEUTICALS, INC.
THE BRIGHAM AND WOMEN'S HOSPITAL, INC.
ELI LILLY AND COMPANY: Método in vitro para identificar inhibidores de la producción del péptido ß-amiloide (ßAP), comprendiendo dicho método cultivar células de mamífero en un […]
METODOS PARA LA IDENTIFICACION DE LOS COMPUESTOS INHIBIDORES DE LA LIBERACION DEL PEPTIDO BETA-AMILOIDE (BETAAP), del 21 de Octubre de 2010, de ELAN PHARMACEUTICALS, INC.
THE BRIGHAM AND WOMEN'S HOSPITAL, INC.
ELI LILLY AND COMPANY: Método in vitro para identificar inhibidores de la producción del péptido ß-amiloide (ßAP), comprendiendo dicho método cultivar células de mamífero en un […]