Proceso para oxidar heparinas no fracccionadas y detectar la presencia o ausencia de glicoserina en heparina y productos de heparina.
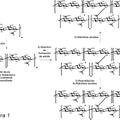
Un compuesto sustancialmente puro que tiene la fórmula: **Fórmula**
Tipo: Patente Europea. Resumen de patente/invención. Número de Solicitud: E10193919.
Solicitante: AVENTIS PHARMA S.A..
Nacionalidad solicitante: Francia.
Dirección: 20, AVENUE RAYMOND ARON 92160 ANTONY FRANCIA.
Inventor/es: MOURIER, PIERRE, VISKOV, CHRISTIAN.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C07H3/06 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07H AZUCARES; SUS DERIVADOS; NUCLEOSIDOS; NUCLEOTIDOS; ACIDOS NUCLEICOS (derivados de ácidos aldónicos o sacáricos C07C, C07D; ácidos aldónicos, ácidos sacáricos C07C 59/105, C07C 59/285; cianohidrinas C07C 255/16; glicales C07D; compuestos de constitución indeterminada C07G; polisacáridos, sus derivados C08B; ADN o ARN concerniente a la ingeniería genética, vectores, p. ej. plásmidos o su aislamiento, preparación o purificación C12N 15/00; industria del azúcar C13). › C07H 3/00 Compuestos que contienen solamente átomos de hidrógeno y radicales sacárido que tienen solamente átomos de carbono, hidrógeno y oxígeno (preparación por hidrólisis de di- o polisácaridos C13; separación o purificación de sucrosa, glucosa, fructosa, lactosa o maltosa C13). › Oligosacáridos, es decir, sacáridos que tienen de tres a cinco radicales sacárido unidos los unos a los otros por enlaces glucosídicos.
- C08B37/00 C […] › C08 COMPUESTOS MACROMOLECULARES ORGANICOS; SU PREPARACION O PRODUCCION QUIMICA; COMPOSICIONES BASADAS EN COMPUESTOS MACROMOLECULARES. › C08B POLISACARIDOS; SUS DERIVADOS (polisacáridos que contienen menos de seis radicales sacáridos unidos entre sí por enlaces glucosídicos C07H; procesos de fermentación o procesos que utilizan enzimas C12P 19/00; producción de celulosa D21). › Preparación de polisacáridos no previstos en los grupos C08B 1/00 - C08B 35/00; Sus derivados (celulosa D21).
- C12Q1/527 C […] › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12Q PROCESOS DE MEDIDA, INVESTIGACION O ANALISIS EN LOS QUE INTERVIENEN ENZIMAS, ÁCIDOS NUCLEICOS O MICROORGANISMOS (ensayos inmunológicos G01N 33/53 ); COMPOSICIONES O PAPELES REACTIVOS PARA ESTE FIN; PROCESOS PARA PREPARAR ESTAS COMPOSICIONES; PROCESOS DE CONTROL SENSIBLES A LAS CONDICIONES DEL MEDIO EN LOS PROCESOS MICROBIOLOGICOS O ENZIMOLOGICOS. › C12Q 1/00 Procesos de medida, investigación o análisis en los que intervienen enzimas, ácidos nucleicos o microorganismos (aparatos de medida, investigación o análisis con medios de medida o detección de las condiciones del medio, p. ej. contadores de colonias, C12M 1/34 ); Composiciones para este fin; Procesos para preparar estas composiciones. › en los que interviene una liasa.
PDF original: ES-2403082_T3.pdf
Fragmento de la descripción:
Proceso para oxidar heparinas no fraccionadas y detectar la presencia o ausencia de glicoserina en heparina y productos de heparina.
En la presente memoria se describe un proceso para oxidar preparaciones de heparina cruda usando al menos una sal de permanganato elegida de permanganato de potasio, permanganato de sodio, y permanganato de amonio cuaternario. Las preparaciones de heparina resultantes carecen relativamente de residuos de glicoserina y son útiles, por ejemplo, para preparar heparinas de bajo peso molecular (LMWH) y heparinas de ultra-bajo peso molecular (ULMWH) que carecen relativamente de residuos de glicoserina. En la presente memoria también se describe un método para detectar la presencia de glicoserina y derivados de glicoserina en preparaciones de heparina y de heparina fragmentada.
Las heparinas son miembros biológicamente activos de la familia glicosaminoglicano y pueden extraerse, por ejemplo, de fuentes bovinas y porcinas. Las heparinas tienen propiedades anticoagulantes y antitrombóticas que las hacen útiles en el tratamiento de trombosis, tales como trombosis arterial y venosa. Como formas aisladas, las moléculas de heparina naturales tienen una alta actividad anticoagulante, que puede dar lugar a hemorragia. Además, las moléculas de heparina son sensibles a factores séricos particulares y, consecuentemente, deben administrarse en dosis altas para proporcionar beneficios antitrombóticos, incrementando en gran medida el riesgo de hemorragia.
Los fragmentos LMWH pueden prepararse por varios procesos a partir de heparina: fraccionamiento mediante disolventes (FR 2.440.376, Pat. U.S. No. 4.692.435) ; fraccionamiento en una resina aniónica (FR 2.453.875) ; filtración en gel (Barrowcliffe, Thromb. Res. 12, 27-36 (1977) ) ; cromatografía de afinidad (Pat. U.S. No. 4.401.758) ; despolimerización controlada mediante un agente químico incluyendo, pero no limitado a, ácido nitroso (EP 14184, EP 37319, EP 76279, EP 623629, FR 2.503.714, Pat. U.S. No. 4.804.652; WO 813276) , beta-eliminación de un éster de heparina (EP 40144, Pat. U.S. No. 5.389.618) , per y odato (EP 287477) , borohidruro de sodio (EP 347588, EP 380943) , ácido ascórbico (Pat. U.S. No. 4.533.549) , peróxido de hidrógeno (Pat. U.S. No. 4.629.699, Pat. U.S. No. 4.791.195) , hidróxido de amonio cuaternario de una sal de amonio cuaternario de heparina (Pat. U.S. No. 4.981.955) , hidróxido de metal alcalino (EP 380943, EP 347588) , por una ruta enzimática (EP 64452, Pat. U.S. No. 4.396.762, EP 244235, EP 244236; Pat. U.S. No. 4.826.827; Pat. U.S. No. 3.766.167) , o mediante irradiación (EP 269981) . Véase también Patente U.S. No. 4.303.651 y Patente U.S. No. 4.757.057. Se indica que las mezclas LMWH resultantes demuestran una actividad antitrombótica más alta, debido a una alta actividad anti-factor Xa (aXa) y una menor actividad anti-factor IIa (alla) , que la heparina no fraccionada, y frecuentemente son mezclas más deseables para la administración a un paciente que necesita tratamiento para trombosis.
Cada fabricante de LMWH de un producto aprobado utiliza un proceso distinto de despolimerización. A no ser que dos fabricantes usen el mismo proceso, esta distinción en el proceso resulta en LMWH con estructuras químicas distintas y, por lo tanto, diferente actividad farmacológica y diferentes indicaciones aprobadas para uso clínico.
Por lo tanto, las LMWH se diferencian estructuralmente por los procesos de despolimerización usados para su fabricación (R.J. Linhardt, et al, Seminars in Thombosis and Hemostatis 1999; 25 (3 Sup.) : 5-16) . Como resultado, las LMWH son más heterogéneas que la heparina. Cada proceso diferente causa modificaciones estructurales únicas y altamente complejas en las cadenas de polisacárido. Estas modificaciones incluyen diferencias en las longitudes de las cadenas y secuencias de las cadenas, así como huellas estructurales. Consecuentemente, cada una de las diferentes LMWH comerciales tienen perfiles farmacológicos distintos y diferentes indicaciones clínicas aprobadas.
Durante el proceso para preparar enoxaparina sódica, vendida con la marca registrada Lovenox® en los EEUU y Clexane® en otros países, a partir de heparina pura, el proceso de despolimerización alcalina en fase acuosa produce una conversión parcial pero característica de las glucosaminas de los extremos reductores de las cadenas de oligosacárido.
La primera etapa de esta conversión consiste en una epimerización glucosamina ↔ manosamina (T. Toida, et al., J. Carbohydrate Chemistr y , 15 (3) , 351-360 (1996) ) ; la segunda etapa es una 6-O-desulfuración de la glucosamina, dando lugar a la formación de derivados llamados "1, 6 anhidro" (Solicitud de patente internacional WO 01/29055) .
Este tipo de derivado se obtiene para cadenas de oligosacárido cuya glucosamina terminal está 6-O-sulfatada.
El porcentaje de cadenas de oligosacárido cuyo extremo está modificado con un enlace 1, 6-anhidro es una característica estructural de la mezcla de oligosacáridos de la enoxaparina sódica Lovenox®. Tomando como base el conocimiento actual, entre 15% y 25% de los componentes de Lovenox® (enoxaparina sódica) tienen una estructura 1, 6-anhidro en el extremo reductor de su cadena.
Recientemente, nuevos procesos para la preparación de fragmentos de heparina que emplean despolimerización en presencia de una base fuerte han rendido heparinas de ultra-bajo peso molecular que tienen un peso molecular promedio en peso que varía de aproximadamente 1.500 a aproximadamente 3.000 Daltons (ULMWH) como se describe, por ejemplo, en Solicitud Publicada de Patente U.S. No. 2002- 0055621 A1, incorporada específicamente por referencia en la presente memoria.
Las composiciones de fragmentos LMWH y ULMWH son heterogéneas y contienen fragmentos de heparina individuales de varias longitudes y pesos moleculares.
Tanto la heparina en sí misma como las mezclas de fragmentos de heparina tienen vidas a temperatura ambiente limitadas debido, al menos en parte, a que se vuelven coloridas durante el almacenamiento. Una vez que desarrollan un color, estas composiciones pueden no ser deseables comercialmente para inyección en pacientes. Un proceso que rinda heparina que resista la coloración es por lo tanto altamente deseable por razones comerciales. Dicha heparina resistente a la coloración puede, por supuesto, usarse para preparar LMWH y/o ULMWH resistentes a la coloración por métodos conocidos por los expertos en la técnica. Además, un método para evaluar el potencial de las preparaciones de heparina para colorearse sería útil en la fabricación de heparina, LMWH, y ULMWH.
US 3.135.660 describe un proceso para purificar carbohidratos sulfatados con agentes oxidantes. US 3.174.904 describe un proceso para decolorar carbohidratos sulfatados y GB 766 992 se refiere a un proceso de preparación de heparina decolorada.
En la presente memoria se describe un proceso para preparar heparina que es resistente a la coloración. La heparina resultante puede emplearse posteriormente para producir mezclas LMWH y ULMWH, particularmente mezclas disponibles comercialmente, tales como fraxiparina, fragmina, innohep (o logiparina) , normiflo, embollex (o sandoparina) , fluxum (o minidalton) , clivarina, e hibor, que son resistentes a la coloración. Puede utilizarse la enoxaparina, vendida comercialmente como Lovenox® (enoxaparina sódica) en los EEUU y Clexane® (enoxaparina sódica) en algunos otros países. La enoxaparina está disponible comercialmente en Aventis Pharma S.A. y Aventis Pharmaceuticals, Inc. También se describe un método para monitorizar la tendencia de la heparina y mezclas de fragmentos de heparina a colorearse.
Se describe un proceso para preparar heparina, que usa al menos una sal de permanganato elegida de permanganato de potasio, permanganato de sodio, y permanganato de amonio cuaternario, tal como permanganato de potasio, en un proceso de oxidación de heparina para producir composiciones heparínicas que carecen de glicoserina. Este proceso se describe más adelante. En la presente memoria se describe que si se utiliza al menos una de estas sales de permanganatos, tal como permanganato de potasio, en la etapa de oxidación, puede obtenerse heparina que carece de glicoserina o baja en glicoserina. También se describió que la eliminación de los residuos de glicoserina y/o los derivados de glicoserina de la heparina puede dar lugar a productos con características comerciales mejoradas. Estos productos con glicoserina reducida son incoloros o casi incoloros y muestran una tendencia disminuida a colorearse respecto a los productos preparados con heparina que no se ha oxidado en presencia de permanganato de potasio.
Además, también se describe un método para detectar... [Seguir leyendo]
Patentes similares o relacionadas:
Separación de contaminantes de polisacárido de Streptococcus pneumoniae por manipulación del pH, del 17 de Junio de 2020, de WYETH LLC: Un procedimiento de reducción del contenido de proteínas y preservar el contenido de polisacárido capsular en un caldo de lisado celular complejo de Streptococcus pneumoniae, […]
Compuestos y sus efectos sobre el control del apetito y la sensibilidad a la insulina, del 10 de Junio de 2020, de IMPERIAL COLLEGE INNOVATIONS LIMITED: Un éster de propionato de inulina para su uso en la terapia para la reducción del apetito, ingesta de alimentos y/o ingesta de calorías y/o para mejorar […]
Evaluación de preparaciones de heparina, del 10 de Junio de 2020, de MOMENTA PHARMACEUTICALS, INC: Un procedimiento para identificar si se utilizó un procedimiento que incluye oxidación u oxidación seguido de tratamiento con un ácido para elaborar […]
Composiciones detergentes, del 3 de Junio de 2020, de DuPont Industrial Biosciences USA, LLC: Una composición que comprende un derivado de polisacárido, en donde el derivado de polisacárido comprende un polisacárido sustituido con: a) uno o más grupos de poliamina; […]
Preparación de poli(ésteres de alfa-1,3-glucano) usando anhídridos orgánicos cíclicos, del 3 de Junio de 2020, de DuPont Industrial Biosciences USA, LLC: Una composición que comprende un compuesto de poli(éster de alfa-1,3-glucano) representado por la estructura **(Ver fórmula)** en donde (i) n es al menos […]
 Método de desacetilación de biopolímeros, del 27 de Mayo de 2020, de GALDERMA S.A.: Un método para la desacetilación al menos parcial de un glucosaminoglucano que comprende grupos acetilo, que comprende:
a1) proporcionar un glucosaminoglucano que comprende […]
Método de desacetilación de biopolímeros, del 27 de Mayo de 2020, de GALDERMA S.A.: Un método para la desacetilación al menos parcial de un glucosaminoglucano que comprende grupos acetilo, que comprende:
a1) proporcionar un glucosaminoglucano que comprende […]
Reticulante de carbohidratos, del 6 de Mayo de 2020, de GALDERMA S.A.: Un producto de hidrogel que comprende moléculas de glucosaminoglucano como el polímero hinchable, en donde las moléculas de glucosaminoglucano se reticulan covalentemente […]
Derivados insaturados de polisacáridos, método de preparación y uso de los mismos, del 18 de Marzo de 2020, de Contipro a.s: Derivados insaturados de polisacáridos que comprenden, en su estructura, al menos un heterociclo que tiene un doble enlace en las posiciones 4 y […]