LIGADURA EXTENDIDA DE CADENA LATERAL.
Procedimiento de ligadura de componentes a través de un enlace amida,
comprendiendo dicho procedimiento: poner en contacto un componente de fórmula J1-C(O)SR con un componente de fórmula NH2-CH(XSH)-J2 en condiciones suficientes para formar un producto de ligadura sustituido con tiol que presenta la fórmula J1-C(O)-NH- CH(XSH)-J2, en la que J 1 es un residuo de una primera molécula diana, polímero o superficie; R es un grupo compatible con tioésteres; XSH es una cadena lateral de aminoácido ramificado que presenta un auxiliar tiol extraíble y se selecciona de entre el grupo constituido por un auxiliar ß-mercapto de fórmula -CH(R')-SH y un auxiliar γ-mercapto de fórmula -CH2- CH(R')-SH, en la que R' es un residuo de una cadena lateral de aminoácido distinto de hidrógeno y se selecciona de entre el grupo constituido por: etileno, fenilo, hidroxifenilo, aliltioalquilo, carbamoílo (-C(O)NH 2), carbamoilalquilo, indolilo, hidroxicarbonilo, guanidina alquilo e imidazolilo; y J 2 es un residuo de una segunda molécula diana, polímero o superficie;
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/EP2006/005815.
Solicitante: AMYLIN PHARMACEUTICALS, INC..
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 9360 TOWNE CENTRE DRIVE SAN DIEGO, CA 92121 ESTADOS UNIDOS DE AMERICA.
Inventor/es: BOTTI,PAOLO, TCHERTCHIAN,Sylvie.
Fecha de Publicación: .
Fecha Solicitud PCT: 16 de Junio de 2006.
Clasificación Internacional de Patentes:
- C07K1/02 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 1/00 Procedimientos generales de preparación de péptidos. › en solución.
- C07K1/04 C07K 1/00 […] › sobre soportes.
Clasificación PCT:
- C07K1/04 C07K 1/00 […] › sobre soportes.
Países PCT: Austria, Bélgica, Suiza, Alemania, Dinamarca, España, Francia, Reino Unido, Grecia, Italia, Liechtensein, Luxemburgo, Países Bajos, Suecia, Mónaco, Portugal, Irlanda, Eslovenia, Finlandia, Rumania, Chipre, Lituania, Letonia.
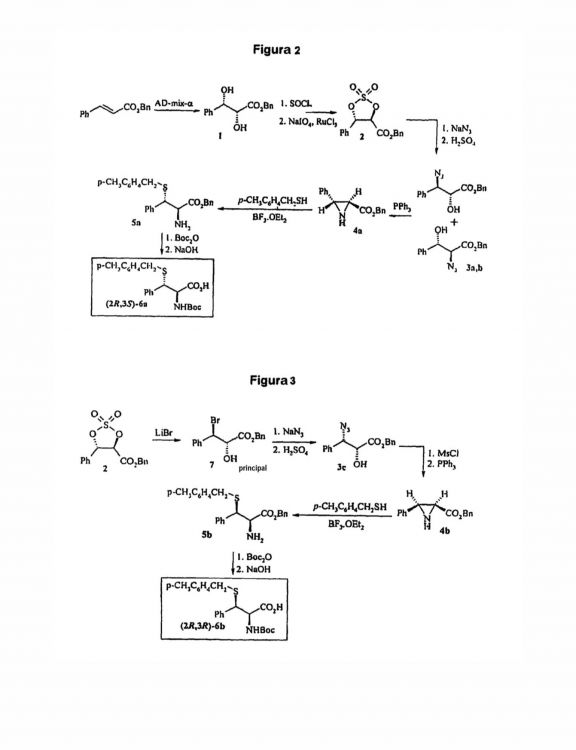
Fragmento de la descripción:
REFERENCIAS CRUZADAS A SOLICITUDES RELACIONADAS
La presente solicitud reivindica prioridad a la solicitud de patente provisional US nº 60/691.396, presentada el 16 de junio de 2005.
ANTECEDENTES DE LA INVENCIÓN 5
La ligadura química implica la formación de un enlace covalente entre un primer componente químico y un segundo componente químico. Los grupos funcionales únicos, mutuamente reactivos, presentes en los primer y segundo componentes, se pueden utilizar para hacer que la reacción de ligadura sea quimioselectiva. Se han utilizado por lo tanto diferentes procedimientos químicos, que comprenden ligadura con formación de amida (Dawson et al, Science 1994, 266, 776-779; Kent et al, documento WO 96/34878; Kent et al, documento WO 98/28434; Botti et al, 10 documento WO 02/20557; y Kent et al, documento WO 02/20034); ligadura química con formación de oxima (Rose et al, J. Amer. Chem. Soc. 1994, 116, 30-34), ligadura con formación de tioéster (Schnölzer et al, Science 1992, 256, 221-225), ligadura con formación de tioéter (Englebretsen et al, Tet. Letts. 1995, 36, 8871-8874), ligadura con formación de hidrazona (Gaertner et al, Bioconj. Chem. 1994, 5, 333-338), ligadura con formación de tiazolidina y ligadura con formación de oxazolidina (Zhang et al, Proc. Natl. Acad. Sci. 1998, 95, 9184-9189; Tam et al, documento WO 95/00846; 15 patente US nº 5.589.356).
La ligadura con formación de amida más utilizada se designa ligadura química nativa ("NCL") (Kent et al, documento WO 96/34878). La ligadura química nativa implica una reacción quimioselectiva entre un primer segmento peptídico o polipeptídico que presenta un resto C-terminal de α-carboxitioéster y un segundo péptido o polipéptido que presenta un residuo N-terminal de cisteína. Una reacción de intercambio tiólico da lugar a un producto intermedio inicial 20 enlazado por tioéster que se reorganiza espontáneamente dando lugar a un enlace amida nativo en el sitio de la ligadura, a la vez que se regenera el diol de la cadena lateral de la cisteína. La ligadura química nativa se ha adaptado a múltiples propósitos, incluyendo la síntesis de polipéptidos y proteínas en fase sólida (Canne et al, documento WO 98/56807; Low et al, documento WO 04/105685), la síntesis de polipéptidos y proteínas de membrana y el acceso general a péptidos difíciles (Kochendoerfer et al, documento WO 00/12536), la síntesis de dominios receptores solubles 25 (Kochendoerfer, G., documento WO 00/53624), la construcción de péptidos y proteínas modificados por polímero (Kochendoerfer et al, documento WO 02/20033), así como modificados para aplicación con grupos protectores solubles en agua (Kochendoerfer et al, documento WO 04/060925), la reducción de las reacciones secundarias (Kochendoerfer et al, documento WO 02/20033; Botti et al, documento WO 04/007661), la expansión de las opciones de los grupos protectores (Kochendoerfer et al, documento WO 02/20033; Villain et al, documento WO 02/098902) y la estimulación de 30 estrategias alternativas de generación de tioéster (Botti et al, documento WO 02/18417; Botti et al, documento WO 03/106615; Miranda et al, documento WO 04/061094; Miranda et al, documento WO 04/011424; Miranda, L., documento WO 04/060863). El principal inconveniente de la técnica original de NCL es que requiere la presencia de una cisteína N-terminal, es decir, que sólo permite la unión de segmentos peptídicos y polipeptídicos que posean una cisteína en el sitio de ligadura. 35
Se ha informado de una ligadura química de formación de amida en posiciones distintas de cisteína. Un procedimiento, denominado ligadura química nativa extendida o ENCL, utiliza el péptido adyacente a un primer péptido que presenta un carboxitioéster C-terminal con un segundo segmento peptídico que presenta un grupo tiol auxiliar amino-sustituido N-terminal que se puede eliminar después de la ligadura (Botti et al, documento WO 02/20557; Botti et al, documento WO 03/042235). Un segundo procedimiento, denominado ligadura química pseudonativa o PNCL, 40 consiste en la reacción entre un péptido de carboxitioéster C-terminal y un segmento peptídico que presenta una cisteína N-terminal (como en el caso de la NCL), seguida por la modificación química del tiol de cadena lateral de la cisteína en el lugar de ligadura a efectos de generar un "pseudoaminoácido" (Kent et al, documento WO 02/20034). Un inconveniente de la ENCL y la PNCL es la variabilidad del rendimiento de reacción en función de los aminoácidos particulares utilizados en el lugar de ligadura. Por ejemplo, como en el caso de la NCL, la ENCL y la PNCL no funcionan 45 demasiado bien en los sitios en los que están presentes aminoácidos β-ramificados.
En consecuencia, existe la necesidad de un sistema de ligadura química de aplicación general y robusto que proporcione alternativas a las técnicas anteriores de ligadura con formación de amida. La presente invención comprende estas y otras necesidades.
BREVE SUMARIO DE LA INVENCIÓN 50
La presente invención se refiere a procedimientos y composiciones para ligaduras químicas extendidas de cadena lateral. Ventajosamente, las reacciones de ligadura tienen velocidades de reacción elevadas y dan lugar a productos de liberación con un rendimiento elevado.
De acuerdo con un aspecto, la presente invención da a conocer un procedimiento de ligadura de componentes a través de un enlace amida. Dicho procedimiento incluye poner en contacto un componente de fórmula J1-C(O)SR con 55 un componente de fórmula NH2-CH(XSH)-J2 en condiciones adecuadas para formar un producto de ligadura sustituido con tiol de fórmula J1-C(O)-NH-CH(XSH)-J2, en el que J1 es un residuo de una primera diana, que es una molécula, un
polímero o una superficie; R es un grupo compatible con tioésteres; XSH es una cadena lateral de un aminoácido ramificado que presenta un auxiliar tiol extraíble y se selecciona de entre el grupo constituido por un auxiliar β-mercapto de fórmula -CH(R')-SH y un auxiliar γ-mercapto de fórmula -CH2-CH(R')-SH, en los que R' se selecciona de entre el grupo constituido por etileno, fenilo, hidroxifenilo, aliltioalquilo, carbamoílo (-C(O)NH2), carbamoilalquilo, indolilo, hidroxicarbonilo, aminoalquilo, guanidina alquilo e imidazolilo, y J2 es un residuo de una segunda diana, que es la 5 molécula, un polímero o una superficie. En otro aspecto, la presente invención también da a conocer un procedimiento para eliminar el auxiliar tiol para generar un producto de ligadura de fórmula J1-C(O)-NH-CH(XH)-J2, en el que XH es una cadena lateral de aminoácido que tiene una fórmula seleccionada de entre el grupo constituido por: -CH2(R') y -CH2-CH2(R').
De acuerdo con otro aspecto, la presente invención da a conocer un componente de fórmula P1-NH-CH(XSH)-10 J2, en el que P1 es un grupo protector de amino extraíble o de hidrógeno; XSH es una cadena lateral de un aminoácido ramificado que presenta un auxiliar tiol extraíble y se selecciona de entre el grupo constituido por un auxiliar β-mercapto de fórmula -CH(R')-SH y un auxiliar γ-mercapto de fórmula -CH2-CH(R')-SH, en los que R' se selecciona de entre el grupo constituido por etileno, fenilo, hidroxifenilo, aliltioalquilo, carbamoílo (-C(O)NH2), carbamoilalquilo, indolilo, hidroxicarbonilo, guanidina alquilo e imidazolilo, y los residuos CH2R' y CH2CH2R' producidos tras la eliminación del 15 auxiliar tiol son cadenas laterales de aminoácidos; y J2 es un residuo de una diana, que es una molécula, un polímero o una superficie.
Según otro aspecto, la presente invención da a conocer un producto de ligadura de fórmula J1-C(O)-NH-CH(XSH)-J2, en el que J1 es un residuo de un primer componente de ligadura, XSH es una cadena lateral de un aminoácido ramificado que presenta un auxiliar tiol extraíble y se selecciona de entre el grupo constituido por un auxiliar 20 β-mercapto de fórmula -CH(R')-SH y un auxiliar γ-mercapto de fórmula -CH2-CH(R')-SH, en los que R' se selecciona de entre el grupo constituido por etileno, fenilo, hidroxifenilo, aliltioalquilo, carbamoílo (-C(O)NH2), carbamoilalquilo, indolilo, hidroxicarbonilo, guanidina alquilo e imidazolilo, y J2 es un residuo de un segundo componente de ligadura.
Haciendo referencia a las partes restantes de la presente memoria, incluyendo las figuras y las reivindicaciones, se darán a conocer otras características y ventajas de la presente invención. Otras características y ventajas de la 25 presente invención, así como la estructura y el funcionamiento de diversas formas de realización...
Reivindicaciones:
1. Procedimiento de ligadura de componentes a través de un enlace amida, comprendiendo dicho procedimiento:
poner en contacto un componente de fórmula J1-C(O)SR con un componente de fórmula NH2-CH(XSH)-J2 en condiciones suficientes para formar un producto de ligadura sustituido con tiol que presenta la fórmula J1-C(O)-NH-5 CH(XSH)-J2,
en la que
J1 es un residuo de una primera molécula diana, polímero o superficie;
R es un grupo compatible con tioésteres;
XSH es una cadena lateral de aminoácido ramificado que presenta un auxiliar tiol extraíble y se selecciona de 10 entre el grupo constituido por un auxiliar β-mercapto de fórmula -CH(R')-SH y un auxiliar γ-mercapto de fórmula -CH2-CH(R')-SH,
en la que R' es un residuo de una cadena lateral de aminoácido distinto de hidrógeno y se selecciona de entre el grupo constituido por: etileno, fenilo, hidroxifenilo, aliltioalquilo, carbamoílo (-C(O)NH2), carbamoilalquilo, indolilo, hidroxicarbonilo, guanidina alquilo e imidazolilo; y 15
J2 es un residuo de una segunda molécula diana, polímero o superficie;
2. Procedimiento según la reivindicación 1, que comprende además:
eliminar dicho auxiliar tiol para generar un producto de ligadura de fórmula J1-C(O)-NH-CH-(XH)-J2, en el que XH es una cadena lateral de aminoácido que presenta una fórmula seleccionada de entre el grupo constituido por: -CH2(R') y -CH2-CH2(R'). 20
3. Procedimiento según la reivindicación 2, en el que J1 y J2 son iguales o diferentes y son seleccionados de entre el grupo constituido por un residuo de un péptido, un polímero y una superficie.
4. Procedimiento según la reivindicación 1, en el que J1 es un residuo de un péptido.
5. Procedimiento según la reivindicación 4, en el que -C(O)SR se encuentra en el extremo C-terminal de dicho péptido. 25
6. Procedimiento según la reivindicación 1, en el que J2 es un residuo de un péptido.
7. Procedimiento según la reivindicación 6, en el que NH2-CH(XSH)- se encuentra en el extremo N-terminal de dicho péptido.
8. Procedimiento según la reivindicación 7, en el que XSH es la cadena lateral de un aminoácido β-ramificado. 30
9. Procedimiento según la reivindicación 8, en el que dicho aminoácido β-ramificado es la fenilcisteína.
10. Procedimiento según la reivindicación 9, en el que dicha fenilcisteína es la syn-fenilcisteína.
11. Componente que presenta la fórmula P1-NH-CH(XSH)-J2, en el que P1 es un grupo protector amino extraíble o hidrógeno; XSH es un componente de cadena lateral de aminoácido ramificado y es seleccionado de entre el grupo constituido por un auxiliar β-mercapto de fórmula -CH(R')-SH y un auxiliar γ-mercapto de fórmula -CH2-CH(R')-SH, 35 en las que
R' es distinto de hidrógeno y es seleccionado de entre el grupo constituido por: etileno, fenilo, hidroxifenilo, aliltioalquilo, carbamoílo (-C(O)NH2), carbamoilalquilo, indolilo, hidroxicarbonilo, aminoalquilo, guanidina alquilo e imidazolilo, y 40
los residuos CH2R' y CH2CH2R' producidos tras la eliminación del auxiliar tiol son cadenas laterales de aminoácidos; y J2 es un residuo de una molécula diana, polímero o superficie.
12. Componente según la reivindicación 11, en el que J2 es seleccionado de entre el grupo constituido por un residuo de una molécula pequeña, un polímero y una superficie.
13. Componente según la reivindicación 11, en el que J2 es un residuo de un péptido. 45
14. Componente según la reivindicación 13, en el que P1-NH-CH(XSH)- se encuentra en el extremo N-terminal de dicho péptido.
15. Componente según la reivindicación 14, en el que XSH es la cadena lateral de un aminoácido β-ramificado.
16. Componente según la reivindicación 15, en el que dicho aminoácido β-ramificado es la fenilcisteína. 5
17. Componente según la reivindicación 16, en el que dicha fenilcisteína es la syn-fenilcisteína.
18. Producto de ligadura que presenta la fórmula J1-C(O)-NH-CH(XSH)-J2, en el que J1 es un residuo de un primer componente de ligadura, XSH es una cadena lateral de aminoácido ramificado que presenta un auxiliar tiol extraíble y se selecciona de entre el grupo constituido por un auxiliar β-mercapto de fórmula -CH(R')-SH y un auxiliar γ-mercapto de fórmula 10
-CH2-CH(R')-SH, en la que R' es un residuo de una cadena lateral de aminoácido distinto de hidrógeno y se selecciona de entre el grupo constituido por: etileno, fenilo, hidroxifenilo, aliltioalquilo, carbamoílo (-C(O)NH2), carbamoilalquilo, indolilo, hidroxicarbonilo, aminoalquilo, guanidina alquilo e imidazolilo, y J2 es un residuo de un segundo componente de ligadura.
19. Producto según la reivindicación 18, en el que J1 y J2 son iguales o diferentes y son seleccionados de 15 entre el grupo constituido por un residuo de una molécula pequeña, un polímero y una superficie.
20. Producto según la reivindicación 18, en el que J1 es un residuo de un péptido.
21. Producto según la reivindicación 18, en el que J2 es un residuo de un péptido.
22. Producto según la reivindicación 18, en el que XSH es un auxiliar β-mercapto de la fórmula -CH(R')-SH, y parte de un aminoácido β-ramificado. 20
23. Producto según la reivindicación 22, en el que dicho aminoácido β-ramificado es la fenilcisteína.
24. Producto según la reivindicación 23, en el que dicha fenilcisteína es la syn-fenilcisteína.
25. Kit que comprende como componente una composición según la reivindicación 11.
Patentes similares o relacionadas:
Secuenciación por síntesis usando óptica de lectura por pulsos, del 19 de Febrero de 2020, de IBIS BIOSCIENCES, INC: Un sistema para fotoescindir y explorar análogos de nucleótidos que comprende: a) un sustrato que comprende una pluralidad de pocillos que contienen cada uno, o están configurados […]
Conjugado de péptido-resina y su utilización, del 18 de Septiembre de 2019, de Chemical & Biopharmaceutical Laboratories of Patras S.A: Un procedimiento para preparar un péptido, o una sal del mismo, de un conjugado de péptido-resina de las Fórmulas (2b), (2c), (2d), (2e) o (2f),**Fórmula** […]
Polipéptidos de relaxina modificados y sus usos, del 5 de Junio de 2019, de AMBRX, INC: Un polipéptido de relaxina modificado que comprende un aminoácido codificado de modo no natural, en donde: (a) el polipéptido de relaxina comprende el polipéptido de cadena […]
Conjugados de polisacáridos y proteínas acoplados reversiblemente a través de enlaces imina, del 3 de Abril de 2019, de THERAPURE BIOPHARMA INC.: Una composición de polisacárido oxidado-proteína para su uso como agente terapéutico o de diagnóstico, en donde la composición comprende un polisacárido oxidado […]
Procedimiento de síntesis de proteínas, del 5 de Marzo de 2019, de CENTRE NATIONAL DE LA RECHERCHE SCIENTIFIQUE (C.N.R.S.): Procedimiento de ensamblaje de fragmentos peptídicos para fabricar un polipéptido que comprende n fragmentos peptídicos y al menos n-1 aminoácidos […]
Procedimientos para la preparación de análogos de oxitocina, del 18 de Febrero de 2019, de F. HOFFMANN-LA ROCHE AG: Procedimiento para la preparación de análogos de oxitocina de fórmula I **Fórmula** en la que R1 es hidrógeno o alquilo C1-7 y R2 es hidrógeno […]
Método para preparar exenatida, del 29 de Octubre de 2018, de Hybio Pharmaceutical Co., Ltd: Un método para la preparación de exenatida, que se caracteriza por comprender las siguientes etapas: Etapa 1: se obtiene serina-resina mediante un primer […]
Síntesis de péptidos en fase sólida con BOC y FMOC, del 18 de Septiembre de 2018, de Ipsen Manufacturing Ireland Limited: Un método para preparar un péptido de fórmula H-D-β-Nal-[Cys-Tyr-D-Trp-Lys-Val-Cys]-Thr-NH2, en donde dicho método comprende las etapas de: (a) anclar […]