NUEVOS COMPUESTOS DE ACTIVIDAD MIXTA DE LA AMILINA.
Compuesto de fórmula: X1-X2-X3-Leu-X4-Glu-Leu-X5-X6-Leu-Gln-Thr-Tyr-Pro-Arg- Thr-Asn-X7-Z3 [SEC ID nº 27] en la que:
(a) X1 es Z1-Ser-Thr-Z2-Val-Leu [SEC ID nº 28], en la que Z1 es un grupo alcanoílo; y Z2 es un residuo aminoácido seleccionado de entre el grupo constituido por Ala, Ser, Cys, y Thr; (b) X2 es un residuo aminoácido seleccionado de entre el grupo constituido por Gly, Glu, Asn o Aib; (c) X3 es un residuo aminoácido seleccionado de entre el grupo constituido por Arg, Orn, Lys y Lys E-amidado con ácido acético; (d) X4 es un grupo de dos residuos aminoácidos seleccionados de entre el grupo constituido por Ser-Gln, Thr-Gln, Ala-Asn y Thr-Asn; (e) X5 es un residuo aminoácido seleccionado de entre el grupo constituido por His, Aib, Ile, Leu y Val; (f) X6 es un residuo aminoácido seleccionado de entre el grupo constituido por Arg, Orn y Lys y derivados E- amidados de los mismos, tales como Lys E-amidado con ácido fórmico (Lys(For)); (g) X7 es un grupo que presenta 6 residuos aminoácidos seleccionados de entre el grupo constituido por: (i) Thr-Gly-Ser-Asn-Thr-Tyr [SEC ID nº 29] (ii) Thr-Gly-Ser-Gly-Thr-Pro [SEC ID nº 30] (iii) Val-Gly-Ser-Asn-Thr-Tyr [SEC ID nº 31] (iv) Val-Gly-Ser-Gly-Thr-Pro [SEC ID nº 32]; y (h) Z3 es OH o NH2; con la condición de que el compuesto no presente la fórmula de cualquiera de las secuencias SEC ID nº 20 ó 22 a 26; y sus sales farmacéuticamente aceptables; o un compuesto de fórmula: 4-metilpentanoil-Ser-Thr-Ala-Val-Leu-Aib-Lys(For)-Leu-Ser-Gln-Glu-Leu-Aib-Lys(For)-Leu-Gln-Thr-Tyr-Pro-Arg- Thr-Asn-Thr-Gly-Ser-Gly-Thr-Pro [SEC ID nº 2]; o 4-metilpentanoil-Ser-Thr-Ala-Val-Leu-Aib-Lys(For)-Leu-Ser-Gln-Glu-Leu-Aib-Lys(For)-Leu-Gln-Thr-Tyr-Pro-Arg- Thr-Asn-Thr-Gly-Ser-Asn-Thr-Tyr [SEC ID nº 10]; o 4-metilpentanoil-Ser-Thr-Cys-Val-Leu-Aib-Lys(For)-Leu-Ser-Gln-Glu-Leu-Aib-Lys(For)-Leu-Gln-Thr-Tyr-Pro- Arg-Thr-Asn-Thr-Gly-Ser-Asn-Thr-Tyr [SEC ID nº 11], y sus sales farmacéuticamente aceptables
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US1999/002603.
Solicitante: AMYLIN PHARMACEUTICALS, INC..
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 9360 TOWNE CENTRE DRIVE SAN DIEGO, CA 92121 ESTADOS UNIDOS DE AMERICA.
Inventor/es: PRICKETT, KATHRYN, S., BEAUMONT, KEVIN, BEELEY,NIGEL,R.,A.
Fecha de Publicación: .
Fecha Solicitud PCT: 5 de Febrero de 1999.
Clasificación Internacional de Patentes:
- C07K14/575 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 14/00 Péptidos con más de 20 aminoácidos; Gastrinas; Somatostatinas; Melanotropinas; Sus derivados. › Hormonas.
Clasificación PCT:
- C07K14/575 C07K 14/00 […] › Hormonas.
Clasificación antigua:
- A61K37/02
- C07K7/10
Países PCT: Austria, Bélgica, Suiza, Alemania, Dinamarca, España, Francia, Reino Unido, Grecia, Italia, Liechtensein, Luxemburgo, Países Bajos, Suecia, Mónaco, Portugal, Irlanda, Finlandia, Chipre.
PDF original: ES-2356595_T3.pdf



Fragmento de la descripción:
CAMPO DE LA INVENCIÓN
La presente invención se refiere a compuestos que inhiben determinadas actividades de la amilina pero que también actúan como agonistas de la amilina con respecto a otras actividades de la amilina. Estos compuestos resultan útiles para tratar alteraciones del metabolismo energético en los mamíferos que comprenden de manera no limitativa la 5 diabetes mellitus, incluyendo la diabetes de tipo I y la diabetes de tipo II, la tolerancia alterada a la glucosa, la resistencia a la insulina y el síndrome X.
ANTECEDENTES E INTRODUCCIÓN A LA INVENCIÓN
La diabetes mellitus es una enfermedad metabólica grave que se define a partir de la presencia de niveles crónicamente elevados de glucosa sanguínea (hiperglucemia). Este estado de hiperglucemia es el resultado de una 10 falta relativa o absoluta de actividad de la hormona peptídica insulina. La insulina es producida y secretada por las células β del páncreas. Se informa que la insulina estimula la utilización de la glucosa, la síntesis de proteínas y la formación y almacenamiento glucídico en forma de glucógeno. La glucosa se almacena en el cuerpo en forma de glucógeno, una forma de glucosa polimerizada, que puede convertirse nuevamente en glucosa para satisfacer los requisitos metabólicos. Bajo condiciones normales, se secreta insulina tanto a tasa basal como a tasas incrementadas 15 tras la estimulación de la glucosa, manteniendo la homeostasis metabólica mediante la conversión de la glucosa en glucógeno.
La expresión diabetes mellitus comprende varios estados hiperglucémicos diferentes. Entre estos estados se incluyen la diabetes de tipo I (diabetes mellitus insulino-dependiente, o IDDM) y la diabetes de tipo II (diabetes mellitus no insulino-dependiente, o NIDDM). La hiperglucemia presente en individuos con diabetes de tipo I se asocia a niveles 20 deficientes, reducidos o nulos de insulina que resultan insuficientes para mantener los niveles sanguíneos de glucosa dentro del rango fisiológico. El tratamiento de la diabetes de tipo I implica la administración de dosis de sustitución de insulina, generalmente mediante una vía parenteral. La hiperglucemia presente en individuos con diabetes de tipo II se asocia inicialmente a niveles normales o elevados de insulina; sin embargo, estos individuos son incapaces de mantener la homeostasis metabólica debido a un estado de resistencia a la insulina en tejidos periféricos y en el hígado 25 y, a medida que avanza la enfermedad, debido a un deterioro progresivo de las células β pancreáticas que son responsables de la secreción de la insulina. De esta manera, la terapia inicial de la diabetes de tipo II puede basarse en cambios de la dieta y del estilo de vida potenciados mediante terapia con agentes hipoglucémicos orales, tales como sulfonilureas. Sin embargo, con frecuencia resulta necesaria la terapia de insulina, especialmente en los últimos estadios de la enfermedad, en un intento de alcanzar cierto control de la hiperglucemia y de minimizar las 30 complicaciones de la enfermedad.
La estructura y la biología de la amilina han sido revisadas anteriormente. Ver, por ejemplo, Young, Current Opinion in Endocrinology and Diabetes 4:282-290, 1997; Gaeta y Rink, Med. Chem. Res. 3:483-490, 1994, y Pittner et al., J. Cell. Biochem. 55S:19-28, 1994). La amilina es una hormona peptídica de 37 aminoácidos. Ha sido aislada, purificada y caracterizada químicamente como el componente principal de los depósitos de amiloide en los islotes de 35 páncreas de personas diabéticas de tipo II fallecidas (Cooper et al., Proc. Natl. Acad. Sci. USA 84:8628-8632, 1987). La molécula de amilina presenta dos modificaciones postraduccionales importantes: el extremo C-terminal se encuentra amidado, es decir, el residuo 37 es tirosinamida, y las cisteínas en las posiciones 2 y 7 se encuentran reticuladas formando un bucle N-terminal intramolecular, resultando esenciales ambas para la actividad biológica completa (Cooper et al., Proc. Natl. Acad. Sci. USA 85:7763-7766, 1988). La amilina es el objeto de la patente US nº 5.367.052, 40 publicada el 22 de noviembre de 1994.
En la diabetes de tipo I y en la diabetes de tipo II de estadio tardío, se ha demostrado la deficiencia en amilina y se ha propuesto la sustitución combinada con insulina como un tratamiento preferido respecto a la insulina sola en todas las formas de diabetes insulino-dependiente. La utilización de amilina y de agonistas de la amilina para el tratamiento de la diabetes mellitus es el objeto de la patente US nº 5.175.145, publicada el 29 de diciembre de 1992. 45 Las composiciones farmacéuticas que contienen amilina y amilina más insulina se describen en la patente US nº 5.124.314, publicada el 23 de junio de 1992.
Se ha informado de que un exceso de acción de la amilina imita características clave de los estadios más tempranos de la diabetes de tipo II y se ha propuesto el bloqueo de la amilina como nueva estrategia terapéutica. Se da a conocer en la patente US nº 5.266.561, publicada el 30 de noviembre de 1993, que la amilina causa una reducción 50 en la incorporación tanto basal como estimulada por la insulina de glucosa marcada en glucógeno en el músculo esquelético. También se ha dado conocer que este último efecto es compartido por el péptido relacionado con el gen de la calcitonina (CGRP) (ver también Leighton y Cooper, Nature 335:632-635, 1988). La amilina y el CGRP eran aproximadamente equipotentes, mostrando una actividad marcada a concentraciones de entre 1 y 10 nM. También se informa de que la amilina reduce la captación estimulada por insulina de la glucosa en el músculo esquelético y reduce 55 el contenido de glucógeno (Young et al., Amer. J. Physiol. 259:45746-1, 1990). Se da a conocer el tratamiento de la diabetes de tipo II y de la resistencia a la insulina con antagonistas de amilina.
La amilina se sintetiza principalmente en las células beta pancreáticas y se secreta en respuesta a estímulos de nutrientes, tales como glucosa y arginina. Los estudios con líneas tumorales de células beta clonadas (Moore et al.,
Biochem. Biophys. Res. Commun. 179(1), 1991) y páncreas de rata perfundidos (Ogawa et al., J. Clin. Invest. 85:973-976, 1990) han demostrado que pulsos cortos, de 10 a 20 minutos, de secretagogos de nutrientes, tales como glucosa y arginina, estimulan la liberación de la amilina, así como de la insulina. La proporción molar de amilina:insulina de las proteínas secretadas varía entre preparaciones de aproximadamente 0,01 a 0,4, aunque aparentemente no varía mucho con estímulos agudos en cualquier otra preparación. Sin embargo, durante la estimulación prolongada por 5 niveles elevados de glucosa, la proporción amilina:insulina puede incrementarse progresivamente (Gedulin et al., Biochem. Biophys. Res. Commun. 180(1):782-789, 1991). De esta manera, la amilina y la insulina no se secretan siempre en una proporción constante.
Se ha descubierto y publicado que determinadas acciones de la amilina son similares a las acciones no metabólicas del CGRP y de la calcitonina; sin embargo, las acciones metabólicas de la amilina descubiertas durante 10 investigaciones de esta proteína recientemente identificada aparentemente reflejan su papel biológico primario. Por lo menos algunas de estas acciones metabólicas son imitadas por el CGRP, aunque a dosis que son marcadamente vasodilatadoras (ver, por ejemplo, Leighton y Cooper, Nature 335:632-635, 1988; Molina et al., Diabetes 39:260-265, 1990).
La primera acción descubierta de la amilina fue la reducción de la incorporación estimulada por insulina de la 15 glucosa en glucógeno en el músculo esquelético de rata (Leighton y Cooper, Nature 335:632-635, 1988); el músculo, de esta manera, se convertía en "resistente a la insulina". Los estudios posteriores con el músculo sóleo de la rata ex vivo e in vivo han indicado que la amilina reduce la actividad de la glucógeno sintasa, estimula la conversión de la glucógeno fosforilasa de la forma b inactiva en la forma a activa, estimula la pérdida neta de glucógeno (en presencia o en ausencia de insulina), incrementa los niveles de glucosa-6-fosfato, y puede incrementar la producción de lactato 20 (ver, por ejemplo, la solicitud de patente internacional nº PCT/US92/00185, publicada el 23 de julio de 1992 (publicación de patente internacional WO 92/11863). La amilina aparentemente no afecta al transporte de glucosa per se (por ejemplo Pittner et al., FEBS Letts. 365(1):98-100, 1995). Los estudios de relaciones de dosis-respuesta con amilina y con insulina demuestran que la amilina actúa como un antagonista no competitivo... [Seguir leyendo]
Reivindicaciones:
1. Compuesto de fórmula:
X1-X2-X3-Leu-X4-Glu-Leu-X5-X6-Leu-Gln-Thr-Tyr-Pro-Arg-
Thr-Asn-X7-Z3 [SEC ID nº 27] en la que:
(a) X1 es Z1-Ser-Thr-Z2-Val-Leu [SEC ID nº 28], en la que Z1 es un grupo alcanoílo; y 5
Z2 es un residuo aminoácido seleccionado de entre el grupo constituido por Ala, Ser, Cys, y Thr;
(b) X2 es un residuo aminoácido seleccionado de entre el grupo constituido por Gly, Glu, Asn o Aib;
(c) X3 es un residuo aminoácido seleccionado de entre el grupo constituido por Arg, Orn, Lys y Lys ε-amidado con ácido acético;
(d) X4 es un grupo de dos residuos aminoácidos seleccionados de entre el grupo constituido por Ser-Gln, Thr-Gln, 10 Ala-Asn y Thr-Asn;
(e) X5 es un residuo aminoácido seleccionado de entre el grupo constituido por His, Aib, Ile, Leu y Val;
(f) X6 es un residuo aminoácido seleccionado de entre el grupo constituido por Arg, Orn y Lys y derivados ε-amidados de los mismos, tales como Lys ε-amidado con ácido fórmico (Lys(For));
(g) X7 es un grupo que presenta 6 residuos aminoácidos seleccionados de entre el grupo constituido por: 15
(i) Thr-Gly-Ser-Asn-Thr-Tyr [SEC ID nº 29]
(ii) Thr-Gly-Ser-Gly-Thr-Pro [SEC ID nº 30]
(iii) Val-Gly-Ser-Asn-Thr-Tyr [SEC ID nº 31]
(iv) Val-Gly-Ser-Gly-Thr-Pro [SEC ID nº 32]; y
(h) Z3 es OH o NH2; 20
con la condición de que el compuesto no presente la fórmula de cualquiera de las secuencias SEC ID nº 20 ó 22 a 26;
y sus sales farmacéuticamente aceptables;
o un compuesto de fórmula:
4-metilpentanoil-Ser-Thr-Ala-Val-Leu-Aib-Lys(For)-Leu-Ser-Gln-Glu-Leu-Aib-Lys(For)-Leu-Gln-Thr-Tyr-Pro-Arg-25 Thr-Asn-Thr-Gly-Ser-Gly-Thr-Pro [SEC ID nº 2]; o
4-metilpentanoil-Ser-Thr-Ala-Val-Leu-Aib-Lys(For)-Leu-Ser-Gln-Glu-Leu-Aib-Lys(For)-Leu-Gln-Thr-Tyr-Pro-Arg-Thr-Asn-Thr-Gly-Ser-Asn-Thr-Tyr [SEC ID nº 10]; o
4-metilpentanoil-Ser-Thr-Cys-Val-Leu-Aib-Lys(For)-Leu-Ser-Gln-Glu-Leu-Aib-Lys(For)-Leu-Gln-Thr-Tyr-Pro-Arg-Thr-Asn-Thr-Gly-Ser-Asn-Thr-Tyr [SEC ID nº 11], 30
y sus sales farmacéuticamente aceptables.
2. Compuesto según la reivindicación 1, en el que Z3 es NH2.
3. Compuesto según la reivindicación 1, en el que X2 es Gly.
4. Compuesto según la reivindicación 3, en el que X5 es His o Aib.
5. Compuesto según la reivindicación 4, en el que X4 es Ser-Gln. 35
6. Compuesto según la reivindicación 5, en el que X7 es:
Thr-Gly-Ser-Asn-Thr-Tyr [SEC ID nº 29] o
Thr-Gly-Ser-Gly-Thr-Pro [SEC ID nº 30].
7. Compuesto según la reivindicación 1, en el que Z1 es un grupo alcanoílo que presenta de 1 a aproximadamente 10 átomos de carbono o Leu. 40
8. Compuesto según la reivindicación 7, en el que Z2 es Ala o Cys.
9. Compuesto según la reivindicación 1, en el que X3 y X6 se encuentran acetamidados.
10. Compuesto según la reivindicación 9, en el que Z2 es Ala.
11. Compuesto según la reivindicación 10, en el que Z1 es 4-metilpentanoílo.
12. Composición que comprende un compuesto según cualquiera de las reivindicaciones 1 a 11 en un 5 portador farmacéuticamente aceptable.
13. Utilización de un compuesto según cualquiera de las reivindicaciones 1 a 11 para la preparación de un medicamento
(a) destinado al tratamiento de la diabetes en un sujeto que necesita tratamiento;
(b) destinado a regular beneficiosamente la motilidad gastrointestinal en un sujeto; o 10
(c) destinado a tratar un trastorno seleccionado de entre el grupo constituido por: tolerancia alterada a la glucosa; hiperglucemia posprandial; obesidad; y síndrome X; en un sujeto.
14. Utilización según la reivindicación 13, en la que dicha diabetes es la diabetes de tipo I o la diabetes de tipo II.
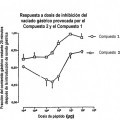
15. Utilización según la reivindicación 13, en la que dicha regulación beneficiosa de la motilidad 15 gastrointestinal comprende retrasar el vaciado gástrico.
Patentes similares o relacionadas:
Antagonistas peptídicos de la familia calcitonina CGRP de hormonas peptídicas y su uso, del 17 de Junio de 2020, de Soares, Christopher, J: Un antagonista del péptido relacionado con el gen de la calcitonina, o una sal farmacéuticamente aceptable del mismo, teniendo dicho antagonista la estructura […]
Una composición para el tratamiento de la diabetes que comprende un análogo de oxintomodulina, del 11 de Marzo de 2020, de HANMI PHARM. CO., LTD.: Una composición para su uso en la prevención o el tratamiento de la diabetes, la composición comprende un conjugado de análogo de oxintomodulina como un ingrediente […]
Modelo de cerdo para la diabetes, del 29 de Enero de 2020, de AARHUS UNIVERSITET: Un cerdo transgénico que comprende un gen de polipéptido amiloide de los islotes (IAPP) mutado humano o parte del mismo, y que muestra al menos […]
Variantes mejoradas de unión de anti-albúmina sérica, del 18 de Diciembre de 2019, de GLAXO GROUP LIMITED: Un conjugado que comprende un fármaco NCE conjugado a un dominio variable único de inmunoglobulina antialbúmina sérica (SA) que comprende la secuencia de aminoácidos de SEQ […]
POLIPÉPTIDOS, del 4 de Diciembre de 2019, de NOVO NORDISK A/S: Un polipéptido de acuerdo con la Fórmula (I): Xaa1-Cys-Xaa3-Thr-Ala-Thr-Cys-Ala-Thr-Gln-Arg-Leu-Ala-Xaa14-Phe-Leu- Xaa17-Xaa18-Ser-Ser- Xaa21- […]
Polipéptidos de acción prolongada y métodos para producirlos y administrarlos, del 4 de Diciembre de 2019, de OPKO Biologics Ltd: Un polipéptido que comprende una actividad biológica, dicho polipéptido comprende un péptido de interés, un solo péptido carboxilo terminal (CTP) de gonadotropina coriónica unido […]
Análogos de cortistatina para el tratamiento de enfermedades inflamatorias y/o inmunes, del 23 de Octubre de 2019, de BCN PEPTIDES, S.A.: Un compuesto análogo de cortistatina de fórmula general (I), R1-AA1-AA2-AA3-AA4-c[Cys-AA5-Asn-X-Y-Trp-Lys-Thr-Z-AA6-Ser-Cys]-AA7-R2 sus […]
Compuestos coagonistas de GIP y GLP-1, del 14 de Agosto de 2019, de ELI LILLY AND COMPANY: Un compuesto de Fórmula: YX1EGTFTSDYSIX2LDKIAQKAX3VQWLIAGGPSSGAPPPS; en la que X1 es Aib; X2 es Aib; K en la posición 20 se modifica químicamente […]