DESPROTECCION DEL AZUFRE POSTERIOR A LA ESCISION PARA LA SINTESIS CONVERGENTE DE PROTEINAS MEDIANTE LIGACION QUIMICA.
Compuesto de fórmula:
Xaai- ... -Xaam-(CH-R)-CO-O-C*H[(CH2)n-S-R'']-Y
en la que:
Xaai es un aminoácido protegido o no protegido para i=1 a m;
m es un número entero entre 2 y 200;
n es un número entero entre 1 y 10;
C* es un carbono quiral en configuración R o S, y sustancialmente libre de la configuración contraria;
R es una cadena lateral de un aminoácido;
R'' es -SR'''',
Y es un grupo aceptor de electrones seleccionado de entre el grupo que consiste de Rc, alquilo C1-3 sustituido con 1 a 3 grupos Rc, -C(O)-Rd, -S(O)p-alquilo C1-3 sustituido con 0 a 3 grupos Rc, y un arilo sustituido con 1 a 3 grupos Rc; cada grupo Rc es independientemente un elemento seleccionado de entre el grupo que consiste de halógeno, polihaloalquilo, bencilo sustituido o no sustituido, arilo sustituido o no sustituido, -C(O)NH2, -C(O)-NHHN2, -S(O)2NH2, hidroxilamina sustituida o no sustituida, ciano, nitro y sales de amonio cuaternario;
p es un número entero entre 1 y 2;
Rd es un elemento seleccionado de entre el grupo que consiste de hidrógeno, -N(Re)2, ORe y -SRe;
cada Re es independientemente un elemento seleccionado de entre el grupo que consiste de hidrógeno, alquilo C1-3 sustituido con 0 a 3 grupos Rc, y -SO2-alquilo C1-3 sustituido con 1 a 3 grupos Rc; alternativamente,
en el caso de que se encuentren presentes dos grupos Re, conjuntamente con el átomo al que se encuentran unidos puede formar un anillo heterocíclico no aromático de 5 a 6 elementos que contiene entre 1 y 3 heteroátomos, cada uno seleccionado independientemente de entre el grupo que consiste de N, O y S, sustituido con 0 a 3 grupos Rc, y
en el que R'''' es un elemento seleccionado de entre el grupo que consiste de etilo, t-butilo y fenilo sustituido
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/IB03/05087.
Solicitante: AMYLIN PHARMACEUTICALS, INC..
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 9360 TOWNE CENTRE DRIVE,SAN DIEGO, CA 92121.
Inventor/es: VILLAIN,MATTEO, BOTTI,PAOLO, MANGANIELLO,SONIA, GAERTNER,HUBERT.
Fecha de Publicación: .
Fecha Concesión Europea: 24 de Febrero de 2010.
Clasificación Internacional de Patentes:
- C07K1/02 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 1/00 Procedimientos generales de preparación de péptidos. › en solución.
- C07K1/04 C07K 1/00 […] › sobre soportes.
- C07K1/107D4
Clasificación PCT:
Clasificación antigua:
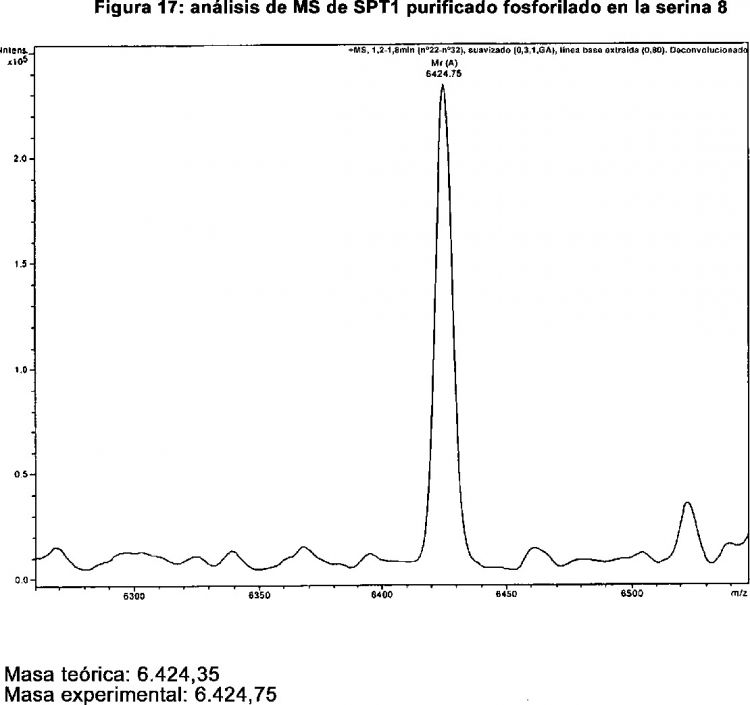
Fragmento de la descripción:
Desprotección del azufre posterior a la escisión para la síntesis convergente de proteínas mediante ligación química.
Antecedentes de la presente invención
La secuenciación del genoma humano ha generado la promesa y la oportunidad de comprender la función de todos los genes y proteínas relevantes a la biología y patología humanas (Peltonen y McKusick, Science 291:1224-1229, 2001). Sin embargo, deben superarse varios obstáculos importantes antes de cumplir por completo dicha promesa. En primer lugar, incluso conociendo la secuencia del genoma humano, todavía resulta difícil distinguir los genes y las secuencias que controlan su expresión. En segundo lugar, aunque el seguimiento de la expresión génica a nivel de transcritos se ha robustecido con el desarrollo de la tecnología de micromatrices, una parte importante de la variabilidad y del control de función se origina en sucesos posteriores a la transcripción, tales como el procesamiento alternativo y el procesamiento y modificación posteriores a la traducción. Finalmente, debido a la escala de la biología molecular humana, potencialmente deberán aislarse y someterse a ensayo varias decenas de miles de genes, y sus productos de expresión, para comprender su papel en los estados de salud y de enfermedad (Dawson y Kent, Annu. Rev. Biochem. 69:923-960, 2000).
Con respecto a la cuestión de la escala, la aplicación de las metodologías recombinantes convencionales para la clonación, expresión, recuperación y aislamiento de proteínas todavía es un procedimiento largo y laborioso, de manera que su aplicación en el cribado de grandes cantidades de productos génicos diferentes para determinar su función ha sido limitada. Recientemente, se ha desarrollado un enfoque de síntesis que puede satisfacer la necesidad de un acceso fácil a cantidades altamente purificadas a escala de investigación de proteínas para el cribado funcional (Dawson y Kent (citado anteriormente), y Dawson et al., Science 266:776-779, 1994). En su implementación más atractiva, un intermediario oligopéptido no protegido que presente un tioéster C-terminal reaccionan con una cisteína N-terminal de otro intermediario oligopéptido bajo condiciones acuosas suaves para formar un enlace tioéster que se reorganiza espontáneamente formando un enlace peptídico natural (Kent et al., patente US nº 6.184.344). El enfoque ha sido utilizado para ensamblar oligopéptidos en proteínas activas tanto en fase solución, por ejemplo Kent et al., patente US nº 6.184.344, y sobre un soporte de fase sólida, por ejemplo Canne et al., J. Am. Chem. Soc. 121:8720-8727, 1999). Recientemente, la técnica se ha extendido, permitiendo el acoplamiento de fragmentos tioéster C-terminales a un abanico más amplio de aminoácidos N-terminales de péptidos correactivos mediante la utilización de un grupo etiltio desplazable unido al nitrógeno N-terminal del correactivo, imitando de esta manera la función de una cisteína N-terminal (Low et al., Proc. Natl. Acad. Sci. 98:6554-6559, 2001).
En la actualidad, la síntesis de tioésteres de oligopéptido se lleva a cabo principalmente utilizando grupos protectores basados en t-butoxicarbonilo ("Boc"). Alternativamente, también pueden utilizarse grupos protectores basados en 9-fluorenilmetoxicarbonilo ("Fmoc"), aunque únicamente en el caso de que los tiempos de reacción sean cortos, debido a que los reactivos nucleofílicos utilizados para desplazar los grupos protectores Fmoc también degradan los tioésteres de los oligopéptidos con el tiempo, tal como indican Botti et al., publicación de patente internacional WO nº 02/18417. Para resolver este problema, Botti et al. han sugerido la utilización de un precursor tioéster estable frente a nucleófilos que es desplazable bajo condiciones no nucleofílicas, en combinación con un grupo protector Fmoc lábil nucleofílico como grupo protector N-terminal. Aunque el trabajo de Botti et al. no facilita el acoplamiento de aminoácidos y oligopéptidos, los carboxiésteres 2-mercapto de Botti et al. son susceptibles de corte nucleofílico en los tiempos de reacción prolongados. Debido a que la preparación de oligopéptidos, polipéptidos y proteínas muy largos requiere tiempos de reacción prolongados, resultaría ventajoso un nuevo método que proporcione grupos protectores N-terminales y C-terminales estables para la preparación de oligopéptidos, polipéptidos y proteínas. Inesperadamente la presente invención proporciona estos métodos.
Descripción resumida de la presente invención
En un aspecto, la presente invención proporciona un método para preparar un producto oligopéptido o polipéptido, que comprende: (a) ligar en una primera reacción un primer y un segundo oligopéptidos, presentando cada uno un extremo N-terminal y un extremo C-terminal, en la que el primer oligopéptido comprende un extremo C-terminal que presenta un grupo tioéster, y un extremo N-terminal que es sustancialmente no reactivo con el grupo tioéster, en el que el segundo oligopéptido comprende un extremo N-terminal que presenta una cisteína no protegida, un 1,2-aminotiol no protegido, o un 1,3-aminotiol no protegido, y un extremo C-terminal que presenta un precursor tioéster inactivo, en el que dicho segundo oligopéptido es un péptido según cualquiera de las reivindicaciones 1, 2 ó 3, y en el que la ligación forma un primer producto de ligación oligopéptido que comprende un extremo C-terminal que presenta un precursor tioéster inactivo, y un extremo N-terminal que es sustancialmente no reactivo con el grupo tioéster, (b) ligar en una segunda reacción un tercer y un cuarto oligopéptidos, presentando cada uno un extremo N-terminal y un extremo C-terminal, en la que el tercer oligopéptido comprende un extremo N-terminal que presenta una cisteína protegida, un 1,2-aminotiol protegido o un 1,3-aminotiol protegido, y un extremo C-terminal que comprende un tioéster, en el que el cuarto oligopéptido comprende un extremo N-terminal que presenta una cisteína no protegida, un 1,2-aminotiol no protegido o un 1,3-aminotiol no protegido, y un extremo C-terminal que es sustancialmente no reactivo con la cisteína no protegida, el 1,2-aminotiol no protegido o el 1,3-aminotiol no protegido, y en el que la ligación forma un segundo producto de ligación oligopéptido que comprende un extremo N-terminal que presenta una cisteína protegida, un 1,2-aminotiol protegido o un 1,3-aminotiol protegido, y un extremo C-terminal que es sustancialmente no reactivo con la cisteína no protegida, el 1,2-aminotiol no protegido o el 1,3-aminotiol no protegido, (c) transformar el precursor tioéster inactivo del primer producto de ligación oligopéptido de la etapa (a) en un tioéster, formando un tercer producto de ligación oligopéptido que presenta un extremo C-terminal que comprende un tioéster, y un extremo N-terminal que es sustancialmente no reactivo con el grupo tioéster, (d) desproteger el extremo N-terminal del segundo producto de ligación oligopéptido de la etapa (b) para formar un cuarto producto de ligación que comprende un extremo N-terminal que presenta una cisteína no protegida, un 1,2-aminotiol no protegido o un 1,3-aminotiol no protegido, y un extremo C-terminal que es sustancialmente no reactivo con la cisteína no protegida, el 1,2-aminotiol no protegido o el 1,3-aminotiol no protegido, y (e) ligar el tercer producto de ligación oligopéptido de la etapa (c) con el cuarto producto de ligación oligopéptido de la etapa (d) para formar un quinto producto de ligación oligopéptido que comprende un extremo N-terminal que es sustancialmente no reactivo con un oligopéptido que porta un grupo tioéster C-terminal, y un extremo C-terminal que es sustancialmente no reactivo con un oligopéptido que porta una cisteína N-terminal no protegida, un 1,2-aminotiol no protegido o un 1,3-aminotiol no protegido.
En otro aspecto, la presente invención proporciona un compuesto que presenta la fórmula siguiente:
en la que Xaai es un aminoácido protegido o no protegido para i=1 a m; m es un número entero entre 2 y 200; n es un número entero entre 1 y 10; C* es un átomo quiral en configuración R o S, y sustancialmente libre de la otra configuración; R es una cadena lateral de un aminoácido; R' es SR''; R'' es un elemento seleccionado de entre el grupo que consiste de alquilo C2-10, arilo sustituido que presenta entre 5 y 12 átomos de carbono, bencilo sustituido, y heteroarilo sustituido que presenta entre 5 y 12 átomos de carbono y entre 1 y 4...
Reivindicaciones:
1. Compuesto de fórmula:
en la que:
2. Compuesto según la reivindicación 1, en el que Y es -C(O)NH2.
3. Compuesto de fórmula:
en la que:
4. Compuesto de fórmula:
en la que:
5. Método para la preparación de un producto oligopéptido o polipéptido, que comprende:
6. Método según la reivindicación 5, que comprende además:
7. Método según la reivindicación 5, en el que dicho extremo N-terminal de dicho quinto producto de ligación oligopéptido de la etapa (e) comprende un aminoácido N-terminal no protegido o un aminoácido N-terminal protegido.
8. Método según la reivindicación 7, en el que dicho aminoácido N-terminal protegido es cíclico.
9. Método según la reivindicación 7, en el que dicho aminoácido N-terminal protegido comprende una cisteína protegida, un 1,2-aminotiol protegido o un 1,3-aminotiol protegido.
10. Método según la reivindicación 5, en el que dicho extremo C-terminal de dicho quinto producto de ligación oligopéptido de la etapa (e) comprende un aminoácido no protegido o un precursor tioéster inactivo.
11. Método según la reivindicación 5, en el que cualquiera de dichos oligopéptidos o productos de ligación oligopéptido que presenta un precursor tioéster inactivo en dicho extremo C-terminal se define mediante la fórmula siguiente:
en la que:
12. Método según la reivindicación 11, en el que R' es un grupo protector de azufre.
13. Método según la reivindicación 11, en el que R' es -SR''.
14. Método según la reivindicación 11, en el que R'' es un elemento seleccionado de entre el grupo que consiste de etilo, t-butilo y fenilo sustituido.
15. Método según la reivindicación 5, en el que dicho producto oligopéptido o polipéptido se prepara según el procedimiento en la figura 10.
16. Método según la reivindicación 11, en el que cada etapa se lleva a cabo en una solución seleccionada de entre el grupo que consiste de un solvente orgánico y una mezcla de un solvente orgánico y un solvente acuoso.
17. Método según la reivindicación 11, en el que Y es -C(O)NH2.
Patentes similares o relacionadas:
Secuenciación por síntesis usando óptica de lectura por pulsos, del 19 de Febrero de 2020, de IBIS BIOSCIENCES, INC: Un sistema para fotoescindir y explorar análogos de nucleótidos que comprende: a) un sustrato que comprende una pluralidad de pocillos que contienen cada uno, o están configurados […]
Conjugado de péptido-resina y su utilización, del 18 de Septiembre de 2019, de Chemical & Biopharmaceutical Laboratories of Patras S.A: Un procedimiento para preparar un péptido, o una sal del mismo, de un conjugado de péptido-resina de las Fórmulas (2b), (2c), (2d), (2e) o (2f),**Fórmula** […]
Polipéptidos de relaxina modificados y sus usos, del 5 de Junio de 2019, de AMBRX, INC: Un polipéptido de relaxina modificado que comprende un aminoácido codificado de modo no natural, en donde: (a) el polipéptido de relaxina comprende el polipéptido de cadena […]
Conjugados de polisacáridos y proteínas acoplados reversiblemente a través de enlaces imina, del 3 de Abril de 2019, de THERAPURE BIOPHARMA INC.: Una composición de polisacárido oxidado-proteína para su uso como agente terapéutico o de diagnóstico, en donde la composición comprende un polisacárido oxidado […]
Procedimiento de síntesis de proteínas, del 5 de Marzo de 2019, de CENTRE NATIONAL DE LA RECHERCHE SCIENTIFIQUE (C.N.R.S.): Procedimiento de ensamblaje de fragmentos peptídicos para fabricar un polipéptido que comprende n fragmentos peptídicos y al menos n-1 aminoácidos […]
Procedimientos para la preparación de análogos de oxitocina, del 18 de Febrero de 2019, de F. HOFFMANN-LA ROCHE AG: Procedimiento para la preparación de análogos de oxitocina de fórmula I **Fórmula** en la que R1 es hidrógeno o alquilo C1-7 y R2 es hidrógeno […]
Método para preparar exenatida, del 29 de Octubre de 2018, de Hybio Pharmaceutical Co., Ltd: Un método para la preparación de exenatida, que se caracteriza por comprender las siguientes etapas: Etapa 1: se obtiene serina-resina mediante un primer […]
Síntesis de péptidos en fase sólida con BOC y FMOC, del 18 de Septiembre de 2018, de Ipsen Manufacturing Ireland Limited: Un método para preparar un péptido de fórmula H-D-β-Nal-[Cys-Tyr-D-Trp-Lys-Val-Cys]-Thr-NH2, en donde dicho método comprende las etapas de: (a) anclar […]