METODOS PARA ACTIVAR CELULAS NKT.
iGb3 para uso en el tratamiento de trastornos cancerosos, infecciosos o autoinmunes al activar la célula NKT que comprende poner en contacto la célula NKT con una cantidad suficiente de iGb3 para inducir secreción de una citoquina proveniente de la célula NKT,
estimular la proliferación de la célula NKT o regular hacia arriba la expresión del marcador de la superficie celular sobre la célula NKT
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2005/031407.
Solicitante: THE UNIVERSITY OF CHICAGO
THE SCRIPPS RESEARCH INSTITUTE
BRIGHAM YOUNG UNIVERSITY.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 5801 SOUTH ELLIS AVENUE,CHICAGO, ILLINOIS 60637.
Inventor/es: BENDELAC,ALBERT, ZHOU,DAPENG, TEYTON,LUC, SAVAGE,PAUL.
Fecha de Publicación: .
Fecha Concesión Europea: 14 de Abril de 2010.
Clasificación Internacional de Patentes:
- C12N5/06B11N
Clasificación PCT:
- A61K31/7032 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › unidos a un poliol, es decir compuestos que tienen varios grupos hidroxilo, libres o esterificados, incluyendo el grupo hidroxilo implicado en el enlace glicosídico, p. ej. monoglucosil-diacilglicéridos, ácido lactobiónico, gangliósidos.
- A61P35/00 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › Agentes antineoplásicos.
- A61P37/02 A61P […] › A61P 37/00 Medicamentos para el tratamiento de problemas inmunológicos o alérgicos. › Inmunomoduladores.
- A61P37/04 A61P 37/00 […] › Inmunoestimulantes.
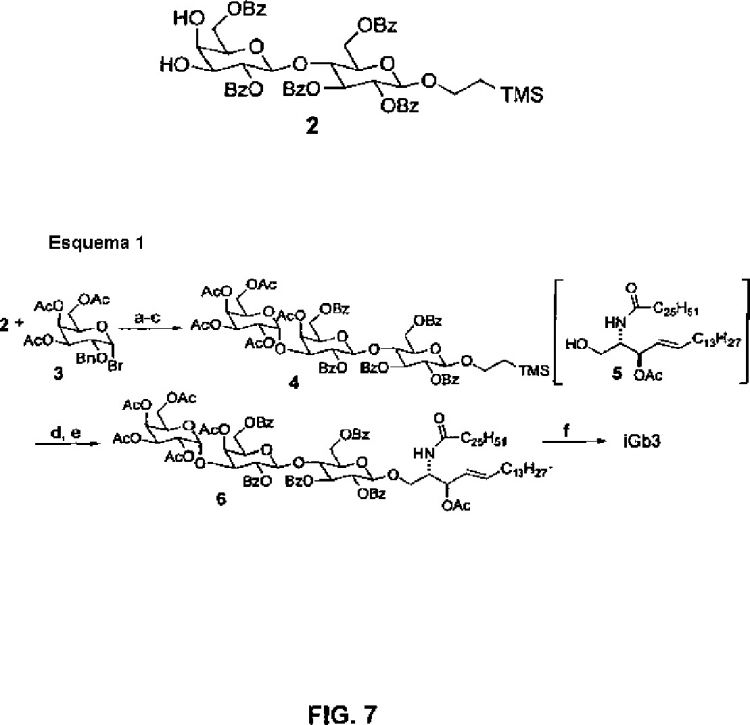
Fragmento de la descripción:
Métodos para activar células NKT.
Referencia cruzada a solicitudes relacionadas
La presente solicitud reivindica el beneficio de prioridad de la solicitud Provisional U.S. Serie No. 60/606,941, presentadas en septiembre 3, 2004, incorporada aquí como referencia.
Declaración con relación a investigación federalmente patrocinada
Esta invención fue hecha con soporte del gobierno de los Estados Unidos otorgado por Institutos Nacionales de Salud, bajo los otorgamientos P01 AL053725, RO1 AL38339 y AL50487. Los Estados Unidos tienen ciertos derechos en esta invención.
Introducción
La molécula CD1d es un miembro de la familia CD1 de las moléculas asociadas a microglobulina ß2. El contraste con las moléculas del complejo de histocompatibilidad principal clase I y clase II (MHC) que presentas los antígenos de péptido presentes a las células T CD8+ y CD4+, respectivamente, las moléculas CD1 han evolucionado para capturar y procesar tanto los antígenos extraños como auto lípido para desplegar un subconjunto particular de células ya conocidos de manera validas con células NKT, células T restringidas con CD1d, células NKT invariantes o iNKT. Las células NKT se caracterizan por reactividad de auto lípido y una respuesta efectuadoras rápidas. Las células NKT expresan tanto marcadores de superficie de célula cecinas naturales (NK) como un receptor de célula T semi-invariante conservado (TCR), específicamente, Va14-ja18 pareado con Vß8 en ratones y Va24-ja18 pareado con Vß11 en humanos.
La células NKT juegan un papel importante en un numero de funciones inmunes, que incluyen las respuestas antimicrobianas, la inmunidad antitumoral.
Y regular el balance entre la tolerancia y el auto inmunidad. Ellas expresan un fenotipo de memoria natural típicamente asociado con el reconocimiento auto reactivo y los ligandos endógenos conservados.
Un número de agonistas naturales y sintéticos para las células NKT se han reportado. El compuesto prototípico utilizado para estudiar la activación de la célula NKT in vitro e in vivo es KRN 7000, un a-galactosilceramida (aGalCer) originalmente aislada de la esponja marina Agelas mauritianus (Kawano, et al., Proc. Natl. Acad. Sci. 278, 1626-29(1997); see also U.S. Patent No. 6,531, 453 to Taniguchi et al.). El trabajo previo también a establecido el requisito para el tráfico Lisosómico de las moléculas CD1d (Chiu, YH et al., Nat. Immunol. 3,55-60(2002)), y los papeles de la propiedad lisosómica (Honey, K et al., Nat. Immunol. 3, 1069-74 (2002)) y las proteínas spingolipidas o saposinas (Zhou, D et al., Science 303, 523-27(2004); Kang SJ et al., Nat Immunol. 5, 175-81 (2004); Winau F et al., Nat. Immunol. 5, 169-74 (2004)). Sin embargo, el ligando natural del receptor de la célula NKT no ha sido previamente identificado.
Ogiso et al., Exp. Eye Res., Academia Press Ltd., 60(2), 193-198, 1995 describe la identificación caracterización de glicoespingolípidos neutros aislado de lentes de rata y analiza las relaciones estructurales entre seis de los glicoespingolípidos neutros identificados. Sin embargo Ogiso et al. no relaciona al iGb3 o su precursor.
La EP 0 988 860, de Van Dommelen et al. J. of Virology 2003, 77(3). 1877 y Smyth et al. Current opinion in Immunology 2002, 14, 165 describe el uso de células NKT activas aGalCer en el tratamiento de enfermedades autoinmunes, infecciones y cáncer. Sin embargo, estos documentos no se relacionan con el iGb3 o su precursor.
Resumen de la invención
Se describe aquí el descubrimiento de los inventores desligando al receptor de célula NKT natural, isoglobotrihexosilceramida (iGb3), un glicoespingolípidos lisosómicos de la función previamente desconocida. No solamente este descubrimiento suministra una herramienta investigativa para estudiar y elucidar la función de la células NKT en contextos múltiples (por ejemplo, enfermedades cancerosas, infecciosas y autoinmunes), si no también suministra una base para la aproximación terapéutica de estas condiciones también.
De acuerdo con esto, se describen aquí métodos para activar la célula NKT que incluye la etapa de poner en contacto la célula NKT con un cantidad suficiente de iGb3 para inducir la secreción de una citoquina proveniente de una célula NKT, estimular la proliferación de las células NKT o la expresión de la regulación hacia arriba de un marcador de superficie celular de la célula NKT.
En otro aspecto, la invención suministra iGb3 para uso en el tratamiento de trastornos cancerosos, infecciones o autoinmunes al activar la célula NKT que comprende poder en contacto la célula NKT con una cantidad suficiente de iGb3 para inducir la secreción de citoquina proveniente de la célula NKT, estimular la proliferación de célula NKT o la expresión de la regulación hacia arriba de el marcador de superficie celular de la célula NKT.
Breve descripción de las figuras
La Figura 1A presenta los perfiles FACS representativos que demuestran la selección tímica deficiente de las células Va14 NKT en el ratones Hexb-/-. Los porcentajes indican en los cuadrantes superiores. Los datos son representativos de cinco pares de compañeros de camada examinados en tres experimentos separados.
La Figura 1B representa los perfiles FACS de los esplenocitos y timocitos teñidos para CD4/CD8 y CD4/CD44 en el ratón es Hexb-/-.
La Figura 2A describe las respuestas alternativas del Va14 ND32.D3 y los hibridomas TCBII-no Va14 contra los timocitos de CD1d- de los compañeros de camada Hexb-/- y Hexb-/-.
La Figura 2B describe las respuestas al estimulo del hibridoma de Va14 DN32.D3 a la células de baso del Hexb-/- (
La Figura 3A es un esquema de la síntesis de iGb3in de Golgi (flechas punteadas, derecha,) y su regradación en el lisosoma (flechas continuas, izquierda). De la puerta superior a la inferior, el iGb4, iGb3 y la Lactosil ceramida.
La Figura 3B describe la frecuencia del hVa24 NKT PBL, doblemente teñido mediante anti-Va24 y CD1d-aGalCer de tetrámeros, en PBMC cultivado durante 4 días en la presencia de 100 ng/ml aGalCer, iGb3, o medio solo como se indicó.
La Figura 3C el panel izquierdo describe la producción IFN-? mediante la línea Va24 NKT humana estimulada con un rango de concertación de iGb3 y aGalCer en la presencia de PBMC como las células que presentan antígeno que expresan CD1d. El panel de la derecha describe la producción de IFN-? vs. IL-4 por la línea de Va24 NKT humana en respuesta al PBMC radiado y 100 ng/ml de iGb3 de origen sintético, purificado y enzimático vs 100/ml de aGalCer, Gb3 o LacCer, como se indicó.
La figura 4A describe la estimulación de ratón de Va14 hibridoma DN32.D3 mediante iGb3 e iGb4 con este derivado de medula ósea DC como CD1d- que expresa antígeno-que presenta células de Hexb-/-, Hexb-/- y ratón CD1-TD como se indicó.
La Figura 4B describe el estimulo de hibridoma Va14 de ratón DN32.D3 mediante iGb3 con células dendríticas derivadas de médula ósea provenientes de compañeros de camada deficientes en (Sap -/-) y insuficientes (Sap -/-), como se indicó.
Figura 4C el panel de la izquierda describe la carga in vitro de iGb3 e iGb4 sobre el CD1d recombinante en la presencia de saposina B, visualizado mediante isoelectroenfoque. El cambio de electro movilidad indica el reemplazo parcial del GTI b mediante iGb3 y iGb4, como se indicó. El panel de la derecha muestra la presentación libre de célula DN32.D3 de iGb3 y iGb4 mediante el CD1d unido aplaca en la presencia saposinas B, como se indicó.
La Figura 5A panel de la izquierda describe la inhibición especifica mediante el IB4 de la estimulación de la línea Va24 NKT humana mediante el iGb3 pero no en PBMC pulsado con aGalCer. El panel de la derecha muestra la inhibición del CD1 d anti-humano de mAb tanto de la estimulación iGb3 como aGalCer.
La figura 5B describe la inhibición especifica de la respuesta autoreactiva del CD1d del Va14+DN32.D3 pero no de los hibridomas no-Va14 TCB 11 y TBA7 al RBL.CD1d mediante isolectina....
Reivindicaciones:
1. iGb3 para uso en el tratamiento de trastornos cancerosos, infecciosos o autoinmunes al activar la célula NKT que comprende poner en contacto la célula NKT con una cantidad suficiente de iGb3 para inducir secreción de una citoquina proveniente de la célula NKT, estimular la proliferación de la célula NKT o regular hacia arriba la expresión del marcador de la superficie celular sobre la célula NKT.
2. iGb3 para uso en el tratamiento de trastornos cancerosos, infecciosos o autoinmunes de acuerdo con la reivindicación 1, en donde el iGb3 es purificado o sintético.
3. iGb3 para uso en el tratamiento de trastornos cancerosos, infecciosos o autoinmunes de acuerdo con la reivindicación 1 o 2, en donde poner en contacto la célula NKT comprende poner en contacto un receptor de célula T y la célula NKT.
4. iGb3 para uso en el tratamiento de trastornos cancerosos, infecciosos o autoinmunes a una cualquiera de las reivindicaciones 1 a 3, en donde el iGb3 se presentó a la célula NKT mediante una célula que presenta antígeno que comprende una molécula CD1d.
5. iGb3 para uso en el tratamiento de trastornos cancerosos, infecciosos o autoinmunes de acuerdo con la reivindicación 4, en donde la célula que presenta antígeno es una célula dendrítica.
6. iGb3 para uso en el tratamiento de trastornos cancerosos, infecciosos o autoinmunes de acuerdo con la reivindicación 5, en donde un precursor iGb3 es suministrado a la célula que antígeno para producir iGb3.
7. iGb3 para uso en el tratamiento de trastornos cancerosos, infecciosos o autoinmunes de acuerdo con la reivindicación 6, en donde un precursor iGb3 es iGb4.
8. iGb3 para uso en el tratamiento de trastornos cancerosos, infecciosos o autoinmunes de acuerdo con la reivindicación 1 a 7, en donde las células NKT es cultivada ex vivo.
9. iGb3 para uso en el tratamiento de trastornos cancerosos, infecciosos o autoinmunes de acuerdo con la reivindicación 1, en donde la citoquina se selecciona el grupo que consiste de IL-1, IL-2, IL-4, IL-5, IL-6, IL-10, IL-13, IL-15, TNF-a, TNF-ß, IFN-? y combinaciones de las mismas.
10. iGb3 para uso en el tratamiento de trastornos cancerosos, infecciosos o autoinmunes de acuerdo a una cualquiera de las reivindicaciones 1 a 9, en donde el marcador de superficie celular es CD69, CD25 un receptor IL-12 o CD40L.
11. iGb3 para uso en el tratamiento de trastornos cancerosos, infecciosos o autoinmunes de acuerdo con la reivindicación 1, en donde la célula NKT es cultivada in vitro.
12. iGb3 o precursor iGb3 para uso en el tratamiento de trastornos cancerosos, infecciosos o autoinmunes.
13. iGb3 para uso en el tratamiento de trastornos cancerosos, infecciosos o autoinmunes de acuerdo con la reivindicación 12, en donde el iGb3 se purifica o se sintetiza.
14. iGb3 para uso en el tratamiento de trastornos cancerosos, infecciosos o autoinmunes de acuerdo con la reivindicación 12, en donde el precursor es iGb3 también se purifica o se sintetiza.
15. iGb3 para uso en el tratamiento de trastornos cancerosos, infecciosos o autoinmunes de acuerdo con la reivindicación 14, en donde el precursor es iGb4.
Patentes similares o relacionadas:
CÉLULAS NKT NO CONVENCIONALES PARA SU USO EN TERAPIA CONTRA EL CÁNCER, del 8 de Noviembre de 2011, de INSERM (INSTITUT NATIONAL DE LA SANTE ET DE LA RECHERCHE SCIENTIFIQUE): Uso de células NKT independientes de CD1d, para la preparación de una composición farmacéutica para el tratamiento de un tumor en un paciente
 GRANZIMA B DEPENDIENTE DE PEPTIDOS HSP70/HSP70 COMO INDUCTORA DE APOPTOSIS EN CELULAS TUMORALES, del 1 de Junio de 2010, de MULTHOFF, GABRIELE, PROF. DR.: Procedimiento ex vivo de inducción o mejora de la expresión de la granzima B en células natural killer (NK) que comprende poner en contacto células NK con
(a)proteína […]
GRANZIMA B DEPENDIENTE DE PEPTIDOS HSP70/HSP70 COMO INDUCTORA DE APOPTOSIS EN CELULAS TUMORALES, del 1 de Junio de 2010, de MULTHOFF, GABRIELE, PROF. DR.: Procedimiento ex vivo de inducción o mejora de la expresión de la granzima B en células natural killer (NK) que comprende poner en contacto células NK con
(a)proteína […]
Formas cristalinas de 6-((6,7-dimetoxiquinazolin-4-il)oxi)-N,2-dimetilbenzofuran-3-carboxamida, del 29 de Julio de 2020, de Hutchison Medipharma Limited: Forma I de 6-((6,7-dimetoxiquinazolin-4-il)oxi)-N,2-dimetilbenzofuran-3-carboxamida, en donde el difractograma de rayos X de polvo de la Forma […]
Compuestos y procedimientos de uso, del 29 de Julio de 2020, de Medivation Technologies LLC: Un compuesto de fórmula (Aa-1): **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, en la que: A representa H, halógeno, amino, […]
Complejos de agentes terapéuticos de base vírica y poli(beta-amino-ésteres) modificados, del 29 de Julio de 2020, de Sagetis Biotech, SL: Un complejo de un agente terapéutico de base vírica con un polímero de fórmula I: **(Ver fórmula)** donde cada L1 y L2 están seleccionados […]
Compuestos de alquinilbenceno heterocíclicos, y composiciones médicas y usos de los mismos, del 29 de Julio de 2020, de Guangzhou Healthquest Pharma Co., Ltd: Un compuesto de alquinilbenceno heterocíclico que tiene la fórmula (I) y una sal farmacéuticamente aceptable, o estereoisómero del mismo, **(Ver […]
 Composiciones y métodos para el tratamiento de trastornos de células plasmáticas y trastornos prolinfocíticos de células b, del 29 de Julio de 2020, de Knopp Biosciences LLC: Una composición que comprende una cantidad terapéuticamente eficaz de dexpramipexol para su uso en el tratamiento de un trastorno de células B caracterizado por niveles elevados […]
Composiciones y métodos para el tratamiento de trastornos de células plasmáticas y trastornos prolinfocíticos de células b, del 29 de Julio de 2020, de Knopp Biosciences LLC: Una composición que comprende una cantidad terapéuticamente eficaz de dexpramipexol para su uso en el tratamiento de un trastorno de células B caracterizado por niveles elevados […]
Derivados de piperidina 1,4 sustituidos, del 29 de Julio de 2020, de 89Bio Ltd: Un compuesto de acuerdo con la Fórmula I: **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, en donde: A se selecciona de […]