CONJUGADOS QUE COMPRENDEN UN ANTICUERPO ESPECIFICO PARA EL DOMINIO ED-B DE FIBRONECTINA Y SU USO PARA LA DETECCION Y TRATAMIENTO DE TUMORES.
Un compuesto que comprende un péptido que comprende
aa) un sitio de fijación de antígeno para el dominio extra B (ED-B) de fibronectina que comprende regiones determinantes de la complementariedad HCDR3 y/o LCDR3 como se muestran en la Tabla 1 o una variación de las mismas que es una deleción,
inserción y/o sustitución de hasta 5 aminoácidos para la región HCDR3 y hasta 6 aminoácidos para la región LCDR3, que tiene la misma función que un péptido de acuerdo con Seq. Id. No. 1,
ab) un sitio de fijación de antígeno para el dominio extra B (ED-B) de fibronectina que comprende regiones determinantes de la complementariedad HCDR1, HCDR2, HCDR3, LCDR1, LCDR2 y LCDR3 como se muestran en la Tabla 1 o una variación de las mismas que es una deleción, inserción y/o sustitución de hasta 3 aminoácidos para la región HCDR1, hasta 8 aminoácidos para la región HCDR2, hasta 5 aminoácidos para la región HCDR3, hasta 6 aminoácidos para la región LCDR1, hasta 4 aminoácidos para la región LCDR2 y hasta 6 aminoácidos para la región LCDR3 que tiene la misma función que un péptido de acuerdo con Seq. Id. No. 1; o
ac) una secuencia de acuerdo con Seq. Id. No. 1 (L19) o una variación de Seq. Id. No. 1 que es una deleción, inserción y/o sustitución de hasta 30 aminoácidos, y que tiene la misma función que un péptido de acuerdo con Seq. Id. No. 1,
y la secuencia de aminoácidos Gly-Gly-Gly-Cys-Ala (Seq. Id. No. 7), en donde el término C de aa), ab) o ac) está fijado al término N de la secuencia de aminoácidos Seq. Id. No. 7 por un enlace peptídico
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/EP03/00009.
Solicitante: BAYER SCHERING PHARMA AKTIENGESELLSCHAFT.
Nacionalidad solicitante: Alemania.
Dirección: MULLERSTRASSE 178,13353 BERLIN.
Inventor/es: HILGER, CHRISTOPH-STEPHAN, DINKELBORG, LUDGER, BERNDORFF, DIETMAR, MOOSMAYER,DIETER,SCHERING AKTIENGESELLSCHAFT, NERI,GIOVANNI,PHILOGEN S.R.L.
Fecha de Publicación: .
Fecha Concesión Europea: 18 de Agosto de 2010.
Clasificación PCT:
- A61K47/48
- A61K51/10 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 51/00 Preparaciones que contienen sustancias radioactivas utilizadas para la terapia o para el examen in vivo. › Anticuerpos o inmunoglobulinas; Sus fragmentos.
- A61P35/00 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › Agentes antineoplásicos.
- C07K19/00 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › Péptidos híbridos (Inmoglobulinas híbridas compuestas solamente de inmoglobulinas C07K 16/46).
Clasificación antigua:
Fragmento de la descripción:
Conjugados que comprenden un anticuerpo específico para el dominio ED-B de fibronectina y su uso para la detección y tratamiento de tumores.
Campo de la invención
La presente invención se refiere a la diagnosis y el tratamiento de tumores, utilizando nuevos péptidos para fijación de radionucleidos.
Breve descripción de la técnica anterior
Los tumores no pueden alcanzar más de cierto peso sin la formación de nuevos vasos sanguíneos (angiogénesis) y se ha consignado una correlación entre la densidad de microvasos y la invasividad tumoral para varios tumores (Folkman (1995), Nature Med., 1, 27-31). Además, la angiogénesis está involucrada en la mayoría de los trastornos oculares que dan como resultado pérdida de visión (Lee et al., Surv. Ophthalmol. 43, 245 - 269 (1998); Friedlander, M. et al., Proc. Natl. Acad. Sci. U.S.A. 93, 9764 - 9769 (1996)). Las moléculas capaces de direccionar selectivamente marcadores de angiogénesis podrían crear oportunidades clínicas para la diagnosis y terapia de los tumores y otras enfermedades caracterizadas por proliferación vascular, tales como la retinopatía diabética y la degeneración macular relacionada con el envejecimiento. Los marcadores de angiogénesis se expresan en la mayoría de los tumores sólidos agresivos en asociación con vasos tumorales y deberían ser por consiguiente fácilmente accesibles a ligantes específicos inyectados por vía intravenosa (Pasqualini et al., (1997), Nature Biotechnol., 15, 542 - 546; Neri et al. (1997), Nature Biotechnol., 15, 1271 - 1275). La oclusión direccionada de la neovasculatura puede dar como resultado el infarto y el colapso del tumor (O'Reilly et al. (1996), Nature Med., 2, 689 - 692; Huang et al. (1997), Science, 275, 547 - 550.
El dominio ED-B de fibronectina, una secuencia de 91 aminoácidos idéntica en ratón, rata y humanos, que se inserta por corte y empalme alternativos en la molécula de fibronectina, se acumula específicamente alrededor de estructuras neo-vasculares (Castellani et al. (1994), Int. J. Cancer 59, 611-618) y podría representar una diana para la intervención molecular. De hecho, se ha demostrado recientemente con técnicas fluorescentes que fragmentos de anticuerpos Fv anti-ED-B monocatenarios (scFv) se acumulan selectivamente alrededor de los vasos sanguíneos tumorales de ratones portadores de tumores, y que la afinidad de anticuerpos parece dictar la eficiencia de direccionamiento (Neri et al. (1997), Nature Biotechnol., 15, 1271-1275; WO 97/45544).
Adicionalmente, los anticuerpos y fragmentos de anticuerpos específicos para fijación del dominio ED-B de la fibronectina con una constante de disociación sub-nanomolar, así como derivados radiomarcados de los mismos se describen en WO 99/58570. La biodistribución de uno de estos fragmentos de anticuerpos humanos de afinidad alta, el fragmento de anticuerpo marcado con 125I denominado L19, fue investigada ya en ratones portadores de tumores (Tarli et al., Blood, Vol. 94, No. 1 (1999), p. 192-198). Conjugados radiomarcados que comprenden anticuerpos L19 y su uso para la detección y el tratamiento de la angiogénesis se describen en WO 01/62800.
La producción recombinante de fragmentos de anticuerpos Fv monocatenarios funcionalizados que se fijan al dominio ED-B de la isoforma B de fibronectina en Pichia pastoris ha sido ya descrita (Marty et al., Protein Expression and Purification 21, 156-164 (2001)).
Adicionalmente, la radiomarcación de fragmentos de anticuerpo scFv con 99mTc por un péptido cisteinilo C-terminal fue descrita por George et al., Proc. Natl. Acad. Sci. USA, Vol. 92 pp. 8358 - 8362, 1995, and por Verhaar et al., J. Nuc. Med., Vol. 37(5), pp. 868 - 872, 1996.
Sin embargo, existe todavía necesidad clínica de proporcionar fragmentos de anticuerpo que tengan propiedades farmacocinéticas mejoradas, y que puedan marcarse fácilmente con radioisótopos de v.g. tecnecio o renio, dado que estos radionucleidos son particularmente adecuados para productos radiofarmacéuticos.
Objeto de la invención
Es por consiguiente un objeto de la invención proporcionar fragmentos de anticuerpo que tienen propiedades farmacocinéticas mejoradas, particularmente especificidad de diana y/o estabilidad in vivo, y que pueden fijar fácilmente radioisótopos, v.g. de tecnecio o renio.
Sumario de la invención
La presente invención se define en las reivindicaciones 1-18.
Los compuestos son preferiblemente fragmentos de anticuerpo monocatenarios, particularmente fragmentos scFv. Adicionalmente, los compuestos están conjugados preferiblemente a un radioisótopo, v.g. un radioisótopo de tecnecio, tal como 94mTc, 99mTc, renio, tales como 186Re, 188Re, u otros isótopos, tales como 203Pb, 67Ga, 68Ga, 43Sc, 44Sc, 47Sc, 110mIn, 111In, 97Ru, 62Cu, 64Cu, 67Cu, 68Cu, 86Y, 88Y, 90Y, 121Sn, 161Tb, 153Sm, 166Ho, 105Rh, 177Lu, 72As y 18F.
La presente invención describe también una composición farmacéutica que comprende el compuesto anterior como agente activo junto con adyuvantes, diluyentes y/o vehículos fisiológicamente aceptables.
La presente invención describe también el uso de un péptido como se define en las reivindicaciones 11-13.
El fragmento de anticuerpo L19 se define por la secuencia siguiente (Seq. Id. No. 1):

Una deleción, inserción y/o sustitución de hasta 30 aminoácidos es una deleción, inserción y/o sustitución de 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29 o 30 aminoácidos de Seq. Id. No. 1. Sin embargo, dentro de las regiones determinantes de complementariedad (CDRs) el péptido reivindicado, v.g. el péptido de Seq. Id. No. 1, una variación que es una deleción, inserción y/o sustitución de aminoácidos (aa) no debería exceder de las variaciones máximas definidas a continuación en la Tabla 1 (HCDR: CDR de la cadena pesada; LCDR: CDR de la cadena ligera).
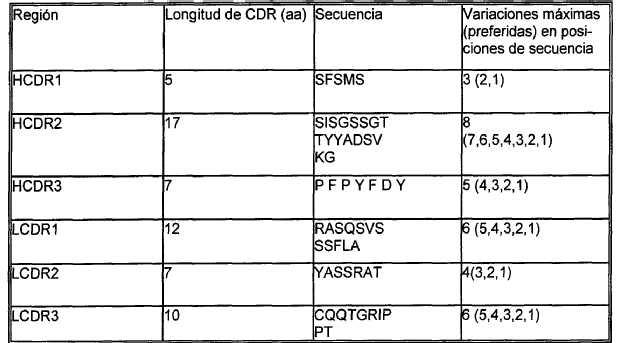
Las CDRs se definieron de acuerdo con E. A. Kabat et al., "Sequences of Proteins of Immunological Interest", U.S. Department of Health and Human Services, National Institutes for Health, Bethesda, MD, 5ª edición, 1991.
Se prefieren péptidos que comprenden una secuencia de acuerdo con Seq. Id. No. 1 (L19) o una variación de Seq. Id. No. 1 que es una deleción, inserción y/o sustitución de hasta 20 aminoácidos.
Un péptido que comprende una variación de las secuencias CDR como se muestran en la Tabla 1 y particularmente una variación de Seq. Id. No. 1 que es una deleción, inserción y/o sustitución, y que tiene la misma función que el péptido de acuerdo con Seq. Id. No. 1, se define como un péptido que se fija al dominio ED-B de fibronectina con una constante de disociación Kd que está comprendida en el intervalo subnanomolar (es decir < 10-9), medida con un instrumento BIAcore (véase WO 99/58570, Ejemplo 2 y Tabla 2).
Secuencias de aminoácidos preferidas Xaa1-Xaa2-Xaa3-Cys (Seq. Id. No. 2) son las secuencias Gly-Gly-Gly-Cys (Seq. Id. No. 5) y Gly-Cys-Gly-Cys (Seq. Id. No. 6). Es muy preferida la secuencia Gly-Gly-Gly-Cys (Seq. Id. No. 5).
Secuencias de aminoácidos preferidas Xaa1-Xaa2-Xaa3-Cys-Xaa4 (Seq. Id. No. 3) son las secuencias Gly-Gly-Gly-Cys-Ala (Seq. Id. No. 7) y Gly-Cys-Gly-Cys-Ala (Seq. Id. No. 8). Es muy preferida la secuencia Gly-Gly-Gly-Cys-Ala (Seq. Id. No. 7).
En los compuestos que comprenden una secuencia de aminoácidos (His)n (Seq. Id. No. 4), se prefieren aquellos compuestos en los cuales n representa el número entero 6.
Radioisótopos preferidos de tecnecio o renio son los isótopos 94mTc, 99mTc, 186Re y 188Re. El más preferido es el radioisótopo 99mTc.
Descripción detallada de la invención
Reivindicaciones:
1. Un compuesto que comprende un péptido que comprende
y la secuencia de aminoácidos Gly-Gly-Gly-Cys-Ala (Seq. Id. No. 7), en donde el término C de aa), ab) o ac) está fijado al término N de la secuencia de aminoácidos Seq. Id. No. 7 por un enlace peptídico.
2. El compuesto de acuerdo con la reivindicación 1 que está conjugado a un radioisótopo.
3. El compuesto de acuerdo con la reivindicación 1 ó 2, que está conjugado a un radioisótopo seleccionado de un radioisótopo de tecnecio, tal como 94mTc, 99mTc, renio, tal como 186Re, 188Re u otros isótopos tales como 203Pb, 67Ga, 68Ga, 43Sc, 44Sc, 47Sc, 110mIn, 111In, 97Ru, 62Cu, 64Cu, 67Cu, 68Cu, 86Y, 88Y, 90Y, 121Sn, 161Tb, 153Sm, 166Ho, 105Rh, 177Lu, 72As y 18F.
4. Un compuesto de acuerdo con la reivindicación 3, en donde el radioisótopo es 99mTc o 188Re.
5. El compuesto de acuerdo con una cualquiera de las reivindicaciones 1-4, en donde el péptido está en forma reducido.
6. Una composición farmacéutica que comprende como agente activo un compuesto de acuerdo con una cualquiera de las reivindicaciones 1-5 junto con adyuvantes, vehículos y/o diluyentes fisiológicamente aceptables.
7. La composición de la reivindicación 6, que se excreta hasta un 70% o más a través de los riñones en 24 horas en los ratones.
8. La composición de la reivindicación 6 ó 7 que tiene una relación de tumor a sangre de 5:1 o más 5 h después de la administración en los ratones.
9. La composición de una cualquiera de las reivindicaciones 6-8 para aplicaciones diagnósticas.
10. La composición de una cualquiera de las reivindicaciones 6-8 para aplicaciones terapéuticas.
11. Uso de un péptido que comprende
y la secuencia de aminoácidos Gly-Gly-Gly-Cys-Ala (Seq. Id. No. 7), en donde el término C de aa), ab) o ac) está fijado al término N de Seq. Id. No. 7 por un enlace peptídico, para fijación de un radioisótopo.
12. El uso de acuerdo con la reivindicación 11, en donde el radioisótopo se selecciona de un radioisótopo de tecnecio, tal como 94mTc, 99mTc, renio, tal como 186Re, 188Re, u otros isótopos, tales como 203Pb, 67Ga, 68Ga, 43Sc, 44Sc, 47Sc, 110mIn, 111In, 97Ru, 62Cu, 64Cu, 67Cu, 68Cu, 86Y, 88Y, 90Y, 121Sn, 161Tb, 153Sm, 166Ho, 105Rh, 177Lu, 72As y 18F.
13. El uso de acuerdo con la reivindicación 12, en donde el radioisótopo es 99mTc o 188Re.
14. Un proceso para la producción de un péptido como se define en la reivindicación 1, caracterizado porque el péptido se expresa en células eucariotas, particularmente en células de levadura.
15. El proceso de acuerdo con la reivindicación 14, en donde las células eucariotas son células de Pichia pastoris.
16. El proceso de acuerdo con la reivindicación 14 ó 15, en donde el péptido se expresa constitutivamente.
17. El proceso de acuerdo con una cualquiera de las reivindicaciones 14-16, en donde el término N del péptido está fusionado directamente al sitio de escisión Kex2 de la secuencia señal a.
18. Un kit para la producción de productos radiofarmacéuticos que comprenden un péptido como se define en una cualquiera de las reivindicaciones 1-5, opcionalmente junto con adyuvantes fisiológicamente aceptables.
Patentes similares o relacionadas:
Derivados de piperidina 1,4 sustituidos, del 29 de Julio de 2020, de 89Bio Ltd: Un compuesto de acuerdo con la Fórmula I: **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, en donde: A se selecciona de […]
Profármacos de gemcitabina, del 29 de Julio de 2020, de NuCana plc: Una formulación farmacéutica que comprende gemcitabina-[fenil-benzoxi-L-alaninil)]-(S)-fosfato 3: **(Ver fórmula)** o una sal o solvato […]
Formas cristalinas de 6-((6,7-dimetoxiquinazolin-4-il)oxi)-N,2-dimetilbenzofuran-3-carboxamida, del 29 de Julio de 2020, de Hutchison Medipharma Limited: Forma I de 6-((6,7-dimetoxiquinazolin-4-il)oxi)-N,2-dimetilbenzofuran-3-carboxamida, en donde el difractograma de rayos X de polvo de la Forma […]
Compuestos y procedimientos de uso, del 29 de Julio de 2020, de Medivation Technologies LLC: Un compuesto de fórmula (Aa-1): **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, en la que: A representa H, halógeno, amino, […]
Complejos de agentes terapéuticos de base vírica y poli(beta-amino-ésteres) modificados, del 29 de Julio de 2020, de Sagetis Biotech, SL: Un complejo de un agente terapéutico de base vírica con un polímero de fórmula I: **(Ver fórmula)** donde cada L1 y L2 están seleccionados […]
Compuestos de alquinilbenceno heterocíclicos, y composiciones médicas y usos de los mismos, del 29 de Julio de 2020, de Guangzhou Healthquest Pharma Co., Ltd: Un compuesto de alquinilbenceno heterocíclico que tiene la fórmula (I) y una sal farmacéuticamente aceptable, o estereoisómero del mismo, **(Ver […]
 Composiciones y métodos para el tratamiento de trastornos de células plasmáticas y trastornos prolinfocíticos de células b, del 29 de Julio de 2020, de Knopp Biosciences LLC: Una composición que comprende una cantidad terapéuticamente eficaz de dexpramipexol para su uso en el tratamiento de un trastorno de células B caracterizado por niveles elevados […]
Composiciones y métodos para el tratamiento de trastornos de células plasmáticas y trastornos prolinfocíticos de células b, del 29 de Julio de 2020, de Knopp Biosciences LLC: Una composición que comprende una cantidad terapéuticamente eficaz de dexpramipexol para su uso en el tratamiento de un trastorno de células B caracterizado por niveles elevados […]
Terapias de combinación para el cáncer, del 22 de Julio de 2020, de MERCK SHARP & DOHME CORP: Una combinación que comprende un anticuerpo anti-PD-1 humano y un Compuesto A y un Compuesto B, en donde: el anticuerpo anti-PD-1 humano comprende […]