Derivados de dibenzo[b,f][1,4]oxazepina como inhibidores de histona desacetilasa.
Compuesto de fórmula (IV) o sal farmacéuticamente aceptable del mismo:
**Fórmula**
en la que:
R140 se selecciona del grupo que consiste en:
H y halo;
1 0 xa y xb indican números que se seleccionan cada uno independientemente de 0, 1 y 2;
R150 y R160 se seleccionan independientemente del grupo que consiste en H, halo, -CN, -CF3, -OCF3, -alquilo C1-C6, -alcoxilo C1-C6, -O-alquil C2-C6-O-R53, -OR53, -alquil C0-C6-S(O)0-2-R53, -alquil C0-C6-C(O)- R53, -alquil C0-C6-C(O)NR50R51, -alquil C0-C6-NR52C(O)-R53, -alquil C0-C6-S(O)2NR50R51, -alquil C0-C6-NR52S(O)2-R53, -alquil C0-C6-OC(O)NR50R51, -alquil C0-C6-NR52C(O)O-R53, -alquil C0-C6-NR52C(O)NR50R51, -alquil C0-C6-C(O)O-R53, -alquil C0-C6-OC(O)-R53, -alquil C0-C6-arilo, -alquil C0-C6-heteroarilo, -alquil C0-C6- cicloalquilo, -alquil C0-C6-heterociclilo, -NH2, -NR50R51, -alquil C1-C6-NR50R51, -O-alquil C2-C6-NR50R51, -NR53-alquil C2-C6-NR50R51 y -O-heterociclil-R53, en los que cada alquilo y heteroalquilo está opcionalmente sustituido con uno o tres sustituyentes seleccionados independientemente del grupo que consiste en F, -OH y oxo, y en los que cada arilo, heteroarilo, cicloalquilo y heterociclilo está opcionalmente sustituido con uno o dos sustituyentes seleccionados independientemente del grupo que consiste en halo, -CN, -alquilo C1-C4, -alcoxilo C1-C4, -O-alquil C2-C4-O-alquilo C1-C4, -CF3, -OCF3, -NO2, -alquil C1-C6-S(O)0-2R53, -NH2, -NR50R51, -alquil C1-C6-NR50R51 y -N(alquil C1-C6)2;
R50 y R51 se seleccionan independientemente del grupo que consiste en H, -alquilo C1-C6, -alquil C2-C6-O- alquilo C1-C6, -alquil C0-C6-cicloalquilo C3-C7, en los que cada alquilo y cicloalquilo está opcionalmente sustituido con uno o más sustituyentes seleccionados independientemente del grupo que consiste en halo, -OH, amino, -CN o -alquilo C1-C4;
o R50 y R51, junto con el átomo de N al que están unidos, forman opcionalmente un anillo heterocíclico de 3- 10 miembros, en el que el heterociclilo está opcionalmente sustituido con de uno a tres sustituyentes seleccionados independientemente del grupo que consiste en halo, -OH, amino, -CN o alquilo C1-C4;
R52 se selecciona independientemente del grupo que consiste en -H, -alquilo C1-C6, -alquil C2-C6-O-alquilo C1-C6, -alquil C0-C6-cicloalquilo C3-C7, en los que cada alquilo y cicloalquilo está opcionalmente sustituido con uno o más sustituyentes seleccionados independientemente del grupo que consiste en halo, -OH, amino, -CN o -alquilo C1-C4; y
R53 se selecciona independientemente del grupo que consiste en -alquilo C1-C6, -alquil C0-C4-cicloalquilo C3-C7, -alquil C0-C4-arilo, -alquil C0-C4-heteroarilo y -alquil C0-C4-heterociclilo, en los que cada alquilo, arilo, heteroarilo y heterociclilo está opcionalmente sustituido con uno o tres sustituyentes seleccionados independientemente del grupo que consiste en halo, -OH, amino, -CN o -alquilo C1-C4;
o un compuesto o una sal farmacéuticamente aceptable del mismo seleccionado del grupo que consiste en:
(Z)-4-(dibenzo[b,f][1,4]tiazepin-11-il)-N-hidroxibenzamida, N-hidroxi-4-(10-metil-10,11-dihidrodibenzo[b,f][1,4]oxazepin-11-il)benzamida,
Tipo: Patente Europea. Resumen de patente/invención. Número de Solicitud: E11152576.
Solicitante: METHYLGENE, INC..
Nacionalidad solicitante: Canadá.
Dirección: 1155 Rene-Levesque Blvd., W. Suite 400 Montreal QC H3B 3V2 CANADA.
Inventor/es: DEZIEL, ROBERT, SHAPIRO, GIDEON, CHESWORTH,RICHARD, TESSIER,PIERRE, MANCUSO,JOHN, SMIL,DAVID, LEIT,SILVANA, BEAULIEU,PATRICK, CHANTIGNY,YVES ANDRE.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C07D267/20 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07D COMPUESTOS HETEROCICLICOS (Compuestos macromoleculares C08). › C07D 267/00 Compuestos heterocíclicos que contienen ciclos de más de seis miembros que tienen un átomo de nitrógeno y un átomo de oxígeno como únicos heteroátomos del ciclo. › [b, f]-condensados.
- C07D281/16 C07D […] › C07D 281/00 Compuestos heterocíclicos que contienen ciclos de más de seis miembros que tienen un átomo de nitrógeno y un átomo de azufre como únicos heteroátomos del ciclo. › [b, f]-condensados.
PDF original: ES-2532899_T3.pdf
Fragmento de la descripción:
Derivados de dibenzo[b, f][1, 4]oxazepina como inhibidores de histona desacetilasa Referencia cruzada a solicitudes relacionadas Esta solicitud reivindica el beneficio de la solicitud estadounidense provisional 60/884287, presentada el 10 de enero de 2007, y la solicitud estadounidense provisional 60/863.347, presentada el 28 de octubre de 2006.
Antecedentes de la invención Campo de la invención Esta invención se refiere a compuestos para la inhibición de histona desacetilasa.
Descripción de la técnica relacionada En células eucariotas, el ADN nuclear se asocia con histonas para formar un complejo compacto denominado cromatina. Las histonas constituyen una familia de proteínas básicas que generalmente están altamente conservadas en todas las especies eucariotas. Las histonas núcleo, denominadas H2A, H2B, H3 y H4, se asocian formando un núcleo de proteína. Se enrolla ADN alrededor de este núcleo de proteína, interaccionando los aminoácidos básicos de las histonas con los grupos fosfato cargados negativamente del ADN. Aproximadamente 146 pares de bases de ADN envuelven un núcleo de histonas constituyendo una partícula de nucleosoma, el motivo estructural de repetición de la cromatina.
Csordas, Biochem. J., 286: 23-38 (1990) enseña que las histonas se someten a acetilación postraduccional de los residuos de lisina N-terminales, una reacción que se cataliza por la histona acetil transferasa (HAT1) . La acetilación neutraliza la carga positiva de la cadena lateral de la lisina, y se cree que tiene un impacto sobre la estructura de la cromatina. De hecho, Taunton et al., Science, 272: 408-411 (1996) , enseñan que el acceso de factores de transcripción a moldes de cromatina se potencia por la hiperacetilación de histonas. Taunton et al. enseñan además que se ha encontrado un enriquecimiento en histona H4 subacetilada en regiones silenciosas transcripcionalmente del genoma.
La acetilación de histonas es una modificación reversible, estando catalizada la desacetilación por una familia de enzimas denominadas histona desacetilasas (HDAC) . La clonación molecular de secuencias génicas que codifican para proteínas con actividad HDAC ha establecido la existencia de un conjunto de isoformas enzimáticas de HDAC diferenciadas. Grozinger et al., Proc. Natl. Acad. Sci. USA, 96:4868-4873 (1999) , enseñan que las HDAC pueden dividirse en dos clases, la primera representada por proteínas de tipo Rpd3 de levaduras, y la segunda representada por proteínas de tipo Hdl de levaduras. Grozinger et al. también enseñan que las proteínas HDAC-1, HDAC-2 y HDAC-3 humanas son miembros de la primera clase de HDACs y dan a conocer nuevas proteínas, denominadas HDAC-4, HDAC-5 y HDAC-6, que son miembros de la segunda clase de HDACs. Kao et al., Gene & Development 14:55-66 (2000) , dan a conocer un miembro adicional de esta segunda clase, denominada HDAC-7. Más recientemente, Hu, E. et al. J. Bio. Chem. 275:15254-13264 (2000) dieron a conocer otro miembro de la primera clase de histona desacetilasas, HDAC-8. Zhou et al., Proc. Natl. Acad. Sci. U.S.A., 98: 10572-10577 (2001) enseñan 45 la clonación y caracterización de una nueva histona desacetilasa, HDAC-9. Kao et al., J. Biol. Chem., 277:187-93 (2002) enseñan el aislamiento y la caracterización de HDAC10 de mamíferos, una histona desacetilasa novedosa. Gao et al, J. Biol. Chem. (en prensa) enseñan la clonación y caracterización funcional de HDAC11, un miembro novedoso de la familia de histona desacetilasa humana. Shore, Proc. Natl. Acad. Sci. U.S.A. 97: 14030-2 (2000) da a conocer otra clase de actividad desacetilsa, la familia de proteínas Sir2. No ha quedado claro qué papeles desempeñan estas enzimas HDAC individuales.
Estudios que utilizan inhibidores de HDAC conocidos han establecido un vínculo entre acetilación y expresión génica. Numerosos estudios han examinado la relación entre HDAC y expresión génica. Taunton et al., Science 272:408-411 (1996) , dan a conocer una HDAC humana que está relacionada con un regulador de la transcripción de 55 levaduras. Cress et al., J. Cell. Phys. 184:1-16 (2000) , dan a conocer que, en el contexto de cáncer en seres humanos, el papel de HDAC es como un correpresor de la transcripción. Ng et al., TIBS 25: Marzo (2000) , dan a conocer HDAC como característica dominante de sistemas de represores transcripcionales. Magnaghi-Jaulin et al., Prog. Cell Cycle Res. 4:41-47. (2000) , dan a conocer HDAC como corregulador transcripcional importante para la progresión del ciclo celular.
Richon et al., Proc. Natl. Acad. Sci. USA, 95: 3003-3007 (1998) , dan a conocer que la actividad HDAC se inhibe por tricostatina A (TSA) , un producto natural aislado de Streptomyces hygroscopicus, que se ha mostrado que inhibe la actividad histona desacetilasa y detiene la progresión del ciclo celular en células en las fases G1 y G2 (Yoshida et al., J. Biol. Chem. 265: 17174-17179, 1990; Yoshida et al., Exp. Cell Res. 177: 122-131, 1988) , y por un compuesto 65 sintético, ácido hidroxámico suberoilanilida (SAHA) . Yoshida y Beppu, Exper. Cell Res., 177: 122-131 (1988) , enseñan que TSA provoca la detención de fibroblastos de rata en las fases G1 y G2 del ciclo celular, lo que implica a
HDAC en la regulación del ciclo celular. De hecho, Finnin et al., Nature, 401: 188-193 (1999) , enseñan que TSA y SAHA inhiben el crecimiento celular, inducen diferenciación terminal e impiden la formación de tumores en ratones. Suzuki et al., patente estadounidense nº 6.174.905, documentos EP 0847992 y JP 258863/96, dan a conocer derivados de benzamida que inducen diferenciación celular e inhiben HDAC. Delorme et al., documentos WO
01/38322 y WO 2001/070675, dan a conocer compuestos adicionales que sirven como inhibidores de HDAC. Otros inhibidores de la actividad histona desacetilasa, incluyendo trapoxina, depudecina, FR901228 (Fujisawa Pharmaceuticals) y butirato, se ha encontrado que inhiben de manera similar la progresión del ciclo celular en células (Taunton et al., Science 272: 408-411, 1996; Kijima et al., J. Biol. Chem. 268 (30) :22429-22435, 1993; Kwon et al., Proc. Natl. Acad. Sci. USA 95 (7) :3356-61, 1998) .
La investigación en la última década ha descubierto una nueva clasificación de enfermedades neurodegenerativas heredadas, las enfermedades por expansión de poliglutaminas (poliQ) . En cada una, la mutación subyacente es una expansión de una repetición de trinucleótidos CAG que codifica para poliQ en la proteína de la enfermedad respectiva. Todos son trastornos progresivos, en última instancia mortales que comienzan normalmente en la edad
adulta y progresan a lo largo de 10 a 30 años. Las características clínicas y el patrón de degeneración neuronal difieren entre las enfermedades, aunque pruebas crecientes sugieren que las enfermedades de poliQ comparten características patogénicas importantes. En particular, conformaciones anómalas de las proteínas promovidas por la expansión de poliQ parecen ser centrales para la patogénesis. Esta clase de enfermedad neurodegenerativa de expansión de PoliQ son enfermedad de Huntington (HD) , atrofia dentato-rubro-pálido-luisiana (DRPLA) , atrofia muscular espinal y bulbar (SBMA) y cinco ataxias espinocerebelosas (SCA1, SCA2, SCA3/MJD (enfermedad de Machado-Joseph) , SCA6 y SCA7) .
Se sabe que determinados inhibidores de HDAC, por ejemplo SAHA, CBHA y prioxiamida pueden cruzar la barrera hematoencefálica en cantidades suficientes para inhibir significativamente la actividad HDAC provocando la acumulación de histonas acetiladas en el cerebro (documento WO 03/032921) . Este descubrimiento prevé por tanto el uso de inhibidores de HDAC para inhibir HDAC en el cerebro, para el tratamiento de enfermedades por expansión de poliglutaminas (poliQ) .
La técnica proporciona datos de que inhibidores de HDAC son agentes terapéuticos novedosos prometedores para enfermedades por expansión de poliglutaminas. Otros datos apoyan un beneficio terapéutico de inhibidores de HDAC para enfermedad de Huntington. Sadri-Vakili y Cha (Nature Clinical Practice Neurology, 2006, 2 (6) :330-338) , y referencias citadas en el mismo, por ejemplo, revisan el estado actual de conocimiento referente al estado de histonas en enfermedad de Huntington y enseñan que estudios recientes han mostrado un papel terapéutico para inhibidores de histona desacetilasa en varios modelos de enfermedad de Huntington. In vivo, inhibidores de HDAC
detienen la degeneración neuronal progresiva en curso inducida por expansión de repeticiones de poliglutamina, y reducen la mortalidad en dos modelos de Drosophila de enfermedad de poliglutamina (Steffan et al., 2001, Nature 413: 739-743) . Se observaron hallazgos similares con butirato de sodio y TSA (Zhao et al., 2005, J. Expt. Biol., 208:697-705)... [Seguir leyendo]
Reivindicaciones:
1. Compuesto de fórmula (IV) o sal farmacéuticamente aceptable del mismo:
en la que:
R140 se selecciona del grupo que consiste en: H y halo;
xa y xb indican números que se seleccionan cada uno independientemente de 0, 1 y 2;
150 160
Ry Rse seleccionan independientemente del grupo que consiste en H, halo, -CN, -CF3, -OCF3,
53 53
-alquilo C1-C6, -alcoxilo C1-C6, -O-alquil C2-C6-O-R, -OR, -alquil C0-C6-S (O) 0-2-R, -alquil C0-C6-C (O)
5051 5253 5051
R, -alquil C0-C6-C (O) NRR, -alquil C0-C6-NRC (O) -R, -alquil C0-C6-S (O) 2NRR, -alquil C0-C6
5253 5051 5253 525051
NRS (O) 2-R , -alquil C0-C6-OC (O) NRR, -alquil C0-C6-NRC (O) O-R, -alquil C0-C6-NRC (O) NRR,
53
-alquil C0-C6-C (O) O-R, -alquil C0-C6-OC (O) -R, -alquil C0-C6-arilo, -alquil C0-C6-heteroarilo, -alquil C0-C6
5051 5051 5051
cicloalquilo, -alquil C0-C6-heterociclilo, -NH2, -NRR, -alquil C1-C6-NRR, -O-alquil C2-C6-NRR,
535051 53
- NR-alquil C2-C6-NRRy -O-heterociclil-R, en los que cada alquilo y heteroalquilo está opcionalmente sustituido con uno o tres sustituyentes seleccionados independientemente del grupo que consiste en F, -OH y oxo, y en los que cada arilo, heteroarilo, cicloalquilo y heterociclilo está opcionalmente sustituido con uno o dos sustituyentes seleccionados independientemente del grupo que consiste en halo, -CN, -alquilo C1-C4,
-alcoxilo C1-C4, -O-alquil C2-C4-O-alquilo C1-C4, -CF3, -OCF3, -NO2, -alquil C1-C6-S (O) 0-2R, -NH2, -NRR, -alquil C1-C6-NR50R51 y -N (alquil C1-C6) 2;
51
Ry Rse seleccionan independientemente del grupo que consiste en H, -alquilo C1-C6, -alquil C2-C6-Oalquilo C1-C6, -alquil C0-C6-cicloalquilo C3-C7, en los que cada alquilo y cicloalquilo está opcionalmente sustituido con uno o más sustituyentes seleccionados independientemente del grupo que consiste en halo, -OH, amino, -CN o -alquilo C1-C4;
o 50 51
Ry R, junto con el átomo de N al que están unidos, forman opcionalmente un anillo heterocíclico de 310 miembros, en el que el heterociclilo está opcionalmente sustituido con de uno a tres sustituyentes seleccionados independientemente del grupo que consiste en halo, -OH, amino, -CN o alquilo C1-C4;
R52 se selecciona independientemente del grupo que consiste en -H, -alquilo C1-C6, -alquil C2-C6-O-alquilo C1-C6, -alquil C0-C6-cicloalquilo C3-C7, en los que cada alquilo y cicloalquilo está opcionalmente sustituido con uno o más sustituyentes seleccionados independientemente del grupo que consiste en halo, -OH,
amino, -CN o -alquilo C1-C4; y
R53 se selecciona independientemente del grupo que consiste en -alquilo C1-C6, -alquil C0-C4-cicloalquilo C3-C7, -alquil C0-C4-arilo, -alquil C0-C4-heteroarilo y -alquil C0-C4-heterociclilo, en los que cada alquilo, arilo, heteroarilo y heterociclilo está opcionalmente sustituido con uno o tres sustituyentes seleccionados 45 independientemente del grupo que consiste en halo, -OH, amino, -CN o -alquilo C1-C4;
o un compuesto o una sal farmacéuticamente aceptable del mismo seleccionado del grupo que consiste en:
(Z) -4- (dibenzo[b, f][1, 4]tiazepin-11-il) -N-hidroxibenzamida,
N-hidroxi-4- (10-metil-10, 11-dihidrodibenzo[b, f][1, 4]oxazepin-11-il) benzamida,
4. ( (10, 11-dihidrodibenzo[b, f][1, 4]oxazepin-11-il) -N-hidroxibenzamida, (Z) -3- (dibenzo[b, f][1, 4]oxazepin-11-il) -N-hidroxibenzamida, (E) -4- ( (dibenzo[b, f][1, 4]oxazepin-11-ilamino) metil) -N-hidroxibenzamida, (E) -4- (2- (dibenzo[b, f][1, 4]oxazepin-11-ilamino) etil) -N-hidroxibenzamida,
2. Compuesto según la reivindicación 1 o sal farmacéuticamente aceptable del mismo que tiene la fórmula V:
en la que: xc es 0 ó 1;y
R170 se selecciona del grupo que consiste en H, halo, -CN, -CF3, -OCF3, -alquilo C1-C6, -alcoxilo C1-C6, -O
53 53 53 5051
alquil C2-C6-O-R, -OR, -alquil C0-C6-S (O) 0-2-R, -alquil C0-C6-C (O) -R, -alquil C0-C6-C (O) NRR,
1253 5051 5253
-alquil C0-C6-NRC (O) -R, -alquil C0-C6-S (O) 2NRR, -alquil C0-C6-NRS (O) 2-R, -alquil C0-C6
5051 5253 525051 53
OC (O) NRR, -alquil C0-C6-NRC (O) O-R, -alquil C0-C6-NRC (O) NRR, -alquil C0-C6-C (O) O-R, -alquil C0-C6-OC (O) -R53, -alquil C0-C6-arilo, -alquil C0-C6-heteroarilo, -alquil C0-C6-cicloalquilo, -alquil C0-C6
5051 5051 5051 535051
heterociclilo, -NH2, -NRR, -alquil C1-C6-NRR, -O-alquil C2-C6-NRR, -NR-alquil C2-C6-NRRy -O-heterociclil-R53, en los que cada alquilo y heteroalquilo está opcionalmente sustituido con uno o tres sustituyentes seleccionados independientemente del grupo que consiste en F, -OH y oxo, en los que cada arilo, heteroarilo, cicloalquilo y heterociclilo está opcionalmente sustituido con uno o dos sustituyentes seleccionados independientemente del grupo que consiste en halo, -CN, -alquilo C1-C4, -alcoxilo C1-C4, -O
5051
alquil C2-C4-O-alquilo C1-C4, -CF3, -OCF3, -NO2, -alquil C1-C6-S (O) 0-2R, -NH2, -NRR, -alquil C1-C6
5051 50 53140150 160
NRRy -N (alquil C1-C6) 2, y xb, R-R, R, Ry Rson tal como se definen en la reivindicación 1.
3. Compuesto según la reivindicación 2 o sal farmacéuticamente aceptable del mismo que tiene la fórmula (VI) :
y en la que R170 es tal como se define en la reivindicación 2.
4. Compuesto o sal farmacéuticamente aceptable del mismo según la reivindicación 1 seleccionado del grupo que consiste en: (Z) -4- (dibenzo[b, f][1, 4]oxazepin-11-il) -N-hidroxibenzamida, (Z) -4- (2-fluorodibenzo[b, f][1, 4]oxazepin-11-il) -N-hidroxibenzamida, (Z) -N-hidroxi-4- (2-metoxidibenzo[b, f][1, 4]oxazepin-11-il) benzamida, (Z) -4- (2- (2- (dimetilamino) etoxi) dibenzo[b, f][1, 4]oxazepin-11-il) -N-hidroxibenzamida, (Z) -N-hidroxi-4- (8- (trifluorometil) dibenzo[b, f][1, 4]oxazepin-11-il) benzamida, (Z) -4- (dibenzo[b, f][1, 4]oxazepin-11-il) -2-fluoro-N-hidroxibenzamida, (Z) -N-hidroxi-4- (3-metoxidibenzo[b, f][1, 4]oxazepin-11-il) benzamida, (Z) -N-hidroxi-4- (8-metildibenzo[b, f][1, 4]oxazepin-11-il) benzamida, (Z) -N-hidroxi-4- (4-metoxidibenzo[b, f][1, 4]oxazepin-11-il) benzamida, (Z) -4- (9-fluorodibenzo[b, f][1, 4]oxazepin-11-il) -N-hidroxibenzamida, (Z) -N-hidroxi-4- (7- (trifluorometil) dibenzo[b, f][1, 4]oxazepin-11-il) benzamida, (Z) -4- (7-clorodibenzo[b, f][1, 4]oxazepin-11-il) -N-hidroxibenzamida, (Z) -4- (2-clorodibenzo[b, f][1, 4]oxazepin-11-il) -N-hidroxibenzamida, (Z) -4- (8-cianodibenzo[b, f][1, 4]oxazepin-11-il) -N-hidroxibenzamida, (Z) -N-hidroxi-4- (4-metildibenzo[b, f][1, 4]oxazepin-11-il) benzamida, (Z) -N-hidroxi-4- (3-metildibenzo[b, f][1, 4]oxazepin-11-il) benzamida, (Z) -4- (3-fluorodibenzo[b, f][1, 4]oxazepin-11-il) -N-hidroxibenzamida, (Z) -4- (8-clorodibenzo[b, f][1, 4]oxazepin-11-il) -N-hidroxibenzamida, (Z) -N-hidroxi-4- (3- (trifluorometil) dibenzo[b, f][1, 4]oxazepin-11-il) benzamida, (Z) -4- (6-fluorodibenzo[b, f][1, 4]oxazepin-11-il) -N-hidroxibenzamida,
(Z) -4- (7-cianodibenzo[b, f][1, 4]oxazepin-11-il) -N-hidroxibenzamida, (Z) -N-hidroxi-4- (4-hidroxidibenzo[b, f][1, 4]oxazepin-11-il) benzamida,
(Z) -N-hidroxi-4- (1-metoxidibenzo[b, f][1, 4]oxazepin-11-il) benzamida, (Z) -N-hidroxi-4- (4- (2-metoxietoxi) dibenzo[b, f][1, 4]oxazepin-11-il) benzamida, (Z) -4- (1-fluorodibenzo[b, f][1, 4]oxazepin-11-il) -N-hidroxibenzamida, (Z) -N-hidroxi-4- (4- (2-morfolinoetoxi) dibenzo[b, f][1, 4]oxazepin-11-il) benzamida, (Z) -4- (2-fluoro-4-metoxidibenzo[b, f][1, 4]oxazepin-11-il) -N-hidroxibenzamida, (Z) -N-hidroxi-4- (4- (metiltio) dibenzo[b, f][1, 4]oxazepin-11-il) benzamida, (Z) -N-hidroxi-4- (4- (trifluorometil) dibenzo[b, f][1, 4]oxazepin-11-il) benzamida, (Z) -N-hidroxi-4- (4- (metilsulfinil) dibenzo[b, f][1, 4]oxazepin-11-il) benzamida, (Z) -N-hidroxi-4- (4- (metilsulfonil) dibenzo[b, f][1, 4]oxazepin-11-il) benzamida, (Z) -N-hidroxi-4- (4-metoxi-8- (trifluorometil) dibenzo[b, f][1, 4]oxazepin-11-il) benzamida, (Z) -N-hidroxi-4- (3-morfolinodibenzo[b, f][1, 4]oxazepin-11-il) benzamida, (Z) -N-hidroxi-4- (4-propildibenzo[b, f][1, 4]oxazepin-11-il) benzamida, (Z) -N-hidroxi-4- (4- (trifluorometoxi) dibenzo[b, f][1, 4]oxazepin-11-il) benzamida, (Z) -N-hidroxi-4- (6-metildibenzo[b, f][1, 4]oxazepin-11-il) benzamida, (E) -4- (dibenzo[b, f][1, 4]oxazepin-11-il) -3-fluoro-N-hidroxibenzamida y (Z) -4- (4-fluorodibenzo[b, f][1, 4]oxazepin-11-il) -N-hidroxibenzamida.
5. Composición farmacéutica que comprende el compuesto según cualquier reivindicación anterior o una sal farmacéuticamente aceptable del mismo y un portador farmacéuticamente aceptable.
6. Método in vitro de inhibición de histona desacetilasa, comprendiendo el método poner en contacto la histona desacetilasa con el compuesto según una cualquiera de las reivindicaciones 1 a 4 o una sal farmacéuticamente aceptable del mismo.
7. Uso del compuesto según una cualquiera de las reivindicaciones 1 a 4 o una sal farmacéuticamente aceptable del mismo para la preparación de un medicamento para tratar una enfermedad por expansión de poliglutaminas.
8. Uso según la reivindicación 7, en el que la enfermedad por expansión de poliglutaminas es enfermedad de Huntington.
9. Compuesto según una cualquiera de las reivindicaciones 1 a 4 o sal farmacéuticamente aceptable del mismo para su uso en el tratamiento de una enfermedad por expansión de poliglutaminas.
10. Compuesto para su uso según la reivindicación 9, en el que la enfermedad por expansión de poliglutaminas es enfermedad de Huntington.
11. Compuesto o sal farmacéuticamente aceptable del mismo según la reivindicación 1, en el que el compuesto es (Z) -4- (dibenzo[b, f][1, 4]oxazepin-11-il) -N-hidroxibenzamida.
12. Composición farmacéutica que comprende el compuesto según la reivindicación 11 o una sal farmacéuticamente aceptable del mismo y un portador farmacéuticamente aceptable.
13. Método in vitro de inhibición de histona desacetilasa, comprendiendo el método poner en contacto la histona desacetilasa con el compuesto según la reivindicación 11 o una sal farmacéuticamente aceptable del mismo, o una composición según la reivindicación 12.
14. Uso del compuesto según la reivindicación 11 o una sal farmacéuticamente aceptable del mismo para la preparación de un medicamento para tratar una enfermedad por expansión de poliglutaminas.
15. Uso según la reivindicación 14, en el que la enfermedad por expansión de poliglutaminas es enfermedad de Huntington.
16. Uso según la reivindicación 14, en el que la enfermedad por expansión de poliglutaminas es atrofia dentatorubro-pálido-luisiana.
17. Uso según la reivindicación 14, en el que la enfermedad por expansión de poliglutaminas es ataxia espinocerebelosa de tipo 3.
18. Compuesto según la reivindicación 11 o sal farmacéuticamente aceptable del mismo para su uso en el
tratamiento de una enfermedad por expansión de poliglutaminas. 10
19. Compuesto para su uso según la reivindicación 18, en el que la enfermedad por expansión de poliglutaminas es enfermedad de Huntington.
20. Compuesto para su uso según la reivindicación 18, en el que la enfermedad por expansión de poliglutaminas es 15 atrofia dentato-rubro-pálido-luisiana.
21. Compuesto para su uso según la reivindicación 18, en el que la enfermedad por expansión de poliglutaminas es ataxia espinocerebelosa de tipo 3.
Patentes similares o relacionadas:
Haptenos de quetiapina para su uso en inmunoensayos, del 2 de Agosto de 2017, de JANSSEN PHARMACEUTICA N.V.: Un compuesto de Fórmula 1:**Fórmula** en el que: en el que R1 es H,**Fórmula** CH2NH2, o CH2NHC(O)(CH2)mCO2H; R2 es H,**Fórmula** CH2NH2, o CH2NHC(O)(CH2)mCO2H; […]
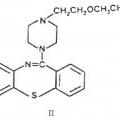 Procedimiento para preparar compuestos de tiazepina con actividad antidopaminérgica, del 12 de Agosto de 2015, de ASTRAZENECA AB: Procedimiento para preparar compuestos de tiazepina con actividad antidopaminérgica, de
fórmula II: **fórmula** o una sal del mismo, caracterizado porque comprende:
(a) […]
Procedimiento para preparar compuestos de tiazepina con actividad antidopaminérgica, del 12 de Agosto de 2015, de ASTRAZENECA AB: Procedimiento para preparar compuestos de tiazepina con actividad antidopaminérgica, de
fórmula II: **fórmula** o una sal del mismo, caracterizado porque comprende:
(a) […]
Derivado de dibenzotiazepina y sus usos, del 26 de Abril de 2013, de ASTRAZENECA AB: Un compuesto de Fórmula I:**Fórmula** donde Z es H, que es 2-fluoro-11-(piperazin-1-il)dibenzo[b,f][1,4]tiazepina o una sal farmacéuticamente aceptable […]
UN DERIVADO CRISTALINO DE DIBENZOTIAZEPINA Y SU USO COMO UN AGENTE ANTIPSICÓTICO, del 6 de Mayo de 2011, de ASTRAZENECA AB: Un compuesto que es 11-(4-[2-(2-hidroxietoxi)etil]-1-piperazinil)dibenzo[b,f][1,4]tiazepina cristalina
PROCESO PARA LA PREPARACIÓN DE 11-(4-[2-(2-HIDROXIETOXI)ETIL]-1-PIPERAZINIL)-DIBENZO[B,F][1,4]TIAZEPINA, del 31 de Enero de 2011, de SK HOLDINGS CO., LTD: Un proceso para la preparación de 11-(4-[2-(2-hidroxietoxi)etil]-1-piperazinil)-dibenzo[b,f][1,4]-tiazepina expresada mediante la fórmula 1, que comprende las […]
PREPARACION DE QUETIAPINA, del 30 de Marzo de 2010, de FERMION OY: Un método para la preparación del compuesto de fórmula I o una sal del mismo
PROCEDIMIENTO PARA LA OBTENCION DE UN DERIVADO DE 11-(4-SUSTITUIDO-1-PIPERAZINIL)DIBENZO(B ,F)(1,4)TIAZEPINA., del 1 de Marzo de 2006, de UNION QUIMICO-FARMACEUTICA S.A.: Procedimiento para la obtención de un derivado de 11-(4- sustituido-1-piperazinil)dibenzo[b ,f][1,4]tiazepina, de fórmúla general I, en la que A significa hidrógeno […]
DERIVADO DE DIBENZOTIAZEPINA CRISTALINO Y SU USO COMO AGENTE ANTIPSICOTICO, del 5 de Febrero de 2010, de ASTRAZENECA AB: Un compuesto que es 11-(4-[2-(2-hidroxi-etoxi)etil]-1-piperazinil)dibenzo[b, f][1, 4]tiazepina cristalina