Antagonistas del factor de crecimiento celular del endotelio vascular y usos de los mismos.
Uso de un antagonista de hVEGF en la fabricación de un medicamento para tratar a un mamífero que tiene edema asociado a una enfermedad o afección no neoplásica,
o para prevenir el edema en un mamífero donde el edema está asociado a una enfermedad o afección no neoplásica.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US1999/029475.
Solicitante: GENENTECH, INC..
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 1 DNA WAY SOUTH SAN FRANCISCO, CA 94080-4990 ESTADOS UNIDOS DE AMERICA.
Inventor/es: FERRARA, NAPOLEONE, VAN BRUGGEN, NICHOLAS.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K38/00 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › Preparaciones medicinales que contienen péptidos (péptidos que contienen ciclos beta-lactama A61K 31/00; dipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina 2,5-dionas, A61K 31/00; péptidos basados en la ergolina A61K 31/48; que contienen compuestos macromoleculares que tienen unidades aminoácido repartidas estadísticamente A61K 31/74; preparaciones medicinales que contienen antígenos o anticuerpos A61K 39/00; preparaciones medicinales caracterizadas por los ingredientes no activos, p. ej. péptidos como soportes de fármacos, A61K 47/00).
- A61K39/395 A61K […] › A61K 39/00 Preparaciones medicinales que contienen antígenos o anticuerpos (materiales para ensayos inmunológicos G01N 33/53). › Anticuerpos (aglutininas A61K 38/36 ); Inmunoglobulinas; Inmunosuero, p. ej. suero antilinfocitario.
- A61K45/00 A61K […] › Preparaciones medicinales que contienen ingredientes activos no previstos en los grupos A61K 31/00 - A61K 41/00.
- A61P11/00 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › Medicamentos para el tratamiento de trastornos del aparato respiratorio.
- A61P17/06 A61P […] › A61P 17/00 Medicamentos para el tratamiento de problemas dermatológicos. › para el tratamiento de la psoriasis.
- A61P19/02 A61P […] › A61P 19/00 Medicamentos para el tratamiento de problemas del esqueleto. › para problemas de las articulaciones, p.ej. artritis, artrosis.
- A61P27/02 A61P […] › A61P 27/00 Medicamentos para tratar los trastornos de los sentidos. › Agentes oftálmicos.
- A61P27/06 A61P 27/00 […] › Agentes antiglaucoma o mióticos.
- A61P29/00 A61P […] › Agentes analgésicos, antipiréticos o antiinflamatorios que no actúan sobre el sistema nervioso central, p. ej. agentes antirreumáticos; Antiinflamatorios no esteroideos (AINEs).
- A61P3/10 A61P […] › A61P 3/00 Medicamentos para el tratamiento de trastornos del metabolismo (de la sangre o de fluido extracelular A61P 7/00). › para la hiperglucemia, p.ej. antidiabéticos.
- A61P35/00 A61P […] › Agentes antineoplásicos.
- A61P43/00 A61P […] › Medicamentos para usos específicos, no previstos en los grupos A61P 1/00 - A61P 41/00.
- A61P7/10 A61P […] › A61P 7/00 Medicamentos para el tratamiento de trastornos de la sangre o del fluido extracelular. › Agentes antiedematosos; Diureticos.
- A61P9/10 A61P […] › A61P 9/00 Medicamentos para el tratamiento de trastornos en el aparato cardiovascular. › para enfermedades isquémicas o ateroscleróticas, p.ej. medicamentos antianginosos, vasodilatadores coronarios,medicamentos para el tratamiento del infarto de miocardio, de la retinopatía, de la insuficiencia cerebrovascular, de la arterioesclerosis renal.
- C07K14/71 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 14/00 Péptidos con más de 20 aminoácidos; Gastrinas; Somatostatinas; Melanotropinas; Sus derivados. › para factores de crecimiento; para reguladores de crecimiento.
- C07K16/22 C07K […] › C07K 16/00 Inmunoglobulinas, p. ej. anticuerpos mono o policlonales. › contra factores de crecimiento.
- C07K16/24 C07K 16/00 […] › contra citoquinas, linfoquinas o interferones.
- C12N15/09 C […] › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › C12N 15/00 Técnicas de mutación o de ingeniería genética; ADN o ARN relacionado con la ingeniería genética, vectores, p. ej. plásmidos, o su aislamiento, su preparación o su purificación; Utilización de huéspedes para ello (mutantes o microorganismos modificados por ingeniería genética C12N 1/00, C12N 5/00, C12N 7/00; nuevas plantas en sí A01H; reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00; nuevas razas animales en sí A01K 67/00; utilización de preparaciones medicinales que contienen material genético que es introducido en células del cuerpo humano para tratar enfermedades genéticas, terapia génica A61K 48/00; péptidos en general C07K). › Tecnología del ADN recombinante.
- C12N9/96 C12N […] › C12N 9/00 Enzimas, p. ej. ligasas (6.); Proenzimas; Composiciones que las contienen (preparaciones para la limpieza de los dientes que contienen enzimas A61K 8/66, A61Q 11/00; preparaciones de uso médico que contienen enzimas A61K 38/43; composiciones detergentes que contienen enzimas C11D ); Procesos para preparar, activar, inhibir, separar o purificar enzimas. › Estabilización de una enzima por formación de un aducto o de una composición; Formación de conjugaciones de enzimas.
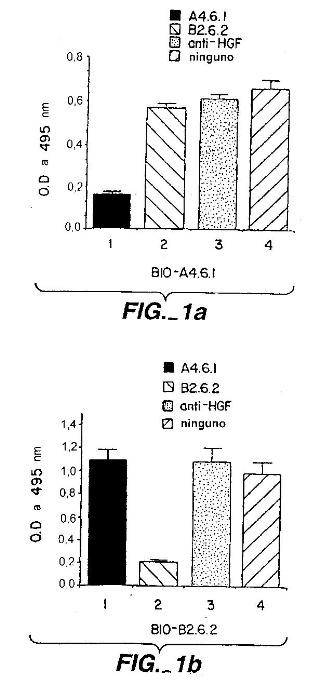
Fragmento de la descripción:
Antagonistas del factor de crecimiento celular del endotelio vascular y usos de los mismos.
Campo de la invención
La presente invención se refiere al uso de antagonistas del factor de crecimiento celular del endotelio vascular (VEGF) en la fabricación de un medicamento para propósitos terapéuticos. En particular, la presente invención se refiere a la fabricación de un medicamento para el tratamiento de edema asociado con una enfermedad o afección no neoplásica.
Antecedentes de la invención
Los dos componentes celulares principales de la vasculatura son las células endoteliales y las células del músculo liso. Las células endoteliales forman el revestimiento de la superficie interna de todos los vasos sanguíneos, y constituyen una superficie de contacto no trombogénica entre la sangre y el tejido. Además, las células endoteliales son un componente importante para el desarrollo de nuevos capilares y vasos sanguíneos. Por tanto, las células endoteliales proliferan durante la angiogénesis, o neovascularización, asociada con crecimiento tumoral y metástasis, así como una diversidad de enfermedades o trastornos no neoplásicos.
Según se dice, diversos polipéptidos de origen natural inducen la proliferación de células endoteliales. Entre esos polipéptidos están los factores de crecimiento de fibroblastos (FGF) básicos o ácidos, Burgess and Maciag, Annual Rev. Biochem., 58:575 (1989), factor de crecimiento de células endoteliales derivado de plaquetas (PD-ECGF), Ishikawa, et al., Nature, 338:557 (1989), y factor de crecimiento del endotelio vascular (VEGF), Leung, et al., Science 246:1306 (1989); Ferrara & Henzel, Biochem. Biophys. Res. Commun. 161:851 (1989); Tischer, et al., Biochem. Biophys. Res. Commun. 165:1198 (1989); Ferrara, et al., Publicación de Patente PCT Nº WO 90/13649 (publicada el 15 de noviembre de 1990).
VEGF se identificó por primera vez en medios condicionados por células foliculares y foliculoestrelladas de pituitaria bovina. Los análisis bioquímicos indican que VEGF bovino es una proteína dimérica con una masa molecular aparente de aproximadamente 45.000 Dalton, y con una especificidad mitogénica aparente para células del endotelio vascular. El ADN que codifica VEGF bovino se aisló explorando una biblioteca de ADNc preparada a partir de dichas células, usando oligonucleótidos basados en la secuencia de aminoácidos amino-terminal de la proteína como sondas de hibridación.
El VEGF humano se obtuvo explorando primero una biblioteca de ADNc preparada a partir de células humanas, usando el ADNc de VEGF bovino como sonda de hibridación. Un ADNc identificado de este modo codifica una proteína de 165 aminoácidos que tiene más del 95% de homología con VEGF bovino, mencionándose dicha proteína como VEGF humano (hVEGF). La actividad mitogénica de VEGF humano se confirmó expresando el ADNc de VEGF humano en células hospedadoras de mamífero. Los medios condicionados por células transfectadas con el ADNc de VEGF humano promovieron la proliferación de células del endotelio capilar, mientras que las células de control no. Véase, Leung, et al., Science 246:1306 (1989).
Se identificaron varios ADNc adicionales en bibliotecas de ADNc humano que codifican isoformas de 121, 189, y 206 aminoácidos de hVEGF (también mencionadas colectivamente como proteínas relacionadas con hVEGF). La proteína de 121 aminoácidos difiere de hVEGF debido a la deleción de los 44 aminoácidos entre los restos 116 y 159 en hVEGF. La proteína de 189 aminoácidos difiere de hVEGF debido a la inserción de 24 aminoácidos en el resto 116 en hVEGF, y aparentemente es idéntica al factor de permeabilidad vascular humano (hVPF). La proteína de 206 aminoácidos difiere de hVEGF debido a una inserción de 41 aminoácidos en el resto 116 en hVEGF. Houck, et al., Mol. Endocrin. 5:1806 (1991); Ferrara, et al., J. Cell. Biochem. 47:211 (1991); Ferrara, et al., Endocrine Reviews 13:18 (1992); Keck, et al., Science 246:1309 (1989); Connolly, et al., J. Biol. Chem. 246:20017 (1989); Keck, et al., Publicación de Patente EPO Nº 0 370 989 (publicada el 30 de mayo de 1990).
Los receptores para VEGF se han descrito en la bibliografía. Se ha descubierto que dos de dichos receptores, flt-1 y flk-1, median los efectos de VEGF [DeVries et al., Science 255:989 (1992); Shibuya et al., Oncogene 5:519 (1990); Matthews et al., Proc. Natl. Acad. Sci. 88:9026 (1991); Terman et al., Oncogene 6:1677 (1991); Terman et al., Biochem. Biophys. Res. Comm. 187:1579 (1992); Neufeld et al., Prog, Growth Factor Res. 5:89-97 (1994); Waltenberger et al., J. Biol. Chem. 269:26988 (1994); Quinn et al., Proc. Natl. Acad. Sci. 90:7533 (1991)], pero su regulación y mecanismos aún no se entienden completamente. Lennmyr et al., J. Neuropathology and Exp. Neurology 57:874-882 (1998). Ambos receptores flt-1 y flk-1 son receptores de membrana y pertenecen a la familia del receptor tirosina quinasa clase III. Barleon et al., J. Cell Biochem. 54:56 (1994); Neufeld et al., supra.
VEGF no sólo estimula la proliferación de células del endotelio vascular, sino que también induce la angiogénesis. La angiogénesis, que implica la formación de nuevos vasos sanguíneos a partir del endotelio preexistente, es un componente importante de una diversidad de enfermedades y trastornos incluyendo crecimiento tumoral y metástasis, artritis reumatoide, psoriasis, aterosclerosis, retinopatía diabética, fibroplasia retrolental, glaucoma neovascular, degeneración macular relacionada con la edad, hemangiomas, rechazo inmune de tejido corneal transplantado y otros tejidos, e inflamación crónica.
En el caso de crecimiento tumoral, la angiogénesis parece ser crucial para la transición de hiperplasia a neoplasia, y para proporcionar alimento al crecimiento del tumor sólido. Folkman, et al., Nature 339:58 (1989). La angiogénesis también permite a los tumores que estén en contacto con el lecho vascular del hospedador que puede proporcionar una vía para la metástasis de las células tumorales. Se proporciona una evidencia del papel de la angiogénesis en la metástasis tumoral, por ejemplo, por estudios que muestran la correlación entre la cantidad y densidad de microvasos en secciones histológicas de carcinoma de mama humano invasivo y la presencia real de metástasis distante. Weidner, et al., New Engl. J. Med. 324:1 (1991).
También se ha informado de que VEGF está implicado en la permeabilidad endotelial y vascular. Véase, Ferrara et al., Endocrine Reviews 18:4-25 (1997); Dobrogowska et al., J. Neurocytology 27:163 (1998). Aunque no se entiende completamente, se cree que VEGF aumenta la filtración de las células endoteliales en la piel, retina, y tejidos tumorales. Collins et al., Brit. J. Pharmacology 109:195 (1993); Connolly et al., J. Clin. Invest. 84:1470 (1989); Sheweiki et al., Nature 359:843 (1992); Monacci et al., Am. J. Physiol. 246:C995 (1993); Stone et al., J. Neurosci. 15:4738 (1995); Detmar et al., J. Invest. Dermatol. 108:263 (1997); Weindel et al., Neurosurgery 35:437 (1994). También se han examinado los efectos potenciales y el papel de VEGF (y sus receptores, particularmente, el receptor flt-1), sobre las células endoteliales y la permeabilidad de la barrera sangre-cerebro. Véase, por ejemplo, Rosenstein et al., Proc. Natl. Acad. Sci. 95:7086 (1998); Dobrogowska, supra; Kovacs et al., Stroke 27:1865 (1996). Se ha observado expresión de ARNm de VEGF relativamente difusa en cerebro de rata adulta pero a abundancia algo baja. Monacci et al., Am. J. Physiol. 146:368-378 (1993). Sin embargo, se ha demostrado que la tensión de oxígeno reducida desencadena la expresión de VEGF [Dor and Keshet, Trends in Cardiovascular Med., 7:289-294 (1998)] y se ha demostrado que se encuentran niveles potenciados de VEGF, flt-1, y flk-1 en cerebro de rata después de la inducción de isquemia cerebral focal. Hayashi et al., Stroke 28:2039 (1997); Kovacs et al., supra; Lennmyr et al., J. Neuropathology and Experimental Neurology, 57:874 (1998). El papel de VEGF en la patogénesis de apoplejía y fallo BBB ha sido...
Reivindicaciones:
1. Uso de un antagonista de hVEGF en la fabricación de un medicamento para tratar a un mamífero que tiene edema asociado a una enfermedad o afección no neoplásica, o para prevenir el edema en un mamífero donde el edema está asociado a una enfermedad o afección no neoplásica.
2. Uso de acuerdo con reivindicación 1, donde el medicamento reduce o inhibe el edema.
3. Uso de acuerdo con la reivindicación 1 ó 2, donde el edema comprende edema del sistema nervioso central.
4. Uso de acuerdo con la reivindicación 3, donde el edema del sistema nervioso central comprende edema cerebral.
5. Uso de acuerdo con una cualquiera de las reivindicaciones 1-4, donde la enfermedad o afección no neoplásica comprende lesión craneal, lesión de la médula espinal, hipertensión aguda, meningitis, encefalitis, abscesos, hemorragia, infección viral, malaria cerebral, radiación, esclerosis múltiple, detención cardiaca, asfixia al nacer, toxicidad por glutamato, encefalopatía, hipoxia, isquemia, o diálisis renal.
6. Uso de acuerdo con una cualquiera de las reivindicaciones 1 a 4, donde la enfermedad o afección no neoplásica comprende apoplejía.
7. Uso de acuerdo con la reivindicación 6, donde la apoplejía es apoplejía isquémica.
8. Uso de acuerdo con la reivindicación 7, donde la apoplejía isquémica es apoplejía trombótica, apoplejía embólica, apoplejía hemodinámica, o apoplejía lacunar.
9. Uso de acuerdo con la reivindicación 6, donde la apoplejía es apoplejía hemorrágica.
10. Uso de acuerdo con la reivindicación 9, donde la apoplejía hemorrágica está asociada a hemorragia intracerebral, subaracnoidea, intraventricular, o subdural.
11. Uso de acuerdo con cualquiera de las reivindicaciones 6-10, donde el medicamento es para tratar al mamífero inmediatamente después de la detección o diagnóstico de la apoplejía.
12. Uso de acuerdo con cualquiera de las reivindicaciones 6-10, donde el medicamento es para tratar al mamífero en 1 a 4 días de la aparición de la apoplejía.
13. Uso de acuerdo con una cualquiera de las reivindicaciones 1 a 12, donde el mamífero es un ser humano.
14. Uso de acuerdo con una cualquiera de las reivindicaciones 1 a 13, donde el antagonista de hVEGF comprende un anticuerpo anti-hVEGF.
15. Uso de acuerdo con la reivindicación 14, donde el anticuerpo anti-hVEGF comprende un anticuerpo quimérico.
16. Uso de acuerdo con la reivindicación 14 ó 15, donde el anticuerpo anti-hVEGF comprende un anticuerpo humanizado.
17. Uso de acuerdo con una cualquiera de las reivindicaciones 14 a 16, donde dicho anticuerpo comprende un anticuerpo monoclonal.
18. Uso de acuerdo con una cualquiera de las reivindicaciones 1 a 13, donde el antagonista de hVEGF comprende una proteína de fusión del receptor de hVEGF.
19. Uso de acuerdo con la reivindicación 18, donde la proteína de fusión del receptor de hVEGF comprende una secuencia del dominio extracelular de un receptor de hVEGF fusionada a una inmunoglobulina.
20. Uso de acuerdo con la reivindicación 18 ó 19, donde la proteína de fusión del receptor de hVEGF comprende una proteína de fusión flt-IgG.
Patentes similares o relacionadas:
 Composiciones y métodos para el tratamiento de trastornos de células plasmáticas y trastornos prolinfocíticos de células b, del 29 de Julio de 2020, de Knopp Biosciences LLC: Una composición que comprende una cantidad terapéuticamente eficaz de dexpramipexol para su uso en el tratamiento de un trastorno de células B caracterizado por niveles elevados […]
Composiciones y métodos para el tratamiento de trastornos de células plasmáticas y trastornos prolinfocíticos de células b, del 29 de Julio de 2020, de Knopp Biosciences LLC: Una composición que comprende una cantidad terapéuticamente eficaz de dexpramipexol para su uso en el tratamiento de un trastorno de células B caracterizado por niveles elevados […]
Derivados de piperidina 1,4 sustituidos, del 29 de Julio de 2020, de 89Bio Ltd: Un compuesto de acuerdo con la Fórmula I: **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, en donde: A se selecciona de […]
Profármacos de gemcitabina, del 29 de Julio de 2020, de NuCana plc: Una formulación farmacéutica que comprende gemcitabina-[fenil-benzoxi-L-alaninil)]-(S)-fosfato 3: **(Ver fórmula)** o una sal o solvato […]
Formas cristalinas de 6-((6,7-dimetoxiquinazolin-4-il)oxi)-N,2-dimetilbenzofuran-3-carboxamida, del 29 de Julio de 2020, de Hutchison Medipharma Limited: Forma I de 6-((6,7-dimetoxiquinazolin-4-il)oxi)-N,2-dimetilbenzofuran-3-carboxamida, en donde el difractograma de rayos X de polvo de la Forma […]
Compuestos y procedimientos de uso, del 29 de Julio de 2020, de Medivation Technologies LLC: Un compuesto de fórmula (Aa-1): **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, en la que: A representa H, halógeno, amino, […]
Complejos de agentes terapéuticos de base vírica y poli(beta-amino-ésteres) modificados, del 29 de Julio de 2020, de Sagetis Biotech, SL: Un complejo de un agente terapéutico de base vírica con un polímero de fórmula I: **(Ver fórmula)** donde cada L1 y L2 están seleccionados […]
Compuestos de alquinilbenceno heterocíclicos, y composiciones médicas y usos de los mismos, del 29 de Julio de 2020, de Guangzhou Healthquest Pharma Co., Ltd: Un compuesto de alquinilbenceno heterocíclico que tiene la fórmula (I) y una sal farmacéuticamente aceptable, o estereoisómero del mismo, **(Ver […]
Inmunoterapia novedosa contra diversos tumores, entre ellos tumores cerebrales y neuronales, del 22 de Julio de 2020, de IMMATICS BIOTECHNOLOGIES GMBH: Péptido que comprende una secuencia de aminoácidos acorde con la SEQ ID N.º 19, en que dicho péptido tiene una longitud total de entre 9 y 16 aminoácidos.