COMPUESTOS MULTICÍCLICOS Y SU USO COMO INHIBIDORES DE ENZIMAS PARP, VEGFR2 Y MLK3.
Un compuesto de fórmula IV: en donde A, B, V, R1, J, R2, E y F se seleccionan de acuerdo con la siguiente Tabla:
Tipo: Patente Europea. Resumen de patente/invención. Número de Solicitud: E08075834.
Solicitante: CEPHALON, INC..
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 145 BRANDYWINE PARKWAY WEST CHESTER, PA 19380 ESTADOS UNIDOS DE AMERICA.
Inventor/es: CHATTERJEE, SANKAR, ATOR, MARK, A., BIHOVSKY, RON, DUNN, DEREK, HUDKINS, ROBERT, L..
Fecha de Publicación: .
Fecha Solicitud PCT: 9 de Mayo de 2001.
Fecha Concesión Europea: 22 de Septiembre de 2010.
Clasificación PCT:
- A61K31/407 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › condensados con sistemas heterocíclicos, p. ej. ketorolac, fisostigmina.
- A61P35/00 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › Agentes antineoplásicos.
- C07D487/04 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07D COMPUESTOS HETEROCICLICOS (Compuestos macromoleculares C08). › C07D 487/00 Compuestos heterocíclicos que contienen átomos de nitrógeno como únicos heteroátomos del ciclo en el sistema condensado, no previstos por los grupos C07D 451/00 - C07D 477/00. › Sistemas condensados en orto.
- C07D491/04 C07D […] › C07D 491/00 Compuestos heterocíclicos que contienen en el sistema cíclico condensado, a la vez uno o más ciclos que tienen átomos de oxígeno como únicos heteroátomos del ciclo, y uno o más ciclos que tienen átomos de nitrógeno como únicos heteroátomos del ciclo, no previstos en los grupos C07D 451/00 - C07D 459/00, C07D 463/00, C07D 477/00 ó C07D 489/00. › Sistemas orto-condensados.
- C07D495/04 C07D […] › C07D 495/00 Compuestos heterocíclicos que contienen en el sistema condensado al menos un heterociclo que tiene átomos de azufre como únicos heteroátomos del ciclo. › Sistemas orto-condensados.
Países PCT: Austria, Bélgica, Suiza, Alemania, Dinamarca, España, Francia, Reino Unido, Grecia, Italia, Liechtensein, Luxemburgo, Países Bajos, Suecia, Mónaco, Portugal, Irlanda, Finlandia, Chipre.
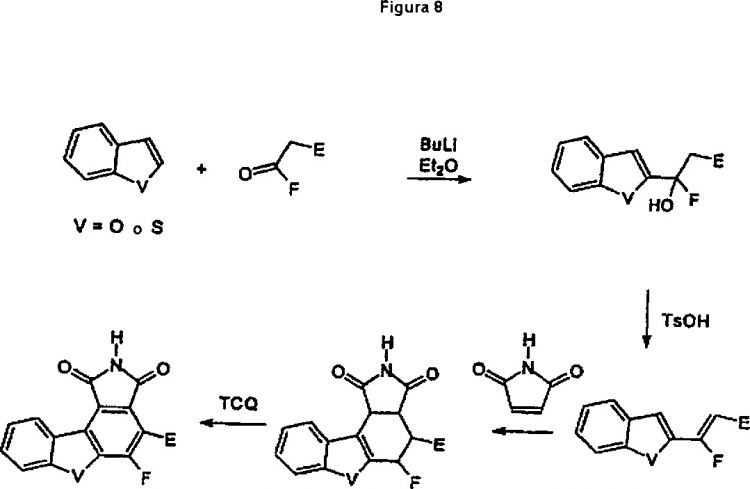
Fragmento de la descripción:
Compuestos multicíclicos y su uso como inhibidores de enzimas PARP, VEGFR2 y MLK3.
La presente invención se refiere a nuevos compuestos multicíclicos y al uso de los mismos. Más particularmente, la presente invención se refiere a nuevos compuestos multicíclicos y a su uso, por ejemplo, para la mediación en la actividad enzimática.
Antecedentes de la invención
Poli(ADP-ribosa) polimerasa (PARP, también denominada poli(ADP-ribosa) sintetasa, o PARS) es una enzima nuclear que cataliza la síntesis de cadenas de poli(ADP-ribosa) a partir de NAD+ en respuesta a roturas en el ADN de cadena sencilla como parte del proceso de reparación del ADN (de Murcia et al. Trends Biochem, Sci., 1994, 19, 172; Alvarez-Gonzalez et al. Mol. Cell. Biochem. 1994, 138, 33). Los sustratos de proteína asociada a cromatina para la ribosilación con ADP, que incluyen histonas, enzimas metabolizantes de ADN y PARP propiamente dicha, están modificados sobre residuos glutamato en la superficie. PARP cataliza la fijación de una unidad de ADP-ribosa a la proteína (iniciación), seguido de la polimerización de tantos como 200 monómeros de ADP-ribosa (alargamiento) a través de enlaces glicosídicos 2'-1''. Además, PARP cataliza la ramificación del polímero a una baja frecuencia.
El papel de PARP en el proceso de reparación del ADN está incompletamente definido. Se sugiere la unión de PARP a ADN de cadena doble mellado para facilitar el proceso de reparación mediante el bloqueo transitorio de la replicación o recombinación de ADN. La subsiguiente poli(ADP-ribosil)ación de PARP e histonas puede dar como resultado la introducción de una carga negativa sustancial, provocando la repulsa de las proteínas modificadas a partir del ADN. Luego se propone relajar la estructura de cromatina, reforzando el acceso de las enzimas de reparación de ADN al sitio de la lesión.
Se establece la hipótesis de que una activación excesiva de PARP en respuesta a la lesión o al estrés de la célula da como resultado la muerte de ésta (Sims et al. Biochemistry 1983, 22, 5188; Yamamoto et al. Nature 1981, 294, 284). La activación de PARP mediante roturas de la cadena de ADN puede ser mediada por óxido nítrico (NO) o diversos compuestos intermedios de oxígeno reactivo. Cuando el grado de lesión del ADN es grande, PARP puede catalizar una cantidad masiva de poli(ADP-ribosil)ación, agotando los niveles de NAD+ de la célula. Dado que la célula intenta conservar la homeostasis al volver a sintetizar NAD+, los niveles de ATP pueden disminuir precipitadamente (dado que la síntesis de una molécula de NAD+ requiere cuatro moléculas de ATP) y la célula puede morir por agotamiento de sus almacenes de energía.
Se ha informado que la activación de PARP juega un papel en la muerte de la célula en un cierto número de estados patológicos, sugiriendo que inhibidores de PARP tendrían una eficacia terapéutica en dichos estados. Se ha observado una poli(ADP-ribosil)ación reforzada tras una isquemia cerebral focal en la rata, consistente con la activación de PARP en la apoplejía (Tokime et al. J. Cereb. Blood Flow Metab. 1998, 18, 991). Una cantidad sustancial de datos farmacológicos y genéticos publicados sustenta la hipótesis de que inhibidores de PARP serían neuroprotectores tras la isquemia cerebral o apoplejía. Inhibidores de PARP protegían frente a una neurotoxicidad inducida por NMDA o NO en los cultivos corticales cerebrales de la rata (Zhang et al., Science 1994, 263, 687; Eliasson et al. Nature Med. 1997, 3, 1089). El grado de neuroprotección observado para la serie de compuestos equiparó directamente su actividad en calidad de inhibidores de PARP.
Los inhibidores de PARP también pueden exhibir una eficacia neuroprotectora en modelos de animales de apoplejía. El potente inhibidor de PARP DPQ (3,4-dihidro-5-[4-(1-piperidinil)butoxi]-1(2H)-isoquinolinona) (Suto et al. patente de EE.UU. nº 5.177.075) proporcionó una reducción del 54% en el volumen de infarto en un modelo de rata de isquemia cerebral focal (MCAo permanente y oclusión bilateral durante 90 min de la arteria carótida común) tras la dosificación i.p. (10 mg/kg) dos horas antes y dos horas después del inicio de la isquemia (Takahashi et al. Brain Res. 1997, 829, 46). La administración intracerebroventricular de un inhibidor de PARP menos potente, 3-aminobenzamida (3-AB), proporcionó una disminución del 47% en el volumen de infarto en ratones tras una oclusión de dos horas del MCA mediante el método de hilos de sutura (Endres et al. J. Cereb. Blood Flow Metab. 1997, 17, 1143). El tratamiento con 3-AB también mejoró la recuperación funcional 24 horas después de la isquemia, atenuó la disminución de los nveles de NAD+ en tejidos isquémicos y disminuyó la síntesis de polímeros de poli(ADP-ribosa) según se determina mediante inmunohistoquímica. De manera similar, 3-AB (10 mg/kg) reducía significativamente el volumen de infarto en un modelo de oclusión por sutura de isquemia focal en rata (Lo et al. Stroke 1998, 29, 830). El efecto neuroprotector de 3-AB (3-30 mg/kg, i.c.v.) también se observó en un modelo de oclusión de la arteria cerebral media permanente de isquemia en la rata (Tokime et al. J. Cereb. Blood Flow Metab. 1998, 18, 991).
La disponibilidad de ratones en los que el gen PARP ha sido convertido en no funcional (Wang, Genes Dev. 1995, 9, 509) también ayudó a validar el papel de PARP en la neurodegeneración. La neurotoxicidad debida a NMDA, NO o la privación de oxígeno-glucosa fue virtualmente abolida en cultivos corticales cerebrales primarios procedentes de ratones PARP-/- (Eliasson et al. Nature Med. 1997, 3, 1089). En el modelo de isquemia por hilos de sutura en el ratón se observó una reducción del 80% en el volumen de infarto en ratones PARP-/-, y se notó una reducción del 65% en ratones PARP+/-. En Endres et al. (1997) se reseñó una reducción del 35% en volumen de infarto en ratones PARP-/- y una reducción del 31% en animales PARP+/-. Además de la neuroprotección, ratones PARP-/- demostraron una mejora en el tanteo neurológico y exhibieron niveles incrementados de NAD+ tras la isquemia.
Existe también una evidencia preclínica, lo que sugiere que inhibidores de PARP puedan ser eficaces en el tratamiento de la enfermedad de Parkinson. Esto es debido a que la pérdida de neuronas dopaminérgicas en la sustancia negra es un distintivo de la enfermedad de Parkinson. El tratamiento de animales o seres humanos experimentales con la neurotoxina 1-metil-4-fenil-1,2,3,6-tetrahidropiridina (MPTP) replica la pérdida de neuronas dopaminérgicas y los síntomas motrices de la enfermedad de Parkinson. MPTP activa PARP en la sustancia negra, y ratones que carecen de PARP son resistentes a los efectos neurodegenerativos de MPTP (Mandir et al. Proc. Nat. Acad. Sci. 1999, 96, 5774). De manera similar, se reseña que el inhibidor de PARP 3-aminobenzamida atenúa la pérdida de NAD+ en el estrato tras la administración de MPTP a ratones (Cosi et al. Brain Res. 1998, 809, 58).
La activación de PARP ha estado implicada en los déficits funcionales que pueden resultar de una lesión traumática del cerebro y de una lesión de la espina dorsal. En un modelo de impacto cortical controlado de lesión traumática del cerebro, ratones PARP-/- exhibían una función motriz y cognitiva significativamente mejorada en comparación con ratones PARP+/+ (Whalen et al. J. Cereb. Blood Flow Metab. 1999, 19, 835). La producción de peroxinitrito y la activación de PARP han sido también demostradas en ratas con lesión del cordón espinal (Scott et al. Ann. Neurol. 1999, 45, 120). Estos resultados sugieren que la inhibición de PARP puede proporcionar una protección de la pérdida de función tras trauma en la cabeza o espinal.
El papel de PARP como un mediador en la muerte de la célula tras la isquemia y reperfusión puede no estar limitado al sistema nervioso. A este respecto, una publicación reciente informó que una diversidad...
Reivindicaciones:
1. Un compuesto de fórmula IV:
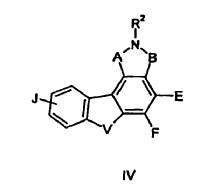
en donde A, B, V, R1, J, R2, E y F se seleccionan de acuerdo con la siguiente Tabla:
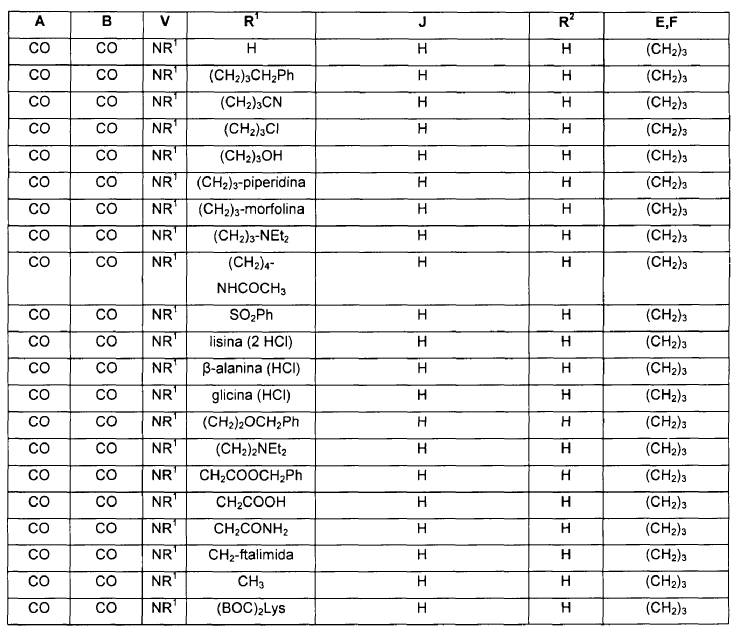
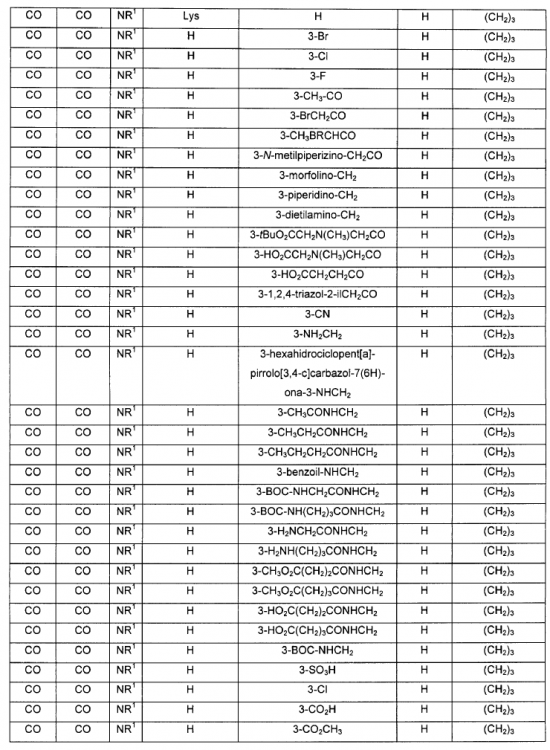
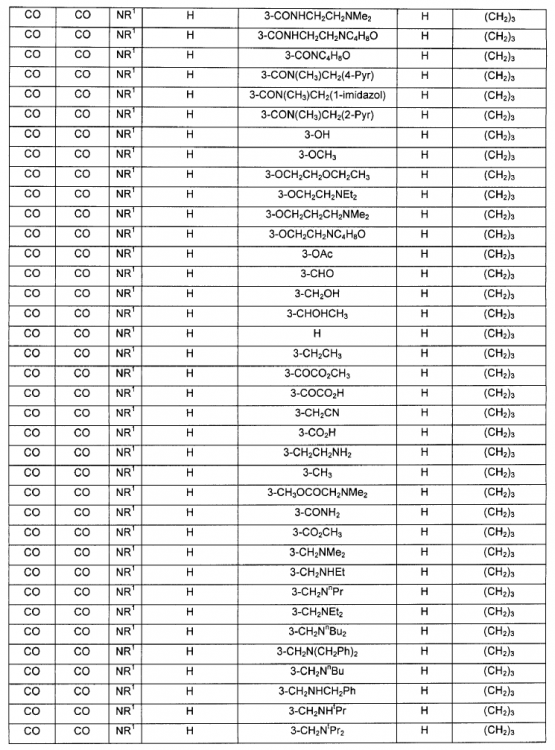
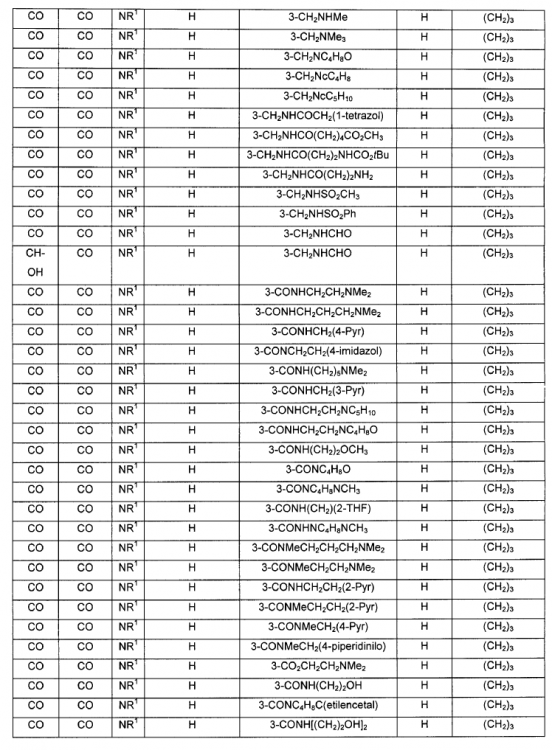
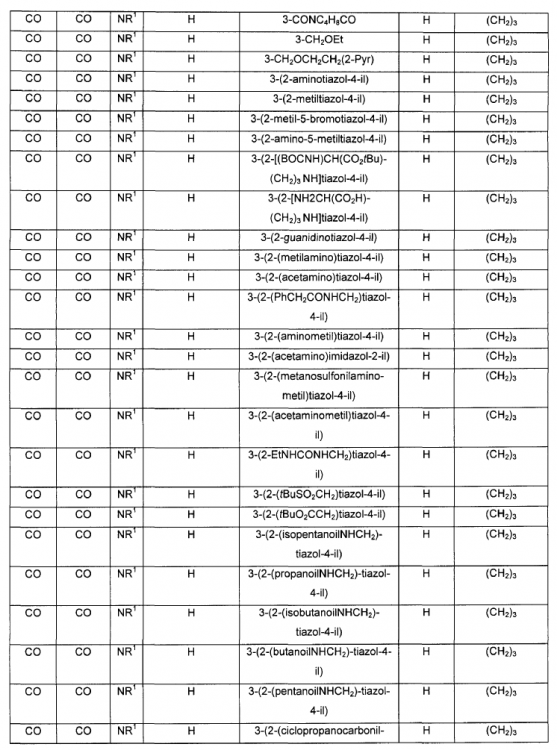
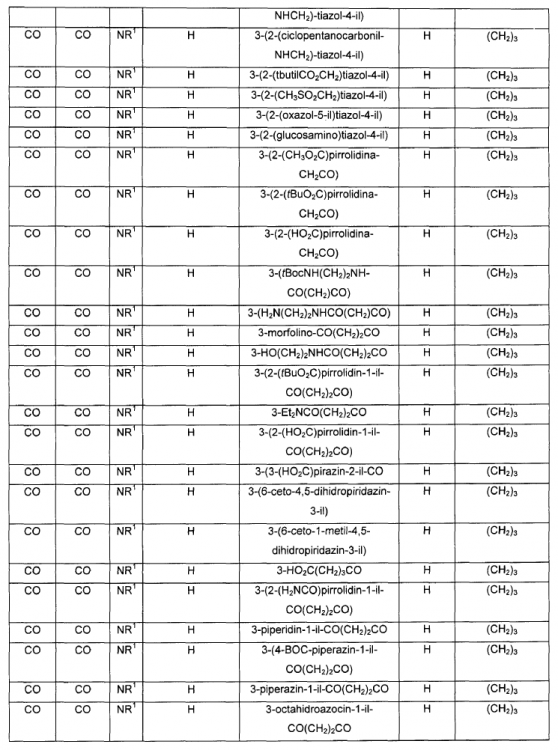
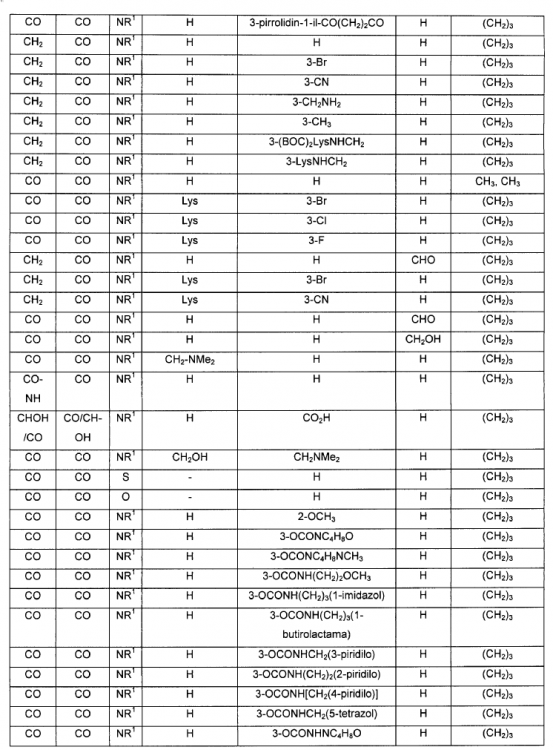
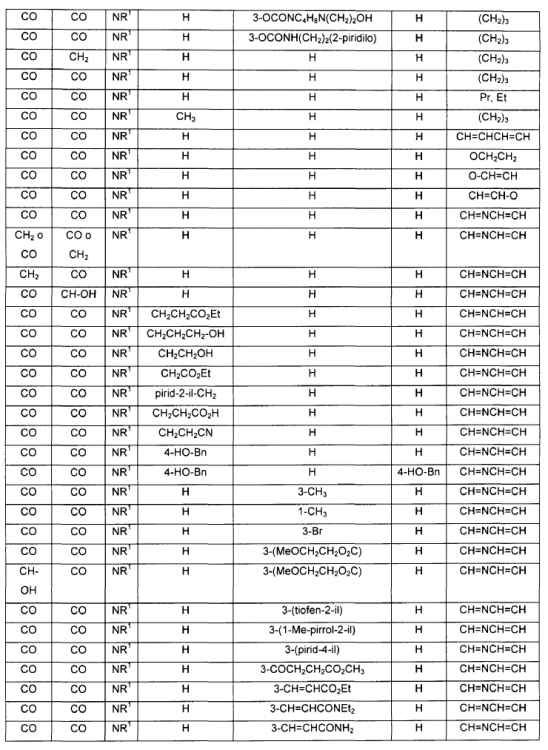
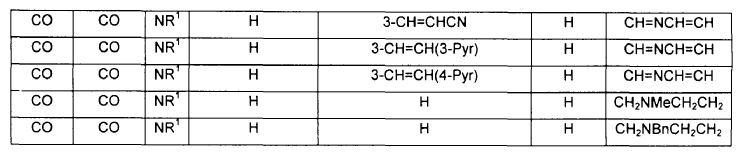
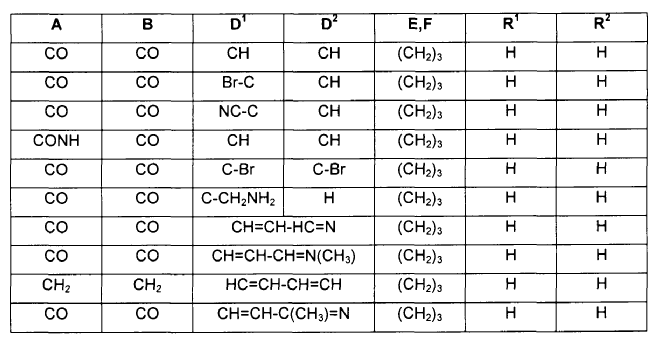
2. Un compuesto de fórmula IIb:
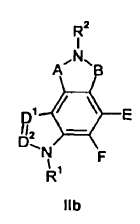
en donde A, B, D1, D2, E, F, R1 y R2 se seleccionan de acuerdo con la siguiente tabla:
Patentes similares o relacionadas:
Profármacos de gemcitabina, del 29 de Julio de 2020, de NuCana plc: Una formulación farmacéutica que comprende gemcitabina-[fenil-benzoxi-L-alaninil)]-(S)-fosfato 3: **(Ver fórmula)** o una sal o solvato […]
Formas cristalinas de 6-((6,7-dimetoxiquinazolin-4-il)oxi)-N,2-dimetilbenzofuran-3-carboxamida, del 29 de Julio de 2020, de Hutchison Medipharma Limited: Forma I de 6-((6,7-dimetoxiquinazolin-4-il)oxi)-N,2-dimetilbenzofuran-3-carboxamida, en donde el difractograma de rayos X de polvo de la Forma […]
Compuestos y procedimientos de uso, del 29 de Julio de 2020, de Medivation Technologies LLC: Un compuesto de fórmula (Aa-1): **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, en la que: A representa H, halógeno, amino, […]
Complejos de agentes terapéuticos de base vírica y poli(beta-amino-ésteres) modificados, del 29 de Julio de 2020, de Sagetis Biotech, SL: Un complejo de un agente terapéutico de base vírica con un polímero de fórmula I: **(Ver fórmula)** donde cada L1 y L2 están seleccionados […]
Compuestos de alquinilbenceno heterocíclicos, y composiciones médicas y usos de los mismos, del 29 de Julio de 2020, de Guangzhou Healthquest Pharma Co., Ltd: Un compuesto de alquinilbenceno heterocíclico que tiene la fórmula (I) y una sal farmacéuticamente aceptable, o estereoisómero del mismo, **(Ver […]
 Composiciones y métodos para el tratamiento de trastornos de células plasmáticas y trastornos prolinfocíticos de células b, del 29 de Julio de 2020, de Knopp Biosciences LLC: Una composición que comprende una cantidad terapéuticamente eficaz de dexpramipexol para su uso en el tratamiento de un trastorno de células B caracterizado por niveles elevados […]
Composiciones y métodos para el tratamiento de trastornos de células plasmáticas y trastornos prolinfocíticos de células b, del 29 de Julio de 2020, de Knopp Biosciences LLC: Una composición que comprende una cantidad terapéuticamente eficaz de dexpramipexol para su uso en el tratamiento de un trastorno de células B caracterizado por niveles elevados […]
Derivados de piperidina 1,4 sustituidos, del 29 de Julio de 2020, de 89Bio Ltd: Un compuesto de acuerdo con la Fórmula I: **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, en donde: A se selecciona de […]
Método de tratamiento del cáncer, del 22 de Julio de 2020, de Intensity Therapeutics, Inc: Una composición que comprende una cantidad terapéuticamente efectiva de un agente terapéutico y un agente mejorador de la permeación intracelular para uso en el tratamiento […]