PROFARMACOS DE PROPOFOL DERIVADOS DEL AMINOACIDO SERINA, COMPOSICIONES, USOS Y FORMAS CRISTALINAS DE LOS MISMOS.
El compuesto ácido 2-amino-3-(2,6-diisopropilfenoxicarboniloxi)-propanoico,
o una sal farmacéuticamente aceptable del mismo, o un solvato farmacéuticamente aceptable de cualquiera de los anteriores
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2005/047458.
Solicitante: XENOPORT, INC..
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 3410 CENTRAL EXPRESSWAY,SANTA CLARA, CA 95051.
Inventor/es: XU, FENG, GALLOP, MARK, A., SASIKUMAR,VIVEK, DILIP,USHA.
Fecha de Publicación: .
Fecha Concesión Europea: 27 de Enero de 2010.
Clasificación Internacional de Patentes:
- C07C229/22 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07C COMPUESTOS ACICLICOS O CARBOCICLICOS (compuestos macromoleculares C08; producción de compuestos orgánicos por electrolisiso electroforesis C25B 3/00, C25B 7/00). › C07C 229/00 Compuestos que contienen grupos amino y carboxilo unidos a la misma estructura carbonada. › estando la estructura carbonada sustituida por átomos de oxígeno.
Clasificación PCT:
- A61K31/198 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › Alfa-amino-ácidos, p. ej. alanina, ácido etilendiamino tetraacético (EDTA) (betaína A61K 31/205; prolina A61K 31/401; triptófano A61K 31/405; histidina A61K 31/4172; péptidos no degradados en aminoácidos individuales A61K 38/00).
- A61P23/00 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › Anestésicos.
- A61P25/00 A61P […] › Medicamentos para el tratamiento de trastornos del sistema nervioso.
- C07C227/42 C07C […] › C07C 227/00 Preparación de compuestos que contienen grupos amino y carboxilo unidos a la misma estructura carbonada. › Cristalización.
- C07C229/22 C07C 229/00 […] › estando la estructura carbonada sustituida por átomos de oxígeno.
Fragmento de la descripción:
Profármacos de propofol derivados del aminoácido serina, composiciones, usos y formas cristalinas de los mismos.
Antecedentes de la invención
La presente invención proporciona un profármaco de propofol y formas cristalinas del mismo, procedimientos de preparación del profármaco de propofol y formas cristalinas del mismo, composiciones farmacéuticas del profármaco de propofol y formas cristalinas del mismo, métodos de uso del profármaco de propofol y formas cristalinas del mismo y composiciones farmacéuticas del mismo para tratar o prevenir enfermedades o trastornos tales como cefalea, náuseas y vómitos postquimioterapia o postcirugía y trastornos neurodegenerativos y trastornos del estado de ánimo.
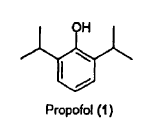
El propofol (2,6-diisopropilfenol), (1), es un fenol de bajo peso molecular que se usa ampliamente como agente sedante-hipnótico intravenoso en la inducción y el mantenimiento de la anestesia y/o la sedación en mamíferos. Las ventajas del propofol como anestésico incluyen un comienzo rápido de la anestesia, un aclaramiento rápido y efectos secundarios mínimos (Langley et al, Drugs 1988, 35, 334-372). El propofol puede mediar efectos hipnóticos por medio de la interacción con el complejo de receptor GABAA, un canal iónico de cloruro dependiente de ligando heterooligomérico (Peduto et al, Anesthesiology 1991, 75, 1000-1009).
El propofol se metaboliza rápidamente en mamíferos, eliminándose el fármaco predominantemente como conjugados glucuronidados y sulfatados de propofol y 4-hidroxipropofol (Langley et al., Drugs 1988, 35, 334-372). El aclaramiento del propofol supera el flujo sanguíneo hepático, lo que indica que los tejidos extrahepáticos contribuyen al metabolismo global del fármaco. La mucosa intestinal humana glucuronida el propofol in vitro y los estudios de dosificación oral en ratas indican que aproximadamente el 90% del fármaco administrado experimenta un metabolismo de primer paso, representando la extracción por la mucosa intestinal la mayor parte de esta eliminación presistémica (Raoof et al, Pharm. Res. 1996, 13, 891-895). Debido a su amplio metabolismo de primer paso, el propofol se administra por inyección o infusión intravenosa y no se ha considerado que la administración por vía oral sea terapéuticamente efectivo.
El propofol tiene una amplia variedad de aplicaciones biológicas y médicas que son evidentes a dosis subanestésicas e incluyen el tratamiento y/o la prevención de la cefalea por migraña intratable (Krusz et al, Headache 2000, 40, 224-230; Krusz, Publicación Internacional Nº WO 00/54588. El propofol, cuando se usa para mantener la anestesia, causa una menor incidencia de nauseas y vómitos postoperatorios (PONV) en comparación con agentes anestésicos por inhalación comunes y numerosos estudios clínicos controlados confirman la actividad antiemética del propofol (Tramer et al, Br. J. Anaesth. 1997, 78, 247-255; Brooker et al, Anaesth. Intensive Care 1998, 26, 625-629; Gan et al, Anesthesiology 1997, 87, 779-784). También se ha demostrado que el propofol tiene actividad antiemética cuando se usa junto con compuestos quimioterápicos (Phelps et al., Ann. Pharmacother. 1996, 30, 290-292; Borgeat et al., Oncology 1993, 50, 456-459; Borgeat et al., Can. J. Anaesth. 1994, 41, 1117-1119; Tomioka et al., Anesth. Analg. 1999, 89, 798-799). Las náuseas, arcadas y/o vómitos inducidos por una diversidad de agentes quimioterápicos (por ejemplo, cisplatino, ciclofosfamida, 5-fluorouracilo, metotrexato, fármacos de antraciclina, etc.) se han controlado por infusión de propofol a baja dosis en pacientes resistentes a la profilaxis con fármacos antieméticos convencionales (por ejemplo, antagonistas de la serotonina y corticosteroides).
También se ha usado propofol para tratar pacientes con estado epiléptico refractario (Brown et al., Pharmacother. 1998, 32, 1053-1059; Kuisma et al., Epilepsia 1995, 36, 1241-1243; Walder et al., Neurology. 2002, 58, 1327-1332; Sutherland et al., Anaesth. Intensive Care 1994, 22, 733-737). Además, los efectos anticonvulsivantes del propofol también se han demostrado en modelos de eficacia en ratas a dosis subanestésicas (Holtkamp et al., Ann. Neurol 2001, 49, 260-263; Hasan et al., Pharmacol. Toxicol. 1994, 74, 50-53).
También se ha usado propofol como antioxidante (Murphy et al., Br. J. Anaesth. 1992, 68, 613-618; Sagara et al., J. Neurochem. 1999, 73, 2524-2530; Young et al., Eur. J. Anaesthesiol. 1997, 14, 320-326; Wang et al., Eur. J. Pharmacol 2002, 452, 303-308). El propofol, a las dosis usadas típicamente para anestesia quirúrgica, tiene efectos antioxidantes observables en seres humanos (De la Cruz et al., Anesth. Analg. 1999, 89, 1050-1055). La patogénesis o las vías de daño posteriores en diversos trastornos neurodegenerativos implican especies de oxígeno reactivo y, por consiguiente, pueden tratarse o prevenirse con antioxidantes (Simonian et al., Pharmacol. Toxicol 1996, 36, 83-106). Los ejemplos de enfermedades neurodegenerativas específicas que pueden tratarse o prevenirse con antioxidantes incluyen, pero sin limitación, enfermedad de Friedrich, enfermedad de Parkinson, enfermedad de Alzheimer, enfermedad de Huntington, esclerosis lateral amiotrófica (ALS), esclerosis múltiple, enfermedad de Pick, enfermedades inflamatorias y enfermedades causadas por mediadores de la inflamación tales como el factor de necrosis tumoral (TNF) e IL-1.
Un problema significativo con la formulación y el uso de propofol es su escasa solubilidad en agua. Por consiguiente, el propofol debe formularse especialmente en medios acuosos usando solubilizantes o emulsionantes (Briggs et al., Anaesthesia 1982, 37, 1099-1101). Por ejemplo, en un producto comercial actual (Diprivan®, Astra-Zeneca) se usa una emulsión de aceite en agua (el emulsionante es la mezcla de lecitina Intralipid®) para formular el propofol (Picard et al., Anesth. Analg. 2000, 90, 963-969). Desgraciadamente, la formulación de emulsión de aceite en agua causa molestias y dolor en el sitio de inyección.
Una solución posible a la escasa solubilidad en agua del propofol, que evita el uso de aditivos, solubilizantes o emulsionantes y el dolor en el sitio de inyección correspondiente, es un profármaco de propofol soluble en agua estable que se convierte en propofol in vivo. (Hendler et al., Publicación Internacional Nº WO 99/58555; Morimoto et al., Publicación Internacional Nº WO 00/48572; Hendler et al., Patente de los Estados Unidos Nº 6.254.853; Stella et al., Solicitud de Patente de los Estados Unidos Nº US2001/0025035; Hendler, Patente de los Estados Unidos Nº 6.362.234; Hendler, Publicación Internacional Nº WO 02/13810; Sagara et al., J. Neurochem. 1999, 73, 2524-2530; Banaszczyk et al., Anesth. Analg. 2002, 95, 1285-1292; Trapani et al., Int. J. Pharm. 1998, 175, 195-204; Trapani et al., J. Med. Chem. 1998, 41, 1846-1854; Anderson et al., J. Med. Chem. 2001, 44, 3582- 3591; y Pop et al., Med. Chem. Res. 1992, 2, 16-21). Se han descrito profármacos de propofol que son suficientemente inestables en condiciones fisiológicas para proporcionar concentraciones terapéuticamente eficaces de propofol, particularmente cuando el profármaco se administra por vía oral (Gallop et al., Solicitud de Patente de los Estados Unidos de Nº de serie 10/766.990).
El documento WO 2004/033434 describe profármacos de propofol solubles en agua que son ésteres de a-aminoácidos de propofol que comprenden un aminoácido cíclico o lineal o un resto poli- u (oligo)sacárido.
Altomare et al., Eur. J. Pharm. Sci., 2003, Vol. 20, Nº 1, págs. 17-26, también describe ciertos ésteres de a-amino ácidos de propofol.
Trapani et al., Int. J. Pharm., 1998, vol. 175, págs. 195-204, describe ciertos derivados de glicinato, acetato, propionato, butirato y carbonato de propofol.
En general, se prefieren...
Reivindicaciones:
1. El compuesto ácido 2-amino-3-(2,6-diisopropilfenoxicarboniloxi)-propanoico, o una sal farmacéuticamente aceptable del mismo, o un solvato farmacéuticamente aceptable de cualquiera de los anteriores.
2. Un compuesto de acuerdo con la reivindicación 1, donde el compuesto es ácido (S)-2-amino-3-(2,6-diisopropilfenoxicarboniloxi)-propanoico, o una sal farmacéuticamente aceptable del mismo o un solvato farmacéuticamente aceptable de cualquiera de los anteriores.
3. Un compuesto de acuerdo con la reivindicación 1, donde la sal farmacéuticamente aceptable se selecciona entre sal clorhidrato, sal mesilato y sal trifluoroacetato.
4. Un compuesto de acuerdo con la reivindicación 2, donde la sal farmacéuticamente aceptable se selecciona entre sal clorhidrato, sal mesilato y sal trifluoroacetato.
5. Un compuesto de acuerdo con la reivindicación 4, donde el compuesto es una forma cristalina de la sal clorhidrato.
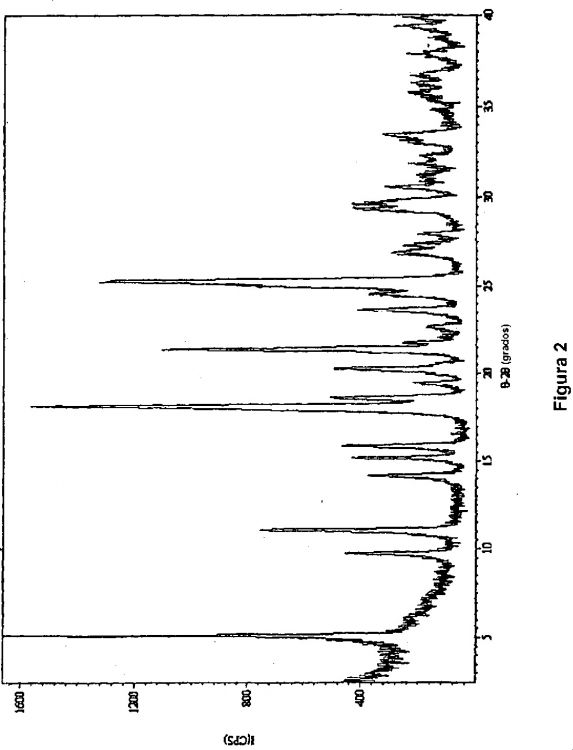
6. Un compuesto de acuerdo con la reivindicación 5, donde la forma cristalina de la sal clorhidrato tiene picos característicos (2?) a 5,1º
7. Un compuesto de acuerdo con la reivindicación 5, donde la forma cristalina de la sal clorhidrato tiene picos característicos (2?) a 5,1º
8. Un compuesto de acuerdo con la reivindicación 5, donde la forma cristalina de la sal clorhidrato tiene un punto de fusión de 188ºC a 189ºC.
9. Un compuesto de acuerdo con la reivindicación 4, donde el compuesto es una forma cristalina de la sal mesilato.
10. Un compuesto de acuerdo con la reivindicación 9, donde la forma cristalina de la sal mesilato tiene picos característicos (2?) a 4,2º
11. Un compuesto de acuerdo con la reivindicación 9, donde la forma cristalina de la sal mesilato tiene picos característicos (2?) a 4,2º
12. Un compuesto de acuerdo con la reivindicación 9, donde la forma cristalina de la sal mesilato tiene un punto de fusión de 166ºC a 167ºC.
13. Un procedimiento de preparación de sal cristalina del ácido 2-amino-3-(2,6-diisopropilfenoxicarboniloxi)-propanoico que comprende:
calentar la sal del ácido 2-amino-3-(2,6-diisopropilfenoxicarboniloxi)-propanoico en un disolvente en el que la solubilidad de la sal del ácido 2-amino-3-(2,6-diisopropilfenoxicarboniloxi)-propanoico depende de la temperatura para proporcionar una solución;
cambiar la temperatura de la solución para disminuir la solubilidad de la sal del ácido 2-amino-3-(2,6-diisopropilfenoxicarboniloxi)-propanoico que contiene para formar la sal cristalina del ácido 2-amino-3-(2,6-diisopropilfenoxicarboniloxi)-propanoico; y
aislar la sal cristalina del ácido 2-amino-3-(2,6-diisopropilfenoxicarboniloxi)-propanoico del disolvente.
14. Un procedimiento de acuerdo con la reivindicación 13, donde la sal se selecciona entre sal clorhidrato, sal mesilato y sal del ácido trifluoroacético.
15. Un procedimiento de acuerdo con la reivindicación 13 ó 14, donde el disolvente comprende etanol y tolueno y la temperatura de la solución es de entre 50ºC y la temperatura de reflujo del disolvente mixture.
16. Un procedimiento de acuerdo con cualquiera de las reivindicaciones 13 a 15, donde cambiar la temperatura de la solución comprende enfriar la temperatura de la solución hasta 25ºC.
17. Una composición farmacéutica que comprende un vehículo farmacéuticamente aceptable y una cantidad terapéuticamente efectiva de un compuesto de acuerdo con cualquiera de las reivindicaciones 1 a 12.
18. Una composición farmacéutica de acuerdo con la reivindicación 17, que comprende adicionalmente un anti-emético.
19. Una composición farmacéutica de acuerdo con la reivindicación 18, donde el anti-emético comprende un corticosteroide.
20. Una composición farmacéutica de acuerdo con la reivindicación 18, donde el anti-emético comprende un antagonista de la serotonina.
21. Una composición farmacéutica de acuerdo con la reivindicación 20, donde el antagonista de la serotonina es azasetrón, dolasetrón, granisetrón, ondansetrón, tropisetrón o palonosetrón.
22. Un compuesto de acuerdo con cualquiera de las reivindicaciones 1 a 12 para uso en un método de tratamiento del cuerpo humano o animal mediante terapia.
23. Un compuesto de acuerdo con cualquiera de las reivindicaciones 1 a 12 para uso en un método de tratamiento de dolor de cabeza, náuseas y vómitos postquimioterapia o postcirugía, un trastorno neurodegenerativo o un trastorno del estado de ánimo.
24. Un compuesto de acuerdo con cualquiera de las reivindicaciones 1 a 12 para uso en un método de tratamiento de migraña.
25. Un compuesto de acuerdo con cualquiera de las reivindicaciones 1 a 12 para uso en un método de tratamiento de epilepsia, enfermedad de Friedrich, enfermedad de Parkinson, enfermedad de Alzheimer, enfermedad de Huntington, esclerosis lateral amiotrófica, esclerosis múltiple o enfermedad de Pick.
26. Un compuesto de acuerdo con cualquiera de las reivindicaciones 1 a 12 para uso en un método de tratamiento de náuseas y vómitos.
27. Uso de un compuesto de acuerdo con cualquiera de las reivindicaciones 1 a 12 en la preparación de un medicamento para el tratamiento de dolor de cabeza, náuseas y vómitos postquimioterapia o postcirugía, un trastorno neurodegenerativo o un trastorno del estado de ánimo.
28. Uso de un compuesto de acuerdo con cualquiera de las reivindicaciones 1 a 12 en la preparación de un medicamento para el tratamiento de migraña.
29. Uso de un compuesto de acuerdo con cualquiera de las reivindicaciones 1 a 12 en la preparación de un medicamento para el tratamiento de epilepsia, enfermedad de Friedrich, enfermedad de Parkinson, enfermedad de Alzheimer, enfermedad de Huntington, esclerosis lateral amiotrófica, esclerosis múltiple o enfermedad de Pick.
30. Uso de un compuesto de acuerdo con cualquiera de las reivindicaciones 1 a 12 en la preparación de un medicamento para el tratamiento de náuseas y vómitos, donde el medicamento comprende adicionalmente un anti-emético.
31. Uso de un compuesto de acuerdo con la reivindicación 30, donde el anti-emético comprende un corticosteroide.
32. Uso de un compuesto de acuerdo con la reivindicación 30, donde el anti-emético comprende un antagonista de la serotonina.
33. Uso de un compuesto de acuerdo con la reivindicación 32, donde el antagonista de la serotonina es azasetrón, dolasetrón, granisetrón, ondansetrón, tropisetrón o palonosetrón.
Patentes similares o relacionadas:
Compuesto capaz de unirse al receptor de S1P y uso farmacéutico del mismo, del 25 de Septiembre de 2019, de ONO PHARMACEUTICAL CO., LTD.: Un compuesto representado por la formula (I-S-7a):**Fórmula** en el que el anillo A representa un grupo carbociclico C3-15; X representa un enlace o un grupo […]
Líquidos iónicos herbicidas con catión de tipo betaína, del 14 de Noviembre de 2018, de Przedsiebiorstwo Produkcyjno-Consultingowe ADOB sp. z o.o. sp.k. (100.0%): Un compuesto de líquido iónico de la fórmula general (I) **Fórmula** en la que - X representa Cl o CH3, - Y representa -CH2- o -CH2-CH(OH)-CH2-, […]
Métodos para la producción de L-carnitina, del 14 de Febrero de 2018, de LONZA LTD.: Un método para la producción de L-carnitina, que comprende las etapas de (a) proporcionar una disolución que comprende al menos 5% (p/p) de carnitina en un primer […]
Sales de adición de ácido del ácido 5-aminolevulínico o sus derivados, del 14 de Junio de 2017, de PHOTOCURE ASA: Una sal de adición de ácido de un éster del ácido 5-aminolevulínico (éster del 5-ALA) con ácido nítrico, en el que dicho éster del 5-ALA es un compuesto de fórmula X: […]
Métodos para sintetizar un elemento estructural de amatoxinas y amatoxinas, del 8 de Junio de 2016, de HEIDELBERG PHARMA GMBH: Método para la síntesis de g,d-dihidroxiisoleucina 1 o de un sintón para el compuesto 1, que comprende la etapa de metilar el compuesto 3 o 3* con yoduro de metilo en […]
Un proceso de hidrogenación de cetoésteres, del 27 de Enero de 2016, de LONZA LTD.: Un proceso para la produccion de un (S)- o (R)-4-halo-3-hidroxibutirato, que comprende la reaccion de un 4- haloacetoacetato con hidrogeno […]
Compuesto capaz de unirse a receptor SIP y uso farmacéutico del mismo, del 17 de Diciembre de 2014, de ONO PHARMACEUTICAL CO., LTD.: Un compuesto representado por la fórmula (I-S-7):**Fórmula** donde el anillo A representa un grupo cíclico; X representa -CH2-, -(CH2)2-, -(CH2)3-, […]
Proceso para la producción de tartrato de L-carnitina, del 3 de Diciembre de 2014, de LONZA LTD.: Un proceso para la producción de tartrato de L-carnitina, en el que el tartrato de L-carnitina se precipita a partir de una mezcla de reacción […]