DERIVADOS DE 3-ARILTIOINDOL-2-CARBOXAMIDA Y SUS ANALOGOS COMO INHIBIDORES DE CASEINA QUINASA I.
El uso de un compuesto para la fabricación de un medicamento para el tratamiento de enfermedades o trastornos del sistema nervioso central asociados a la disfunción del reloj circadiano humano,
que comprende administrar a un paciente una cantidad terapéuticamente eficaz de un compuesto de fórmula I, o un estereoisómero, enantiómero, racemato, tautómero o su sal farmacéuticamente aceptable,
Tipo: Resumen de patente/invención. Número de Solicitud: W05029306US.
Solicitante: AVENTIS PHARMACEUTICALS INC..
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 300 SOMERSET CORPORATE BOULEVARD,BRIDGEWATER, NEW JERSEY 08807.
Inventor/es: METZ,WILLIAM ARTHUR,JR.
Fecha de Publicación: .
Fecha Concesión Europea: 14 de Octubre de 2009.
Clasificación Internacional de Patentes:
- A61K31/404 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › Indoles, p. ej. pindolol.
Clasificación PCT:
- A61K31/404 A61K 31/00 […] › Indoles, p. ej. pindolol.
- A61P25/00 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › Medicamentos para el tratamiento de trastornos del sistema nervioso.
- A61P25/24 A61P […] › A61P 25/00 Medicamentos para el tratamiento de trastornos del sistema nervioso. › Antidepresivos.
Fragmento de la descripción:
Derivados de 3-ariltioindol-2-carboxamida y sus análogos como inhibidores de caseína quinasa I.
Antecedentes de la invención
Esta invención se refiere a métodos de uso de 3-ariltioindol-2-carboxamidas, 3-ariltioindol-2-carboxamidas 5-sustituidas y análogos relacionados como inhibidores de la fosforilación de caseína quinasa Ie humana de la proteína del reloj humano Period (hPER) que, por lo tanto, son útiles como agentes farmacéuticos, especialmente en el tratamiento y/o prevención de enfermedades y trastornos asociados con el sistema nervioso central.
Muchos organismos, que varían desde células sencillas hasta el ser humano, presentan variaciones rítmicas en el comportamiento. Cuando el ritmo persiste en condiciones constantes y tiene un periodo de aproximadamente un día, dependiendo un poco de la temperatura, el ritmo se denomina "circadiano" (Konopka, R.J. y Benzer, S. (1971) Proc. Nat. Acad. Sci. USA 68, 2112-2116).
Los ritmos circadianos son generados por marcapasos biológicos endógenos (relojes circadianos) y están presentes en la mayoría de los organismos vivos, incluyendo seres humanos, hongos, insectos y bacterias (Dunlap, J.C. (1999) Cell 96, 271-290; Hastings, J.W. et al. Circadian Rhythms, The Physiology of Biological Timing. En: Prosser, C.L. ed. "Neural and Integrative Animal Physiology", New York: Wiley-Liss (1991) 435-546; Allada, R. et al. (1998) Cell 93, 791-804; Kondo et al. (1994) Science 266, 1233-1236; Crosthwaite, S.K. et al. (1997) Science 276, 763-769; Shearman, L.P. et al. (1997) Neuron, 19, 1261-1269). Los ritmos circadianos son auto-mantenidos y constantes incluso en condiciones de oscuridad total, pero pueden sincronizarse con un nuevo régimen de día/noche por señales ambientales tales como ciclos de luz y temperatura (Pittendrigh, C. S. (1993) Annu. Rev. Physiol., 55, 16-54; Takahashi, J. S. (1995) Annu. Rev. Neurosci. 18, 531-553; Albrecht, U. et al. (1997) Cell, 91, 1055-1064). Los relojes circadianos son esenciales para el mantenimiento de los ritmos biológicos y regulan una diversidad de comportamientos circadianos tales como fluctuaciones diurnas en el comportamiento, ingesta de alimentos y ciclo de sueño/vigilia, así como cambios fisiológicos tales como secreción de hormonas y fluctuaciones en la temperatura corporal (Hastings, M. (1997) Trends Neurosci. 20, 459-464; Reppert, S.M. y Weaver, D.R. (1997) Cell 89, 487-490).
Estudios genéticos y moleculares de la mosca de la fruta Drosophila melanogaster condujeron al esclarecimiento de algunos de los genes implicados en los ritmos circadianos. Estos estudios condujeron al reconocimiento de una ruta que está muy auto-regulada y compuesta por un bucle de retroalimentación negativa basada en la transcripción/traducción (Dunlap, J.C. (1999) Cell, 96, 271-290; Dunlap, J.C. (1996) Annu. Rev. Genet. 30, 579-601; Hall, J.C. (1996) Neuron, 17, 799-802). Los elementos nucleares del oscilador circadiano en Drosophila consisten en dos proteínas estimuladoras dCLOCK/dBMAL (CYCLE) y dos proteínas inhibidoras dPERIOD (dPER) y dTIMELESS (dTIM). dCLOCK y dBMAL heterodimerizan formando el factor de transcripción dCLOCK/dBMAL que promueve la expresión de dos genes que se denominan Drosophila Period (dper) y Drosophila Timeless (dtim). Finalmente, se transcriben los ARNm de estos genes para producir las proteínas dPER y dTIM, respectivamente. Durante varias horas, los productos proteicos dPER y dTIM se sintetizan y fosforilan en el citoplasma, alcanzan un nivel crítico y forman heterodímeros que se translocan al núcleo. Una vez en el núcleo, dPER y dTIM funcionan como reguladores negativos de su propia transcripción, disminuye la acumulación de dPER y dTIM y comienza de nuevo la activación de dper y dtim por dCLOCK/dBMAL (Zylka, M.J. et al. (1998) Neuron 20, 1103-1110; Lowrey, P.L. et al. (2000) 288, 483-491). Se ha demostrado que el gen dper es un elemento necesario para controlar los ritmos circadianos en el comportamiento de eclosión de adultos (la aparición de la mosca adulta desde la pupa) y la actividad locomotora (Konopka, R.J., & Benzer, S. (1971) Proc. Natl. Acad. Sci. USA, 68, 2112-2116). Algunas mutaciones de sentido equívoco (missense) del gen per pueden acortar (perS) o alargar (perL) el periodo de ritmos circadianos, mientras que algunas mutaciones sin sentido (perO) producen una arritmicidad en sus comportamientos (Hall, J.C. (1995) Trends Neurosci. 18, 230-240).
En mamíferos, los núcleos supraquiasmáticos (SCN) del hipotálamo anterior son el sitio de un reloj biológico principal (como revisión, véase Panda et al., (2002) Nature 417, 329-335; Reppert, S. M. y Weaver, D. R. (1997) Cell 89, 487-490). El reloj de los SCN se embarca en el día de 24 horas por el ciclo diario de luz-oscuridad, actuando la luz a través de rutas de retina a SCN tanto directas como indirectas (Klein, D.C. et al. (1991) "Suprachiasmatic Nuclei: The Mind's Clock", Oxford Univeristy Press, New York). En los SCN de roedores, se han identificado y clonado tres genes Per, y se denominan Per1 de ratón (mPer1), mPer2 y mPer3. Las proteínas producto de estos genes de mamífero (mPER1, mPER2, mPER3) comparten varias regiones de homología entre ellas y cada gen Per de mamífero codifica una proteína con un dominio de dimerización de proteínas denominado PAS (PAS es un acrónimo de las tres primeras proteínas, PER, ARNT y SIM, encontradas que comparten este dominio de dimerización importante desde el punto de vista funcional) que es muy homólogo con el dominio PAS del PER de insectos. Todos los niveles de proteína y de ARN mensajero (ARNm) de Per oscilan durante el día circadiano y están implicados íntimamente en la regulación tanto positiva como negativa del reloj biológico, pero sólo mPER1 y mPER2 oscilan en respuesta a la luz (Zylka, M.J. et al. (1998) Neuron 20, 1103-1110; Albrecht, U. et al., (1997) Cell 91, 1055-1064; Shearman, L.P. et al. (1997) Neuron 19, 1261-1269). El homólogo en mamíferos del gen Drosophila tim ha sido clonado y se ha denominado mTim. Sin embargo, no había pruebas de interacciones mPER-mTIM análogas a las observadas en Drosophila, y se sugirió que las interacciones PER-PER pueden haber reemplazado la función de dímeros PER-TIM en las tareas moleculares del reloj circadiano de mamíferos (Zylka, M.J. et al., (1998) Neuron 21, 1115-1122). Otra posibilidad es que los ritmos en PER1 y PER2 forman bucles de retroalimentación negativa que regulan la actividad transcripcional de la proteína Clock (a través de sus dominios PAS) que, a su vez, dirige la expresión de uno o los dos genes Per (Shearman, L.P. et al. (1997) Neuron 19, 1261-1269).
La comprensión de las funciones de los tres genes mPer en el reloj de los mamíferos ha sido el objeto de muchas investigaciones. La homología estructural de las proteínas mPER con dPER condujo a la expectativa de que las proteínas mPER funcionaran como elementos negativos en el bucle de retroalimentación de mamíferos. Se piensa que PER1 está implicada en la desregulación de su propia transcripción en el bucle de retroalimentación, aunque pruebas recientes apuntan a que está implicada en la ruta de entrada (Hastings, M:H. et al. (1999) Proc. Natl. Acad. Sci. USA 26, 15211-15216). La PER2 es la proteína mejor caracterizada y los ratones mutantes para la PER2 (mPer2Brdm1), a los que les faltan los restos 87 en la porción carboxílica del dominio de dimerización PAS, tienen un ciclo circadiano más corto con regulaciones normales de luz-oscuridad, pero presentan arritmia en completa oscuridad. La mutación también disminuye la expresión oscilante tanto de mPer1 como de mPer2 en los SCN, indicando que mPer2 puede regular mPer1 in vivo (Zheng, B. et al. (1999) Nature 400, 169-173). Se ha demostrado que PER2 tiene una función doble en la regulación de los "engranajes" del reloj central (Shearman, L.P. et al. (2000) Science 288, 1013-1018). En ese estudio, se demostró que PER2 se unía a proteínas...
Reivindicaciones:
1. El uso de un compuesto para la fabricación de un medicamento para el tratamiento de enfermedades o trastornos del sistema nervioso central asociados a la disfunción del reloj circadiano humano, que comprende administrar a un paciente una cantidad terapéuticamente eficaz de un compuesto de fórmula I, o un estereoisómero, enantiómero, racemato, tautómero o su sal farmacéuticamente aceptable,
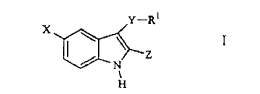
donde
X es H, Cl, F, Br, NO2, CN, OR2, NR2R2, HNSO2-alquilo C1-3, o NHCO-alquilo C1-3;
Y es -S(O)n- o -O- donde n es 0, 1 ó 2;
R1 es
- 1) arilo, sin sustituir o sustituido con uno o más de:
- 2) un heterociclo, sustituido o sin sustituir con uno o más:
- 3) alquilo C1-5, sustituido o sin sustituir con uno o más de:
Z es
- 1) C(=O)NR2R3 o
- 2) C(=O)R4;
R2 es hidrógeno o alquilo C1-3;
R3 es hidrógeno, alquilo C1-5, o cicloalquilo C3-6; y
R4 es 1-piperidinilo, 1-pirrolidinilo, 1-piperazinilo o 4-morfolinilo, sin sustituir o sustituido con uno o más de:
- 1) alquilo C1-5,
- 2) alcoxi C1-5,
- 3) OH,
- 4) halógeno, o
- 5) NR2R2.
2. El uso según se describe en la reivindicación 1, en el que dicho tratamiento causa una prolongación del periodo del ritmo circadiano.
3. El uso según se describe en la reivindicación 1, en el que la enfermedad o el trastorno es un trastorno del estado de ánimo o un trastorno del sueño.
4. El uso según se describe en la reivindicación 3, en el que el trastorno es un trastorno del estado de ánimo.
5. El uso según se describe de acuerdo con la reivindicación 4, en el que el trastorno del estado de ánimo se selecciona del grupo que consiste en un trastorno depresivo y un trastorno bipolar.
6. El uso según se describe en la reivindicación 5, en el que el trastorno depresivo es un trastorno depresivo mayor.
7. El uso según se describe en la reivindicación 5, en el que el trastorno bipolar se selecciona del grupo que consiste en un trastorno bipolar I y un trastorno bipolar II.
8. El uso según se describe en la reivindicación 3, en el que el trastorno es un trastorno del sueño.
9. El uso según se describe en la reivindicación 8, en el que el trastorno del sueño es un trastorno del sueño del ritmo circadiano.
10. El uso según se describe en la reivindicación 9, en el que el trastorno del sueño del ritmo circadiano se selecciona entre el grupo que consiste en trastorno del sueño por cambio de turno, síndrome de desfase horario, síndrome de la fase del sueño avanzada y síndrome de la fase del sueño retardada.
11. El uso de la reivindicación 1 en el que Y es S(O)2,
Z es C(=O)NH2 o C(=O)NHCH3, y
R1 es fenilo o piridinilo.
12. El uso de la reivindicación 11 en el que
Z es C(=O)NH2, y
R1 es fenilo.
13. El uso de la reivindicación 12 en el que el compuesto se selecciona entre el grupo que consiste en:
amida del ácido 3-bencenosulfonil-5-cloro-1H-indol-2-carboxílico, y
amida del ácido 3-bencenosulfonil-1H-indol-2-carboxílico.
14. El uso de la reivindicación 11 en el que
Y es S,
Z es C(=O)NHCH3, y
R1 es fenilo o piridinilo.
15. El uso de la reivindicación 14 en el que el compuesto se selecciona entre el grupo que consiste en:
metilamida del ácido 3-fenilsulfanil-1H-indol-2-carboxílico, y
metilamida del ácido 3-(piridin-2-ilsulfanil)-1H-indol-2-carboxílico.
16. El uso de la reivindicación 1 en el que
V es O3,
Z es C(=O)NH2, y
R1 es fenilo, fenilo sustituido, alquilo C1-5 o alquilo C1-5 sustituido.
17. El uso de la reivindicación 16 en el que el compuesto se selecciona entre el grupo que consiste en:
amida del ácido 3-fenoxi-1H-indol-2-carboxílico,
amida del ácido 3-(4-metoxi-fenoxi-1H-indol-2-carboxílico,
amida del ácido 3-(4-fluoro-fenoxi-1H-indol-2-carboxílico,
amida del ácido 3-(2-fluoro-fenoxi-1H-indol-2-carboxílico,
amida del ácido 3-(4-cloro-fenoxi-1H-indol-2-carboxílico,
amida del ácido 3-metoxi-1H-indol-2-carboxílico,
amida del ácido 3-etoxi-1H-indol-2-carboxílico,
amida del ácido 3-isopropoxi-1H-indol-2-carboxílico,
amida del ácido 3-terc-butoxi-1H-indol-2-carboxílico, y
amida del ácido 3-benciloxi-1H-indol-2-carboxílico.
18. El uso de la reivindicación 1, en el que:
Y es S, SO o S(O)2,
Z es C(=O)R4, y
R4 es 1-piperidinilo, 1-pirrolidinilo, 1-piperazinilo o 4-morfolinilo.
19. El uso de la reivindicación 18 en el que el compuesto se selecciona entre el grupo que consiste en:
(3-bencenosulfonil-5-cloro-1H-indol-2-il)-morfolin-4-il-metanona,
(5-fluoro-3-p-tolilsulfanil-1H-indol-2-il)-pirrolidin-1-il-metanona,
(3-fenilsulfanil1H-indol-2-il)-piperidin-1-il-metanona,
(5-fluoro-3-fenilsulfanil-1H-indol-2-il)-pirrolidin-1-il-metanona,
[3-(2-amino-fenilsulfanil)-1H-indol-2-il]-pirrolidin-1-il-metanona,
[3-(2-amino-fenilsulfanil)-1H-indol-2-il]-piperidin-1-il-metanona,
[3-(2-amino-fenilsulfanil)-5-fluoro-1H-indol-2-il]-piperidin-1-il-metanona,
[5-fluoro-3-(p-tolueno-4-sulfinil)-1H-indol-2-il]-pirrolidin-1-il-metanona,
hidrocloruro de (3-fenilsulfanil-1H-indol-2-il)-piperazin-1-il-metanona,
[5-fluoro-3-(piridin-2-ilsulfanil)-1H-indol-2-il]-pirrolidin-1-il-metanona,
[3-(piridin-2-ilsulfanil)-1H-indol-2-il]-pirrolidin-1-il-metanona,
piperidin-1-il-[3-(piridin-2-ilsulfanil)-1H-indol-2-il]-metanona, y
[5-fluoro-3-(piridin-2-ilsulfanil)-1H-indol-2-il]-piperidin-1-il-metanona.
20. El uso de la reivindicación 1 en el que
Y es S,
Z es C(=O)NH2; y
R1 es piridinilo.
21. El uso de la reivindicación 20 en el que el compuesto es amida del ácido 3-(piridin-2-ilsulfanil)-1H-indol-2-carboxílico.
22. El uso de la reivindicación 1 en el que
Y es S,
Z es C(=O)NH2, y
R1 es fenilo o fenilo sustituido.
23. El uso de la reivindicación 22 en el que el compuesto se selecciona entre el grupo que consiste en:
amida del ácido 3-fenilsulfanil-1H-indol-2-carboxílico,
amida del ácido 5-bromo-3-fenilsulfanil-1H-indol-2-carboxílico,
amida del ácido 3-(2-amino-fenilsulfanil)-5-metoxi-1H-indol-2-carboxílico,
amida del ácido 3-(3-fluoro-fenilsulfanil-1H-indol-2-carboxílico,
amida del ácido 3-(2-amino-fenilsulfanil)-5-bromo-1H-indol-2-carboxílico, y
amida del ácido 3-(2-amino-fenilsulfanil)-1H-indol-2-carboxílico.
Patentes similares o relacionadas:
Composiciones que comprenden una proteína de fusión de VIP-ELP para su uso en el tratamiento de fibrosis quística, del 29 de Julio de 2020, de Phasebio Pharmaceuticals, Inc: Una composición farmacéutica que comprende una proteína de fusión que comprende un péptido intestinal vasoactivo (VIP) y uno o más péptidos de tipo elastina (ELP), que […]
Análogos de indolina y usos de los mismos, del 8 de Julio de 2020, de Oncternal Therapeutics, Inc: Un compuesto que tiene la fórmula (I): **(Ver fórmula)** o un estereoisómero, una sal farmacéuticamente aceptable, o solvato del mismo, donde A se […]
Tratamiento de disfunción eréctil y otras indicaciones, del 1 de Julio de 2020, de STRATEGIC SCIENCE & TECHNOLOGIES, LLC: Una composición para su uso en un método de tratamiento de la disfunción sexual en un sujeto, preferiblemente un sujeto humano, comprendiendo la composición: […]
Forma de dosificación para su inserción en la boca, del 17 de Junio de 2020, de Nal Pharmaceutical Group Limited: Composición farmacéutica para aplicación a la mucosa oral que comprende: una matriz soluble en agua que comprende una cantidad eficaz de un agente farmacéuticamente […]
Compuestos heterocíclicos y métodos para su uso, del 8 de Abril de 2020, de NOVARTIS AG: Un compuesto de formula (I): **(Ver fórmula)** donde: X esta ausente e Y es -CHR3CH2-, -CH2CHR3-, -CHR3CHR4CH2-, -CH2CHR3CHR4-, -CH2CH2CHR3-, -CR3=CHCH2-, […]
Composiciones para el tratamiento del síndrome X frágil, del 8 de Abril de 2020, de CENTRE NATIONAL DE LA RECHERCHE SCIENTIFIQUE: Un abridor de un canal de potasio maxi-K para su uso en el tratamiento del síndrome X frágil, donde dicho abridor de canal de potasio […]
ACILHIDRAZONAS PARA EL TRATAMIENTO DE ENFERMEDADES NEUROLÓGICAS, del 2 de Abril de 2020, de CONSEJO SUPERIOR DE INVESTIGACIONES CIENTIFICAS (CSIC): La presente invención se refiere a un grupo de compuestos con un núcleo estructural de acilhidrazona que presentan capacidad moduladora de la interacción […]
Medicamentos para el tratamiento o la prevención de enfermedades fibróticas, del 25 de Marzo de 2020, de BOEHRINGER INGELHEIM INTERNATIONAL GMBH: 3-Z-[1-(4-(N-((4-metil-piperazin-1-il)-metilcarbonil)-N-metil-amino)-anilino)-1-fenil-metilen]-6-metoxicarbonil-2- indolinona, los tautómeros, los diastereómeros,…