Formas novedosas de éster metílico de CDDO.
Forma sólida vítrea de éster metílico de CDDO, que tiene un espectro de difracción de rayos X de polvo con un pico de halo a aproximadamente 13,
5ºde 2θ, tal como se muestra en la figura 2C, y una Tg.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2008/009703.
Solicitante: REATA PHARMACEUTICALS, INC.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 2801 GATEWAY DRIVE, SUITE 150 IRVING, TX 75063-2648 ESTADOS UNIDOS DE AMERICA.
Inventor/es: WALLING,John, PARENT,Stephan D, JONAITIS,David T, KRAL,Robert M.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K45/06 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 45/00 Preparaciones medicinales que contienen ingredientes activos no previstos en los grupos A61K 31/00 - A61K 41/00. › Mezclas de ingredientes activos sin caracterización química, p. ej. compuestos antiflojísticos y para el corazón.
- A61P35/00 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › Agentes antineoplásicos.
PDF original: ES-2382571_T3.pdf
Fragmento de la descripción:
Formas novedosas de éster metílico de CDDO
Referencia cruzada a solicitudes de patente relacionadas
Esta solicitud reivindica la prioridad de la solicitud provisional estadounidense 60/955.939, presentada el 15 de agosto de 2007.
Antecedentes de la invención
Los triterpenoides se biosintetizan en plantas mediante la ciclación de escualeno. Aunque son candidatas para uso medicinal, estas moléculas que se producen de manera natural presentan una actividad biológica relativamente débil. Por consiguiente, los químicos han tratado de sintetizar análogos de potencia aumentada (Honda et al., 1997 & 1998) .
Se notifican varios análogos sintéticos para suprimir la formación de novo de iNOS y COX-2 en macrófagos que se han estimulado mediante IFN-y o LPS (Suh et al., 1998; Honda et al., 2002) . Otro triterpenoide sintético, 2-ciano3, 12-dioxolean-1, 9 (11) -dien-28-oato (CDDO) , presenta actividad antiinflamatoria y antiproliferativa (Honda et al., 1998 & 2000) .
El estudio del éster metílico de CDDO, que es 2-ciano-3, 12-dioxoleana-1, 9 (11) -dien-28-oato de metilo (éster metílico de CDDO) , Bore et al. (2002) determinó una estructura cristalina. En esa forma, que está hidratada, el agua coordina interacciones que generan una estructura y un empaquetamiento cristalinos particulares.
Sumario de la invención
En una realización de la presente invención, se proporciona una forma cristalina no hidratada de éster metílico de CDDO. La forma cristalina no hidratada tiene preferiblemente un grupo espacial de P43 212 con dimensiones de la celda unidad de a = 14, 2 Å, b = 14, 2 Å y c = 81, 6 Å. La invención también contempla una composición farmacéutica en forma de dosificación sólida, que comprende (i) una cantidad terapéuticamente eficaz de una forma cristalina no hidratada de éster metílico de CDDO con (ii) un vehículo comestible.
Adicionalmente, la presente invención se presenta en una forma sólida vítrea de éster metílico de CDDO, que tiene un espectro de difracción de rayos X de polvo con un pico de halo a aproximadamente 13, 5º de 28, tal como se muestra en la figura 2C, y una temperatura de transición vítrea (Tg) . En realizaciones particulares, la Tg puede oscilar entre aproximadamente 120ºC y aproximadamente 135ºC. En otras realizaciones, la Tg oscila entre aproximadamente 125ºC y aproximadamente 130ºC. La forma sólida vítrea de éster metílico de CDDO puede tenerun espectro de PDF con picos similares a los de la figura 28 de desde aproximadamente 5 Å hasta aprox 20 Å.
Además, la invención proporciona una composición farmacéutica en forma de dosificación sólida, que comprende (i) una cantidad terapéuticamente eficaz de una forma sólida vítrea de éster metílico de CDDO con (ii) un vehículo comestible. A este respecto, una aplicación de la invención es una metodología para tratar un paciente con cáncer, que comprende: administrar una composición farmacéutica de este tipo a un paciente con cáncer. Una aplicación de la invención también contempla administrar la forma vítrea de éster metílico de CDDO en combinación con otro fármaco anticancerígeno. Por ejemplo, el fármaco anticancerígeno puede ser gemcitabina y el cáncer puede ser cáncer de páncreas. Una aplicación de la invención engloba también una metodología para el tratamiento de enfermedades o trastornos que implican inflamación y estrés oxidativo agudos o crónicos, particularmente los que se caracterizan en parte por la sobreexpresión de óxido nítrico sintasa inducible (iNOS) o ciclooxigenasa inducible (COX-2) .
Además, la invención se centra en una forma de solvato de dimetanol de éster metílico de CDDO, que tiene un espectro de difracción de rayos X de polvo con picos característicos tal como se muestra en la tabla 18 y un espectro de DSC tal como se muestra en la figura 24. De conformidad con la invención, la forma de solvato de dimetanol puede usarse como producto intermedio para la producción de una forma sólida vítrea de éster metílico de CDDO. Un método para la producción de la forma sólida vítrea de éster metílico de CDDO, a través de la forma de solvato de dimetanol, comprende preparar una forma de solvato de dimetanol de éster metílico de CDDO y secar la forma de solvato de dimetanol.
Según otra realización, la invención se centra en un método de crecimiento de un cristal de dimetanolato de éster metílico de CDDO, que comprende preparar una disolución de éster metílico de CDDO purificado en metanol anhidro caliente, añadir la disolución caliente a un recipiente de metanol enfriado, y fitrar los cristales resultantes.
Según otra realización, la invención se centra en una composición farmacéutica que comprende (i) una cantidad terapéuticamente eficaz de éster metílico de CDDO y (ii) un excipiente que es un formador de vidrio, de manera que la composición tiene una Tg.
El excipiente puede seleccionarse, por ejemplo, del grupo que consiste en (A) un hidrato de carbono, derivado de hidrato de carbono, o polímero de hidrato de carbono, (B) un polímero orgánico sintético, (C) una sal de ácido orgánico, (D) una proteína, un polipéptido, o péptido, y (E) un polisacárido de alto peso molecular. Son ilustrativos de la clase de excipientes de polímero orgánico sintético una hidroxipropil-metilcelulosa, tal como éster de ftalato de hidroxipropil-metilcelulosa, un poli[1- (2-oxo-1-pirrolidinil) etileno o copolímero del mismo, tal como PVP/VA, y un copolímero de ácido metacrílico, tal como copolímero de ácido metacrílico - acrilato de etilo (1:1) .
Otro excipiente a modo de ejemplo a este respecto es copovidona, que es copolímero de 1-vinil-2-pirrolidona acetato de vinilo (3:2) .
Breve descripción de los dibujos
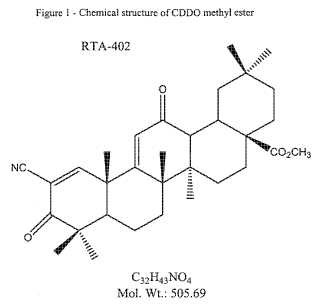
La figura 1 representa la estructura química del éster metílico de CDDO.
La figura 2 presenta el espectro de XRPD de la forma A (parte superior) y la forma B (parte inferior) . De arriba hacia abajo parte superior a parte inferior: forma A no micronizada; forma A micronizada; y forma B. La figura 3 muestra la curva de DSC y TG del éster metílico de CDDO (forma A) . La figura 4 muestra en análisis en platina caliente de la forma A - no micronizada. La figura 5 muestra la isoterma de sorción dinámica de vapor de la forma A - no micronizada. La figura 6 muestra las imágenes de SEM de la forma A - no micronizada. La figura 7 muestra la forma A antes (parte superior) y después (parte inferior) de estrés a 195ºC. La figura 8 muestra el espectro de RMN de la forma A - no micronizada. La figura 9 muestra la curva de MDSC de la forma B de éster metílico de CDDO. La figura 10 muestra la forma B de éster metílico de CDDO antes (parte superior) y después (parte inferior) de estrés térmico a 200ºC/HR ambiental durante 60 minutos. La figura 11 muestra el espectro de RMN de la forma B de éster metílico de CDDO. La figura 12 muestra un dibujo de ORTEP de una molécula individual de la forma A con marcaje. Se representan los átomos mediante elipsoides térmicos anisotrópicos de una probabilidad del 50%.
La figura 13 muestra un dibujo de ORTEP del contenido de la unidad asimétrica de los cristales de la forma A. Se representan los átomos mediante elipsoides térmicos anisotrópicos de una probabilidad del 50%. La figura 14 muestra un diagrama de empaquetamiento de los cristales de la forma A observados a lo largo del eje a cristalográfico.
La figura 15 muestra un diagrama de empaquetamiento de los cristales de la forma A observados a lo largo del eje b cristalográfico. La figura 16 muestra un diagrama de empaquetamiento de los cristales de la forma A observados a lo largo del eje c
cristalográfico. La figura 17 muestra el espectro de polvo de rayos X calculado de la forma A La figura 18 muestra el XRPD experimental de la forma A. La figura 19 presenta una comparación de los espectros de XRPD calculado y experimental para la forma A de éster metílico de CDDO. La figura 20 muestra un gráfico representativo del área bajo la curva para la forma A y la forma B, tras una administración oral de 4, 1 mg/kg a monos macacos. Cada punto de dato representa la concentración en plasma media de éster metílico de CDDO en 8 animales. Las barras de error representan la desviación estándar dentro de la población de la que se tomaron muestras. La figura 21 muestra una comparación de la concentración en plasma de la forma B de éster metílico de CDDO
frente a la forma A en el animal 505M (panel superior)... [Seguir leyendo]
Reivindicaciones:
1. Forma sólida vítrea de éster metílico de CDDO, que tiene un espectro de difracción de rayos X de polvo con un pico de halo a aproximadamente 13, 5ºde 28, tal como se muestra en la figura 2C, y una Tg.
2. Forma de solvato de dimetanol de éster metílico de CDDO, que tiene un espectro de difracción de rayos X de polvo con picos característicos tal como se muestra en la tabla 18 y un espectro de DSC tal como se muestra en la figura 24.
3. Composición farmacéutica en forma de dosificación sólida, que comprende (i) una cantidad terapéuticamente eficaz de la forma sólida vítrea de éster metílico de CDDO según la reivindicación 1 con (ii) un vehículo comestible.
4. Método para la producción de la forma sólida vítrea de éster metílico de CDDO según la reivindicación 1, que comprende (a) preparar una forma de solvato de dimetanol de éster metílico de CDDO, que tiene un espectro de difracción de rayos X de polvo con picos característicos tal como se muestra en la tabla 18 y un espectro de DSC tal como se muestra en la figura 24, y (b) secar la forma de solvato de dimetanol para obtener dicha forma sólida vítrea.
5. Forma sólida vítrea de éster metílico de CDDO según la reivindicación 1, que tiene un espectro de PDF con lospicos característicos de la figura 28 de desde aproximadamente 5 Å hasta aproximadamente 20 Å.
6. Composición farmacéutica según la reivindicación 3, para su uso en el tratamiento de un estado canceroso.
7. Composición farmacéutica según la reivindicación 6, que comprende además otro fármaco anticancerígeno.
8. Composición farmacéutica según la reivindicación 7, en la que el otro fármaco anticancerígeno es gemcitabina y el estado canceroso es cáncer de páncreas.
9. Forma sólida vítrea de éster metílico de CDDO según la reivindicación 1, que tiene un valor de Tg en el intervalo de aproximadamente 120ºC a aproximadamente 135ºC.
10. Forma sólida vítrea de éster metílico de CDDO según la reivindicación 1, que tiene un valor de Tg en el intervalo de aproximadamente 125ºC a aproximadamente 130ºC.
11. Composición farmacéutica que comprende (i) una cantidad terapéuticamente eficaz de éster metílico de CDDO y
(ii) un excipiente que es un formador de vidrio, de manera que dicha composición tiene una Tg.
12. Composición farmacéutica según la reivindicación 11, en la que el excipiente se selecciona del grupo que consiste en (A) un hidrato de carbono, derivado de hidrato de carbono o polímero de hidrato de carbono, (B) un polímero orgánico sintético, (C) una sal de ácido orgánico, (D) una proteína, un polipéptido o péptido, y (E) un polisacárido de alto peso molecular.
13. Composición farmacéutica según la reivindicación 12, en la que el excipiente es un polímero orgánico sintético.
14. Composición farmacéutica según la reivindicación 13, en la que el excipiente se selecciona del grupo que consiste en una hidroxipropil-metilcelulosa, un poli[1- (2-oxo-1-pirrolidinil) etileno o copolímero de los mismos, y un copolímero de ácido metacrílico.
15. Composición farmacéutica según la reivindicación 14, en la que el excipiente es éster de ftalato de hidroxipropilmetilcelulosa.
16. Composición farmacéutica según la reivindicación 14, en la que el excipiente es PVP/VA.
17. Composición farmacéutica según la reivindicación 14, en la que el excipiente es copolímero de ácido metacrílico
- acrilato de etilo (1:1) .
18. Composición farmacéutica según la reivindicación 13, en la que el excipiente es copovidona.
Patentes similares o relacionadas:
Compuestos y procedimientos de uso, del 29 de Julio de 2020, de Medivation Technologies LLC: Un compuesto de fórmula (Aa-1): **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, en la que: A representa H, halógeno, amino, […]
Complejos de agentes terapéuticos de base vírica y poli(beta-amino-ésteres) modificados, del 29 de Julio de 2020, de Sagetis Biotech, SL: Un complejo de un agente terapéutico de base vírica con un polímero de fórmula I: **(Ver fórmula)** donde cada L1 y L2 están seleccionados […]
Compuestos de alquinilbenceno heterocíclicos, y composiciones médicas y usos de los mismos, del 29 de Julio de 2020, de Guangzhou Healthquest Pharma Co., Ltd: Un compuesto de alquinilbenceno heterocíclico que tiene la fórmula (I) y una sal farmacéuticamente aceptable, o estereoisómero del mismo, **(Ver […]
 Composiciones y métodos para el tratamiento de trastornos de células plasmáticas y trastornos prolinfocíticos de células b, del 29 de Julio de 2020, de Knopp Biosciences LLC: Una composición que comprende una cantidad terapéuticamente eficaz de dexpramipexol para su uso en el tratamiento de un trastorno de células B caracterizado por niveles elevados […]
Composiciones y métodos para el tratamiento de trastornos de células plasmáticas y trastornos prolinfocíticos de células b, del 29 de Julio de 2020, de Knopp Biosciences LLC: Una composición que comprende una cantidad terapéuticamente eficaz de dexpramipexol para su uso en el tratamiento de un trastorno de células B caracterizado por niveles elevados […]
Derivados de piperidina 1,4 sustituidos, del 29 de Julio de 2020, de 89Bio Ltd: Un compuesto de acuerdo con la Fórmula I: **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, en donde: A se selecciona de […]
Profármacos de gemcitabina, del 29 de Julio de 2020, de NuCana plc: Una formulación farmacéutica que comprende gemcitabina-[fenil-benzoxi-L-alaninil)]-(S)-fosfato 3: **(Ver fórmula)** o una sal o solvato […]
Formas cristalinas de 6-((6,7-dimetoxiquinazolin-4-il)oxi)-N,2-dimetilbenzofuran-3-carboxamida, del 29 de Julio de 2020, de Hutchison Medipharma Limited: Forma I de 6-((6,7-dimetoxiquinazolin-4-il)oxi)-N,2-dimetilbenzofuran-3-carboxamida, en donde el difractograma de rayos X de polvo de la Forma […]
Utilización de anticuerpos optimizados en ADCC para tratar a los pacientes con bajo nivel de respuesta, del 22 de Julio de 2020, de LABORATOIRE FRANCAIS DU FRACTIONNEMENT ET DES BIOTECHNOLOGIES: Utilización de una composición de anticuerpo monoclonal quimérico, humanizado o humano de isotipo IgG1 anti- Rhesus del glóbulo rojo humano cuya […]