SALES MAGNÉSICAS DE INHIBIDORES DE LA REDUCTASA HMG-COA.
Forma cristalina de una sal magnésica de atorvastatina
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/IB2006/051396.
Solicitante: RANBAXY LABORATORIES LIMITED.
Nacionalidad solicitante: India.
Dirección: 12th Floor, Devika Tower 06, Nehru Place New Delhi 110019 INDIA.
Inventor/es: KUMAR, YATENDRA, KUMAR,Saridi Madhava Dileep, SATHYANARAYANA,Swargam.
Fecha de Publicación: .
Fecha Solicitud PCT: 3 de Mayo de 2006.
Clasificación Internacional de Patentes:
- C07D207/34 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07D COMPUESTOS HETEROCICLICOS (Compuestos macromoleculares C08). › C07D 207/00 Compuestos heterocíclicos que contienen ciclos de cinco miembros no condensados con otros ciclos, con solamente un átomo de nitrógeno como heteroátomo. › con heteroátomos o con átomos de carbono que tienen tres enlaces a heteroátomos con a lo sumo un enlace a halógeno, p. ej. radicales éster o nitrilo, unidos directamente a los átomos de carbono del ciclo.
Clasificación PCT:
- A61K31/40 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › que tienen ciclos con cinco eslabones con un nitrógeno como único heteroátomo de un ciclo, p. ej. sulpirida, succinimida, tolmetina, buflomedil.
- A61P3/00 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › Medicamentos para el tratamiento de trastornos del metabolismo (de la sangre o de fluido extracelular A61P 7/00).
- C07D207/34 C07D 207/00 […] › con heteroátomos o con átomos de carbono que tienen tres enlaces a heteroátomos con a lo sumo un enlace a halógeno, p. ej. radicales éster o nitrilo, unidos directamente a los átomos de carbono del ciclo.
Países PCT: Austria, Bélgica, Suiza, Alemania, Dinamarca, España, Francia, Reino Unido, Grecia, Italia, Liechtensein, Luxemburgo, Países Bajos, Suecia, Mónaco, Portugal, Irlanda, Eslovenia, Finlandia, Rumania, Chipre, Lituania, Letonia, Ex República Yugoslava de Macedonia, Albania.
PDF original: ES-2304911_T1.pdf




Fragmento de la descripción:
Sector de la presente invención
La presente invención se refiere a sales magnésicas cristalinas de atorvastatina de fórmula estructural I, procesos para su preparación, composiciones farmacéuticas de las mismas y composiciones para el tratamiento de mamíferos que sufren de hipercolesterolemia.
**(Ver fórmula)**
10 Antecedentes de la invención
La atorvastatina se representa por la Fórmula II y es un miembro de la clase de fármacos denominados estatinas. Las estatinas son actualmente los fármacos terapéuticamente más eficaces disponibles para la reducción de la concentración de partículas de lipoproteína de baja densidad (LDL) en el torrente sanguíneo de pacientes en riesgo de enfermedad cardiovascular.
**(Ver fórmula)**
20 El mecanismo de acción de las estatinas se ha elucidado con cierto detalle. Éstas interfieren con la síntesis del colesterol y otros esteroles en el hígado inhibiendo competitivamente la enzima reductasa 3-hidroxi-3-metil-glutaril-coenzima A ("reductasa HMG-CoA"). La reductasa HMG-CoA cataliza la conversión de HMG a mevalonato, que es la etapa determinante de la velocidad en la biosíntesis del colesterol. Esta inhibición conduce a una reducción en la concentración de colesterol en el hígado.
25 El documento EP 1336405 describe la atorvastatina amorfa que incluye atorvastatina magnésica amorfa. Describe además la atorvastatina amorfa de un tamaño de partícula determinado y la estabilización de la atorvastatina con un aditivo de sal de metal alcalino. Se hace referencia a la atorvastatina cristalina en términos de la formulación comercial de Lipitor®, que es atorvastatina cálcica cristalina.
30 El documento WO 2006/054308 (publicado el 26 de mayo de 2006) da a conocer una sal cálcica o magnésica de la atorvastatina, que puede ser amorfa o cristalina, específicamente la forma cristalina (VI) de la atorvastatina cálcica.
El documento WO 2006/084474 (publicado el 17 de agosto de 2006) se refiere una composición farmacéutica que contiene un inhibidor de reductasa HMGCoA a partir de un grupo extenso que comprende atorvastatina. Se menciona la atorvastatina magnésica cristalina sin dar a conocer ningún detalle sobre su caracterización o preparación.
El documento WO 2006/070248 (publicado el 6 de julio de 2006) se refiere a una mezcla de atorvastatina y
40 amlodipino. Se expone en términos generales que la atorvastatina, que incluye atorvastatina magnésica, puede existir en cualquiera de las formas en estado sólido disponibles, tales como amorfa, cristalina o cualquier otra forma polimérica.
Características de la invención
La presente invención da a conocer una forma cristalina de la sal magnésica de la atorvastatina que tiene
(a) un patrón de difracción de RX que comprende picos en valores de 2θ de aproximadamente 8,60, 16,14, 17,96 y 21,44 ± 0,2, y/o
(b) un espectro de IR que comprende bandas de absorción en aproximadamente 510,0, 525,0, 614,3, 692,0, 716,4, 755,9, 811,9, 847,4, 885,9, 916,9, 970,6, 1014,0, 1031,7, 1076,2, 1092,0, 1110,7, 1155,4, 1222,5, 1313,0, 1435,8, 1506,1, 1524,4, 1594,4, 1654,4, 1898,2, 1947,3, 2954,3, 3283,6, 3405,8, y 3667,3 cm-1 .
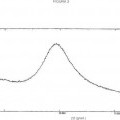
De este modo, la presente invención da a conocer una forma cristalina de una sal magnésica de la atorvastatina que tiene un patrón de difracción de RX esencialmente tal como el que se muestra en la figura 1.
La presente invención da a conocer además una forma cristalina de una sal magnésica de la atorvastatina que tiene un espectro de IR tal como el que se muestra en la figura 2.
Aún en otro aspecto se da a conocer un proceso para la preparación de éstas formas cristalinas de una sal magnésica de la atorvastatina, que comprende poner en contacto una sal de metal alcalino de atorvastatina con una sal magnésica de un ácido en un disolvente adecuado para formar atorvastatina magnésica.
En otro aspecto se da a conocer una composición farmacéutica que comprende la forma cristalina de la atorvastatina magnésica y uno o más de los excipientes, diluyentes y portadores farmacéuticamente aceptables.
En otro aspecto se dan a conocer las formas cristalinas anteriores de una sal magnésica de la atorvastatina para la inhibición de reductasa HMG-CoA en un mamífero. La aplicación comprende la administración, a un mamífero con necesidad de la misma, de una cantidad terapéuticamente eficaz de estas formas cristalinas de la atorvastatina magnésica.
En otro aspecto se dan a conocer las formas cristalinas anteriores de una sal magnésica de la atorvastatina para el tratamiento de hipercolesterolemia primaria, disbetalipoproteinemia o hipercolesterolemia homocigótica familiar. La aplicación comprende la administración, a un mamífero con necesidad de la misma, de una cantidad terapéuticamente eficaz de estas formas cristalinas de la atorvastatina magnésica.
Breve Descripción de los Dibujos
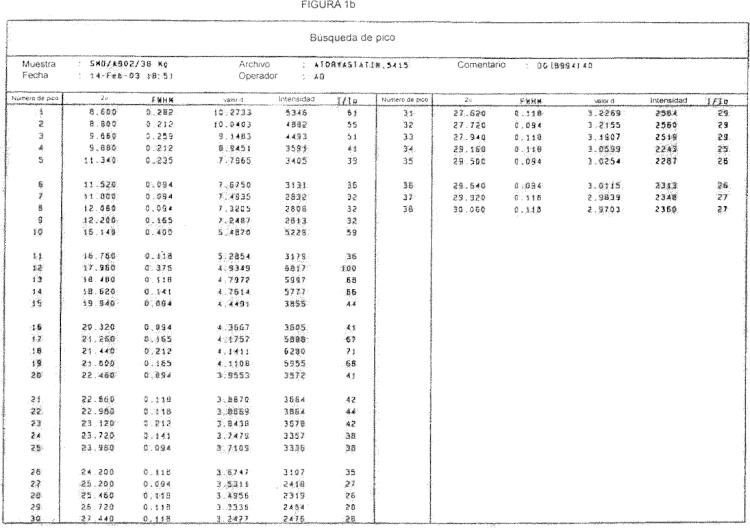
La figura 1a es un patrón de difracción de RX que muestra los picos característicos de la forma cristalina de la sal magnésica de la atorvastatina. La figura 1b es una lista de valores de pico e intensidades del patrón de difracción de RX de la figura 1a. La figura 2 es un espectro de infrarrojo que muestra las bandas de absorción características de la forma cristalina de la sal magnésica de la atorvastatina. La figura 3, como comparación, es un patrón de difracción de RX que muestra un halo que es característico de la atorvastatina magnésica amorfa. La figura 4, como comparación, es un espectro de infrarrojo que muestra las bandas de absorción características de la atorvastatina magnésica amorfa.
Descripción detallada de la invención
El término "atorvastatina magnésica" tal como se utiliza en la presente memoria descriptiva hace referencia a una sal, que incluye aniones atorvastatina y cationes magnésicos, en una forma cristalina.
Además, el término "atorvastatina magnésica" incluye además proporciones estequiométricas, como también no estequiométricas, de aniones atorvastatina y cationes magnésicos. La proporción de atorvastatina con respecto a magnesio no es necesariamente 1:1 para que se denomine atorvastatina magnésica. La atorvastatina magnésica puede estar formada como una sal que tiene una proporción molar 2:1 entre aniones atorvastatina y cationes magnésicos (es decir, atorvastatina hemimagnésica). La atorvastatina hemimagnésica se puede formar incluso cuando se utiliza un exceso de atorvastatina o un exceso de sal magnésica de un ácido en la formación de la sal.
La atorvastatina magnésica y particularmente la atorvastatina hemimagnésica puede existir en forma anhidra, hidratada y solvatada.
La forma cristalina de sal magnésica de la atorvastatina se puede caracterizar por DRX, con un patrón que se puede expresar en términos de la 2θ, los espaciados d y las intensidades relativas. Un ejemplo ilustrativo se muestra en la figura 1.
2**(Ver fórmula)**
(± 0,2) Espaciado d Intensidad I/Io 8,600 10,2733 5346 61 8,800 10,0403 4882 55 9,660 9,1483 4493 51 9,880 8,9451 3591 41 11,340 7,7965 3405 39 11,520 7,6750 3131 36 11,800 7,4935 2832 32 12,080 7,3205 2808 32 12,200 7,2487 2813 32 16,140 5,4870 5228 59 16,760 5,2854 3179 36 17,960 4,9349 8817 100 18,480 4,7972 5997 68 18,620 4,7614 5777 66 19,940 4,4491 3855 44 20,320 4,3667 3605 41 21,260 4,1757 5888 67 21,440 4,1411 6280 71 21,600 4,1108 5955 68 22,460 3,9553 3572 41 22,860 3,8870 3684 42 22,980 3,8669 3864 44 23,120 3,8438 3678 42 23,720 3,7479 3357 38 23,960 3,7109 3336 38 24,200 3,6747 3107 35 25,200 3,5311 2418 27 25,460 3,4956 2319 26 26,720 3,3336 2484 28 27,440 3,2477 2476 28 27620 3,2269 2564 29 27,720 3,2155 2560 29 27,940 3,1907 2519 29 29,160 3,0599 2243 25 29,500 3,0254 2287 26 29,640 3,0115 2313 26 29,920 2,9839 2348 27 30,060 2,9703 2360 27La forma cristalina de una sal magnésica de la atorvastatina se puede caracterizar por su espectro de IR. Un ejemplo ilustrativo de un espectro de este tipo en bromuro potásico se muestra en la figura 2. Se observan bandas de absorción características de la forma cristalina de la atorvastatina magnésica en 510,0, 525,0, 614,3, 692,0, 716,4, 755,9, 811,9, 847,4, 885,9, 916,9, 970,6, 1014,0, 1031,7, 1076,2, 1092,0, 1110,7, 1135,4, 1222,5, 1313,0, 1435,8, 1506,1, 1524,4, 1594,4, 1654,4, 1898,2, 1947,3, 2954,3, 3283,6, 3405,8, y 3667,3 cm-1 .
Además, la presente invención... [Seguir leyendo]
Reivindicaciones:
1. Forma cristalina de una sal magnésica de atorvastatina.
2. Forma cristalina, según la reivindicación 1, que tiene un patrón de difracción de RX substancialmente como el mostrado en la figura 1.
3. Forma cristalina, según la reivindicación 1, que tiene un espectro de IR substancialmente como el mostrado la figura 2.
4. Forma cristalina, según la reivindicación 1, que tiene un patrón de difracción de RX que comprende picos a valores de 2θ de, aproximadamente, 8,60, 16,14, 17,96, y 21,44
5. Forma cristalina, según la reivindicación 4, que comprende además picos característicos a valores de 2θ de, aproximadamente, 9,66 y 11,34
6. Forma cristalina, según la reivindicación 4, que comprende además picos característicos a valores de 2θ de, aproximadamente, 8,80, 18,48, 18,62, 21,26, y 21,60
7. Forma cristalina, según la reivindicación 1, en la que la sal magnésica de atorvastatina es una sal hemimagnésica.
8. Proceso para la preparación de la sal magnésica cristalina de atorvastatina, que comprende poner en contacto una sal de metal alcalino de atorvastatina con una sal magnésica de un ácido, en presencia de un disolvente, para formar una atorvastatina magnésica cristalina.
9. Proceso, según la reivindicación 8, en el que la sal de metal alcalino comprende una o más de atorvastatina potásica, de atorvastatina sódica y de atorvastatina lítica.
10. Proceso, según la reivindicación 8, en el que la sal magnésica de un ácido comprende una sal magnésica de cualquier ácido inorgánico u orgánico.
11. Proceso, según la reivindicación 8, en el que la sal magnésica de un ácido comprende uno o más de cloruro magnésico, nitrato magnésico, sulfato magnésico, fosfato magnésico, carbonato magnésico, dihidrogenofosfato magnésico, oxalato magnésico, acetato magnésico, lactato magnésico, succinato magnésico y citrato magnésico.
12. Proceso, según la reivindicación 8, en el que el disolvente comprende unos o más disolventes hidroxílicos.
13. Proceso, según la reivindicación 12, en el que los disolventes hidroxílicos comprenden agua, alcanoles menores y mezclas de los mismos.
14. Proceso, según la reivindicación 13, en el que los alcanoles menores comprenden alcoholes primarios, secundarios y terciarios que tienen de uno a seis átomos de carbono.
15. Proceso, según la reivindicación 13, en el que los alcanoles menores comprenden alcoholes primarios, secundarios y terciarios que tienen de uno a cuatro átomos de carbono.
16. Proceso, según la reivindicación 15, en el que los alcanoles menores comprenden uno o más de metanol, etanol, n-propanol, isopropanol, isobutanol, n-butanol y t-butanol.
17. Forma amorfa de una sal magnésica de atorvastatina.
18. Forma amorfa, según la reivindicación 17, que tiene un patrón de difracción de RX substancialmente como el mostrado en la figura 3.
19. Forma amorfa, según la reivindicación 17, que tiene un espectro de IR substancialmente como el mostrado en la figura 4.
20. Proceso para la obtención de atorvastatina magnésica amorfa que comprende:
a) disolver una atorvastatina magnésica cristalina en uno o más disolventes, y
b) eliminar el disolvente de la solución para obtener una atorvastatina magnésica amorfa.
21. Proceso, según la reivindicación 20, en el que se añade un codisolvente a la solución antes de la eliminación del disolvente.
22. Proceso para la obtención de atorvastatina magnésica amorfa que comprende:
a) disolver una atorvastatina magnésica cristalina en uno o más disolventes, y
b) añadir uno o más contra disolventes a la solución para obtener una atorvastatina magnésica amorfa.
23. Composición farmacéutica que comprende atorvastatina magnésica, según la reivindicación 1 o la reivindicación 17, y uno o más de los excipientes, diluyentes y portadores farmacéuticamente aceptables.
24. Método de tratamiento de la hipercolesterolemia primaria, disbetalipoproteinemia o hipercolesterolemia homocigótica familiar, que comprende la administración de una cantidad terapéuticamente efectiva de atorvastatina magnésica, según la reivindicación 1 o la reivindicación 17, a un mamífero en necesidad de la misma.
25. Método de inhibición de la reductasa HMG-CoA, que comprende la administración de una cantidad terapéuticamente efectiva de atorvastatina magnésica, según la reivindicación 1 o la reivindicación 17, a un mamífero en necesidad de la misma.
Patentes similares o relacionadas:
Proceso para la preparación de antagonistas de receptor androgénico e intermedios de los mismos, del 26 de Febrero de 2020, de ORION CORPORATION: Un proceso para la preparación de 2-cloro-4-(1H-pirazol-3-il)benzonitrilo de fórmula (V) **(Ver fórmula)** que comprende las etapas de […]
Derivados de pirrolamida sustituidos con glioxamida y su uso como medicamentos para el tratamiento de la hepatitis B, del 4 de Diciembre de 2019, de Janssen Sciences Ireland Unlimited Company: Un compuesto seleccionado entre los siguientes compuestos 1-102: Compuesto 1: (R)-4-(2-(sec-butilamino)-2-oxoacetil)-N-(4-fluoro-3-metilfenil)-1-metil-1H-pirrol-2-carboxamida; […]
Fenilpirrolcarboxamidas sustituidas con actividad terapéutica en VIH, del 6 de Noviembre de 2019, de NEW YORK BLOOD CENTER, INC.: Un compuesto representado por una fórmula A: **(Ver fórmula)** en donde Ph es fenilo opcionalmente sustituido; **(Ver fórmula)** […]
Compuestos de heteroarilo con una unidad acíclica como puente, del 31 de Julio de 2019, de INTERVET INTERNATIONAL B.V: Un compuesto de fórmula (I) y solvatos, N-óxidos y sales farmacéuticamente aceptables del mismo,**Fórmula** en la que R1 es halógeno, alquilo, […]
Formas de sal de de atorvastatina con benetamina, del 3 de Julio de 2019, de PFIZER PRODUCTS INC.: Una Forma A de atorvastatina con benetamina que tiene un patrón de difracción de rayos x en polvo que contiene los siguientes máximos 2θ medidos usando […]
Cristal de (S)-1-(2-Hidroxietil)-4-metil-N-[4-(metilsulfonil)fenil]-5-[2-(trifluorometil)fenil]-1H-pirrol-3-carboxamida, del 20 de Febrero de 2019, de DAIICHI SANKYO COMPANY, LIMITED: Un cristal de (S)-1-(2-hidroxietil)-4-metil-N-[4-(metilsulfonil)fenil]-5-[2-(trifluorometil)fenil]-1H-pirrol-3- carboxamida representado por el […]
Derivados de pirrol bicíclicos útiles como agonistas de GPR120, del 9 de Enero de 2019, de JANSSEN PHARMACEUTICA NV: Un compuesto de fórmula (I)**Fórmula** en el que R1 se selecciona del grupo que consiste de 3-fluorofenilo, 4-fluorofenilo, 2,4-difluorofenilo, […]
Derivados de pirrolamida sustituidos con glioxamida y su uso como medicamentos para el tratamiento de la hepatitis B, del 21 de Febrero de 2018, de Janssen Sciences Ireland UC: Un compuesto de Fórmula (IA)**Fórmula** o un estereoisómero o una forma tautomérica de este, donde: cada X representa independientemente CR7; R1, R2 […]