ESPIROPIPERIDILRIFAMICINAS PARA EL TRATAMIENTO DE INFECCIONES MICOBACTERIANAS.
Los compuestos de fórmula (1), sus sales farmacéuticamente aceptables y sus solvatos,
donde R1 es un radical seleccionado entre hidrógeno y alquilo; R2 se selecciona entre hidroxialquilo, fenilo,fenilo mono-sustituido y fenilo di-sustituido en posiciones 3 y4; R3 se selecciona entre fenilo, fenilo mono-sustituido y fenilodi-sustituido en posiciones 3 y 4; siendo los sustituyentes delfenilo de R2 y R3 seleccionados entre halógeno, (C1-C4)-alquilo y(C1-C4)- alcoxilo y R4 se selecciona entre hidrógeno, alquilo, alilo y homoalilo, son útiles para el tratamiento de infecciones micobacterianas, en particular para el tratamiento de infeccionesproducidas por Mycobacterium tuberculosis, Mycobacterium avium-intracellulare complex, o Mycobacterium kansasii
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/ES2005/000380.
Solicitante: UNIVERSIDAD DE OVIEDO.
Nacionalidad solicitante: España.
Provincia: ASTURIAS.
Inventor/es: BARLUENGA MUR,JOSE, AZNAR GOMEZ,FERNANDO, CABAL NAVES,MARIA-PAZ, GARCIA DELGADO,ANA-BELEN, VALDES GOMEZ,CARLOS.
Fecha de Publicación: .
Fecha Solicitud PCT: 4 de Julio de 2005.
Fecha Concesión Europea: 13 de Octubre de 2010.
Clasificación Internacional de Patentes:
- C07D519/00 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07D COMPUESTOS HETEROCICLICOS (Compuestos macromoleculares C08). › Compuestos heterocíclicos que contienen varios sistemas con varios heterociclos determinantes condensados entre sí o condensados con un sistema carbocíclico común no previstos en los grupos C07D 453/00 ó C07D 455/00.
Clasificación PCT:
- A61K31/438 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › estando el ciclo condensado en espiro con sistemas carbocíclicos o heterocíclicos.
- A61P31/04 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › A61P 31/00 Antiinfecciosos, es decir antibióticos, antisépticos, quimioterápicos. › Agentes antibacterianos.
- C07D235/14 C07D […] › C07D 235/00 Compuestos heterocíclicos que contienen ciclos de diazol-1,3 o diazol-1,3 hidrogenado, condensados con otros ciclos. › Radicales sustituidos por átomos de nitrógeno (por radicales nitro C07D 235/10).
- C07D307/83 C07D […] › C07D 307/00 Compuestos heterocíclicos que contienen ciclos de cinco miembros que tienen un átomo de oxígeno como único heteroátomo del ciclo. › Atomos de oxígeno.
- C07D498/22 C07D […] › C07D 498/00 Compuestos heterocíclicos que contienen en el sistema condensado al menos un heterociclo que tienen átomos de nitrógeno y oxígeno como únicos heteroátomos del ciclo (4-oxa-1-azabiciclo [3.2.0] heptanos, p. ej. oxapenicilinas C07D 503/00; 5-oxa-1-azabiciclo [4.2.0] octanos, p. ej. oxacefalosporinas C07D 505/00; aquéllos de sus análogos que tienen el átomo de oxígeno del ciclo en otra posición C07D 507/00). › en los que el sistema condensado contiene cuatro o más heterociclos.
Países PCT: Austria, Bélgica, Suiza, Alemania, Dinamarca, España, Francia, Reino Unido, Grecia, Italia, Liechtensein, Luxemburgo, Países Bajos, Suecia, Mónaco, Portugal, Irlanda, Eslovenia, Finlandia, Rumania, Chipre, Lituania, Letonia.
Fragmento de la descripción:
Espiropiperidilrifamicinas para el tratamiento de infecciones micobacterianas.
Esta invención se refiere a nuevos derivados de rifamicina de la familia de las espiropiperidilrifamicinas, que exhiben una alta actividad antibiótica, y también a un procedimiento para su preparación.
Estado de la técnica
La tuberculosis multirresistente se define como aquella tuberculosis que está ocasionada por cepas de Mycobacterium tuberculosis resistentes simultáneamente al menos a isoniacida y rifampicina. Su incidencia se ha incrementado en los últimos años de manera alarmante en numerosas regiones a lo largo del mundo. La importancia de este problema queda patente en la decisión tomada por la OMS en 1994 de poner en marcha un plan para el control y vigilancia a nivel mundial de la tuberculosis multirresistente (cfr. Guidelines for surveillance of drug resistance in tuberculosis WHO/TB/2003.320-WHO/CDS/RMD/2003.3). Entre las estrategias que se han planteado para hacer frente a este grave problema que amenaza la salud mundial, se encuentra el desarrollo de nuevos fármacos que permitan combatir con eficacia el tipo de cepas implicadas.
Los fármacos para el tratamiento de la tuberculosis se dividen en "fármacos de primera línea" y "fármacos de segunda línea". Los primeros, de mayor efectividad, resultan imprescindibles en cualquier régimen terapéutico para garantizar la curación de esta enfermedad. Solamente cuatro fármacos integran el primer grupo, a saber: isoniacida, rifampicina, pirazinamida, y etambutol. El resto de fármacos actualmente disponibles se engloban dentro de los "fármacos de segunda línea".
Para el tratamiento de la tuberculosis multirresistente es necesario usar combinaciones de fármacos durante largos períodos de tiempo. Actualmente, el tratamiento de elección tiene una duración de seis meses y contempla la administración al paciente de la asociación de isoniacida, rifampicina y pirazinamida durante dos meses, seguido de la administración de la asociación isoniacida y rifampicina cuatro meses más. Resulta pues de vital importancia desarrollar nuevos fármacos que permitan reforzar o mejorar el tratamiento de la tuberculosis multirre- sistente.
Por otro lado, relacionado con la epidemia del SIDA y debido al uso generalizado en la medicina moderna de fármacos antitumorales e inmunosupresores, se han incrementado las infecciones producidas por las denominadas "micobacterias atípicas" (también conocidas como "micobacterias ambientales oportunistas" o como "micobacterias no-tuberculosas"). Este término engloba a un buen número de especies diferentes de las que se desconoce tanto su modo de transmisión como sus mecanismos de resistencia a los antimicobacterianos. Dichas micobacterias atípicas se comportan como microorganismos habitualmente resistentes a los fármacos con actividad antimicobacteriana y suponen una seria amenaza. De las numerosas especies aisladas destaca por su frecuencia Mycobacterium avium-intracellulare complex, que produce serias infecciones diseminadas y que produce patología pulmonar indistinguible de la que produce M. tuberculosis. Mycobacterium avium-intracellulare complex se comporta como multirresistente a fármacos de "primera" y "segunda línea". En todos los regímenes terapéuticos se contempla la rifabutina como tratamiento de elección, asociado a un macrólido y a una quinolona. La elevada toxicidad in vivo de la rifabutina representa un inconveniente habitual. También destaca Mycobacterium kansasii que suele tener un patrón de sensibilidad mucho más variable, si bien suele exhibir resistencia a isoniacida y etambutol.
Las rifamicinas son unas sustancias químicas naturales que se aislaron por primera vez en 1959 de cultivos de Nocardia Mediterranei como una mezcla compleja de rifamicinas A-E (cfr. P. Sensi et al., Il Fármaco, Ed. Sc. 1959, vol. 14, pp. 146-147). Pertenecen a la familia de las ansamicinas, antibióticos de gran interés frente a bacterias Gram-positivas y micobacterias como M. tuberculosis. También poseen actividad frente a la DNA-dependiente RNA polimerasa bacteriana (cfr. C. Bartolucci et al., Fármaco 1992, vol. 47, p. 1367; C. Bartolucci et al., Pharm. Pharmacol. Lett, 1993, vol. 3, p. 1).
La estructura de las rifamicinas fue determinada por degradación química de la rifamicina S y por estudios espectroscópicos de RMN. Presentan como característica estructural común una cadena alifática de 17 átomos de carbono, llamada ansa, que conecta dos posiciones no adyacentes de un núcleo aromático plano cromóforo de naftohidroquinona unido por un grupo amida.
La actividad de estos compuestos es consecuencia de la inhibición específica de la RNA polimerasa bacteriana mediante la formación de un complejo 1:1 muy estable entre el fármaco y el enzima, como se ha puesto de manifiesto en una investigación sobre la rifampicina. Se ha propuesto un modelo en el que el enzima envuelve al fármaco por la cara hidrófila y por debajo del núcleo aromático, de tal forma que las posiciones C3 y C4 no participan en la unión. Los estudios de relación estructura-actividad llevados a cabo con distintas rifamicinas concluyen que para poder mantener la actividad inhibitoria son necesarios los siguientes elementos estructurales: grupo hidroxilo o cetona en C1 y C8, grupos hidroxilos en posición C21 y C23, una relación espacial determinada entre los grupos funcionales y un puente ansa (cfr. P. Sensi, P. Appl. Chem. 1975, vol. 41, pp. 15-29).
Se han preparado cientos de rifamicinas semisintéticas en un intento de obtener sustancias con mejores actividades biológicas; la mayor parte de ellas presentan modificaciones en las posiciones C4 (rifamida) y C3 (rifampicina). Estos cambios estructurales no afectan a la acción de las sustancias sobre el enzima de una forma crítica, sino que modifican otros parámetros importantes como la permeabilidad de las membranas celulares, las propiedades farmacocinéticas y la resorción (cfr. S. Lancini et al., "Structure-Activity Relationship among the Semisynthetic Antibiotics". D. Perlmann, Ed., Academic Press, N.Y. 1977, pp. 531-600).
Las espiropiperidilrifamicinas son una clase de antibióticos semisintéticos derivados de las rifamicinas en las cuales los carbonos C3 y C4 están incorporados a un anillo de imidazol que, a su vez, posee una piperidina espirocíclica (cfr. A. Sanfilippo et al., J. Antib. 1980, vol. 33, p. 1193; L. Marsili et al., J. Antib. 1981, vol. 34, p. 1033). El átomo de nitrógeno del anillo de la piperidina puede poseer diversos sustituyentes (restos alquilo lineales y ramificados, alquilos funcionalizados, bencilo, acetilo y etoxicarbonilo) (cfr. US 4.086.225; DE 2.825.445-A). Entre estas espiropiperidilrifamicinas, la rifabutina se ha empleado con fines terapéuticos como un multifármaco para el tratamiento de la tuberculosis y contra las infecciones Mycobacterium Avium-Mycobacterium intracellulare Complex (MAC) en pacientes con SIDA (cfr. US. 4.219.478).
De lo que se conoce en la técnica se deriva que es muy deseable proporcionar nuevos fármacos que posean actividad biológica no sólo contra la Mycobacterium tuberculosis, sino también contra las infecciones micobacterianas en general.
Explicación de la invención
Los inventores han encontrado nuevos derivados estructurales de espiropiperidilrifamicinas con actividad antimicobacteriana que es comparable, en muchos casos superior, a la que presentan los fármacos existentes en la actua- lidad.
Así, según un aspecto de la presente invención se proporciona un compuesto de fórmula (1), sus sales farmacéuticamente aceptables y sus solvatos, incluyendo hidratos, donde: R1 es hidrógeno; R2 se selecciona entre el grupo formado por fenilo, fenilo mono-sustituido, y fenilo di-sustituido en posiciones 3 y 4, siendo los sustituyentes del fenilo seleccionados entre el grupo formado por halógeno, (C1-C4)-alquilo y (C1-C4)-alcoxilo; R3 se selecciona entre el grupo formado por fenilo, fenilo mono-sustituido, y fenilo di-sustituido en posiciones 3 y 4 siendo los sustituyentes del fenilo seleccionados entre el grupo formado por halógeno, (C1-C4)-alquilo y (C1-C4)-alcoxilo; y R4 se selecciona...
Reivindicaciones:
1. Compuesto de fórmula (1),
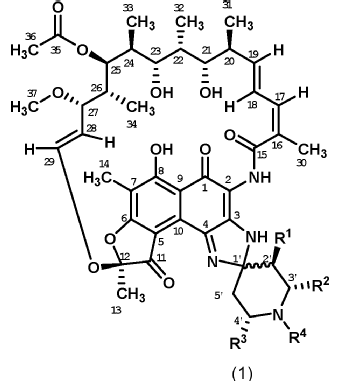
sus sales farmacéuticamente aceptables y sus solvatos, incluyendo hidratos, donde:
R1 es hidrógeno;
R2 se selecciona entre el grupo formado por fenilo, fenilo mono-sustituido y fenilo di-sustituido en posiciones 3 y 4, siendo los sustituyentes seleccionados entre el grupo formado por halógeno, (C1-C4)-alquilo y (C1-C4)-alcoxilo;
R3 se selecciona entre el grupo formado por fenilo, fenilo mono-sustituido y fenilo di-sustituido en posiciones 3 y 4, siendo los sustituyentes seleccionados entre el grupo formado por halógeno, (C1-C4)-alquilo y (C1-C4)-alcoxilo; y
R4 se selecciona entre el grupo formado por hidrógeno, (C1-C4)-alquilo; alilo, y homoalilo.
2. Compuesto según la reivindicación 1 donde, cuando R2 y R3 son fenilo mono- o di-sustituido, los sustituyentes del fenilo son independientemente seleccionados entre halógeno y (C1-C4)-alcoxilo.
3. Compuesto según la reivindicación 2, donde el alcoxilo es un metoxilo.
4. Compuesto según la reivindicación 1, donde R1 y R4 son hidrógeno; y R2 y R3 son fenilo.
5. Compuesto según la reivindicación 1, donde R1 y R4 son hidrógeno; y R2 y R3 son 4-metoxifenilo.
6. Compuesto según la reivindicación 1, donde R1 y R4 son hidrógeno; y R2 y R3 son 4-fluorofenilo.
7. Compuesto según la reivindicación 1, donde R1 y R4 son hidrógeno; y R2 y R3 son 2-iodofenilo.
8. Compuesto según la reivindicación 1, donde R1 es hidrógeno; R2 y R3 son fenilo; y R4 es alilo.
9. Compuesto según la reivindicación 1, donde R1 es hidrógeno; R2 y R3 son 4-metoxifenilo; y R4 es alilo.
10. Compuesto según la reivindicación 1, donde R1es hidrógeno; R2 y R3 son 3,4-dimetoxifenilo; y R4 es alilo.
11. Compuesto según la reivindicación 1, donde R1es hidrógeno; R2 y R3 son 4-fluorofenilo; y R4 es alilo.
12. Compuesto según la reivindicación 1, donde R1 es hidrógeno; R2 y R3 son 4-clorofenilo; y R4 es alilo.
13. Compuesto según la reivindicación 1, donde R1 es hidrógeno; R2 y R3 son 2-bromofenilo; y R4 es alilo.
14. Compuesto según la reivindicación 1, donde R1 es hidrógeno; R2 y R3 son 3-bromofenilo; y R4 es alilo.
15. Compuesto según la reivindicación 1, donde R1 es hidrógeno, R2 y R3 son 2-iodofenilo; y R4 es alilo.
16. Compuesto según la reivindicación 1, donde R1 es hidrógeno; R2 y R3 son fenilo; y R4 es homoalilo.
17. Compuesto según la reivindicación 1, donde R1 es hidrógeno; R2 y R3 son fenilo; y R4 es butilo.
18. Procedimiento de preparación del compuesto definido en la reivindicación 1, que comprende hacer reaccionar, en un disolvente adecuado, la 3-amino-4-iminorifamicina S de fórmula (3) con una 4-piperidona sustituida de fórmula (2) donde R1, R2, R3 y R4 tienen el mismo significado que en la reivindicación 1.
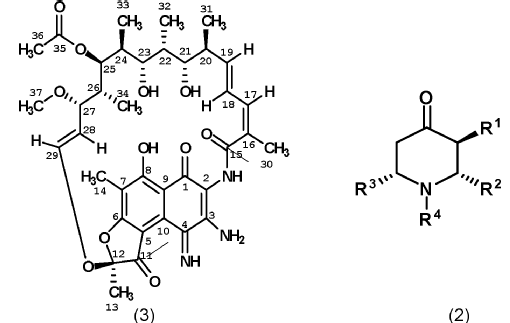
19. Procedimiento según las reivindicación 18, donde el disolvente es un éter cíclico.
20. Procedimiento según la reivindicación 19, donde el éter cíclico es el tetrahidrofurano.
21. Procedimiento según cualquiera de las reivindicaciones 18-20, donde la reacción se lleva a cabo en presencia de una base.
22. Procedimiento según la reivindicación 21, donde la base es acetato amónico.
23. Procedimiento según cualquiera de las reivindicaciones 18-21, donde la temperatura a la que se lleva a cabo la reacción es la temperatura de reflujo del disolvente.
24. Uso del compuesto definido en cualquiera de las reivindicaciones 1-17 para la preparación de un medicamento para el tratamiento de una infección micobacteriana.
25. Uso según la reivindicación 24, donde la infección micobacteriana es producida por una bacteria seleccionada entre el grupo formado por Mycobacterium tuberculosis, Mycobacterium avium-intracellulare complex, y Mycobacterium kansasii.
26. Composición farmacéutica para el tratamiento de infecciones micobacterianas, que comprende una cantidad terapéuticamente efectiva del compuesto definido en cualquiera de las reivindicaciones 1-17, juntamente con excipientes o portadores farmacéuticamente aceptables.
27. Compuesto definido en cualquiera de las reivindicaciones 1-17, para uso en el tratamiento de una infección micobacteriana.
28. Compuesto definido en cualquiera de las reivindicaciones 1-17, para uso según la reivindicación 27, donde la infección bacteriana se produce por una bacteria seleccionada del grupo formado por Mycobacterium tuberculosis, Mycobacterium avium-intracellulare complex, y Mycobacterium kansasii.
Patentes similares o relacionadas:
Derivados de z)-2-(1h-indol-3-il)-3-(isoquinolin-5-il)acrilonitrilo y compuestos relacionados con actividad inhibitoria de lisosoma y antimitótica para el tratamiento de enfermedades hiperproliferativas, del 10 de Junio de 2020, de NATIONAL UNIVERSITY OF SINGAPORE: Compuesto según la fórmula I, **(Ver fórmula)** donde, Z representa N o CR4; L representa -C(R6a)=C(R6b)-; X1 a X5 son independientemente […]
Derivados de benzodiazepina citotóxicos, del 10 de Junio de 2020, de IMMUNOGEN, INC.: Un compuesto citotóxico representado por la siguiente fórmula: **(Ver fórmula)** o una sal farmacéuticamente aceptable de estos, en donde: […]
Compuestos de piridina heterocíclicos de cinco miembros y método de preparación y uso de los mismos, del 3 de Junio de 2020, de SHANGHAI INSTITUTE OF MATERIA MEDICA, CHINESE ACADEMY OF SCIENCES: Un compuesto de piridina fusionado con heterociclo de 5 miembros que tiene una estructura de Fórmula (II), sales farmacéuticamente aceptables o solvatos […]
Compuestos policíclicos como inhibidores de quinasa de tirosina de Bruton, del 3 de Junio de 2020, de JANSSEN PHARMACEUTICA NV: Un compuesto de Fórmula (I): **(Ver fórmula)** en donde R1 es H; R2 se selecciona del grupo que consiste en: CH2-ciclohexilo, en donde el ciclohexilo está […]
Derivados de podofilotoxina y su uso, del 3 de Junio de 2020, de CALIFORNIA PACIFIC MEDICAL CENTER: Un compuesto de fórmula (I): **(Ver fórmula)** o un N-óxido del mismo, o una sal farmacéuticamente aceptable de cada uno de los mismos, […]
Compuestos y composiciones para inhibir la actividad de shp2, del 20 de Mayo de 2020, de NOVARTIS AG: Un compuesto seleccionado de formula I y II: **(Ver fórmula)** en el que: R1 se selecciona de: **(Ver fórmula)** R2 y R3 junto con el nitrogeno al que estan […]
Compuesto de pirimidina condensado o sal del mismo, del 15 de Abril de 2020, de TAIHO PHARMACEUTICAL CO., LTD.: Un compuesto de pirimidina condensado representado por la siguiente fórmula (I): **(Ver fórmula)** en el que, en la fórmula, X representa un grupo […]
Derivados de 4-amino-2-(1H-pirazolo[3,4-b]piridin-3-il)-6-oxo-6,7-dihidro-5H-pirrolo[2,3-d]pirimidina y los respectivos derivados de (1H-indazol-3-il) como moduladores de GMPc para el tratamiento de enfermedades cardiovasculares, del 1 de Abril de 2020, de MERCK SHARP & DOHME CORP: Un compuesto de la Fórmula (I) **(Ver fórmula)** o una de sus sales farmacéuticamente aceptables, en la que: X es C(H) o N; cada R1 es independientemente […]