CONJUGADOS QUE COMPRENDEN UNA PORCION DE GM-CSF Y UN POLIMERO.
Una composición farmacéutica que comprende: (i)un producto conjugado que comprende un GM-CSF humano unido covalentemente,
directamente o a través de un radical espaciador compuesto de uno o más átomos, a un polímero soluble en agua, que tiene la siguiente estructura: donde cada (n) es independientemente un número entero que tiene un valor de 3 a 4.000, y que tiene un peso molecular medio ponderal de más de 5.000 Daltons; y (ii)un excipiente farmacéuticamente aceptable, donde al menos aproximadamente 85% de los productos conjugados en la composición tienen de uno a dos polímeros anclado al GM-CSF humano
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2005/025052.
Solicitante: NEKTAR THERAPEUTICS.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 201 INDUSTRIAL ROAD SAN CARLOS, CA 94070 ESTADOS UNIDOS DE AMERICA.
Inventor/es: BOSSARD,Mary,J. , ZHANG,Ping.
Fecha de Publicación: .
Fecha Solicitud PCT: 14 de Julio de 2005.
Clasificación Internacional de Patentes:
- A61K47/48H4P
Clasificación PCT:
- A61K47/48
- A61P35/00 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › Agentes antineoplásicos.
Países PCT: Austria, Bélgica, Suiza, Alemania, Dinamarca, España, Francia, Reino Unido, Grecia, Italia, Liechtensein, Luxemburgo, Países Bajos, Suecia, Mónaco, Portugal, Irlanda, Eslovenia, Finlandia, Rumania, Chipre, Lituania, Letonia, Ex República Yugoslava de Macedonia, Albania.
Fragmento de la descripción:
Conjugados que comprenden una porción de GM-CSF y un polímero.
Campo de la invención
La presente invención se refiere generalmente a productos conjugados que comprenden una porción de GM-CSF (es decir, una porción que tiene actividad GM-CSF) y un polímero. Además, la invención se refiere a composiciones que comprenden los productos conjugados.
Antecedentes de la invención
Una función importante del sistema hematopoyético humano es la reposición de una diversidad de glóbulos blancos (incluyendo macrófagos, neutrófilos, y basófilos/mastocitos), glóbulos rojos (es decir, eritrocitos) y células formadoras de coágulos (p. ej., megacariocitos/plaquetas). Cada una de estas células especializadas se forma a partir de células precursoras hematopoyéticas localizadas en la médula ósea. Glicoproteínas de tipo hormona específicas denominadas "factores estimuladores de colonias" controlan la diferenciación y la maduración de las células precursoras hematopoyéticas en cada una de las varias células sanguíneas especializadas.
Uno de tales factores estimuladores de colonias es el factor estimulador de colonias de granulocitos y macrófagos o "GM-CSF". Como su nombre implica, este factor estimulador de colonias promueve la proliferación y la diferenciación de glóbulos blancos tales como granulocitos y macrófagos, si bien GM-CSF puede promover también la formación de otros tipos celulares. El GM-CSF es producido por varios tipos celulares diferentes (incluyendo células T activadas, células B, macrófagos, mastocitos, células endoteliales y fibroblastos) en respuesta a citoquinas, estímulos inmunitarios e inflamatorios. El GM-CSF nativo es una glicoproteína de 127 aminoácidos y puede tener una diversidad de pesos moleculares dependiendo del grado de glicosilación.
Farmacológicamente, el GM-CSF ha sido administrado a pacientes con cáncer con el fin de acelerar la reposición de glóbulos blancos que son destruidos durante los tratamientos de quimioterapia. Con el propósito similar de acelerar la reposición de glóbulos blancos, este factor estimulador de colonias ha sido administrado a pacientes con leucemia que experimentan terapia de reposición de médula ósea. Se han propuesto aplicaciones adicionales, tales como la curación acelerada de heridas. Véase, por ejemplo, la Patente de los Estados Unidos Núm. 6.689.351.
Una desventaja asociada con las formas actuales de terapia con GM-CSF es la frecuencia de dosificación. Puesto que la terapia con GM-CSF requiere por lo general inyecciones diarias, los pacientes tienen aversión por la inconveniencia y la incomodidad asociadas con este régimen. Asociado con el hecho de que los pacientes requieren análisis de sangre frecuentes para determinar los recuentos de glóbulos blancos (que requieren visitas a un profesional de la salud), muchos pacientes preferirían una alternativa que fuera menos incómoda y/o implicara una reducción del número de inyecciones.
Una solución propuesta a estos problemas ha sido proporcionar una forma de liberación prolongada de GM-CSF. Por ejemplo, la Patente de los Estados Unidos Núm. 5.942.253 describe microesferas de poli(ácido láctico-co-ácido glicólico) u otros polímeros biodegradables de GM-CSF. La formación de microesferas, no obstante, puede ser un proceso complejo, que requiere varias etapas sintéticas. De este modo, este enfoque de liberación prolongada adolece de complejidades que se evitan idealmente.
La PEGilación, o el anclaje de un derivado de poli(etilenglicol) a una proteína, se ha descrito como un medio para prolongar la vida media in vivo de una proteína, dando como resultado la prolongación de la actividad farmacológica. Por ejemplo, la Patente de los Estados Unidos Núm. 5.880.255 describe un producto conjugado de GM-CSF y poli(etilenglicol) formado a partir de una reacción con monometoxipoli(etilenglicol) lineal derivatizado con 2,2,2-trifluoroetanosulfonato que tiene un peso molecular de 5.000 Daltons.
Saifer et al "Polymer Preprints", vol 38, 1997 págs. 576-577, describen productos conjugados de PEG-GH-CSF donde las cadenas de PEG son lineales.
No obstante, a pesar de este producto conjugado descrito, persiste la necesidad de otros productos conjugados de GM-CSF que posean, por ejemplo, un polímero que tenga un peso molecular mayor de 5.000 Daltons, un polímero que tenga una estructura diferente (p. ej., una estructura ramificada y/o en tenedor), diferentes sitios de anclaje, sitios de anclaje de sitio específico o de sitio selectivo, etcétera.
De este modo, persiste la necesidad en la técnica de proporcionar productos conjugados de porciones de GM-CSF-polímero adicionales. Entre otras cosas, una o más realizaciones de la presente invención están dirigidas por lo tanto a tales productos conjugados así como a composiciones que comprenden los productos conjugados y métodos relacionados descritos en la presente memoria, que se cree que son nuevos y no han sido propuestos en absoluto por la técnica.
Compendio de la invención
Una composición farmacéutica que comprende:
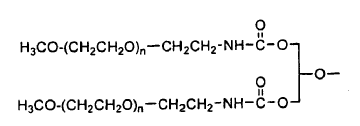
donde al menos aproximadamente 85% de los productos conjugados en la composición tienen de uno a dos polímeros anclados a GM-CSF humano.
Breve descripción de las figuras
La Fig. 1 es el cromatograma que sigue al análisis SEC-HPLC de una solución de producto conjugado como se describe en el Ejemplo 1.
La Fig. 2 es el cromatograma que sigue a la purificación de intercambio aniónico de una composición descrita en el Ejemplo 1.
La Fig. 3 muestra los resultados de la SDS-PAGE de las fracciones de producto conjugado como se describe en el Ejemplo 1.
La Fig. 4 es el cromatograma que sigue al análisis SEC-HPLC de una solución de producto conjugado como se describe en el Ejemplo 2.
La Fig. 5 es el cromatograma que sigue a la purificación de intercambio aniónico de una composición como se describe en el Ejemplo 3.
La Fig. 6 es el cromatograma que sigue al análisis SEC-HPLC de una solución de producto conjugado como se describe en el Ejemplo 4.
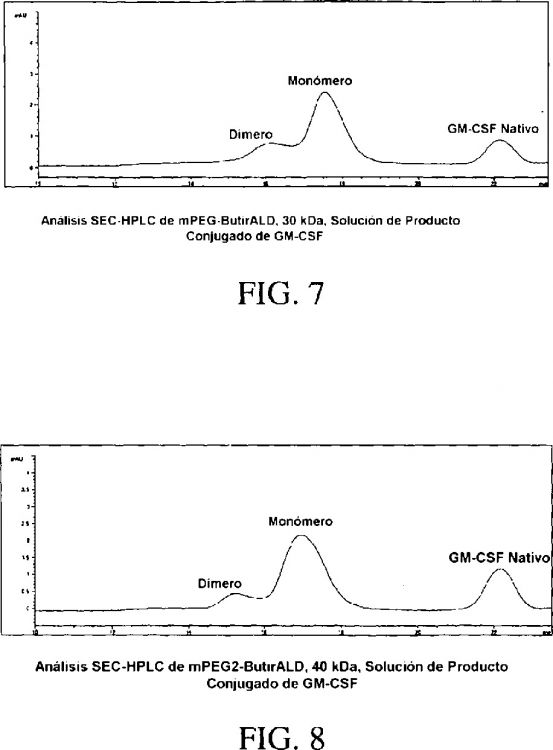
La Fig. 7 es el cromatograma que sigue al análisis SEC-HPLC de una solución de producto conjugado como se describe en el Ejemplo 5.
La Fig. 8 es el cromatograma que sigue al análisis SEC-HPLC de una solución de producto conjugado como se describe en el Ejemplo 6.
Descripción detallada de la invención
La porción de GM-CSF
La porción de GM-CSF se puede obtener a partir de métodos no recombinantes o a partir de métodos recombinantes.
La porción de GM-CSF se puede obtener no recombinantemente. Por ejemplo, el GM-CSF se puede obtener de fuentes derivadas de sangre. En particular, el GM-CSF se puede aislar de plasma o tejidos humanos utilizando técnicas (p. ej., técnicas de precipitación, técnicas de centrifugación, técnicas cromatográficas) conocidas por los expertos normales en la técnica.
La porción de GM-CSF se puede obtener a partir de métodos recombinantes. Por ejemplo, se ha aislado, caracterizado, y clonado en vectores de expresión el ADNc que codifica el GM-CSF humano. Véanse, p. ej., las Patentes de los Estados Unidos Núms. 5.078.996 y 5.891.429, y Wong et al. (1985) "Human GM-CSF: Molecular Cloning of the Complementary DNA y Purification of the Natural and Recombinant Proteins", Science 218:819, y Cantrell et al. (1985) "Cloning, Sequence, and Expression of a Human Granulocyte/Macrophage Colony-Stimulating Factor," Proc. Natl. Acad. Sci. U.S.A., Vol. 82: 6250. Se pueden utilizar las porciones de GM-CSF expresadas en sistemas de expresión bacterianos...
Reivindicaciones:
1. Una composición farmacéutica que comprende:
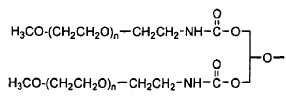
donde al menos aproximadamente 85% de los productos conjugados en la composición tienen de uno a dos polímeros anclado al GM-CSF humano.
2. La composición de la reivindicación 1, donde el poli(etilenglicol) tiene un peso molecular medio ponderal total en el intervalo de más de 5.000 Daltons a aproximadamente 150.000 Daltons.
3. La composición de la reivindicación 2, donde el poli(etilenglicol) tiene un peso molecular medio ponderal total en el intervalo de aproximadamente 6.000 Daltons a aproximadamente 100.000 Daltons.
4. La composición de la reivindicación 3, donde el poli(etilenglicol) tiene un peso molecular medio ponderal total en el intervalo de aproximadamente 15.000 Daltons a aproximadamente 85.000 Daltons.
5. La composición de la reivindicación 4, donde el poli(etilenglicol) tiene un peso molecular medio ponderal total en el intervalo de aproximadamente 20.000 Daltons a aproximadamente 85.000 Daltons.
6. La composición de la reivindicación 5, donde el poli(etilenglicol) tiene un peso molecular medio ponderal total en el intervalo de aproximadamente 20.000 Daltons a aproximadamente 60.000 Daltons.
7. La composición de la reivindicación 1, con la condición de que el polímero soluble en agua ramificado carece de un residuo de lisina utilizado para efectuar la ramificación.
8. La composición de la reivindicación 1, donde el GM-CSF humano comprende una secuencia de aminoácidos de SEQ ID NO: 1.
9. La composición de la reivindicación 6, donde el GM-CSF humano comprende una secuencia de aminoácidos del SEQ ID NO: 2.
10. La composición de la reivindicación 6, donde el GM-CSF humano es obtenido recombinantemente.
11. La composición de la reivindicación 9, donde el GM-CSF humano no está glicosilado.
12. La composición de la reivindicación 9, donde el GM-CSF humano está glicosilado.
13. La composición de la reivindicación 1, donde la composición está sustancialmente libre de albúmina.
14. La composición de la reivindicación 1, donde la composición está sustancialmente libre de proteínas que no tienen actividad GM-CSF.
15. La composición de la reivindicación 1, donde la composición está sustancialmente libre de polímeros solubles en agua unidos no covalentemente.
16. La composición de la reivindicación 1, en forma liofilizada.
17. La composición de la reivindicación 1, en forma líquida.
18. La composición de la reivindicación 1, donde al menos aproximadamente 90% de los productos conjugados en la composición tienen de uno a dos polímeros anclados al GM-CSF humano.
19. La composición de la reivindicación 18, donde al menos aproximadamente 95% de los productos conjugados en la composición tienen de uno a dos polímeros anclados al GM-CSF humano.
20. La composición farmacéutica de reivindicación 1, para su uso en terapia.
21. La composición de la reivindicación 20, en una forma adecuada para su inyección subcutánea.
Patentes similares o relacionadas:
INTERLEUCINA-10 PEGILADA, del 10 de Noviembre de 2011, de SCHERING CORPORATION: Una interleucina-10 monopegilada (mono-PEG-IL-10) que comprende una o varias moléculas de polietilenglicol (PEG) unidas covalentemente mediante un conector a un resto […]
COPOLÍMERO DE BLOQUES PARA CONJUGADOS DE FÁRMACO Y SUS COMPOSICIONES FARMACÉUTICAS, del 20 de Septiembre de 2011, de NANOCARRIER CO., LTD: Un copolímero de bloques para un conjugado de fármaco, comprendiendo dicho copolímero una región de polímero soluble en agua que consiste en polietilenglicol y una […]
NUEVAS COMPOSICIONES QUÍMICAMENTE MODIFICADAS DE PROTEÍNA QUE ESTIMULAN ERITROPOYETINA Y MÉTODOS, del 20 de Septiembre de 2011, de AMGEN INC.: Una preparación de nueva proteína estimulante de eritropoyetina químicamente modificada (NESP), opcionalmente en un diluyente, portador o […]
ANTAGONISTAS DE LEPTINA, del 18 de Julio de 2011, de YISSUM RESEARCH DEVELOPMENT COMPANY OF THE HEBREW UNIVERSITY OF JERUSALEM LTD. INSTITUT NATIONAL DE LA RECHERCHE AGRONOMIQUE (INRA) UNIVERSITÉ PIERRE ET MARIE CURIE (PARIS VI): Un antagonista de leptina sintético que consiste en: (a) un polipéptido de leptina de mamífero en el que el sitio de unión hidrófobo LDFI en las posiciones correspondientes […]
 INHIBIDORES DUALES ANTITROMBÓTICOS ANTICOAGULANTES QUE COMPRENDEN UNA MARCA DE BIOTINA, del 27 de Junio de 2011, de N. V. ORGANON: Un compuesto antitrombótico de fórmula I oligosacárido-espaciador-antagonista de GpIIb/IIIa (I), donde el oligosacárido es un residuo de pentasacárido cargado […]
INHIBIDORES DUALES ANTITROMBÓTICOS ANTICOAGULANTES QUE COMPRENDEN UNA MARCA DE BIOTINA, del 27 de Junio de 2011, de N. V. ORGANON: Un compuesto antitrombótico de fórmula I oligosacárido-espaciador-antagonista de GpIIb/IIIa (I), donde el oligosacárido es un residuo de pentasacárido cargado […]
 CONJUGADOS DE ERITROPOYETINA (EPO) CON POLIETILENGLICOL (PEG), del 22 de Junio de 2011, de F. HOFFMANN-LA ROCHE AG: Conjugado, comprendiendo dicho conjugado una glucoproteína eritropoyetina que presenta un grupo α-amino Nterminal y que presenta la actividad biológica in […]
CONJUGADOS DE ERITROPOYETINA (EPO) CON POLIETILENGLICOL (PEG), del 22 de Junio de 2011, de F. HOFFMANN-LA ROCHE AG: Conjugado, comprendiendo dicho conjugado una glucoproteína eritropoyetina que presenta un grupo α-amino Nterminal y que presenta la actividad biológica in […]
 CONJUGADOS DE PEG-OXIDASA DE URATO Y SU USO, del 14 de Junio de 2011, de MOUNTAIN VIEW PHARMACEUTICALS, INC. DUKE UNIVERSITY: Un conjugado compuesto por una uricasa purificada conjugada a un poli(etilenglicol) (PEG), en la que al menos el 90% de dicha uricasa se halle en una forma tetramérica
CONJUGADOS DE PEG-OXIDASA DE URATO Y SU USO, del 14 de Junio de 2011, de MOUNTAIN VIEW PHARMACEUTICALS, INC. DUKE UNIVERSITY: Un conjugado compuesto por una uricasa purificada conjugada a un poli(etilenglicol) (PEG), en la que al menos el 90% de dicha uricasa se halle en una forma tetramérica
 PROCEDIMIENTO PARA FIJAR MOLÉCULAS EFECTORAS A PROTEÍNAS, del 13 de Junio de 2011, de UCB PHARMA, S.A.: Un procedimiento para fijar una o varias moléculas efectoras a una o a varias cisteínas en una proteína que comprende: a) activar una o varias cisteínas en la proteína […]
PROCEDIMIENTO PARA FIJAR MOLÉCULAS EFECTORAS A PROTEÍNAS, del 13 de Junio de 2011, de UCB PHARMA, S.A.: Un procedimiento para fijar una o varias moléculas efectoras a una o a varias cisteínas en una proteína que comprende: a) activar una o varias cisteínas en la proteína […]