ANTICUERPOS MONOCLONALES COMPLETAMENTE HUMANOS PARA IL-13.
Un anticuerpo humano, humanizado o quimérico aislado que se une a IL-13,
donde el anticuerpo humano aislado se une a IL-13 humana con una KD de menos de 55 pM, donde dicha KD se determina por medio de un análisis Biacore o KinExA basado en una solución y donde: i. el anticuerpo se une específicamente a un polipéptido que consiste en los aminoácidos 20-29 del SEQ ID NO: 96; o ii. el anticuerpo se une a los residuos 21-33 o 70-80 del SEQ ID NO: 72; o iii. el anticuerpo comprende los aminoácidos del SEQ ID NO: 50 de la cadena pesada y comprende los aminoácidos del SEQ ID NO: 52 de la cadena ligera; o iv. el anticuerpo comprende los aminoácidos del SEQ ID NO: 38 de la cadena pesada y comprende los aminoácidos del SEQ ID NO: 40 de la cadena ligera; o v. el anticuerpo comprende los aminoácidos de las CDR1, CDR2 y CDR3 del SEQ ID NO: 50 de la cadena pesada, como se muestra en la Tabla 18 y comprende los aminoácidos de las CDR1, CDR2 y CDR3 del SEQ ID NO: 52 de la cadena ligera, como se muestra en la Tabla 20; o vi. el anticuerpo comprende los aminoácidos de las CDR1, CDR2 y CDR3 del SEQ ID NO: 38 de la cadena pesada, como se muestra en la Tabla 18 y comprende los aminoácidos de las CDR1, CDR2 y CDR3 del SEQ ID NO: 40 de la cadena ligera, como se muestra en la Tabla 20
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2005/041536.
Solicitante: AMGEN INC..
Nacionalidad solicitante: Estados Unidos de América.
Dirección: ONE AMGEN CENTER DRIVE THOUSAND CAKS 91320-1799, CALIFORNIA ESTADOS UNIDOS DE AMERICA.
Inventor/es: FOLTZ,IAN, SENALDI,GIORGIO, KANG,JASPAL,S, FOORD,ORIT, KLAKAMP,SCOTT, RATHANASWAMI,PALANISWAMI, FAGGIONI,RAFFAELLA, MANCHULENKO,Kathy, AHLUWALIA,Kiran.
Fecha de Publicación: .
Fecha Solicitud PCT: 15 de Noviembre de 2005.
Clasificación PCT:
- A61K39/395 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 39/00 Preparaciones medicinales que contienen antígenos o anticuerpos (materiales para ensayos inmunológicos G01N 33/53). › Anticuerpos (aglutininas A61K 38/36 ); Inmunoglobulinas; Inmunosuero, p. ej. suero antilinfocitario.
- A61P11/06 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › A61P 11/00 Medicamentos para el tratamiento de trastornos del aparato respiratorio. › Antiasmáticos.
- A61P11/12 A61P 11/00 […] › Mucolíticos.
- A61P35/00 A61P […] › Agentes antineoplásicos.
- C07K16/24 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 16/00 Inmunoglobulinas, p. ej. anticuerpos mono o policlonales. › contra citoquinas, linfoquinas o interferones.
Países PCT: Austria, Bélgica, Suiza, Alemania, Dinamarca, España, Francia, Reino Unido, Grecia, Italia, Liechtensein, Luxemburgo, Países Bajos, Suecia, Mónaco, Portugal, Irlanda, Eslovenia, Finlandia, Rumania, Chipre, Lituania, Letonia.
PDF original: ES-2358339_T3.pdf




Fragmento de la descripción:
CAMPO DE LA INVENCIÓN
La presente invención hace referencia a anticuerpos humanos que se unen específicamente a interleuquina-13 y pueden afectar a la actividad de IL-13, así como a los ácidos nucleicos que codifican tales anticuerpos, a las células anfitrionas transformadas con dicho ácido nucleico, a un método para elaborar los anticuerpos reivindicados, a un medicamento que contiene los anticuerpos reivindicados y al uso de los anticuerpos en el tratamiento de un trastorno relacionado con IL-13.
ANTECEDENTES DE LA INVENCIÓN
La interleuquina 13 (IL-13) es una citoquina que fue reconocida primero por sus efectos sobre las células B y los monocitos, donde regula al alza la expresión de clase II, promueve el cambio de clase IgE e inhibe la producción de citoquinas inflamatorias. El receptor de IL-13 comparte la cadena alfa del receptor de IL-4 con el receptor de IL-4. Como resultado, la IL-13 tiene muchas actividades biológicas similares a IL-4.
La IL-13 inhibe la liberación de citoquinas proinflamatorias y tiene actividad anti-inflamatoria in vivo. La IL-13 juega un papel en las respuestas alérgicas mediadas por IgE y es un mediador central del asma alérgica (Wills-Karp M., Curr. Opin. Pulm. Med., 2003; 9:21-27). En el pulmón regula la inflamación eosinofílica, la secreción de mucus, y la hipersensibilidad de las vías respiratorias. Además del asma, la IL-13 está implicada en la patogénesis de un gran número de enfermedades (Wynn TA. Annu. Rev. Immunol. 2003, 21:425-456).
La solicitud de Patente WO 03/0846451 describe el uso de un anticuerpo anti-IL-13 de ratón de rata monoclonal neutralizador en un modelo de asma aguda inducida por ovoalbúmina en ratones. El anticuerpo anti-IL-13 inhibe la hipersensibilidad de las vías respiratorias, la hiperplasia de las células caliciformes y la producción de mucus. Además, el tratamiento con el anticuerpo también inhibe la producción de IL-5, IL-6, eotaxina, KC, MIP-1 y MCP-1 en el pulmón.
COMPENDIO DE LA INVENCIÓN
La invención es la propuesta en las reivindicaciones.
Los aspectos de la invención hacen referencia a anticuerpos y medicamentos para tratar trastornos relacionados con IL-13.
Los anticuerpos aislados pueden ser anticuerpos monoclonales o anticuerpos quiméricos y/o anticuerpos humanos o humanizados.
Una realización incluye moléculas de ácido nucleico aisladas que codifican cualquiera de los anticuerpos descritos en la presente memoria.
BREVE DESCRIPCIÓN DE LOS DIBUJOS
La invención se comprenderá mejor a partir de la Descripción Detallada y de los dibujos adjuntos, que están destinados a ilustrar y no a limitar la invención.
La FIG.1 muestra una representación gráfica de la concentración de anticuerpo relativa frente a los datos de neutralización para cada pocillo. Los datos se utilizan para identificar pocillos con los anticuerpos de potencia más elevada.
La FIG. 2 es una representación gráfica que representa la relación de un DO- ELISA de cada anticuerpo frente a la concentración de anticuerpo a un recubrimiento con antígeno de 31 ng/mL.
La FIG. 3 es un gráfico que representa el porcentaje de inhibición de la liberación de eotaxina inducida por IL-13 por anticuerpos recombinantes 643 y 731 en comparación con un control de isotipo coincidente.
La FIG. 4 es un diagrama de barras que compara la capacidad de IL-13 o IL-13Q110R par inhibir la unión de 731 o 623 a placas de ELISA recubiertas con IL-13.
La FIG. 5A es un diagrama de barras que compara la competición de receptores sobre la célula entre el anticuerpo 643 y un control de isotipo.
La FIG. 5B es un diagrama de barras que compara la competición de receptores sobre la célula entre el anticuerpo 731 y un control de isotipo.
**(Ver fórmula)**
La FIG. 5C es una viñeta que representa el protocolo y los diferentes resultados pronosticados a partir de la FIG. 5A y la FIG. 5E. La FIG. 5D es una viñeta que representa el protocolo y los diferentes resultados pronosticados a partir de la FIG. 5B. La FIG. 5E es un diagrama de barras que compara la competición de receptores sobre la célula entre el anticuerpo
623 y un control de isotipo.
La FIG. 6A muestra el alineamiento de un péptido derivado de la presentación en fagos reconocido por el anticuerpo 693 y parte de la secuencia de IL-13. La FIG. 6B es un diagrama que muestra la estructura secundaria de IL-13 (SEQ ID NO: 72) e indica qué regiones de
la IL-13 humana fueron remplazadas por IL-13 de ratón para la construcción de las proteínas quiméricas.
La FIG. 7A y la FIG. 7B son diagramas de barras que demuestran que las células T CD4+ de ratones inmunizados con IL-13 producen IL-13 humana pero no IL-13 murina. La FIG. 8 es un gráfico que demuestra que los anticuerpos anti-IL-13 731 y 623 inhiben la hipersensibilidad de las
vías respiratorias. La FIG. 9 es un diagrama de barras que demuestra que 731 y 623 inhiben la producción de mucus. La FIG. 10 es una descripción de una secuencia de aminoácidos que pone de relieve un sitio de unión de mAb 623. Las FIG. 11A-D son gráficos que representan el porcentaje de inhibición de liberación de eotaxina inducida por IL-13
o la variante IL-13Q110R por los anticuerpos recombinantes 623 y 731 en comparación con un control de isotipo coincidente.
Las FIG. 12A y 12B son gráficos que demuestran la inhibición de la proliferación de la línea celular L-1236 (A) y HDLM-2 (B) por 623 y 731. Se añadieron mAb 623, mAb 731 o control de isotipo coincidente a la placa para concentraciones finales de 0,017 a 330 nM (titulado 1:3).
La FIG. 13 es un gráfico que presenta el impacto de mAb 623 y 731 y hIL-13Ralfa2Fc sobre la expresión de CD23 en células B de sangre completa.
La FIG. 14 es un gráfico que presenta la inhibición de la producción de mucus inducida por OVA por mAb 623 y mAb 731 en ratones humanizados para IL-13.
La FIG. 15 es un gráfico que presenta un experimento en el cual el tratamiento con mAb 623 o 731 tuvo un pequeño efecto observable sobre el reclutamiento de leucocitos inducido por OVA en BALF.
La FIG. 16 es un gráfico que presenta la inhibición de AHR inducida por OVA por 623 y 731 en ratones humanizados para IL-13 de una manera sensible a la dosificación.
La FIG. 17 es un gráfico que presenta la inhibición de mucus inducida por OVA por 623 y 731 en ratones humanizados para IL-13 de una manera sensible a la dosificación.
La FIG. 18 es un gráfico que presenta el efecto de 623 y 731 sobre la infiltración de leucocitos inducida por OVA en BALF de ratones humanizados para IL-13 de una manera sensible a la dosificación.
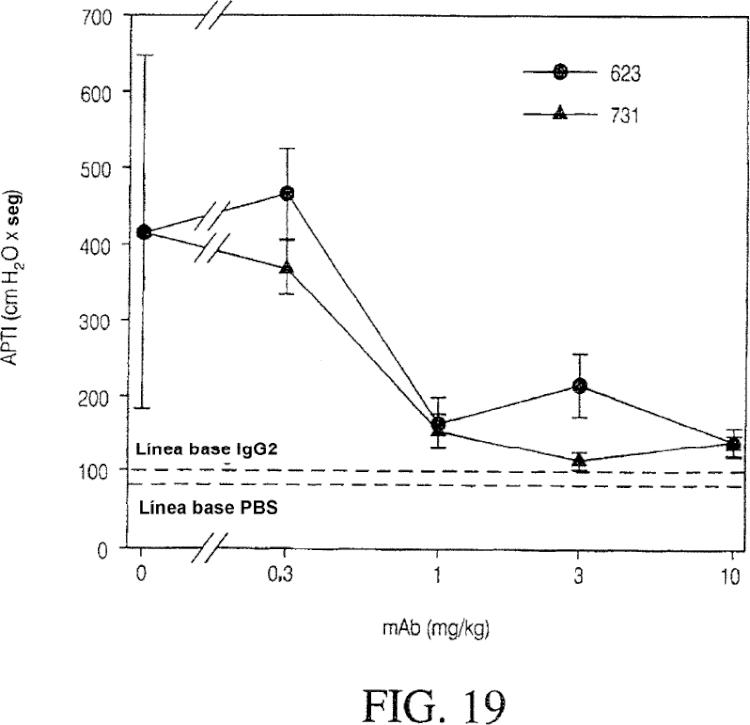
La FIG. 19 es un gráfico que presenta una inhibición de la respuesta a la dosis de AHR inducida por HDM por 623 y
La FIG. 20 es un gráfico que presenta una inhibición de la respuesta a la dosis de la producción de mucus inducida por HDM por 623 y 731 en ratones humanizados para IL-13.
La FIG. 21 es un gráfico que presenta una inhibición de la respuesta a la dosis de 623 y 731 sobre la infiltración de leucocitos inducida por HDM en BALF de ratones humanizados para IL-13.
La FIG. 22A y 22B son gráficos que presentan el efecto de la administración profiláctica y terapéutica de 623 sobre la AHR inducida por HDM y la infiltración de leucocitos en BALF de ratones humanizados para IL-13.
La FIG. 23 es un gráfico que presenta los niveles de TARC en suero inducidos por OVA en ratones de tipo salvaje.
**(Ver fórmula)**
La FIG. 24 es un gráfico que presenta los niveles de eotaxina en suero inducidos por OVA en ratones de tipo salvaje.
La FIG. 25 es un gráfico que presenta los niveles de C10 en suero inducidos por OVA en ratones de tipo salvaje.
La FIG. 26 es un gráfico que presenta la inhibición por el mAb 623 de los niveles de TARC en suero inducidos por OVA en ratones humanizados para IL-13.
La FIG. 27 es un gráfico que presenta la inhibición por el mAb 623 de los niveles de eotaxina en suero inducidos por OVA en ratones humanizados para IL-13.
La FIG. 28 es un gráfico que presenta el efecto del tratamiento con el mAb 623 sobre los niveles... [Seguir leyendo]
Reivindicaciones:
1. Un anticuerpo humano, humanizado o quimérico aislado que se une a IL-13, donde el anticuerpo humano aislado se une a IL-13 humana con una KD de menos de 55 pM, donde dicha KD se determina por medio de un análisis Biacore o KinExA basado en una solución y donde:
i. el anticuerpo se une específicamente a un polipéptido que consiste en los aminoácidos 20-29 del SEQ ID NO: 96; o
ii. el anticuerpo se une a los residuos 21-33 o 70-80 del SEQ ID NO: 72; o
iii. el anticuerpo comprende los aminoácidos del SEQ ID NO: 50 de la cadena pesada y comprende los aminoácidos del SEQ ID NO: 52 de la cadena ligera; o
iv. el anticuerpo comprende los aminoácidos del SEQ ID NO: 38 de la cadena pesada y comprende los aminoácidos del SEQ ID NO: 40 de la cadena ligera; o
v. el anticuerpo comprende los aminoácidos de las CDR1, CDR2 y CDR3 del SEQ ID NO: 50 de la cadena pesada, como se muestra en la Tabla 18 y comprende los aminoácidos de las CDR1, CDR2 y CDR3 del SEQ ID NO: 52 de la cadena ligera, como se muestra en la Tabla 20; o
vi. el anticuerpo comprende los aminoácidos de las CDR1, CDR2 y CDR3 del SEQ ID NO: 38 de la cadena pesada, como se muestra en la Tabla 18 y comprende los aminoácidos de las CDR1, CDR2 y CDR3 del SEQ ID NO: 40 de la cadena ligera, como se muestra en la Tabla 20.
2. El anticuerpo humano aislado de la reivindicación 1, donde el anticuerpo humano aislado se une a IL-13 con una KD de menos de 50 pM.
3. El anticuerpo aislado, según la reivindicación 1 o la reivindicación 2, donde el anticuerpo es un anticuerpo monoclonal.
4. Un medicamento que comprende un anticuerpo aislado, como se reivindica en una cualquiera de las reivindicaciones 1 a 3.
5. Un ácido nucleico que codifica un anticuerpo como se reivindica en una cualquiera de las reivindicaciones 1 a 3.
6. Un vector viral que comprende el ácido nucleico de la reivindicación 5.
7. Una célula anfitriona transformada con un ácido nucleico como se reivindica en la reivindicación 5 o un vector viral como se reivindica en la reivindicación 6.
8. Un método para elaborar un anticuerpo, como se reivindica en una cualquiera de las reivindicaciones 1 a 3, que comprende la expresión del anticuerpo a partir de una célula anfitriona como se reivindica en la reivindicación 7.
9. El anticuerpo humano aislado de una cualquiera de las reivindicaciones 1 a 3 o semejante anticuerpo en un medicamento como se reivindica en la reivindicación 4, para su uso en el tratamiento de un trastorno relacionado con IL-13.
10. Un anticuerpo aislado o medicamento para su uso como se reivindica en la reivindicación 9, donde el trastorno relacionado con IL-13 es una enfermedad inflamatoria, una enfermedad pulmonar obstructiva crónica o asma.
11. El uso de un anticuerpo, como se reivindica en una cualquiera de las reivindicaciones 1 a 3, en la fabricación de un medicamento para el tratamiento de un trastorno relacionado con IL-13.
12. El uso de un anticuerpo como se reivindica en la reivindicación 11, donde el trastorno relacionado con IL-13 es una enfermedad inflamatoria, una enfermedad pulmonar obstructiva crónica o asma.
Patentes similares o relacionadas:
Compuestos y procedimientos de uso, del 29 de Julio de 2020, de Medivation Technologies LLC: Un compuesto de fórmula (Aa-1): **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, en la que: A representa H, halógeno, amino, […]
Complejos de agentes terapéuticos de base vírica y poli(beta-amino-ésteres) modificados, del 29 de Julio de 2020, de Sagetis Biotech, SL: Un complejo de un agente terapéutico de base vírica con un polímero de fórmula I: **(Ver fórmula)** donde cada L1 y L2 están seleccionados […]
Compuestos de alquinilbenceno heterocíclicos, y composiciones médicas y usos de los mismos, del 29 de Julio de 2020, de Guangzhou Healthquest Pharma Co., Ltd: Un compuesto de alquinilbenceno heterocíclico que tiene la fórmula (I) y una sal farmacéuticamente aceptable, o estereoisómero del mismo, **(Ver […]
 Composiciones y métodos para el tratamiento de trastornos de células plasmáticas y trastornos prolinfocíticos de células b, del 29 de Julio de 2020, de Knopp Biosciences LLC: Una composición que comprende una cantidad terapéuticamente eficaz de dexpramipexol para su uso en el tratamiento de un trastorno de células B caracterizado por niveles elevados […]
Composiciones y métodos para el tratamiento de trastornos de células plasmáticas y trastornos prolinfocíticos de células b, del 29 de Julio de 2020, de Knopp Biosciences LLC: Una composición que comprende una cantidad terapéuticamente eficaz de dexpramipexol para su uso en el tratamiento de un trastorno de células B caracterizado por niveles elevados […]
Derivados de piperidina 1,4 sustituidos, del 29 de Julio de 2020, de 89Bio Ltd: Un compuesto de acuerdo con la Fórmula I: **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, en donde: A se selecciona de […]
Profármacos de gemcitabina, del 29 de Julio de 2020, de NuCana plc: Una formulación farmacéutica que comprende gemcitabina-[fenil-benzoxi-L-alaninil)]-(S)-fosfato 3: **(Ver fórmula)** o una sal o solvato […]
Formas cristalinas de 6-((6,7-dimetoxiquinazolin-4-il)oxi)-N,2-dimetilbenzofuran-3-carboxamida, del 29 de Julio de 2020, de Hutchison Medipharma Limited: Forma I de 6-((6,7-dimetoxiquinazolin-4-il)oxi)-N,2-dimetilbenzofuran-3-carboxamida, en donde el difractograma de rayos X de polvo de la Forma […]
Utilización de anticuerpos optimizados en ADCC para tratar a los pacientes con bajo nivel de respuesta, del 22 de Julio de 2020, de LABORATOIRE FRANCAIS DU FRACTIONNEMENT ET DES BIOTECHNOLOGIES: Utilización de una composición de anticuerpo monoclonal quimérico, humanizado o humano de isotipo IgG1 anti- Rhesus del glóbulo rojo humano cuya […]