UTILIZACION DEL G-CSF COMO TRATAMIENTO ADYUVANTE EN LA RECONSTRUCCION DE TEJIDOS CONJUNTIVOS.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/FR02/00480.
Solicitante: POURQUIER, DIDIER
MOUKOKO, DIDIER.
Nacionalidad solicitante: Francia.
Dirección: 3 BIS, RUE DES CORONILLES,34070 MONTPELLIER.
Inventor/es: POURQUIER,DIDIER, MOUKOKO,DIDIER.
Fecha de Publicación: .
Fecha Concesión Europea: 19 de Mayo de 2010.
Clasificación Internacional de Patentes:
- A61K38/19B
Clasificación PCT:
- A61K38/19 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 38/00 Preparaciones medicinales que contienen péptidos (péptidos que contienen ciclos beta-lactama A61K 31/00; dipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina 2,5-dionas, A61K 31/00; péptidos basados en la ergolina A61K 31/48; que contienen compuestos macromoleculares que tienen unidades aminoácido repartidas estadísticamente A61K 31/74; preparaciones medicinales que contienen antígenos o anticuerpos A61K 39/00; preparaciones medicinales caracterizadas por los ingredientes no activos, p. ej. péptidos como soportes de fármacos, A61K 47/00). › Citoquinas; Linfoquinas; Interferones.
- A61P19/00 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › Medicamentos para el tratamiento de problemas del esqueleto.
Clasificación antigua:
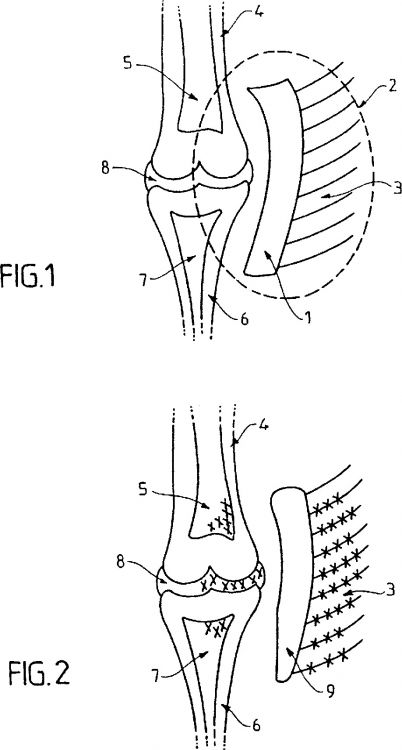
Fragmento de la descripción:
Utilización del G-CSF como tratamiento adyuvante en la reconstrucción de tejidos conjuntivos.
La presente invención se refiere a una nueva aplicación terapéutica del G-CSF y más particularmente a su utilización para la preparación de un medicamento útil en medicina humana o veterinaria.
El G-CSF (abreviatura de "Granulocyte Colony-Stimulating Factor", es decir "Factor de Estimulación de las Colonias de Granulocitos") es un factor de crecimiento. Corresponde a una de las clases de citoquinas denominadas factores de crecimiento hematopoyético o CSF (Colony-Stimulating Factors). Los CFS forman una familia de glicoproteínas que tienen unas funciones capitales en la formación de las células sanguíneas. El G-CSF estimula la producción de las células hematopoyéticas y de manera predominante la producción de polinucleares. El G-CSF es una glicoproteína y el producto de la expresión de un gen situado en el cromosoma 17. Está producido por diferentes células, tales como los fibroblastos, macrófagos, células endoteliales, y células epiteliales. El G-CSF es detectable en la sangre, y se puede purificar a partir de sobrenadantes de cultivos de células tumorales humanas.
La ingeniería biológica permite asimismo producir un alotipo humano de G-CSF, el G-CSF recombinante humano (rHuG-CSF). Se debe observar que el rHuG-CSF es eficaz en otras especies animales (Gratwohl et al.: Transplantation of G-CSF mobilized allogeneic peripheral blood stem cells in rabbits. Bone Marrow Transplant 1995; 16(1):63-68).
Diferentes procedimientos de producción del G-CSF se han descrito en las publicaciones de patentes siguientes: US nº 4.810.643, EP 0 169 566, WO 87 01132 y JP 15 327 384.
En Francia, están disponibles dos medicamentos que pertenecen a la clase del G-CSF: el Neupogen® (rmetHuG-CSF, Filgrastim, comercializado por Amgen/Produits Roche), y el Granocyte® (rHuG-CSF, Lenograstim, comercializado por los laboratorios Rhône-Poulenc Rorer), estos dos medicamentos se utilizan por vía de inyección sub-cutánea o por perfusión intravenosa, para una administración sistémica, a unas dosis comprendidas generalmente entre 5 y 10 µg por kilogramo de peso corporal y por día.
Las indicaciones actuales del G-CSF en terapéutica humana son el tratamiento de las neutropenias crónicas severas, la reducción de las neutropenias inducidas por los tratamientos quimioterapéuticos anticancerígenos mielotóxicos, la reducción de las neutropenias inducidas por las terapias mielosupresivas (quimioterapia o radioterapia) seguidas de injerto de médula en el tratamiento de los cánceres o de las leucemias, la movilización de las células cepas hematopoyéticas para constituir un injerto con vistas a un injerto de médula (autoinjerto o aloinjerto).
Se debe subrayar que, en esta última utilización, el objetivo del tratamiento es extraer de la médula ósea las células cepas hematopoyéticas y hacerlas pasar a la sangre circulante. Estas células cepas se recogen entonces mediante citaféresis sucesivas y constituirán el injerto. Se trata por lo tanto de movilizar al máximo hacia la sangre circulante este contingente de células cepas hematopoyéticas que, en el estado normal, se encuentran en cantidad muy reducida en la sangre circulante, lo cual no permite constituir un injerto de calidad suficiente.
Esta técnica de recolección del injerto mediante citaféresis después de la movilización de las células cepas ha sustituido ventajosamente la recolección directa de la médula ósea mediante citopunción que necesita una anestesia del paciente y múltiples punciones de médula. El injerto así constituido se transfunde al paciente, cuya propia médula ha sido destruida por la quimioterapia o la radioterapia; constituye entonces la nueva fuente de producción de las células sanguíneas.
El G-CSF se utiliza de manera diaria para estas diferentes indicaciones. Su inocuidad ampliamente reconocida permite utilizarlo asimismo en personas con buena salud para constituir unos injertos de médula en el marco de los aloinjertos.
Conviene recordar que la médula ósea, repartida en los diferentes huesos del organismo, es el lugar de producción de las células sanguíneas maduras (eritrocitos, plaquetas, polinucleares, monocitos, linfocitos). La producción de estas células sanguíneas se efectúa a partir de la multiplicación y de la diferenciación de una población de células cepas pluripotentes (Célula Cepa Hematopoyética, abreviado "CSH"). Estas últimas representan cuantitativamente una fracción muy reducida de la población celular de la médula ósea. Están caracterizadas habitualmente por la expresión de un marcador celular denominado CD34 (cluster de diferenciación 34).
Sin embargo, se ha descrito otro tipo de células cepas de la médula ósea (Pittenger et al.: Multilineage potential of human mesenchymal stem cells. Science 1999; 284: 143-147; Dennis et at.: A quadripotential mesenchymal progenitor cell isolated from the marrow of an adult mouse. J Bone Miner Res 1999; 14(5): 700-709). Se trata de una población de células capaz de una vía de diferenciación conjuntiva; estas células cepas se denominan Células Cepas Mesenquimatosas (abreviado "CSM"). Esta población de células cepas constituye asimismo en el estado normal un contingente muy reducido de los elementos celulares de la médula ósea pero presenta la capacidad de diferenciarse en múltiples direcciones de naturaleza conjuntiva (hueso, cartílago, fibrotendón, músculo, grasa). Actualmente se discute la existencia de un precursor común (célula cepa CD34 negativa) al conjunto de las líneas hematopoyéticas y conjuntivas (Seshi et al.: Human bone marrow stromal cell: coexpression of markers specific for multiple mesenchymal stem lineage. Blood Cell Mol Dis 2000(3): 234-246; Lange et al.: Hematopoietic reconstruction of syngenic mice with a peripheral blood-derived, monoclonal CD34-, Sca-1+, Thy1(low), c-kit+ stem cell ligne. J Hematother Stem Cell Res. 1999; 8(4): 335-342).
Esta población de células cepas constituye actualmente el objeto de una actividad de investigación intensiva, en particular en el campo de la cirugía plástica, de la reparación ósea y de la osteoporosis, en el marco de los campos emergentes de la medicina que son la ingeniería tisular y la terapia celular. Sin embargo, constituyendo al principio esta población de CSM una cantidad de células particularmente baja, las técnicas utilizadas recurren a un paso in vitro. Para resumir, se recoge la médula ósea, y después, in vitro, se separa el contingente de las células mesenquimatosas del resto de las células de la médula, y estas células se cultivan y se multiplican a continuación todavía in vitro. Eventualmente, crecen asimismo artificialmente en el sentido de una diferenciación específica. A continuación, se reinyectan o se reimplantan en un sitio anatómico en el que contribuyen a la reconstrucción de un tejido conjuntivo deteriorado, que puede ser un hueso (Bruder et al.: Bone regeneration by implantation of purified culture-expended human mesenchymal stem cells. J Ortho Res 1998; 16(2): 155-162) o bien un tendon (Awad et al.: Autologous mesenchymal stem cell-mediated repair of tendon. Tissue Eng 1999; 5(3): 267-277; Butler et al.: Perspectives on cell and collagen composites for tendon repair. Clin Orthop 1999; 367 Supl.: S 324-332).
Estas técnicas necesitan sin embargo una colaboración con unos laboratorios muy especializados y la obtención de un injerto conjuntivo de calidad no siempre está asegurada (Solchaga et al.: High variability in rabbit bone marrow-derived mesenchymal cell preparation. Cell Transplant 1999; 8(5): 511-519). La proliferación y la diferenciación de las CSM están inducidas por la Bone Morphogenetic Protein-2 {BMP-2} (Fromigue et al.: Bone morphogenetic protein 2 and transforming growth factor-beta 2 interact to modulate human bone marrow stromal cell proliferation and differenciation. J Cell Biochem. 1998; 68(4): 411-426), pero también los Transforming Growth Factor beta 1 (Andrades et al.: A recombinant TGF-beta 1 fusion protein with collagen-binding domain promotes migration, growth, and differentiation of bone marrow mesenchymal cells. Exp Cell Res 1999; 250(2): 485-498).
En el campo de la reparación de las fracturas óseas, el proceso de reparación óseo después de una fractura de un hueso se describe clásicamente en dos grandes fases. La primera fase es un periodo de unión que comprende sucesivamente un periodo de hematoma, un periodo de proliferación celular de células mesenquimatosas...
Reivindicaciones:
1. Utilización del G-CSF (factor de estimulación de las colonias de granulocitos) para la preparación de un medicamento útil como tratamiento adyuvante en un proceso de reconstrucción de tejidos conjuntivos in situ en un ser vivo.
2. Utilización según la reivindicación 1, caracterizada porque el G-CSF se utiliza como medicamento en el tratamiento de las fracturas óseas, osteocartilaginosas, de las pseudoartrosis, de los retrasos de consolidación de las fracturas óseas, de las lesiones cartilaginosas, o también de las roturas o secciones de tendones o ligamentos y de las lesiones de los músculos, y está destinado a la administración por vía general.
3. Utilización según la reivindicación 1, caracterizada porque el G-CSF se utiliza como medicamento en el tratamiento de alargamiento de los miembros y está destinado a la administración por vía general.
4. Utilización según la reivindicación 1, caracterizada porque el G-CSF se utiliza como medicamento en el tratamiento que asocia un gesto quirúrgico de reconstrucción ósea o cartilaginosa por transferencia de colgajo de periostio, y de manera general en la cirugía de regeneración tisular de los miembros y del aparato locomotor, y está destinado a la administración por vía general.
5. Utilización según una de las reivindicaciones 1 a 4, caracterizada porque el G-CSF se utiliza como medicamento destinado a la administración por vía general y se combina con por lo menos otro factor destinado a la administración local o por vía general.
6. Utilización según la reivindicación 5, caracterizada porque este otro factor se selecciona de entre por lo menos uno de los factores siguientes: BMP (Bone Morphogenetic Protein), SCF (stem cell factor), FGF (fibroblast growth factor), EGF (epidermal growth factor), IGF (insuline-like growth factor), Insulina, KGF (keratinocyte growth factor), TGF (transforming growth factor), Interferón, Interleucina, VEGF (vascular endothélial growth factor), TNF (tumor necrosing factor), GDNF (glial cell ligne-derived neurotrophic factor), NGF (neurotrophin nerve growth factor), GM-CSF (granulocytemacrophage colony stimulating factor), HGF (hepatocyte growth factor), Eritropoyetina, PDGF (platelet-derived growth factor), Sulfato de heparano, Prostaglandinas, Osteoglicina (osteoinductive factor), BCDF (B cell differentiation factor), GDF-5 (growth and differentiation factor-5), Hormona de crecimiento; M-CSF (macrophage colony stimulating factor); o cualquier otro factor de crecimiento conocido de origen humano o animal, de extracción o recombinante.
7. Utilización según una de las reivindicaciones 1 a 6, caracterizada porque el G-CSF es un recombinante humano.
8. Utilización según una de las reivindicaciones 1 a 6, caracterizada porque el G-CSF es el Filgrastim.
9. Utilización según una de las reivindicaciones 1 a 6, caracterizada porque el G-CSF es el Lenograstim.
10. Utilización según una de las reivindicaciones 1 a 9, caracterizada porque el medicamento se utiliza con una dosificación en G-CSF de 0,1 a 1.000 µg (0,01 a 100 MU), preferentemente de 5 a 10 µg, por kilogramo de peso corporal y por día.
11. Utilización según una de las reivindicaciones 1 a 9, caracterizada porque el medicamento se utiliza en medicina humana.
12. Utilización según una de las reivindicaciones 1 a 10, caracterizada porque el medicamento se utiliza en medicina veterinaria.
Patentes similares o relacionadas:
APLICACIÓN TERAPÉUTICA DEL G-CSF, del 14 de Diciembre de 2011, de POURQUIER, DIDIER MOUKOKO, DIDIER: Utilización del G-CSF (Factor de estimulación de las colonias de granulocitos) para la preparación de un medicamento útil como tratamiento adyuvante en un proceso de […]
COMBINACIÓN FARMACÉUTICA DE G-CSF Y PLGF ÚTIL PARA CÉLULAS MADRE DE SANGRE, del 1 de Diciembre de 2011, de DOMPE S.P.A.: Preparación farmacéutica combinada que contiene G-CSF y P1GF como sustancias activas, para uso en la estimulación de la movilización de células progenitoras de sangre periférica […]
PROCEDIMIENTO PARA EL CONTROL DEL COLESTEROL CON UNA MEZCLA DE CITOCINA LIBRE DE SUERO Y LIBRE DE MITÓGENOS, del 3 de Noviembre de 2011, de CEL-SCI CORPORATION: Mezcla de citocina libre de suero y de mitógenos compuesta de proporciones específicas de citocinas seleccionadas de entre el grupo de IL-1β, TNF-α, […]
COMPOSICONES Y PROCEDIMIENTOS PARA EL TRATAMIENTO DE TRASTORNOS FIBRÓTICOS, del 22 de Julio de 2011, de AMGEN INC.: Un antagonista de la linfopoyetina estromal tímica (LPET) para su uso en reducir o prevenir fibrosis en un sujeto que padece un trastorno fibrótico, […]
MICELAS INVERSAS BASADAS EN FITOESTEROLES Y ACILGLICEROLES Y USO TERAPÉUTICO DE LAS MISMAS, del 9 de Junio de 2011, de MEDESIS PHARMA SA: Sistema micelar inverso que se obtiene mediante el método siguiente: a) poner en contacto i) fitoesterol, ii) acilglicerol, iii) agua y iv) al […]
ANTICUERPO QUIMÉRICO DIRIGIDO CONTRA CD20, EL RITUXAN, PARA USO EN EL TRATAMIENTO DE LA LEUCEMIA LINFOCÍTICA CRÓNICA, del 1 de Febrero de 2011, de BIOGEN IDEC, INC.: Uso de rituximab en la fabricación de un medicamento para el tratamiento de la leucemia linfocítica crónica (CLL) en un paciente humano, en el que el medicamento es para su […]
METODOS PARA PREVENIR Y TRATAR METASTASIS DE CANCER Y PERDIDA DE HUESO ASOCIADA CON LA METASTASIS DE CANCER, del 5 de Octubre de 2010, de NOVARTIS VACCINES AND DIAGNOSTICS, INC.: Un anticuerpo antagonista no murina que enlaza a M-CSF, para uso en prevención o tratamiento de metástasis ósea en un sujeto afligido con cáncer […]
Composiciones farmacéuticas que contienen una leucocidina E mutada, del 22 de Julio de 2020, de NEW YORK UNIVERSITY: Una composición que comprende: una proteína Leucocidina E (LukE) aislada que comprende la secuencia de aminoácidos de la SEQ ID NO: 4, o un polipéptido […]