OLIGOMEROS NO AGREGANTES Y SIN BLOQUEO DE LA FLUORESCENCIA QUE COMPRENDEN ANALOGOS DE NUCLEOTIDOS; METODOS DE SINTESIS Y USO DE LOS MISMOS.
Un conjugado que comprende:
(a) un polímero que comprende una serie de unidades de monómero;
y
(b) un fluoróforo unido covalentemente a ellos,
en el que uno o más de las unidades de monómero comprende un análogo de base, en el que el análogo de base se selecciona de entre el grupo que consiste de pirazolopirimidinas, como el análogo de bases retiene la especificidad de emparejamiento de bases de las bases para las que se sustituyen, y conduce a una reducción en el bloqueo de la fluorescencia del fluoróforo y/o auto-asociación del polímero reducida
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US00/32265.
Solicitante: EPOCH BIOSCIENCES, INC.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 21720 23RD DRIVE, SE, SUITE 150,BOTHELL, WA 98021.
Inventor/es: VERMEULEN, NICOLAAS M.J., KUTYAVIN,IGOR,V, GALL,ALEXANDER,A, DEMPCY,ROBERT,O.
Fecha de Publicación: .
Fecha Concesión Europea: 5 de Mayo de 2010.
Clasificación Internacional de Patentes:
- C07D487/04 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07D COMPUESTOS HETEROCICLICOS (Compuestos macromoleculares C08). › C07D 487/00 Compuestos heterocíclicos que contienen átomos de nitrógeno como únicos heteroátomos del ciclo en el sistema condensado, no previstos por los grupos C07D 451/00 - C07D 477/00. › Sistemas condensados en orto.
- C07H21/00C4
- C07K14/00B1
- C07K5/06H
- C12Q1/68B8
Clasificación PCT:
- C07D487/04 C07D 487/00 […] › Sistemas condensados en orto.
- C07H21/00 C07 […] › C07H AZUCARES; SUS DERIVADOS; NUCLEOSIDOS; NUCLEOTIDOS; ACIDOS NUCLEICOS (derivados de ácidos aldónicos o sacáricos C07C, C07D; ácidos aldónicos, ácidos sacáricos C07C 59/105, C07C 59/285; cianohidrinas C07C 255/16; glicales C07D; compuestos de constitución indeterminada C07G; polisacáridos, sus derivados C08B; ADN o ARN concerniente a la ingeniería genética, vectores, p. ej. plásmidos o su aislamiento, preparación o purificación C12N 15/00; industria del azúcar C13). › Compuestos que contienen al menos dos unidades mononucleótido que tienen cada una grupos fosfato o polifosfato distintos unidos a los radicales sacárido de los grupos nucleósido, p. ej. ácidos nucleicos.
- C07K14/00 C07 […] › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › Péptidos con más de 20 aminoácidos; Gastrinas; Somatostatinas; Melanotropinas; Sus derivados.
- C07K5/06 C07K […] › C07K 5/00 Péptidos con hasta cuatro aminoácidos en una secuencia totalmente determinada; Sus derivados. › Dipéptidos.
- C12Q1/68 C […] › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12Q PROCESOS DE MEDIDA, INVESTIGACION O ANALISIS EN LOS QUE INTERVIENEN ENZIMAS, ÁCIDOS NUCLEICOS O MICROORGANISMOS (ensayos inmunológicos G01N 33/53 ); COMPOSICIONES O PAPELES REACTIVOS PARA ESTE FIN; PROCESOS PARA PREPARAR ESTAS COMPOSICIONES; PROCESOS DE CONTROL SENSIBLES A LAS CONDICIONES DEL MEDIO EN LOS PROCESOS MICROBIOLOGICOS O ENZIMOLOGICOS. › C12Q 1/00 Procesos de medida, investigación o análisis en los que intervienen enzimas, ácidos nucleicos o microorganismos (aparatos de medida, investigación o análisis con medios de medida o detección de las condiciones del medio, p. ej. contadores de colonias, C12M 1/34 ); Composiciones para este fin; Procesos para preparar estas composiciones. › en los que intervienen ácidos nucleicos.
Clasificación antigua:
- C12Q1/68 C12Q 1/00 […] › en los que intervienen ácidos nucleicos.
Fragmento de la descripción:
Oligómeros no agregantes y sin bloqueo de la fluorescencia que comprenden análogos de nucleótidos; métodos de síntesis y uso de los mismos.
Campo técnico
La descripción se refiere al uso de análogos de nucleótidos para proporcionar propiedades mejoradas a las sondas de hibridación, que incluye sondas de DNA y RNA y sondas de ácidos nucleicos modificados, como péptidos de ácidos nucleicos (PNA), y sondas quiméricas que contienen dos o más tipos de ácidos nucleicos y/o ácidos nucleicos modificados.
Antecedentes
El análisis de hibridación es central para una serie de técnicas en biología molecular y diagnóstico, incluyendo el clonaje de genes, identificación de genes, análisis forense, farmacogenómica e identificación de polimorfismos genéticos. Puede utilizarse la hibridación como objetivo de un ensayo, en el que la presencia de sondas hibridadas constituye la lectura para el ensayo; o la hibridación puede utilizarse como el paso inicial en un ensayo, en el que un evento posterior a la hibridación (como, por ejemplo, extensión de un cebador hibridado o hidrólisis de una sonda hibridada) se utiliza como lectura.
Tradicionalmente, las sondas de hibridación y los cebadores han sido moléculas de DNA; no obstante, existen ciertas desventajas en el uso de DNA como sonda o cebador. Por ejemplo, la composición de bases de una molécula de DNA puede afectar a su efectividad como sonda o cebador de varias maneras. Una molécula de DNA con una alta concentración de residuos G es a menudo difícil de manejar (por ejemplo, problemas con la agregación y pobre solubilidad) y puede proporcionar un gran ruido de fondo en las reacciones de hibridación. También se sabe que las moléculas de DNA ricas en G son propensas a la producción de artefactos en el análisis de las secuencias de DNA mediante electroforesis en gel, presumiblemente debido a la adopción de estructuras secundarias mediante estas moléculas, a pesar de las condiciones desnaturalizantes bajo las que se realizan dichos análisis.
Se han utilizado varias formas modificadas de DNA y análogos de DNA para intentar de superar algunas de las desventajas de la utilización de moléculas de DNA como sondas y cebadores. Entre estas están los péptidos de ácidos nucleicos (PNA, también conocidos como poliamidas de ácidos nucleicos). Nielsen et al. (1991) Science 254:1497-1500. Los PNA contienen unidades de bases heterocíclicas, como se encuentran en el DNA y RNA, que están unidos mediante un esqueleto de poliamida, en lugar del esqueleto característico de azúcar-fosfato del DNA y RNA. Los PNA son capaces de hibridar con secuencias diana complementarias de DNA y RNA y, de hecho, hibridan más fuertemente que la correspondiente sonda de ácido nucleico. Además, los PNA son resistentes a muchos tipos de nucleasas que atacan los esqueletos de azúcar-fosfato del DNA y RNA. Otras ventajas de los PNA incluye la capacidad de los PNA modificados específicamente para cruzar la barrera hematoencefálica y la observación que los PNA inyectados por vía intratecal pueden mediar efectos antisentido in vivo. During et al. (1999) Nature Biotechnol. 17:753-754.
La síntesis de oligómeros de PNA y monómeros reactivos utilizados en la síntesis de oligómeros de PNA se ha descrito en las Patentes Estadounidenses Nº 5.539.082; 5.714.331; 5.773.571; 5.736.336 y 5.766.855. Las aproximaciones alternativas a la síntesis de PNA y, los monómeros para la síntesis de PNA se resumen en Uhlmann et al. (1998) Angew. Chem. Int. Ed 37: 2796-2823.
No obstante, como se han empezado a utilizar ampliamente, también se han visto las desventajas de los PNA. Por ejemplo, los oligómeros de PNA largos, dependiendo de su secuencia, son propensos a agregarse, difíciles de purificar y difíciles de caracterizar. Además, los oligómeros de PNA ricos en purinas tienden a agregar y son poco solubles en medio acuoso. Gangamani et al. (1997) Biochem. Biophys. Res. Comm. 240:778-782; Egholm, Cambridge Healthtech Institute's Seventh Annual nucleic acid-Based Technologies, 21-23 de Junio de 1999, Washington, D.C.; Uhlmann, Cambridge Healthtech Institute's Seventh Annual nucleic acid -Based Technologies, 21-23 Junio de 1999, Washington, D.C. Como consecuencia, el uso efectivo de los PNA en la hibridación está limitado a las secuencias en las que no hay más de 4-5 purinas consecutivas, no más de 6 purinas en cualquier porción de 10 bases de la secuencia, y/o no más de 3 residuos G consecutivos. Véase, por ejemplo, http://www.resgen.com/perseptivedesign.html. Además, ya que las interacciones PNA-PNA son aún más fuertes que las interacciones PNA-DNA, las sondas que contienen PNA y los cebadores que contienen secuencias autocomplementarias no pueden utilizarse generalmente para la hibridación de una secuencia diana. Otra consecuencia de la fuerte interacción entre PNA y las moléculas de DNA y/o RNA complementarias es que es difícil obtener una discriminación de desemparejamiento sencillo de nucleótido utilizando sondas de PNA. Demidov et al. (1995) Proc. Natl. Acad. Sci. USA 92:2637-2641.
Uhlmann et al., supra revisan las aproximaciones para aumentar la solubilidad de los PNA, que incluye la síntesis de quimeras de PNA/DNA y la adición de residuos terminales de lisina a un oligómero de PNA. No describen el uso de análogos de nucleótidos para aumentar la solubilidad y mejorar las propiedades de hibridación de los oligómeros de PNA.
Restricciones similares de diseño se requieren en la síntesis de sondas y cebadores de oligonucleótidos que no contienen PNA. Véase, por ejemplo, la publicación titulada "Diseño de Ensayo Cuantitativo y Optimización de los Sistemas de Detección de Secuencias", PE Biosystems, Nº de reserva. 117MI02-01. En estos casos, el contenido de G/C de un oligómero debe mantenerse dentro del rango de 20-80% y debe evitarse la utilización de un nucleótido idéntico, particularmente guanina (G). En particular, la publicación mencionada advierte sobre los tramos de cuatro o más residuos G y frente a la presencia de un residuo G en el extremo 5' terminal de una sonda marcada con fluorescencia en 5'. En el caso de los cebadores, los cinco nucleótidos en el extremo 3' no pueden comprender más de dos residuos G y/o C.
Se ha descrito la síntesis de nucleósidos pirazolo[3,4-d]pirimidina y 7-deazapurina, así como sus monómeros de fosforamidita para su uso en la síntesis de oligómeros. Seela et al. (1985) Nucl. Acids Res. 13:911-926; Seela et al. (1986a) Helv Chim. Acta 69:1191-1198; Seela et al. (1986b) Helv. Chim. Acta 69:1813-1823; y Seela et al. (1987) Biochem. 26:2232-2238. Se describen los nucleósidos de pirazolo[3,4-d]pirimidina y 7-deazapurina para su uso en la secuenciación de DNA y como agentes antivirales en la PE 286 028. La publicación compartida PCT WO 99/51775 describe el uso de oligonucleótidos que contienen pirazolo[3,4-d]pirimidina para hibridación y discriminación de desemparejamientos. Se ha descrito que la incorporación de 2'-deoxi-7-deazaguanosina en el DNA elimina la compresión de bandas en los tramos ricos en GC durante el análisis de la secuencia de DNA mediante electroforesis en gel (Patente Estadounidense Nº 5.844.106), disminuye la formación de tetraplex por secuencias ricas en G (Murchie et al. (1994) EMBO J. 13:993-1001) y reduce la formación de agregados característicos de moléculas de DNA que contienen 2'-deoxiguanosina (Patente Estadounidense Nº 5.480.980). No obstante, la sustitución de oligonucleótidos con 7-deazaadenosina (en lugar de A) o 7-deazaguanosina (en lugar de G) disminuye la Tm de los híbridos formados por dichos oligonucleótidos sustituidos, con más de un grado de reducción en la Tm por base sustituida. Seela et al. (1987) supra; y Seela et al. (1986) Nucl. Acids Res. 14:2319-2332.
Por otro lado, se ha descrito la estabilización de los duplex mediante análogos de la base pirazolopirimidina. Seela et al. (1988) Helv. Chim. Acta. 71:1191-1198; Seela et al. (1988) Helv. Chim Acta. 71:1813-1823; y Seela et al. (1989) nucleic acid Res. 17:901-910. Los oligonucleótidos en los que uno o más residuos de purina se han sustituido por pirazolo[3,4-d]pirimidinas muestran la capacidad mejorada de formación de duplex y triplex, como se describe, por ejemplo, en Belousov et al. (1998) nucleic acid Res. 26:1324-1328; Patente Estadounidense Nº 5.594.121 y publicación PCT compartida WO 98/49180. Los residuos pirazolo[3,4-d]pirimidina en los oligonucleótidos son también útiles como sitios de unión de varios grupos colgantes a oligonucleótidos. Véase...
Reivindicaciones:
1. Un conjugado que comprende:
(a) un polímero que comprende una serie de unidades de monómero; y
(b) un fluoróforo unido covalentemente a ellos,
en el que uno o más de las unidades de monómero comprende un análogo de base, en el que el análogo de base se selecciona de entre el grupo que consiste de pirazolopirimidinas, como el análogo de bases retiene la especificidad de emparejamiento de bases de las bases para las que se sustituyen, y conduce a una reducción en el bloqueo de la fluorescencia del fluoróforo y/o auto-asociación del polímero reducida.
2. El conjugado de la reivindicación 1, en el que el análogo de base posee la estructura
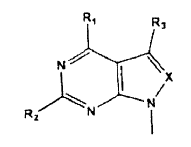
en el que R1 y R2 son independientemente -H, -OH, -SH, o -NH2; R3 es -H, -CN, halógeno (F, Cl, Br o I), o -R12-Y, en el que R12 es C1-C12 alquilo, alquenilo o alquinilo y Y es -H, -OH, -NH2 o -SH; y X es N.
3. El conjugado de la reivindicación 1, que comprende además un bloqueador de la fluorescencia.
4. El conjugado de la reivindicación 1, en el que el polímero comprende DNA.
5. El conjugado de la reivindicación 1, en el que el polímero comprende un péptido de ácido nucleico (PNA) o una quimera PNA/DNA.
6. El conjugado de la reivindicación 4 o 5, en el que el análogo de base está presente independientemente en la porción de DNA o PNA del polímero.
7. El conjugado de cualquiera de las reivindicaciones 2-6, en el que el análogo de base se selecciona de entre el grupo que consiste en pirazolopirimidiniladenina (PPA), pirazolopirimidinilguanina (PPG) y pirazolopirimidinilhipoxantina (PPI).
8. El conjugado de cualquiera de las reivindicaciones 1-7, que posee al menos cuatro residuos consecutivos de purina en el polímero, en el que al menos uno de los cuatro residuos consecutivos de purina en el polímero esté sustituido por un análogo de base.
9. El conjugado de la reivindicación 8, en el que el polímero contiene tres o más guaninas consecutivas que están sustituidas por PPG.
10. El conjugado de la reivindicación 3, en el que el fluoróforo emite entre 400 y 800 nm y en el que el bloqueador de la fluorescencia absorbe entre 400 y 800 nm.
11. El conjugado de cualquiera de las reivindicaciones 1-10, que comprende además un ligando de unión al surco menor.
12. El uso del conjugado de cualquiera de las reivindicaciones 1-11 como sonda para detectar una secuencia diana en una reacción de amplificación (ensayo de sonda hidrolizable).
13. Un microchip de oligómeros, que comprende uno o más oligómeros de acuerdo con cualquiera de las reivindicaciones 1-11.
14. El uso del oligómero de cualquiera de las reivindicaciones 1-11 como una sonda para detectar una secuencia diana en un polinucleótido mediante hibridación.
15. El uso de la reivindicación 12 o 14, en el que la secuencia diana se distingue de una secuencia relacionada que tiene un desemparejamiento de nucleótido sencillo con respecto a la secuencia diana.
Patentes similares o relacionadas:
Compuestos de heteroaril carboxamida como inhibidores de RIPK2, del 29 de Julio de 2020, de BOEHRINGER INGELHEIM INTERNATIONAL GMBH: Un compuesto de fórmula (I): **(Ver fórmula)** o sus sales farmacéuticamente aceptables, en la que: X es N y Y es CH; o X es CH y Y es N; […]
Compuestos de alquinilbenceno heterocíclicos, y composiciones médicas y usos de los mismos, del 29 de Julio de 2020, de Guangzhou Healthquest Pharma Co., Ltd: Un compuesto de alquinilbenceno heterocíclico que tiene la fórmula (I) y una sal farmacéuticamente aceptable, o estereoisómero del mismo, **(Ver […]
1,5-Dihidro-4H-pirazolo[3,4-d]pirimidin-4-onas y 1,5-dihidro-4H-pirazolo[4,3-c]piridin-4-onas como inhibidores de la PDE1, del 29 de Julio de 2020, de H. LUNDBECK A/S: Un compuesto de fórmula (I) **(Ver fórmula)** en donde Y es N o CH; R1 se selecciona del grupo que consiste en alquilo C2-C8 lineal o ramificado, cicloalquilo […]
Compuestos y procedimientos de uso, del 29 de Julio de 2020, de Medivation Technologies LLC: Un compuesto de fórmula (Aa-1): **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, en la que: A representa H, halógeno, amino, […]
Ureas cíclicas como inhibidores de ROCK, del 22 de Julio de 2020, de BRISTOL-MYERS SQUIBB COMPANY: Un compuesto de acuerdo con la Fórmula (I): **(Ver fórmula)** o un enantiómero, un diastereómero, un estereoisómero, un tautómero, una sal farmacéuticamente aceptable […]
Derivado heteroarilo o sal farmacéuticamente aceptable del mismo, método de preparación del mismo y composición farmacéutica para prevenir o tratar enfermedades asociadas con PI3 quinasas, que contiene el mismo como principio activo, del 22 de Julio de 2020, de KOREA RESEARCH INSTITUTE OF CHEMICAL TECHNOLOGY: Un compuesto representado por la fórmula 1, un isómero óptico del mismo o una sal farmacéuticamente aceptable del mismo: **(Ver fórmula)** en la fórmula […]
Derivado de dihidropiridazin-3,5-diona, del 15 de Julio de 2020, de CHUGAI SEIYAKU KABUSHIKI KAISHA: Un compuesto representado por la fórmula (I) o una sal del mismo, o un solvato del compuesto o la sal: **(Ver fórmula)** en donde R1, R4 y R5 se definen […]
Derivados de 5-[2-(piridin-2-ilamino)-1,3-tiazol-5-il]-2,3-dihidro-1H-isoindol-1-ona y su uso como inhibidores dobles de fosfatidilinositol··3-cinasa delta y gamma, del 15 de Julio de 2020, de ASTRAZENECA AB: Compuesto de formula (I) **(Ver fórmula)** donde X es C(O) o SO2; Y es SO2NHR5 o SO2R6; R1 se selecciona de alquilo C1-4, […]