Métodos y reactivos para detectar la inhibición de la fluorescencia.
Un compuesto de sonda de oligonucleótidos con la fórmula siguiente:
donde
Ar1 y Ar2 son, cada uno de ellos independientemente, un grupo arilo sustituido o no sustituido, y uno de los elementos Ar1 o Ar2 es directa o indirectamente sustituido por un grupo arilo sustituido (Ar3), donde Ar3 amplía la capacidad de resonancia del sistema aromático Ar1-N≥N-Ar2 y, por tanto, aumenta la absorbancia de longitud de onda máxima del compuesto;
MGB es un grupo de unión al surco menor;
FL es un grupo fluorescente que tiene una máxima de emisión en la región de 400 a 900 nm;
K es un grupo de unión cíclico o acíclico que tiene entre 1 y 30 átomos del esqueleto seleccionados entre C, N, O, S y P;
W es un grupo de unión que tiene entre 3 y 100 átomos del esqueleto seleccionados entre C, N, O, S, Si y P, siendo dicho grupo de unión cíclico, acíclico, aromático o una combinación de los mismos;
[A-B]n es un oligonucleótido natural o modificado donde el subíndice n es un número entero de 4 a 10; y
el subíndice zz es 1.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2002/017787.
Solicitante: EPOCH BIOSCIENCES, INC.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 21720 23RD DRIVE SE, SUITE 150 BOTHELL, WA 98021 ESTADOS UNIDOS DE AMERICA.
Inventor/es: VERMEULEN, NICOLAAS M.J., GALL,ALEXANDER,A, DEMPCY,ROBERT,O, REED,Michael W, LUKHTANOV,Eugeny Alexander.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C07H19/00 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07H AZUCARES; SUS DERIVADOS; NUCLEOSIDOS; NUCLEOTIDOS; ACIDOS NUCLEICOS (derivados de ácidos aldónicos o sacáricos C07C, C07D; ácidos aldónicos, ácidos sacáricos C07C 59/105, C07C 59/285; cianohidrinas C07C 255/16; glicales C07D; compuestos de constitución indeterminada C07G; polisacáridos, sus derivados C08B; ADN o ARN concerniente a la ingeniería genética, vectores, p. ej. plásmidos o su aislamiento, preparación o purificación C12N 15/00; industria del azúcar C13). › Compuestos que contienen un heterociclo que comparten un heteroátomo del ciclo con un radical sacárido; Nucleósidos; Mononucleótidos; Sus anhidro-derivados.
- C07H21/00 C07H […] › Compuestos que contienen al menos dos unidades mononucleótido que tienen cada una grupos fosfato o polifosfato distintos unidos a los radicales sacárido de los grupos nucleósido, p. ej. ácidos nucleicos.
- C07H21/02 C07H […] › C07H 21/00 Compuestos que contienen al menos dos unidades mononucleótido que tienen cada una grupos fosfato o polifosfato distintos unidos a los radicales sacárido de los grupos nucleósido, p. ej. ácidos nucleicos. › con ribosilo como radical sacárido.
- C07H21/04 C07H 21/00 […] › con desoxirribosilo como radical sacárido.
- C09B29/00 C […] › C09 COLORANTES; PINTURAS; PULIMENTOS; RESINAS NATURALES; ADHESIVOS; COMPOSICIONES NO PREVISTAS EN OTRO LUGAR; APLICACIONES DE LOS MATERIALES NO PREVISTAS EN OTRO LUGAR. › C09B COLORANTES ORGANICOS O COMPUESTOS ESTRECHAMENTE RELACIONADOS PARA PRODUCIR COLORANTES; MORDIENTES; LACAS (procesos de fermentación o procesos que utilizan enzimas para la síntesis de un compuesto dado C12P). › Colorantes monoazo preparados por diazoación y copulación.
- C12Q1/68 C […] › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12Q PROCESOS DE MEDIDA, INVESTIGACION O ANALISIS EN LOS QUE INTERVIENEN ENZIMAS, ÁCIDOS NUCLEICOS O MICROORGANISMOS (ensayos inmunológicos G01N 33/53 ); COMPOSICIONES O PAPELES REACTIVOS PARA ESTE FIN; PROCESOS PARA PREPARAR ESTAS COMPOSICIONES; PROCESOS DE CONTROL SENSIBLES A LAS CONDICIONES DEL MEDIO EN LOS PROCESOS MICROBIOLOGICOS O ENZIMOLOGICOS. › C12Q 1/00 Procesos de medida, investigación o análisis en los que intervienen enzimas, ácidos nucleicos o microorganismos (aparatos de medida, investigación o análisis con medios de medida o detección de las condiciones del medio, p. ej. contadores de colonias, C12M 1/34 ); Composiciones para este fin; Procesos para preparar estas composiciones. › en los que intervienen ácidos nucleicos.
PDF original: ES-2421085_T3.pdf
Fragmento de la descripción:
Métodos y reactivos para detectar la inhibición de la fluorescencia.
Antecedentes de la invención 5
Campo de la invención
La invención se refiere a conjugados de oligonucleótido-inhibidor de fluorescencia-colorante fluorescente que presentan características mejoradas y a reactivos adecuados para incorporar nuevas fracciones de inhibidor de 10 fluorescencia y colorante fluorescente a los oligonucleótidos. La invención también se refiere al uso de conjugados de oligonucleótido-inhibidor de fluorescencia-colorante fluorescente en métodos de detección de dianas de ácido nucleico.
Descripción del campo relacionado 15
Los oligonucleótidos sintéticos se han utilizado durante años como sondas de secuencia específica para dianas de ADN y ARN complementarias. Estos métodos se aplican mucho en la ciencia forense, la biología molecular y el diagnóstico médico, dado que permiten la identificación y cuantificación de dianas de ácido nucleico específicas. Los primeros usos de sondas de ADN empleaban la radioactividad (típicamente 32P) como etiqueta, mientras que los 20 métodos recientes utilizan moléculas reporteras que incluyen grupos quimioluminiscentes y fluorescentes. La mejora de la instrumentación ha permitido que la sensibilidad de estos métodos espectroscópicos se aproxime o incluso supere a los métodos de radioetiquetas. Los métodos de detección desarrollados recientemente emplean el procedimiento de transferencia de energía de resonancia de fluorescencia (FRET) en lugar de la detección directa de la intensidad de la fluorescencia para detectar la sonda de hibridación. En este tipo de ensayo, la FRET se 25 produce entre un fluoróforo donante (reportero) y una molécula aceptadora (inhibidora de fluorescencia) , cuando el espectro de absorción de la molécula inhibidora de fluorescencia se solapa con el espectro de emisión del fluoróforo donante y las dos moléculas se encuentran muy próximas. La energía del estado excitado del fluoróforo donante es transferida a la aceptadora vecina mediante una interacción dipolo-dipolo inducido por resonancia, que produce una inhibición de la fluorescencia del donante. Si la molécula aceptadora es un fluoróforo, en ocasiones su fluorescencia 30 puede aumentar. La eficiencia de la transferencia de energía entre la molécula donante y la aceptadora depende en gran medida de la distancia que las separa. Las ecuaciones que describen esta relación son conocidas. La distancia de Forster (R0) se describe como la distancia entre la molécula donante y la aceptadora en la que la transferencia de energía alcanza una eficiencia del 50%. También se conocen otros mecanismos de inhibición de la fluorescencia, tales como la inhibición por colisión y transferencia de carga. 35
Los métodos de detección típicos basados en la FRET están diseñados de forma que el fluoróforo donante y la molécula aceptadora se encuentran muy cerca y la inhibición de la fluorescencia del donante resulta eficiente. Durante el ensayo, la molécula donante y la aceptadora mantienen una separación tal que se produce la fluorescencia. Los ensayos de detección basados en la FRET han sido desarrollados en los ámbitos de la 40 enzimología y la hibridación de ácido nucleico. Se revisan varias formas de ensayos de hibridación por FRET (Nonisotopic DNA Probe Techniques, Academic Press, Inc., San Diego 1992, pp. 311 -352) . La inhibición de la fluorescencia también se puede producir mediante mecanismos diferentes a la FRET, como la inhibición por colisión (véase, Wei et al., Anal. Chem. 66:1500-1506 (1994) ) .
Desde su descubrimiento, la reacción en cadena de polimerasa (PCR) ha revolucionado la biología molecular. Esta técnica permite la amplificación de secuencias de ADN específicas, lo que hace posible que los ensayos sobre sondas de ADN se ejecuten con una única copia de la diana de ADN. Inicialmente los ensayos de diagnóstico basados en la PCR no se han empleado de forma rutinaria, en parte debido a los problemas asociados a la manipulación de las muestras y a una posible contaminación con ADN de origen diferente. Recientemente se han 50 descrito nuevos ensayos homogéneos de ADN basados en la fluorescencia que pueden detectar el progreso de la PCR a medida que se produce (detección de PCR «en tiempo real») , utilizando cicladores de temperatura espectrofluorométricos. Dos populares formatos de ensayo utilizan sondas de ADN que se vuelven fluorescentes cuando se produce la amplificación del ADN (sondas fluorogénicas) .
El primer formato para la PCR «en tiempo real» utiliza sondas de ADN conocidas como «balizas moleculares» (Tyagi et al., Nat. Biotech., 16: 49-53 (1998) ) . Las balizas moleculares presentan una estructura de horquilla, en la que el colorante inhibidor de la fluorescencia y el colorante reportero mantienen un fuerte contacto entre sí en el extremo del tallo de la horquilla. Tras la hibridación con una secuencia complementaria, el bucle de la estructura de horquilla pasa a ser de cadena doble y fuerza la separación del colorante reportero y del inhibidor de la 60 fluorescencia, generando así una señal fluorescente. Tyagi et al. documentaron el uso de los colorantes inhibidores no fluorescentes, como dabcilo (fracción de 4-{[4- (dimetilamino) fenil]-diazenil}benzoico, absorbancia máx = 453 nm) empleado en combinación con colorantes reporteros fluorescentes con una longitud de onda de emisión muy variable (475-615 nm) . En ese momento resultó sorprendente porque la FRET exige un solapamiento significativo del espectro de absorción del inhibidor de fluorescencia con el espectro de emisión del reportero. En el caso de un inhibidor de fluorescencia que contenía una fracción de dabcilo (en adelante «dabcilo») y algunos colorantes fluorescentes, el solapamiento espectral era extremadamente bajo, aunque la eficiencia de la inhibición de la fluorescencia era elevada. Por tanto, se propuso que el mecanismo de inhibición de la fluorescencia para la forma de horquilla de las balizas no era la FRET, sino la inhibición por colisión. De hecho, los espectros UV del inhibidor de 5 fluorescencia varían en la forma de horquilla de la baliza, lo que demuestra el contacto molecular y, por tanto, la inhibición por colisión. Un método de detección relacionado utiliza cebadores de horquilla como sonda fluorogénica (Nazarenko et al., Nucl. Acid Res. 25:2516-2521 (1997) ) .
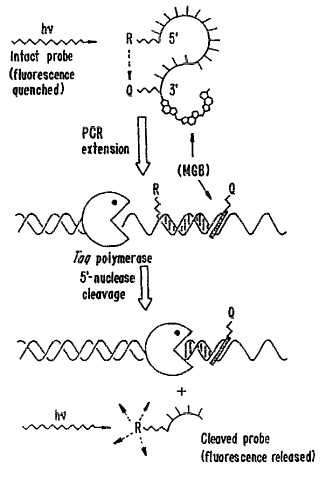
El segundo formato para la PCR «en tiempo real» utiliza sondas de ADN denominadas «sondas de 5’ nucleasa» 10 (Lee et al., Nucl. Acid Res., 21: 3761-3766 (1993) ) . Estas sondas fluorogénicas se preparan típicamente con el inhibidor de fluorescencia en el extremo 3’ de una cadena simple de ADN y el fluoróforo en el extremo 5’. Durante cada ciclo de PCR, la actividad de 5’ nucleasa de la Taq ADN polimerasa cliva la cadena de ADN, separando así el fluoróforo del inhibidor de fluorescencia y liberando la señal fluorescente. El ensayo de 5’ nucleasa exige que la sonda se hibride con la cadena de plantilla durante el paso de extensión del cebador (60-65ºC) . También divulgan la 15 detección simultánea «en tiempo real» de más de una secuencia de polinucleótidos en el mismo ensayo, utilizando más de un par de fluoróforo/inhibidor de fluorescencia. El ensayo de PCR de 5’ nucleasa se ilustra en la Figura 1.
Inicialmente se pensaba que las sondas de 5’ nucleasa se tenían que preparar con el inhibidor de fluorescencia (habitualmente tetrametilrodamina (TAMRA) ) posicionado en un nucleótido interno muy próximo al 5’ fluoróforo 20 (habitualmente fluoresceína (FAM) o tetraclorofluoresceína (TET) ) para conseguir una FRET eficiente. Más tarde se descubrió que esto no es necesario, y que el inhibidor de fluorescencia y el fluoróforo pueden estar posicionados en los extremos 3’ y 5’ del ODN, respectivamente. Se ha propuesto que las estructuras en espiral aleatorias que forman estas sondas fluorogénicas en solución permiten que un 3’ colorante inhibidor de la fluorescencia pase dentro del radio de Forster del 5’ fluoróforo durante el estado excitado de la molécula. 25
Anteriormente se han descrito diversos pares de donante/aceptor. Para la presente invención es importante el dabcilo, que se emplea, por ejemplo, como inhibidor de la fluorescencia de la sulfonamida de dansilo en los quimiosensores (Rothman & Still (1999) Med. Chem. Lett. 22:509-512) .
Sorprendentemente, no se ha publicado ningún informe sobre el uso de dabcilo en sondas de 5’ nucleasa u otras sondas de FRET que emplean fluoróforos de longitud de onda larga. Como se ha mencionado anteriormente, el dabcilo se empleó en las sondas tipo baliza, pero este es un mecanismo de inhibición de la fluorescencia... [Seguir leyendo]
Reivindicaciones:
1. Un compuesto de sonda de oligonucleótidos con la fórmula siguiente:
donde 5
Ar1 y Ar2 son, cada uno de ellos independientemente, un grupo arilo sustituido o no sustituido, y uno de los elementos Ar1 o Ar2 es directa o indirectamente sustituido por un grupo arilo sustituido (Ar3) , donde Ar3 amplía la capacidad de resonancia del sistema aromático Ar1-N=N-Ar2 y, por tanto, aumenta la absorbancia de longitud de onda máxima del compuesto;
MGB es un grupo de unión al surco menor; 10
FL es un grupo fluorescente que tiene una máxima de emisión en la región de 400 a 900 nm;
K es un grupo de unión cíclico o acíclico que tiene entre 1 y 30 átomos del esqueleto seleccionados entre C, N, O, S y P;
W es un grupo de unión que tiene entre 3 y 100 átomos del esqueleto seleccionados entre C, N, O, S, Si y P, siendo dicho grupo de unión cíclico, acíclico, aromático o una combinación de los mismos; 15
[A-B]n es un oligonucleótido natural o modificado donde el subíndice n es un número entero de 4 a 10; y
el subíndice zz es 1.
2. Un compuesto de la reivindicación 1 donde Ar2 es sustituido por Ar3.
3. Un compuesto de la reivindicación 2 donde Ar2 es indirectamente sustituido por Ar3.
4. Un compuesto de la reivindicación 3, donde Ar2 es indirectamente sustituido por Ar3 a través de un anillo o anillos aromáticos y/o de un enlace o enlaces dobles.
5. Un compuesto de la reivindicación 4, donde Ar2 es indirectamente sustituido por Ar3 a través de un enlace doble seleccionado de los enlaces dobles de carbono-carbono y nitrógeno-nitrógeno.
6. Un compuesto de la reivindicación 5, donde Ar2 es indirectamente sustituido por Ar3 a través de un grupo seleccionado entre - (C≡C) t- y - (CR'=CR') t donde t es 0-5 y R' es independientemente seleccionado entre hidrógeno, 30 (C1-C8) alquilo y heteroalquilo, arilo y heteroarilo no sustituido, (arilo no sustituido) - (C1-C4) alquilo, y (arilo no sustituido) oxi- (C1-C4) alquilo.
7. Un compuesto de la reivindicación 1, donde al menos Ar1, Ar2 o bien Ar3 es sustituido por -halógeno, -OR', -OC (O) R' -NR'R", -SR' -R', -CN, -NO2, -CO2R', -CONR'R", -C (O) R', -OC (O) NR'R", -NR"C (O) R', -NR"C (O) 2R', -NR, -35 C (O) NR"R"', -NH-C (NH2) =NH, -NR'C (NH2) =NH, -NH-C (NH2) =NR', -S (O) R', -S (O) 2R', -S (O) 2NR'R", -N3, -CH (Ph) 2, perfluoro (C1-C4) alcoxilo, y perfluoro (C1-C4) alquilo, en un número que oscila entre cero y el número total de valencias abiertas en el sistema de anillo aromático; y donde R', R" y R"' son seleccionados, independientemente, entre hidrógeno, (C1-C8) alquilo y heteroalquilo, y (arilo no sustituido) oxi- (C1-C4) alquilo.
8. Un compuesto de la reivindicación 7 donde Ar2 es indirectamente sustituido por Ar3 a través de un enlace doble.
9. Un compuesto de la reivindicación 8, donde Ar2-N=N-Ar1- tiene la estructura siguiente:
45
10. Un compuesto de la reivindicación 7 donde Ar2 es directamente sustituido por Ar3.
11. Un compuesto de la reivindicación 10, donde Ar2-N=N-Ar1- tiene la estructura siguiente:
12. Un compuesto de la reivindicación 1, donde W comprende un grupo arilo substituido (Ar3) que está directa o indirectamente unido a Ar1 y amplía la capacidad de resonancia del sistema aromático Ar1-N=N-Ar2 y, por tanto, aumenta la absorbancia de longitud de onda máxima del compuesto. 5
13. Un compuesto de la reivindicación 12, donde Ar1 es indirectamente sustituido por Ar3 a través de un anillo o anillos aromáticos y/o de un enlace o enlaces dobles.
14. Un compuesto de la reivindicación 13, donde Ar1 es indirectamente sustituido por Ar3 a través de un enlace 10 doble seleccionado entre los enlaces dobles de carbono-carbono y nitrógeno-nitrógeno.
15. Un compuesto de la reivindicación 14, donde Ar1 es indirectamente sustituido por Ar3 a través de un grupo seleccionado entre - (C≡C) t y - (CR'=CR') t donde t es 0-5 y R' es independientemente seleccionado entre hidrógeno, (C1-C8) alquilo y heteroalquilo, arilo y heteroarilo no sustituido, (arilo no sustituido) - (C1-C4) alquilo, y (arilo no 15 sustituido) oxi- (C1-C4) alquilo.
Patentes similares o relacionadas:
Un procedimiento de marcaje enzimático específico de sitio de ácidos nucleicos in vitro mediante la incorporación de nucleótidos no naturales, del 4 de Diciembre de 2019, de THE SCRIPPS RESEARCH INSTITUTE: Un compuesto que comprende un análogo de nucleobase de cualquiera de las fórmulas siguientes: **(Ver fórmula)** en las que R es hidrógeno […]
Composiciones que comprenden profármaco de nucleótidos y oligonucleótidos, del 5 de Noviembre de 2019, de Spring Bank Pharmaceuticals, Inc: Una composición para su uso en medicina, en la que la composición comprende un compuesto de fórmula (III):**Fórmula** o una sal, racemato, enantiómero, diastereómero, […]
Tratamiento de enfermedades relacionadas con la Sirtuina 1 (SIRT1) por inhibición del transcrito antisentido natural de la Sirtuina 1, del 11 de Septiembre de 2019, de CuRNA, Inc: Un oligonucleótido antisentido que se une a un transcrito antisentido natural de Sirtuina 1 (SIRT1) para su uso como compuesto terapéutico, donde el […]
Nucleósidos sustituidos, nucleótidos y sus análogos, del 25 de Abril de 2019, de Alios Biopharma, Inc: Un compuesto de Fórmula (I), o una de sus sales farmacéuticamente aceptable, para su uso en la mejora o el tratamiento de una infección vírica causada por un virus seleccionado […]
Nucleósidos sustituidos, nucleótidos y sus análogos, del 27 de Febrero de 2019, de Alios Biopharma, Inc: Un compuesto de Fórmula (I), o una de sus sales farmacéuticamente aceptable:**Fórmula** en donde: B1A se selecciona del grupo que consiste en: **Fórmula** en donde: […]
Análogos nucleotídicos para secuenciación, del 16 de Enero de 2019, de IBIS BIOSCIENCES, INC: Un análogo nucleotídico que comprende: a) un nucleótido que comprende un resto fosfato, una base y un azúcar; b) un resto de terminación fotoescindible, detectable […]
Análogos de 2''-cloro nucleósidos para infección por VHC, del 18 de Abril de 2018, de Idenix Pharmaceuticals LLC: Un compuesto de acuerdo con la Fórmula (III): **Fórmula** o una sal, solvato, forma tautomérica o forma polimórfica farmacéuticamente aceptable de los mismos; […]
Moléculas conectoras fotoescindibles con esqueleto de diarilsulfuro para la síntesis transitoria de bioconjugados, del 29 de Noviembre de 2017, de VENTANA MEDICAL SYSTEMS, INC.: Un compuesto fotoescindible de la fórmula **Fórmula** en el que A es -CH2-, -CH2-CH2-, -CH(CH3)- o -CH(CH3)-CH2-, R3 es H, un grupo metilo […]