OLIGONUCLEÓTIDOS MODIFICADOS PARA LA DISCRIMINACIÓN DE DESAPAREAMIENTOS.
Un oligonucleótido modificado que comprende al menos una base de pirazolo[3,
4 d]pirimidina no sustituida y al menos una base de pirazolo[3,4-d]pirimidina 3-sustituida
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2001/006900.
Solicitante: EPOCH BIOSCIENCES, INC.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 21720 23RD DRIVE SE, SUITE 150 BOTHELL, WA 98021 ESTADOS UNIDOS DE AMERICA.
Inventor/es: VERMEULEN, NICOLAAS M.J., KUTYAVIN,IGOR,V, GALL,ALEXANDER,A, DEMPCY,ROBERT,O, AFONINA,IRINA,A, SINGER,MICHAEL,J, LOKHOV,SERGEY,G.
Fecha de Publicación: .
Fecha Solicitud PCT: 1 de Marzo de 2001.
Fecha Concesión Europea: 18 de Agosto de 2010.
Clasificación PCT:
- A61K31/7115 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › Acidos nucleicos u oligonucleótidos que tienen bases modificadas, es decir distintas de la adenina, la guanina, la citosina, el uracilo o la timina.
- C07H19/06 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07H AZUCARES; SUS DERIVADOS; NUCLEOSIDOS; NUCLEOTIDOS; ACIDOS NUCLEICOS (derivados de ácidos aldónicos o sacáricos C07C, C07D; ácidos aldónicos, ácidos sacáricos C07C 59/105, C07C 59/285; cianohidrinas C07C 255/16; glicales C07D; compuestos de constitución indeterminada C07G; polisacáridos, sus derivados C08B; ADN o ARN concerniente a la ingeniería genética, vectores, p. ej. plásmidos o su aislamiento, preparación o purificación C12N 15/00; industria del azúcar C13). › C07H 19/00 Compuestos que contienen un heterociclo que comparten un heteroátomo del ciclo con un radical sacárido; Nucleósidos; Mononucleótidos; Sus anhidro-derivados. › Radicales de pirimidina.
- C07H19/10 C07H 19/00 […] › con el radical sacárido esterificado por ácidos fosfóricos o polifosfóricos.
- C07H19/16 C07H 19/00 […] › Radicales de purina.
- C07H19/20 C07H 19/00 […] › con el radical sacárido esterificado por ácidos fosfóricos o polifosfóricos.
- C07H21/00 C07H […] › Compuestos que contienen al menos dos unidades mononucleótido que tienen cada una grupos fosfato o polifosfato distintos unidos a los radicales sacárido de los grupos nucleósido, p. ej. ácidos nucleicos.
- C12Q1/68 C […] › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12Q PROCESOS DE MEDIDA, INVESTIGACION O ANALISIS EN LOS QUE INTERVIENEN ENZIMAS, ÁCIDOS NUCLEICOS O MICROORGANISMOS (ensayos inmunológicos G01N 33/53 ); COMPOSICIONES O PAPELES REACTIVOS PARA ESTE FIN; PROCESOS PARA PREPARAR ESTAS COMPOSICIONES; PROCESOS DE CONTROL SENSIBLES A LAS CONDICIONES DEL MEDIO EN LOS PROCESOS MICROBIOLOGICOS O ENZIMOLOGICOS. › C12Q 1/00 Procesos de medida, investigación o análisis en los que intervienen enzimas, ácidos nucleicos o microorganismos (aparatos de medida, investigación o análisis con medios de medida o detección de las condiciones del medio, p. ej. contadores de colonias, C12M 1/34 ); Composiciones para este fin; Procesos para preparar estas composiciones. › en los que intervienen ácidos nucleicos.
Clasificación antigua:
- C12Q1/68 C12Q 1/00 […] › en los que intervienen ácidos nucleicos.
Países PCT: Austria, Bélgica, Suiza, Alemania, Dinamarca, España, Francia, Reino Unido, Grecia, Italia, Liechtensein, Luxemburgo, Países Bajos, Suecia, Mónaco, Portugal, Irlanda, Eslovenia, Finlandia, Rumania, Chipre, Lituania, Letonia, Ex República Yugoslava de Macedonia, Albania.
Fragmento de la descripción:
ANTECEDENTES DE LA INVENCIÓN
Esta solicitud se engloba en el campo de la biología molecular que se refiere al uso de oligonucleótidos como sondas y cebadores en ensayos en fase líquida, sólida y mixta. La solicitud se refiere además al uso de bases de ácidos nucleicos modificadas y oligonucleótidos modificados para mejorar las propiedades de hibridación y las capacidades discriminatorias de oligonucleótidos que se emplean en matrices y como sondas y cebadores.
Muchas técnicas actualmente en uso en la biología molecular emplean oligonucleótidos como sondas y/o cebadores. A menudo resulta ventajoso, en la práctica de estas tecnologías, ser capaz de distinguir entre dos o más secuencias que están relacionadas pero que se diferencian en uno o más nucleótidos. Por ejemplo, muchas mutaciones de importancia clínica se diferencian sólo en un único nucleótido con respecto a la secuencia de tipo salvaje. Los polimorfismos en los genomas de mamífero a menudo también se caracterizan por diferencias en la secuencia de uno
o unos pocos nucleótidos. La capacidad para realizar tal distinción se conoce como discriminación de desapareamientos. En términos prácticos, la discriminación de desapareamientos describe la propiedad mediante la cual un oligonucleótido de secuencia definida, a una rigurosidad concreta, se hibrida con gran fuerza (una manifestación de ello es que los híbridos tienen un alto punto de fusión) con una secuencia diana con la que es complementaria a lo largo de su longitud completa (un híbrido perfecto o un apareamiento perfecto), pero se hibrida, de una manera detectable, de forma más débil con una secuencia diana que no es complementaria con la secuencia del oligonucleótido en uno o unos pocos nucleótidos (un desapareamiento). Las diferencias en la fuerza de hibridación son tales que puede seleccionarse una rigurosidad concreta en la que un apareamiento perfecto es detectable como un híbrido y un desapareamiento no puede formar un híbrido.
En un dúplex de ácido nucleico, cada par de bases contribuye a la estabilidad. Por tanto, cuanto más corto sea el dúplex, mayor será la contribución relativa de cada par de bases individual a la estabilidad del dúplex. Como resultado, la diferencia en la estabilidad entre un apareamiento perfecto y un desapareamiento será mayor para oligonucleótidos más cortos. Sin embargo, los oligonucleótidos cortos se hibridan de forma débil, incluso con una secuencia perfectamente complementaria, y por tanto deben hibridarse bajo condiciones de rigurosidad reducida. Por tanto, el poder discriminatorio potencial de oligonucleótidos cortos no puede obtenerse con facilidad excepto bajo condiciones de baja rigurosidad.
En la técnica se necesitan nuevos procedimientos para la discriminación de desapareamientos, en particular desapareamientos de un único nucleótido, bajo condiciones de alta rigurosidad, por ejemplo, a las elevadas temperaturas características de la mayoría de las reacciones de amplificación de ácidos nucleicos. De forma sorprendente, la presente invención proporciona dichos procedimientos, junto con nuevos reactivos y composiciones que pueden utilizarse en los procedimientos.
El documento WO 99/51775 describe oligonucleótidos que contienen análogos de pirazolo[3,4-d]pirimidinas para la hibridación y la discriminación de desapareamientos. SUMARIO DE LA INVENCIÓN
La presente invención proporciona una serie de oligonucleótidos modificados que se ha descubierto que poseen unas propiedades y una utilidad excepcionales en una diversidad de ensayos. Por consiguiente, la presente invención también proporciona procedimientos para utilizar los oligonucleótidos modificados descritos en la presente.
En un aspecto, la presente invención proporciona oligonucleótidos modificados que tienen al menos una base de pirazolo[3,4-d]pirimidina no sustituida y al menos una base de pirazolo[3,4d]pirimidina 3-sustituida. En realizaciones preferidas, los oligonucleótidos tienen bases modificadas que comprenden además otros restos, tales como marcadores detectables, extintores de fluorescencia y de quimioluminiscencia y/o ligantes del surco menor y/u otros tipos de bases modificadas o análogos de bases.
El alcance de la presente invención se define por las reivindicaciones y cualquier información que no se encuentre dentro de las reivindicaciones se proporciona sólo como información.
En otro aspecto, la presente invención proporciona procedimientos para distinguir polinucleótidos que tienen secuencias relacionadas.
En otro aspecto, la presente invención proporciona procedimientos para detectar la presencia de una secuencia diana en un polinucleótido.
En otros aspectos, la presente invención proporciona procedimientos para la extensión de cebadores, y procedimientos para determinar la secuencia de nucleótidos de un polinucleótido.
En aspectos relacionados, la presente invención proporciona procedimientos para estudiar la expresión génica en una célula, y procedimientos para identificar una mutación o un polimorfismo en una secuencia diana de un gen de interés.
En otro aspecto, la presente invención proporciona una serie de bases modificadas que son útiles para preparar oligonucleótidos modificados para los procedimientos descritos en la presente y otros procedimientos y ensayos convencionales.
En otro aspecto, la presente invención proporciona matrices de oligonucleótidos modificados en las que los miembros de la matriz tienen unas Tm dentro de un intervalo de aproximadamente 1-2 ºC, y unas longitudes dentro de un intervalo de 1-2 bases entre ellos. También se proporcionan procedimientos para determinar las secuencias de los miembros de la matriz.
BREVE DESCRIPCIÓN DE LOS DIBUJOS
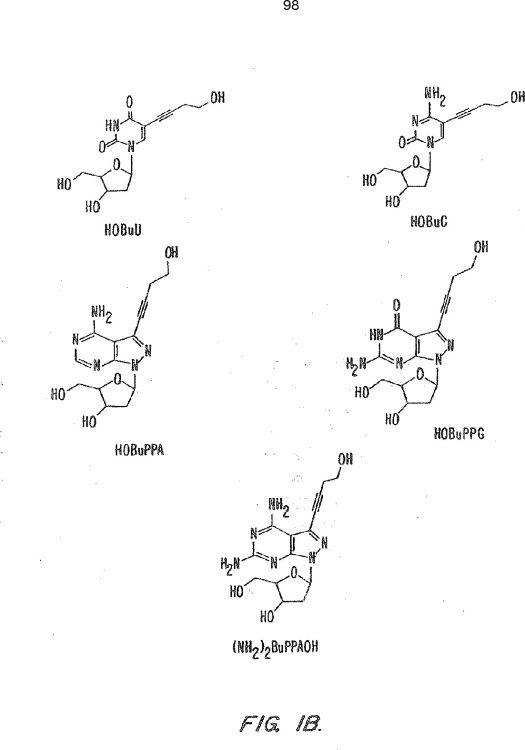
Las figuras 1A y 1B proporcionan las estructuras de varias bases modificadas y sus abreviaturas. La línea ondulada se utiliza para indicar la posición de un resto azúcar unido (sin proteger, protegido, activado y similares).
La figura 2 es una gráfica que ilustra el equilibrio de la Tm de sondas 8-meras ricas en GC y ricas en AT con diferentes combinaciones de MGB, PPPA y PU.
La figura 3 es un gráfica que ilustra una ventaja lograda mediante el uso de PPPA y PPG en sondas oligonucleotídicas modificadas con MGB. Como puede observarse en la figura, las bases modificadas permiten acortar la sonda que muestre una mayor discriminación de desapareamientos en una PCR a tiempo real. Ã es PPPA y G es PPG. Sonda FAM modificada con MGB = SEQ ID NO:1; complemento de la sonda FAM modificada con MGB = SEQ ID NO:2; complemento de la sonda FAM modificada con MGB que contiene PPPA y PPG = SEQ ID NO:3; sonda FAM modificada con MGB que contiene PPPA y PPG = SEQ ID NO:4.
La figura 4 ilustra un ensayo Invader™ en que pueden utilizarse los oligonucleótidos modificados de la invención.
La figura 5 ilustra la comparación de la actuación de la sonda de Invader™ con diferentes números de PPG (SEQ ID NO:5-7). DESCRIPCIÓN DE LA INVENCIÓN Abreviaturas y definiciones
Las abreviaturas para una serie de bases modificadas descritas en la presente se proporcionan como sigue (las estructuras de estas bases se muestran en las figuras 1A y 1B): 6amino-3-prop-1-inil-5-hidropirazolo[3,4-d]pirimidin-4-ona, PPPG; 6-amino-3-(3-hidroxiprop-1inil)-5-hidropirazolo[3,4-d]pirimidin-4-ona, HOPPPG; 6-amino-3-(3-aminoprop-1-inil)-5hidropirazolo[3,4-d]pirimidin-4-ona, NH2PPPG; 4-amino-3-(prop-1-inil)pirazolo[3,4-d]pirimidina, PPPA; 4-amino-3-(3-hidroxiprop-1-inil)pirazolo[3,4-d]pirimidina, HOPPPA; 4-amino-3-(3aminoprop-1-inil)pirazolo[3,4-d]pirimidina, NH2PPPA; 3-prop-1-inilpirazolo[3,4-d]pirimidin-4,6diamino, (NH2)2PPPA; 2-(4,6-diaminopirazolo[3,4-d]pirimidin-3-il)etin-1-ol, (NH2)2PPPAOH; 3-(2aminoetinil)pirazolo[3,4-d]pirimidin-4,6-diamina, (NH2)2PPPANH2; 5-prop-1-inil-1,3dihidropirimidin-2,4-diona, PU; 5-(3-hidroxiprop-1-inil)-1,3-dihidropirimidin-2,4-diona, HOPU; 6amino-5-prop-1-inil-3-dihidropirimidin-2-ona, PC; 6-amino-5-(3-hidroxiprop-1-inil)-1,3dihidropirimidin-2-ona, HOPC; y 6-amino-5-(3-aminoprop-1-inil)-1,3-dihidropirimidin-2-ona, NH2PC; 5-[4-amino-3-(3-metoxiprop-1-inil)pirazol[3,4-d]pirimidinil]-2-(hidroximetil)oxolan-3-ol, CH3OPPPA; 6-amino-1-[4-hidroxi-5-(hidroximetil)oxolan-2-il]-3-(3-metoxiprop-1-inil)-5hidropirazolo[3,4-d]pirimidin-4-ona, CH3OPPPG; 5-(4-hidroxibut-1-inil)-1,3-dihidropirimidin-2,4diona, HOBuU; 6-amino-5-(4-hidroxibut-1-inil)-3-hidropirimidin-2-ona, HOBuC; 4-(4aminopirazolo[3,4-d]pirimidin-3-il)but-3-in-1-ol,...
Reivindicaciones:
1. Un oligonucleótido modificado que comprende al menos una base de pirazolo[3,4d]pirimidina no sustituida y al menos una base de pirazolo[3,4-d]pirimidina 3-sustituida. 2. Un oligonucleótido modificado de la reivindicación 1, que comprende además un 5 ligante del surco menor unido de modo covalente. 3. Un oligonucleótido modificado de la reivindicación 1, que comprende además al menos un grupo indicador unido de modo covalente. 4. Un oligonucleótido modificado de la reivindicación 1, que comprende además al menos un extintor unido de modo covalente. 10 5. Un oligonucleótido modificado de la reivindicación 3, en el que dicho grupo indicador es un fluoróforo. 6. Un oligonucleótido modificado de la reivindicación 3, en el que dicho grupo indicador es un fluoróforo, y dicho oligonucleótido modificado comprende además un extintor unido. 7. Un oligonucleótido modificado de la reivindicación 1, que comprende de 4 a 70 bases. 15 8. Un oligonucleótido modificado de la reivindicación 1, que comprende de 4 a 70 bases, y que comprende además un ligante del surco menor unido. 9. Un oligonucleótido modificado de la reivindicación 1, que comprende de 4 a 70 bases, y que comprende además un fluoróforo unido y un extintor. 10. Un oligonucleótido modificado de la reivindicación 2, que comprende de 4 a 70 20 bases, y que comprende además un fluoróforo unido y un extintor.
11. Un oligonucleótido modificado de la reivindicación 1, en el que al menos una base de dichas al menos dos bases es una base de pirazolo[3,4-d]pirimidina no sustituida que tiene la fórmula:
**(Ver fórmula)**
y al menos una de dichas al menos dos bases es una base de pirazolo[3,4-d]pirimidina 325 sustituida que tiene la fórmula:
**(Ver fórmula)**
en las que:
cada uno de dichos grupos X1 y X2 es un miembro seleccionado independientemente del grupo que consiste en H, OH, NH2 y un grupo amino protegido; y
cada uno de dichos grupos R1 es un miembro seleccionado independientemente del grupo que consiste en heteroalquilo(C1-C12), heteroalquenilo(C2-C12), heteroalquinilo(C2-C12), -O(alquilo C1-C12), -O-(alquenilo C2-C12), -O-(alquinilo C2-C12), -S-(alquilo C1-C12), -S-(alquenilo C2C12), -S-(alquinilo C2-C12), heterociclil(alquilo C1-C12), heterociclil(alquenilo C2-C12), heterociclil(alquinilo C2-C12), aril(alquilo C1-C12), aril(alquenilo C2-C12), aril(alquinilo C2-C12), arilo, heterociclilo, halógeno, -CN, -CONH2 y sus formas protegidas.
12. Un oligonucleótido modificado de la reivindicación 1, que tiene la fórmula:
**(Ver fórmula)**
10 R2 representa un primer extremo de dicho oligonucleótido modificado;
R3 representa un segundo extremo de dicho oligonucleótido modificado;
el subíndice n es un número entero de 4 a 70;
cada B es un miembro seleccionado independientemente del grupo que consiste en
adenina, timina, citosina, guanina, uracilo, una pirazolo[3,4-d]pirimidina, y una pirazolo[3,415 d]pirimidina 3-sustituida; en el que al menos un B es una pirazolo[3,4-d]pirimidina no sustituida y al menos un B es una pirazolo[3,4-d]pirimidina 3-sustituida; y cada M es un miembro seleccionado del grupo que consiste en un azúcar formador de oligómero y un aminoácido formador de ácidos nucleicos peptídicos. 13. Un oligonucleótido modificado de la reivindicación 12, en el que al menos un M es 20 un azúcar formador de oligómero no natural. 14. Un compuesto que tiene la fórmula:
**(Ver fórmula)**
en la que: Z1 es un miembro seleccionado del grupo que consiste en H, F y ORa, en el que Ra es un miembro seleccionado del grupo que consiste en H, alquilo(C1-C8) y un grupo protector de 25 hidroxi;
Z2
es un miembro seleccionado del grupo que consiste en H y alquilo(C1-C8), u opcionalmente Z2 se combina con Z1 para formar un anillo de cinco o siete miembros;
Y1 es O-P1, en el que P1 es una fosforamidita o un grupo H-fosfonato; Y2
es un miembro seleccionado del grupo que consiste en OH y un grupo hidroxi protegido; y B es un nucleótido modificado seleccionado del grupo que consiste en:
**(Ver fórmula)**
5 en las que X11 y X12 se seleccionan cada uno independientemente del grupo que consiste en H, NH2 y un grupo amino protegido; y cada R12 se selecciona independientemente del grupo que consiste en las formas protegidas o desprotegidas de 3-hidroxiprop-1-inilo, 3-aminoprop-1-inilo, 3-aminoprop-1-inilo, 3metoxiprop-1-inilo, 4-hidroxi-1-butinilo, 3-(hidroximetil)-4-hidroxi-1-butinilo, heterociclil(alquilo C1C12), heterociclil(alquenilo C2-C12), heterociclil(alquinilo C2-C12), y heterociclilo, con la condición de que R12 sea distinto de 2-piridiletinilo.
15. Un compuesto que tiene la fórmula:
**(Ver fórmula)**
en la que:
15 Z1 es un miembro seleccionado del grupo que consiste en H, F y ORa, en el que Ra es un miembro seleccionado del grupo que consiste en H, alquilo(C1-C8) y un grupo protector de hidroxi;
Z2
es un miembro seleccionado del grupo que consiste en H y alquilo(C1-C8), u opcionalmente Z2 se combina con Z1 para formar un anillo de cinco o siete miembros; Y1
20 es un miembro seleccionado del grupo que consiste en OH y un grupo hidroxi protegido; Y2 es O-P2, en el que P2 es una fosforamidita, H-fosfonato, monofosfato, difosfato o trifosfato; y B es un nucleótido modificado seleccionado del grupo que consiste en:
**(Ver fórmula)**
en las que X11 y X12 se seleccionan cada uno independientemente del grupo que consiste en H, NH2 y un grupo amino protegido; y
cada R12 se selecciona independientemente del grupo que consiste en las formas protegidas o desprotegidas de 3-hidroxiprop-1-inilo, 3-aminoprop-1-inilo, 3-aminoprop-1-inilo, 3metoxiprop-1-inilo, 4-hidroxi-1-butinilo, 3-(hidroximetil)-4-hidroxi-1-butinilo, heterociclil(alquilo C1C12), heterociclil(alquenilo C2-C12), heterociclil(alquinilo C2-C12), y heterociclilo, con la condición de que R12 sea distinto de 2-piridiletinilo.
16. Un compuesto de la reivindicación 14 ó 15, en el que B es
**(Ver fórmula)**
17. Un compuesto de la reivindicación 14 ó 15, en el que B es
**(Ver fórmula)**
18. Un compuesto de la reivindicación 16, en el que X11 y X12 son cada uno NH2.
19. Un compuesto de la reivindicación 18, en el que Y1 es O-P1, Y2 es un hidroxi protegido, Z1 es H, R12 se selecciona del grupo que consiste en 3-hidroxiprop-1-inilo, 3aminoprop-1-inilo, 4-hidroxi-1-butinilo y 3-(hidroximetil)-4-hidroxi-1-butinilo.
15 20. Un compuesto de la reivindicación 19, en el que Y1 es -O-[(2-cianoetil)-N,N
diisopropilfosforamidita] e Y2 es -O-(4,4'-dimetoxitritilo). 21. Un compuesto de la reivindicación 16, en el que X11 es NH2, y X12 es H. 22. Un compuesto de la reivindicación 21, en el que Y1 es O-P1, Y2 es un hidroxi
protegido, Z1 es H, R12 se selecciona del grupo que consiste en 3-hidroxiprop-1-inilo, 320 aminoprop-1-inilo, 4-hidroxi-1-butinilo y 3-(hidroximetil)-4-hidroxi-1-butinilo.
23. Un compuesto de la reivindicación 22, en el que Y1 es -O-[(2-cianoetil)-N,Ndiisopropilfosforamidita] e Y2 es -O-(4,4'-dimetoxitritilo).
24. Un compuesto de la reivindicación 17, en el que X12 es H o NH2.
25. Un compuesto de la reivindicación 24, en el que Y1 es O-P1, Y2 es un hidroxi protegido, Z1 es H, R12 se selecciona del grupo que consiste en 3-hidroxiprop-1-inilo, 3aminoprop-1-inilo, 4-hidroxi-1-butinilo y 3-(hidroximetil)-4-hidroxi-1-butinilo.
26. Un compuesto de la reivindicación 25, en el que Y1 es -O-[(2-cianoetil)-N,Ndiisopropilfosforamidita] e Y2 es -O-(4,4'-dimetoxitritilo).
27. Una matriz de oligonucleótidos modificados, comprendiendo dicha matriz un soporte sólido y una pluralidad de oligonucleótidos unidos, en la que al menos 50% de los oligonucleótidos en dicha matriz contienen una pirazolo[3,4-d]pirimidina no sustituida y una pirazolo[3,4-d]pirimidina 3-sustituida.
28. Una matriz de oligonucleótidos modificados de la reivindicación 27, en la que dichos oligonucleótidos unidos tienen unas Tm dentro de un intervalo de aproximadamente 2 ºC entre sí, y unas longitudes de pares de bases dentro de un intervalo de aproximadamente 2 bases entre sí.
29. Una matriz de oligonucleótidos modificados de la reivindicación 27, en la que dichos oligonucleótidos unidos tienen unas Tm dentro un intervalo de de aproximadamente 1 ºC entre sí, y unas longitudes de pares de bases dentro de un intervalo de aproximadamente 2 bases entre sí.
30. Una matriz de oligonucleótidos modificados de la reivindicación 27, en la que dicha matriz comprende de aproximadamente 10 a aproximadamente 10.000 oligonucleótidos unidos, teniendo cada uno unas Tm dentro de un intervalo de aproximadamente 2 ºC entre sí, y unas longitudes de pares de bases dentro de un intervalo de aproximadamente 2 bases entre sí.
31. Una matriz de oligonucleótidos modificados de la reivindicación 27, en la que dicha matriz comprende de aproximadamente 10 a aproximadamente 10.000 oligonucleótidos unidos, teniendo una porción de dichos oligonucleótidos unidos un ligante del surco menor unido de modo covalente.
32. Una composición que comprende una pluralidad de oligonucleótidos modificados que tienen al menos una pirazolo[3,4-d]pirimidina no sustituida y al menos una pirazolo[3,4d]pirimidina 3-sustituida, y que tienen además un fluoróforo unido.
33. Una composición de la reivindicación 32, en la que cada uno de dicha pluralidad de oligonucleótidos comprende un fluoróforo unido y un extintor unido.
34. Una composición de la reivindicación 33, en la que cada uno de dichos oligonucleótidos modificados tiene una longitud de 4 a 30 bases, y tiene unas Tm que están dentro de un intervalo de aproximadamente 2 ºC entre sí.
35. Una composición de la reivindicación 34, en la que dicha pluralidad es de aproximadamente 6 a aproximadamente 100.
36. Un procedimiento para distinguir polinucleótidos con secuencias relacionadas, comprendiendo dicho procedimiento:
(a) poner en contacto un oligonucleótido modificado que tiene una secuencia definida que comprende al menos una pirazolo[3,4-d]pirimidina 3-sustituida y al menos una pirazolo[3,4d]pirimidina no sustituida en lugar de una base de purina, con al menos dos polinucleótidos, en el que uno de los polinucleótidos tiene una secuencia diana que es perfectamente complementaria con el oligonucleótido modificado y al menos uno de los otros polinucleótidos tiene una secuencia diana con al menos una base desapareada; y
(b) determinar el grado de hibridación entre el oligonucleótido modificado y cada uno de los polinucleótidos. 37. Un procedimiento según la reivindicación 36, en el que dicho oligonucleótido modificado comprende además un grupo indicador. 38. Un procedimiento según la reivindicación 37, en el que dicho grupo indicador es un fluoróforo. 39. Un procedimiento según la reivindicación 36, en el que dicho oligonucleótido modificado comprende además un ligante del surco menor. 40. Un procedimiento según la reivindicación 36, en el que dicho oligonucleótido modificado comprende además un ligante del surco menor y un fluoróforo. 41. Un procedimiento según la reivindicación 36, en el que dicho oligonucleótido modificado comprende además un ligante del surco menor, un fluoróforo y un extintor.
42. Un procedimiento para detectar la presencia de una secuencia diana en un polinucleótido, comprendiendo dicho procedimiento:
(a) incubar un polinucleótido que se va a ensayar para la presencia de la secuencia diana con un oligonucleótido modificado que tiene una secuencia que es sustancialmente complementaria con la secuencia diana bajo condiciones de hibridación; e
(b) identificar los ácidos nucleicos hibridados; en el que dicho oligonucleótido modificado comprende al menos una pirazolo[3,4-d]pirimidina 3sustituida y al menos pirazolo[3,4-d]pirimidina no sustituida en lugar de un resto purina.
43. Un procedimiento según la reivindicación 42, en el que dicha incubación se realiza
en presencia de una enzima cleavasa.
44. Un procedimiento según la reivindicación 42, en el que dicho oligonucleótido modificado comprende además un grupo indicador.
45. Un procedimiento según la reivindicación 44, en el que dicho grupo indicador es un fluoróforo.
46. Un procedimiento según la reivindicación 45, en el que dicho oligonucleótido modificado comprende además un extintor unido.
47. Un procedimiento según la reivindicación 42, en el que dicho oligonucleótido modificado comprende además un ligante del surco menor unido.
48. Un procedimiento para la extensión de cebadores, comprendiendo dicho procedimiento incubar un polinucleótido que contiene una secuencia diana con uno o más cebadores oligonucleotídicos complementarios con la secuencia diana, en presencia de una enzima polimerizante y sustratos de nucleótidos bajo condiciones favorables para la polimerización, en el que al menos uno de los cebadores oligonucleotídicos contiene una pirazolo[3,4-d]pirimidina no sustituida y una pirazolo[3,4-d]pirimidina 3-sustituida en lugar de una base de purina.
49. Un procedimiento según la reivindicación 48, en el que uno de dichos cebadores oligonucleotídicos se extiende con una sola base.
50. Un procedimiento según la reivindicación 48, en el que al menos uno de dichos cebadores oligonucleotídicos comprende además un ligante del surco menor unido.
51. Un procedimiento según la reivindicación 48, en el que dicha incubación es parte de una reacción de amplificación.
52. Un procedimiento según la reivindicación 51, en el que dicha reacción de amplificación es una reacción en cadena de polimerasa.
53. Un procedimiento según la reivindicación 48, en el que dicho oligonucleótido modificado comprende además un ligante del surco menor unido de modo covalente.
54. Un procedimiento para determinar la secuencia de nucleótidos de un polinucleótido, comprendiendo dicho procedimiento:
(a) incubar el polinucleótido con una matriz de oligonucleótidos modificados bajo condiciones de hibridación; y
(b) determinar cuáles son los oligonucleótidos modificados en la matriz con los que se hibrida el polinucleótido; en el que una pluralidad de los oligonucleótidos modificados comprende al menos una pirazolo[3,4-d]pirimidina 3-sustituida y al menos una pirazolo[3,4-d]pirimidina no sustituida en lugar de una base de purina.
55. Un procedimiento según la reivindicación 54, en el que dicha matriz comprende de 10 a 100.000 oligonucleótidos modificados diferentes.
56. Un procedimiento según la reivindicación 54, en el que dicha matriz comprende de 10 a 1000 oligonucleótidos modificados diferentes.
57. Un procedimiento para determinar la secuencia de nucleótidos de una secuencia diana en un polinucleótido, comprendiendo dicho procedimiento:
(a) poner en contacto un polinucleótido que comprende la secuencia diana con al menos dos oligonucleótidos de secuencia conocida, en el que dos o más restos purina de los oligonucleótidos están reemplazados por al menos una pirazolo[3,4-d]pirimidina 3-sustituida y al menos una pirazolo[3,4-d]pirimidina no sustituida, y en el que uno de dichos al menos dos oligonucleótidos tiene una secuencia que es perfectamente complementaria con la secuencia diana y al menos otro de los oligonucleótido tiene una secuencia diana relacionada, e incubar cada uno de los oligonucleótidos con el polinucleótido bajo condiciones de hibridación; y
(b) determinar el grado de hibridación entre cada uno de los oligonucleótidos y el polinucleótido. 58. Un procedimiento según la reivindicación 57, en el que al menos uno de dichos oligonucleótidos modificados comprende además un grupo indicador. 59. Un procedimiento según la reivindicación 57, en el que al menos uno de dichos oligonucleótidos modificados comprende además un ligante del surco menor.
60. Un procedimiento según la reivindicación 57, en el que al menos uno de dichos oligonucleótidos modificados comprende además un ligante del surco menor y un grupo indicador.
61. Un procedimiento para estudiar la expresión génica en una célula, comprendiendo dicho procedimiento:
(a) incubar una población de polinucleótidos representativa de los genes expresados en la célula con una matriz de oligonucleótidos que comprende una pluralidad de oligonucleótidos modificados de diferentes secuencias bajo condiciones de hibridación; y
(b) determinar cuáles son los oligonucleótidos modificados en la matriz que se hibridan con los polinucleótidos; en el que dichos oligonucleótidos modificados comprenden al menos una pirazolo[3,4-d]pirimidina 3-sustituida y al menos una pirazolo[3,4-d]pirimidina no sustituida en lugar de una purina.
62. Un procedimiento para identificar una mutación en una secuencia diana de un gen de interés, comprendiendo dicho procedimiento:
(a) incubar un polinucleótido que comprende la secuencia diana con una matriz de oligonucleótidos de diferentes secuencias, en el que las diferentes secuencias incluyen la
secuencia diana de tipo salvaje y diferentes secuencias diana mutantes, bajo condiciones de hibridación; y
(b) determinar cuáles son los oligonucleótidos en la matriz que se hibridan con el polinucleótido;
5 en el que dos o más restos purina en cada uno de los oligonucleótidos están reemplazados por al menos una pirazolo[3,4-d]pirimidina 3-sustituida y al menos una pirazolo[3,4-d]pirimidina no sustituida.
63. Un compuesto de la reivindicación 14, en el que Y1 es un grupo fosforamidita. 64. Un compuesto de la reivindicación 63, en el que Y2 es un grupo hidroxi protegido. 10 65. Un compuesto de la reivindicación 64, en el que el grupo hidroxi protegido es un grupo 4,4'-dimetoxitritiloxi. 66. Un compuesto de la reivindicación 63, en el que el grupo fosforamidita es -O-(2cianoetil)-N,N-diisopropilfosforamidita. 67. Un compuesto de la reivindicación 65, en el que el grupo fosforamidita es -O-(215 cianoetil)-N,N-diisopropilfosforamidita. 68. Un compuesto de la reivindicación 63, en el que B es
**(Ver fórmula)**
69. Un compuesto de la reivindicación 68, en el que X11 y X12 son grupos amino protegidos. 70. Un compuesto de la reivindicación 69, en el que Y1 es -O-(2-cianoetil)-N,N20 diisopropilfosforamidita, e Y2 es un grupo 4,4'-dimetoxitritiloxi. 71. Un compuesto de la reivindicación 69, en el que uno o ambos de los grupos amino protegidos comprenden un grupo protector de análogo de benzoílo. 72. Un compuesto de la reivindicación 63, en el que B es
**(Ver fórmula)**
73. Un compuesto de la reivindicación 72, en el que X12 es un grupo amino protegido. 74. Un compuesto de la reivindicación 73, en el que X12 es -N=CH-N(CH3)2.
75. Un compuesto de la reivindicación 74, en el que Y1 es -O-(2-cianoetil)-N,Ndiisopropilfosforamidita, e Y2 es un grupo 4,4'-dimetoxitritiloxi.
76. Un compuesto de la reivindicación 63, en el que B es
**(Ver fórmula)**
y X11 y X12 son grupos amino protegidos. 5 77. Un compuesto de la reivindicación 76, en el que Y2 es un grupo hidroxi protegido. 78. Un compuesto de la reivindicación 77, en el que el grupo fosforamidita es -O-(2
cianoetil)-N,N-diisopropilfosforamidita. 79. Un compuesto de la reivindicación 78, en el que Y2 es un grupo 4,4'-dimetoxitritiloxi. 80. Un compuesto de la reivindicación 77, en el que uno o ambos de los grupos amino
10 protegidos comprenden un grupo protector de análogo de benzoílo. 81. Un compuesto de la reivindicación 63, en el que Z1 y Z2 se combinan para formar un
anillo de cinco a siete miembros. 82. Un compuesto de la reivindicación 15, en el que Y2 es un grupo fosforamidita. 83. Un compuesto de la reivindicación 82, en el que Y1 es un grupo hidroxi protegido.
15 84. Un compuesto de la reivindicación 83, en el que el grupo hidroxi protegido es un grupo 4,4'-dimetoxitritiloxi. 85. Un compuesto de la reivindicación 82, en el que el grupo fosforamidita es -O-(2cianoetil)-N,N-diisopropilfosforamidita. 86. Un compuesto de la reivindicación 84, en el que el grupo fosforamidita es -O-(220 cianoetil)-N,N-diisopropilfosforamidita. 87. Un compuesto de la reivindicación 82, en el que B es
**(Ver fórmula)**
88. Un compuesto de la reivindicación 87, en el que X11 y X12 son grupos amino protegidos. 89. Un compuesto de la reivindicación 88, en el que Y2 es -O-(2-cianoetil)-N,N25 diisopropilfosforamidita, e Y1 es un grupo 4,4'-dimetoxitritiloxi.
90. Un compuesto de la reivindicación 88, en el que uno o ambos de los grupos amino protegidos comprenden un grupo protector de análogo de benzoílo.
91. Un compuesto de la reivindicación 82, en el que B es
**(Ver fórmula)**
92. Un compuesto de la reivindicación 91, en el que X12 es un grupo amino protegido. 93. Un compuesto de la reivindicación 92, en el que X12 es -N=CH-N(CH3)2. 94. Un compuesto de la reivindicación 93, en el que Y2 es -O-(2-cianoetil)-N,N
diisopropilfosforamidita, e Y1 es un grupo 4,4'-dimetoxitritiloxi. 95. Un compuesto de la reivindicación 82, en el que B es
**(Ver fórmula)**
y X11 y X12 son grupos amino protegidos. 10 96. Un compuesto de la reivindicación 95, en el que el otro de Y1 es un grupo hidroxi protegido. 97. Un compuesto de la reivindicación 96, en el que el grupo fosforamidita es -O-(2cianoetil)-N,N-diisopropilfosforamidita. 98. Un compuesto de la reivindicación 97, en el que Y1 es un grupo 4,4'-dimetoxitritiloxi. 15 99. Un compuesto de la reivindicación 96, en el que uno o ambos de los grupos amino protegidos comprenden un grupo protector de análogo de benzoílo. 100. Un compuesto de la reivindicación 82, en el que Z1 y Z2 se combinan para formar un anillo de cinco a siete miembros.
Patentes similares o relacionadas:
Proteínas de unión a interleuquina-13, del 15 de Julio de 2020, de AbbVie Bahamas Ltd: Un anticuerpo anti-IL-13 recombinante, o fragmento de unión a antígeno del mismo, en donde dicho anticuerpo anti-IL-13 recombinante, o fragmento de unión a antígeno del mismo, […]
Polinucleótidos aislados y métodos y plantas que usan los mismos para regular la acidez de las plantas, del 10 de Junio de 2020, de The State of Israel, Ministry of Agriculture and Rural Development, Agricultural Research Organization, (A.R.O.), Volcani Cent: Una célula de planta o una planta que comprende una construcción de ácido nucleico que comprende una secuencia de ácido nucleico que codifica un polipéptido […]
Métodos y composiciones para modular PD1, del 13 de Mayo de 2020, de Sangamo Therapeutics, Inc: Célula aislada que comprende una inserción o una deleción en un gen de PD1 endógeno dentro de, o entre, las secuencias mostradas en SEQ ID NO: 56 y SEQ ID NO: 60 del gen de PD1 […]
Métodos de preparación de polinucleótidos usando composiciones de sales de catiónicas multivalentes, del 6 de Mayo de 2020, de GERON CORPORATION: Un método para preparar un polinucleótido, comprendiendo el método: a) poner en contacto una primera composición polinucleotídica con una sal catiónica […]
Compuesto de tioéter para la protección del grupo 2''-hidroxi en nucleósidos que van a ser utilizados en la síntesis de oligonucleótidos, del 6 de Mayo de 2020, de Bonac Corporation: Un éter representado por la siguiente fórmula química : **(Ver fórmula)** en dicha fórmula química , R4 es un grupo alquilo de cadena lineal o ramificada […]
Nucleótidos modificados para secuenciación de polinucleótidos, del 8 de Abril de 2020, de ILLUMINA CAMBRIDGE LIMITED: Una molécula de nucleótido que tiene una unidad estructural de azúcar ribosa o desoxirribosa y una base enlazada a un marcador detectable a través de […]
Análogos de oligonucleótidos que incorporan 5-aza-citosina en los mismos, del 8 de Enero de 2020, de Astex Pharmaceuticals, Inc: Un análogo de oligonucleótido aislado o sintético, o una sal o éster del mismo, de fórmula general 5'-DpG-3' o 5'-GpD-3', en los que D es decitabina; p es un […]
Nucleótidos modificados, del 1 de Enero de 2020, de ILLUMINA CAMBRIDGE LIMITED: Un kit que comprende cuatro moléculas de nucleótido trifosfato modificadas, cada una de las cuales comprende una base de purina o pirimidina y una unidad estructural […]