COMPOSICION ESTABLE PARA LA ADMINISTRACION ORAL DE UNA DOSIS DE LIBERACION PROLONGADA, QUE CONTIENE PSEUDOEFEDRINA Y DESLORATADINA.
Una composición sólida de dosificación oral de liberación prolongada,
recubierta con película que comprende (a) un núcleo que comprende una cantidad efectiva de pseudoefedrina o de una sal farmacéuticamente aceptable de la misma, (b) un recubrimiento de película que recubre uniformemente el núcleo, y (c) un segundo recubrimiento de película que recubre uniformemente el primer recubrimiento y que comprende una cantidad efectiva de desloratadina, y en donde la cantidad de pseudoefedrina o de una sal farmacéuticamente aceptable de la misma es eficaz para producir una media geométrica de concentración máxima en plasma de pseudoefedrina de 345 ng/ml hasta 365 ng/ml en un periodo de 7,60 horas hasta 8,40 horas, y la cantidad de desloratadina es eficaz para producir una media geométrica de concentración máxima en plasma de desloratadina de 2,10 ng/ml hasta 2,45 ng/ml en un periodo de 4,0 horas hasta 4,5 horas, después de la administración de una única dosis de dicha composición
Tipo: Patente Europea. Resumen de patente/invención. Número de Solicitud: E00311445.
Solicitante: SCHERING CORPORATION.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 2000 GALLOPING HILL ROAD,KENILWORTH, NEW JERSEY 0703.
Inventor/es: KOU, JIM, H.
Fecha de Publicación: .
Fecha Solicitud PCT: 20 de Diciembre de 2000.
Fecha Concesión Europea: 7 de Abril de 2010.
Clasificación Internacional de Patentes:
- A61K31/445 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › Piperidinas no condensadas, p. ej. piperocaína.
- A61K9/20K4B
Clasificación PCT:
- A61K31/445 A61K 31/00 […] › Piperidinas no condensadas, p. ej. piperocaína.
- A61K9/20 A61K […] › A61K 9/00 Preparaciones medicinales caracterizadas por un aspecto particular. › Píldoras, pastillas o comprimidos.
Clasificación antigua:
- A61K31/445 A61K 31/00 […] › Piperidinas no condensadas, p. ej. piperocaína.
- A61K9/20 A61K 9/00 […] › Píldoras, pastillas o comprimidos.
Países PCT: Austria, Bélgica, Suiza, Alemania, Dinamarca, España, Francia, Reino Unido, Grecia, Italia, Liechtensein, Luxemburgo, Países Bajos, Suecia, Mónaco, Portugal, Irlanda, Eslovenia, Finlandia, Rumania, Chipre, Lituania, Letonia, Ex República Yugoslava de Macedonia, Albania.
Fragmento de la descripción:
Composición estable para la administración oral de una dosis de liberación prolongada, que contiene pseudoefedrina y desloratadina.
La invención se refiere a una composición sólida para la dosificación oral, de liberación prolongada, que contiene un descongestivo nasal, por ejemplo, pseudoefedrina en un núcleo de liberación controlada, y un recubrimiento de película exterior que contiene el antihistamínico no sedante, desloratadina. Las composiciones sólidas de dosificación oral de esta invención son útiles para tratar a pacientes que presentan los signos y síntomas asociados con trastornos alérgicos y/o inflamatorios tales como catarro común, así como signos y síntomas asociados con trastornos alérgicos y/o inflamatorios de la piel o de las vías respiratorias superiores tales como rinitis alérgica, rinitis estacional y congestión nasal, enfermedades de las vías respiratorias superiores, rinitis alérgica y congestión nasal.
Desloratadina, llamada también descarbetoxiloratadina, se describe en la Patente de EE.UU. Nº 4.659.716 como un antihistamínico no sedante de utilidad como agente antialérgico. La Patente de EE.UU. Nº 6.100.274 describe composiciones que contienen desloratadina. La Patente de EE.UU. Nº 5.595.997 describe métodos y composiciones para tratar los síntomas de la rinitis alérgica estacional usando desloratadina. Desloratadina, tras su absorción oral, sufre una hidroxilación en posición 3 para producir el metabolito, 3-hidroxildesloratadina.
Las Patentes de EE. UU. Nº 4.990.535 y 5.100.675 describen un comprimido de liberación sostenida, que se toma dos veces al día, en el que el recubrimiento del comprimido comprende descarbetoxiloratadina y un polímero hidrófilo y polietilenglicol, y el núcleo del comprimido comprende acetaminofen, pseudoefedrina o una sal de los mismos, un polímero hidrófilo hinchable y excipientes farmacéuticamente aceptables.
La Patente de EE.UU. Nº 5.314.697 describe un comprimido de liberación prolongada que contiene un núcleo de matriz que comprende sulfato de pseudoefedrina y un recubrimiento que comprende loratadina.
Ningún documento de la técnica anterior describe la composición sólida de dosificación oral, recubierta con película, que se administra una vez al día, de esta invención.
Sería deseable el desarrollo eficaz de una formulación de un producto de desloratadina-pseudoefedrina, de administración una vez al día, pero requeriría conseguir un perfil de velocidad de liberación para el componente pseudoefedrina durante un período prolongado de tiempo, superior a doce horas y, preferentemente, de al menos 16 horas, manteniendo simultáneamente el suministro de una eficaz dosis de desloratadina una vez al día.
Para estimular la adherencia del paciente, sería deseable disponer de un producto de liberación prolongada de desloratadina-pseudoefedrina, efectivo y seguro en su administración una vez al día para el tratamiento, terapia y/o alivio de los signos y síntomas asociados con el catarro común, así como de trastornos alérgicos y/o inflamatorios de la piel o de las vías respiratorias superiores e inferiores tales como la rinitis alérgica estacional y la congestión nasal.
Resumen de la invención
Los presentes inventores han descubierto un producto de desloratadina-pseudoefedrina, que se administra una vez al día, que produce un perfil de velocidad de liberación para la pseudoefedrina durante un periodo prolongado, superior a doce horas y, preferentemente, de al menos 16 horas, mientras mantiene el suministro de una dosis efectiva, una vez al día, de desloratadina.
Por lo tanto, la presente invención ofrece una composición sólida de dosificación oral, recubierta con película, de liberación prolongada, que comprende (a) un núcleo que comprende una cantidad efectiva de pseudoefedrina o una sal farmacéuticamente aceptable de la misma, (b) un recubrimiento de película que recubre uniformemente el núcleo, y (c) un segundo recubrimiento de película, que recubre uniformemente la primera película, y que comprende una cantidad efectiva de desloratadina, en donde la cantidad de pseudoefedrina o de una sal farmacéuticamente aceptable de la misma es eficaz para producir una media geométrica de concentración máxima en plasma de pseudoefedrina de aproximadamente 345 ng/ml hasta aproximadamente 365 ng/ml, en un periodo de aproximadamente 7,60 horas hasta aproximadamente 8,40 horas, y la cantidad de desloratadina es eficaz para producir una media geométrica de concentración máxima en plasma de desloratadina de aproximadamente 2,10 ng/ml hasta aproximadamente 2,45 ng/ml, en un periodo de aproximadamente 4,0 horas hasta aproximadamente 4,5 horas después de la administración de una única dosis de dicha composición.
Formas de realización preferidas de la composición sólida de dosificación oral, de liberación prolongada y recubierta con película de la presente invención producen también una media geométrica de concentración máxima en plasma de 3-hidroxidesloratadina de aproximadamente 0,75 ng/ml hasta aproximadamente 1,15 ng/ml en un periodo de aproximadamente 5,50 horas hasta aproximadamente 6,25 horas después de la administración de una única dosis de dicha composición.
Formas de realización más preferidas de la composición sólida de dosificación oral, de liberación prolongada y recubierta con película de la presente invención también producen una media geométrica de concentración máxima en plasma de desloratadina de aproximadamente 2,10 ng/ml hasta aproximadamente 2,45 ng/ml en un periodo de aproximadamente 4,0 horas hasta aproximadamente 4,5 horas, y una media geométrica de concentración máxima en plasma de 3-hidroxidesloratadina de aproximadamente 0,75 ng/ml hasta aproximadamente 1,15 ng/ml en un periodo de aproximadamente 5,50 horas hasta aproximadamente 6,25 horas después de la administración de una única dosis de dicha composición.
Por lo tanto, en una forma de realización preferida, esta invención ofrece una composición farmacéutica que comprende una cantidad terapéuticamente efectiva de sulfato de pseudoefedrina en un núcleo, y una cantidad efectiva de desloratadina en un recubrimiento de película, que conserva los parámetros farmacocinéticos deseables de desloratadina, 3-hidrodesloratadina y pseudoefedrina enumerados anteriormente, y que contiene menos que aproximadamente 2% de productos de descomposición de la desloratadina, tales como N-formil-desloratadina, preferentemente menos que aproximadamente 1,4% hasta aproximadamente 1,6% de los productos de descomposición de la desloratadina tales como N-formil-desloratadina, de manera inicial, así como cuando estas composiciones se almacenan a 25ºC y aproximadamente 60% de humedad relativa durante periodos de al menos aproximadamente 24 meses.
Los presentes inventores han descubierto que depositando un primer recubrimiento entre el recubrimiento de película que comprende desloratadina y el núcleo que comprende un descongestivo nasal, por ejemplo, una sal de pseudoefedrina, preferentemente sulfato de pseudoefedrina, se logra la liberación de desloratadina desde el segundo recubrimiento de película, y una liberación prolongada del descongestivo nasal sulfato de pseudoefedrina desde el núcleo, preferentemente un núcleo de matriz, durante un periodo superior a doce horas, mientras se conservan los parámetros farmacocinéticos deseados de desloratadina, 3-hidroxidesloratadina y pseudoefedrina enumerados más arriba en este documento, y produciendo menos de 2% de degradación de desloratadina a N-formil-desloratadina.
De esta forma, en una forma de realización preferida, la presente invención proporciona una composición sólida de dosificación oral, de liberación prolongada y recubierta con película, que comprende:
(a) un núcleo de matriz que comprende:
(b) un primer recubrimiento de película que recubre uniformemente el núcleo de matriz, que comprende:
Reivindicaciones:
1. Una composición sólida de dosificación oral de liberación prolongada, recubierta con película que comprende (a) un núcleo que comprende una cantidad efectiva de pseudoefedrina o de una sal farmacéuticamente aceptable de la misma, (b) un recubrimiento de película que recubre uniformemente el núcleo, y (c) un segundo recubrimiento de película que recubre uniformemente el primer recubrimiento y que comprende una cantidad efectiva de desloratadina, y en donde la cantidad de pseudoefedrina o de una sal farmacéuticamente aceptable de la misma es eficaz para producir una media geométrica de concentración máxima en plasma de pseudoefedrina de 345 ng/ml hasta 365 ng/ml en un periodo de 7,60 horas hasta 8,40 horas, y la cantidad de desloratadina es eficaz para producir una media geométrica de concentración máxima en plasma de desloratadina de 2,10 ng/ml hasta 2,45 ng/ml en un periodo de 4,0 horas hasta 4,5 horas, después de la administración de una única dosis de dicha composición.
2. La composición sólida de dosificación oral de liberación prolongada, recubierta con película según la reivindicación 1, en la que la cantidad de desloratadina es eficaz para producir una media geométrica de concentración máxima en plasma de 3-hidroxidesloratadina de 0,75 ng/ml hasta 1,15 ng/ml en un periodo de 5,50 horas hasta 6,26 horas, después de la administración de una única dosis de dicha composición.
3. La composición sólida de dosificación oral de liberación prolongada, recubierta con película según la reivindicación 1, en la que el núcleo es un núcleo de matriz y en la que hay un primer recubrimiento que recubre uniformemente el núcleo de matriz, y un segundo recubrimiento de película que recubre uniformemente el primer recubrimiento, que comprende una cantidad efectiva de desloratadina.
4. La composición sólida de dosificación oral de liberación prolongada, recubierta con película según la reivindicación 3, en la que (a) el núcleo comprende:
y en la que (b) el primer recubrimiento de película que recubre uniformemente el núcleo de matriz comprende:
y en la que (c) el segundo recubrimiento de película que recubre uniformemente el primer recubrimiento comprende:
5. La composición sólida de dosificación oral de liberación prolongada, recubierta con película según la reivindicación 4, en la que la cantidad de desloratadina es eficaz para producir una media geométrica de concentración máxima en plasma de 3-hidroxidesloratadina de 0,75 ng/ml hasta 1,15 ng/ml en un periodo de 5,50 horas a 6,25 horas, después de la administración de una única dosis de dicha composición.
6. La composición sólida de dosificación oral de liberación prolongada, recubierta con película según la reivindicación 1, en la que la composición sólida de dosificación oral de liberación prolongada, recubierta con película contiene menos que aproximadamente 2% de N-formil-desloratadina.
7. La composición sólida de dosificación oral de liberación prolongada, recubierta con película según la reivindicación 3 ó 4 que comprende, adicionalmente, un tercer recubrimiento de película que recubre uniformemente el segundo recubrimiento de película, en donde dicho tercer recubrimiento comprende:
8. La composición sólida de dosificación oral de liberación prolongada, recubierta con película según la reivindicación 7, en la que el modificador de película soluble en agua es una hidroxipropil metilcelulosa, hidroxietil metilcelulosa o carboximetilcelulosa sódica de baja viscosidad, o un polietilenglicol seleccionado de polietilenglicol 200 hasta polietilenglicol 8000, o mezclas de los mismos.
9. La composición sólida de dosificación oral de liberación prolongada, recubierta con película según la reivindicación 4, en la que la sal de calcio, magnesio o aluminio insoluble en agua en el núcleo de matriz es un carbonato, fosfato, silicato o sulfato de calcio, magnesio o aluminio, o mezclas de los mismos.
10. La composición sólida de dosificación oral de liberación prolongada, recubierta con película según la reivindicación 1, en la que el núcleo de matriz comprende:
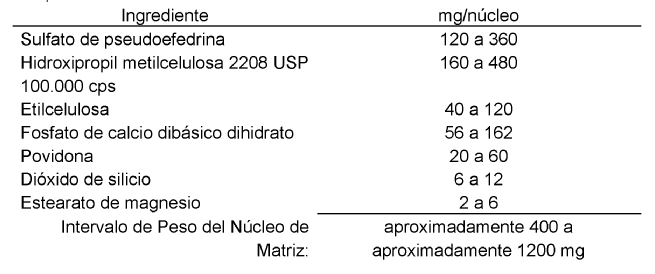
11. La composición sólida de dosificación oral de liberación prolongada, recubierta con película según la reivindicación 4, en la que el primer recubrimiento de película comprende:
12. La composición sólida de dosificación oral de liberación prolongada, recubierta con película según la reivindicación 4, en la que el segundo recubrimiento de película comprende:
13. La composición sólida de dosificación oral de liberación prolongada, recubierta con película según la reivindicación 2 que comprende, adicionalmente, un tercer recubrimiento de película que recubre uniformemente el segundo recubrimiento de película, y en la que el tercer recubrimiento de película comprende:
14. La composición sólida de dosificación oral de liberación prolongada, recubierta con película según la reivindicación 12, en la que la cantidad de desloratadina es efectiva para producir una media geométrica de concentración máxima en plasma de 3-hidroxidesloratadina de 0,75 ng/ml hasta 1,15 ng/ml en un periodo de 5,50 horas hasta 6,25 horas, después de la administración de una única dosis de dicha composición.
Patentes similares o relacionadas:
Compuestos y procedimientos de uso, del 29 de Julio de 2020, de Medivation Technologies LLC: Un compuesto de fórmula (Aa-1): **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, en la que: A representa H, halógeno, amino, […]
Triple combinación de antagonistas del receptor 5-HT6 puros, inhibidores de la acetilcolinesterasa y antagonista del receptor NMDA, del 15 de Julio de 2020, de SUVEN LIFE SCIENCES LIMITED: Una combinación que comprende un antagonista del receptor 5-HT6 puro, un inhibidor de la acetilcolinesterasa y un antagonista del receptor NMDA, en el que el antagonista […]
Combinación de agonistas inversos del receptor de histamina-3 con inhibidores de acetilcolinesterasa, del 24 de Junio de 2020, de SUVEN LIFE SCIENCES LIMITED: Una combinación que comprende un agonista inverso del receptor de histamina-3 y un inhibidor de acetilcolinesterasa; en donde el agonista inverso del receptor de histamina-3 […]
Compuestos inhibidores de la acetilcolinesterasa y agonistas de los receptores serotoninérgicos 5HT4, con efecto paramnesiante, sus procedimientos de preparación y composiciones farmacéuticas que los contienen, del 10 de Junio de 2020, de Université de Caen: Compuesto de fórmula general (I): **(Ver fórmula)** en la que: X representa un átomo de hidrógeno, o un átomo de halógeno […]
Nuevos derivados de piperazina y piperidina, síntesis y uso de los mismos en la inhibición de la oligomerización de VDAC, la apoptosis y la disfunción mitocondrial, del 3 de Junio de 2020, de The National Institute for Biotechnology in the Negev Ltd: Compuesto de Fórmula general (Id): **(Ver fórmula)** en la que L2 es un grupo de enlace seleccionado del grupo que consiste en un alquilamidileno […]
Compuestos de benzaldehído sustituidos y métodos para su uso en el aumento de la oxigenación tisular, del 27 de Mayo de 2020, de Global Blood Therapeutics, Inc: Un compuesto de Fórmula (I): **(Ver fórmula)** o un tautómero o una sal farmacéuticamente aceptable del mismo, para su uso en el tratamiento […]
Composición farmacéutica en comprimido que comprende bilastina, del 27 de Mayo de 2020, de Alfred E. Tiefenbacher (GmbH & Co. KG): Una composición farmacéutica en forma de comprimido, que comprende a) una forma cristalina de bilastina, en donde la forma cristalina tiene picos característicos a 6,53, […]
Nuevas composiciones para prevenir y/o tratar trastornos degenerativos del sistema nervioso central, del 27 de Mayo de 2020, de AMICUS THERAPEUTICS, INC: Un compuesto de Fórmula III: **(Ver fórmula)** en donde: R1 es C(R2)(R3)(R4); R2 es hidrógeno, -OH o halógeno; R3 es hidrógeno, -OH, halógeno o -CH3; […]