Preparación de nucleósidos de ribofuranosilpirimidinas.
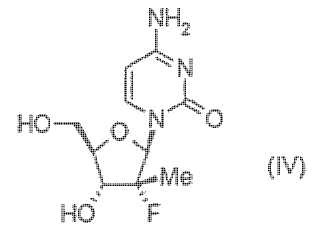
Un procedimiento de preparación de 4-amino-1-((2R,3R,4R,5R)-3-fluoro-4-hidroxi-5-hidroximetil-3-metil-tetrahidrofuran-2-il)-1H-pirimidin-2-ona de fórmula **Fórmula**
que comprende
a) trasformar un (2R,
3R,4R)-2-(aril)alcanoiloximetil-4-fluoro-4-metil-5-oxo-tetrahidro-furan-3-il éster del ácido(aril)alcanoico de fórmula II **Fórmula**
en la que R es arilo o alquilo
en un (2R,3R,4R)-2-(aril)alcanoiloxi metil-5-cloro-4-fluoro-4-metil-tetrahidro-furan-3-il éster del ácido(aril)alcanoico de fórmula III**Fórmula**
en la que R es arilo o alquilo.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2007/021548.
Solicitante: Gilead Pharmasset LLC.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: c/o Gilead Sciences, Inc., 333 Lakeside Drive Foster City, CA 94404 ESTADOS UNIDOS DE AMERICA.
Inventor/es: SARMA, KESHAB, ZHU, JIANG, JIN, QINGWU, AXT, STEVEN, D., CHUN,Byoung-Kwon, VITALE,JUSTIN, ROSS,BRUCE, RACHAKONDA,SUGUNA.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C07H19/06 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07H AZUCARES; SUS DERIVADOS; NUCLEOSIDOS; NUCLEOTIDOS; ACIDOS NUCLEICOS (derivados de ácidos aldónicos o sacáricos C07C, C07D; ácidos aldónicos, ácidos sacáricos C07C 59/105, C07C 59/285; cianohidrinas C07C 255/16; glicales C07D; compuestos de constitución indeterminada C07G; polisacáridos, sus derivados C08B; ADN o ARN concerniente a la ingeniería genética, vectores, p. ej. plásmidos o su aislamiento, preparación o purificación C12N 15/00; industria del azúcar C13). › C07H 19/00 Compuestos que contienen un heterociclo que comparten un heteroátomo del ciclo con un radical sacárido; Nucleósidos; Mononucleótidos; Sus anhidro-derivados. › Radicales de pirimidina.
- C07H5/02 C07H […] › C07H 5/00 Compuestos que contienen radicales sacárido en los que heteroenlaces al oxígeno han sido reemplazados por el mismo número de heteroenlaces a halógeno, nitrógeno, azufre, selenio o teluro. › a halógeno.
PDF original: ES-2429290_T3.pdf
Fragmento de la descripción:
Preparación de nucleósidos de ribofuranosilpirimidinas La presente solicitud fue presentada el 5 de octubre de 2007, como una solicitud de Patente Internacional PCT a nombre de PHARMASSET, INC., de Estados Unidos y de F. HOFFMANN LA-ROCHE AG, de Suiza, solicitantes a 5 efectos de la designación para todos los países excepto los Estados Unidos, y Steven D. Axt, ciudadano estadounidense; Keshab Sarma, ciudadano estadounidense; Justin Vitale, ciudadano estadounidense; Jiang Zhu, ciudadano canadiense; Bruce Ross, ciudadano estadounidense; Suguna Rachakonda, ciudadano indio; Qingwu Jin, ciudadano chino; y Byoung-Kwon Chun, ciudadano coreano; como los solicitantes a fines de la designación únicamente de los Estados Unidos, y reivindica la prioridad de la solicitud de patente provisional estadounidense con Nº de Serie 60/850.962, presentada el 10 de octubre de 2006.
La presente invención se refiere a un procedimiento mejorado para la preparación de la 4-amino-1- ( (2R, 3R, 4R, 5R) 3-fluoro-4-hidroxi-5-hidroximetil-3-metil-tetrahidrofuran-2-il) -1H-pirimidin-2-ona de la fórmula que es un potente inhibidor de la polimerasa NS5B del virus de la hepatitis C (VHC) .
La publicación PCT WO 2006/012440 da a conocer un procedimiento de acuerdo con el siguiente esquema. El procedimiento requiere la laboriosa separación de los anómeros XIII y XIV.
Un objeto de la presente invención es proporcionar un procedimiento me 4-amino-1- ( (2R, 3R, 4R, 5R) -3-fluoro-4-hidroxi-5-hidroximetil-3-metil-tetrahidro-furan-2-il) -1H-pirimidin-2-ona de la 20 fórmula que evite los inconvenientes conocidos en la técnica. El procedimiento de la presente invención comprende a) trasformar un éster (2R, 3R, 4R) -2- (aril) alcanoiloximetil-4-fluoro-4-metl-5-oxo-tetrahidrofuran-3-il del ácido (aril) alcanoico de fórmula II
en la que R es arilo o alquilo En un (2R, 3R, 4R) -2- (aril) alcanoiloximetil-5-cloro-4-fluoro-4-metil-tetrahidro-furan-3-il éster del ácido (aril) alcanoico de fórmula III
en la que R es arilo o alquilo;
b) convertir el (2R, 3R, 4R) -2- (aril) alcanoiloximetil-5-cloro-4-fluoro-4-metil-tetrahidrofuran-3-il éster del ácido (aril) alcanoico de fórmula III en un (2R, 3R, 4R, 5R) -3- (aril) alcanoiloxi-5- (4-benzoilamino-2-oxo-2H-pirimidin-1il) -4-fluoro-4-metil-tetrahidro-furan-2-ilmetil éster del ácido (aril) alcanoico de fórmula I
en la que R es arilo o alquilo y Bz es benzoilo y c) hidrolizar el (2R, 3R, 4R, 5R) -3- (aril) alcanoiloxi-5- (4-benzoilamino-2-oxo-2H-pirimidin-1-il) -4-fluro-4-metil
tetrahidro-furan-2-ilmetil éster del ácido (aril) alcanoico de fórmula I para dar como resultado la 4-amino-1 ( (2R, 3R, 4R, 5 5 R) -3-fluoro-4-hidroxi-5-hidroximetil-3-metil-tetrahidro-furan-2-il) -1H-pirimidin-2-ona de fórmula IV.
El término ácido (aril) alcanoico, tal como se usa en el presente documento, se refiere a un grupo RCO2H en el que R es cualquiera de alquilo o arilo y estos términos se han definido en el presente documento. De manera correspondiente, el término éster (aril) alcanoico se refiere a un grupo RCO2R’ en el que R es cualquiera de alquilo o arilo. De la forma más típica, el R’ representa la (s) posición (ones) 3’ y/o 5’ de un anillo de ribosa. Los términos “ (aril) alcanoílo” y “ (aril) alcanoiloxi” se refieren a los grupos RCO-y RCOO-respectivamente, en los que R es tal como se ha descrito anteriormente. El término “ (aril) alcanoiloximetilo” se refiere a un grupo RCOOCH2-en el que R es tal como se ha descrito anteriormente.
El término “alquilo” tal como se usa en el presente documento denota un resto hidrocarburo monovalente, saturado, de cadena no ramificada o ramificada que contiene 1 a 10 átomos de carbono.
El término “arilo” tal como se usa en el presente documento, se refiere a un grupo fenilo.
En una realización preferida de la presente invención, R tiene el significado de fenilo.
En general, la nomenclatura utilizada en esta Solicitud se basa en AUTONOM™ v.4.0, un sistema informatizado del
Instituto Beilstein para la generación de la nomenclatura sistemática de la IUPAC. Si existe una discrepancia entre una estructura representada gráficamente y el nombre dado a dicha estructura, la estructura representada
gráficamente tendrá más peso. Además, si la estereoquímica de la estructura o de una parte de una estructura no está indicada con, por ejemplo, líneas en negrita o punteadas, se va a interpretar que la estructura o parte de la estructura abarca todos los estereoisómeros de esta.
La trasformación de la etapa a) comprende una reducción en presencia de un agente reductor y una posterior cloración en presencia de un agente clorante.
Un agente reductor adecuado es el hidruro de sodio bis- (2-metoxietoxi) (2, 2, 2-trifluoroetoxi) aluminio que está comercialmente disponible con el nombre comercial RedAI® en forma de una disolución en tolueno.
La reducción tiene lugar normalmente en un disolvente orgánico tal como un hidrocarburo halogenado de tipo diclorometano a una temperatura de reacción por debajo de 0º C, preferentemente por debajo de -5º C.
Tras finalizar la reducción, la mezcla de reacción se somete a una reacción de cloración.
El agente clorante es habitual seleccionarlo entre cloruro de sulfurilo, cloruro de tionilo u oxicloruro de fósforo.
Se utiliza preferentemente cloruro de sulfurilo en presencia de cantidades catalíticas de bromuro de tetrabutil amonio.
La etapa de cloración se lleva a cabo rápidamente a una temperatura de reacción de entre 0º C y 40º C.
El (2R, 3R, 4R) -2- (aril) alcanoiloxi metil-5-cloro-4-fluoro-4-metil-tetrahidro-furan-3-il éster del ácido (aril) alcanoico de fórmula (III) se puede separar de la mezcla de reacción aplicando las técnicas que conoce el experto en la materia.
La conversión de la etapa b) comprende hacer reaccionar el (2R, 3R, 4R) -2- (aril) alcanoiloxi metil-5-cloro-4-fluoro-4metil-tetrahidro-furan-3-il éster del ácido (aril) alcanoico de fórmula (III) con O-trimetil silil-N4-benzoilcitosina en presencia de un ácido de Lewis.
La O-trimetil silil-N4-benzoilcitosina se puede preparar in situ haciendo reaccionar N-benzoil citosina con hexametildisilazano en presencia de sulfato de amonio en clorobenceno en condiciones de temperatura de reflujo.
Los ácidos de Lewis habituales conocidos en la técnica son adecuados para la conversión de la etapa b) . Se han conseguido buenos resultados con cloruro estánnico.
La reacción se lleva a cabo normalmente a temperatura elevada, por ejemplo, a aproximadamente 70º C hasta que se completa el acoplamiento.
El (2R, 3R, 4R, 5R) -3- (aril) alcanoiloxi-5- (4-benzoilamino-2-oxo-2H-pirimidin-1-il) -4-fluoro-4-metil-tetrahidro-furan-2ilmetil éster del ácido (aril) alcanoico de formula I obtenido de esta manera se puede separar de la mezcla de reacción aplicando las técnicas conocidas por los expertos en la materia.
La hidrólisis de la etapa c) se lleva a cabo en presencia de una base.
Las bases adecuadas son bases orgánicas del tipo de los alcóxidos de metales alcalinos. Preferentemente, se utiliza metóxido de sodio en metanol como disolvente.
La reacción se lleva a cabo a temperatura elevada, por ejemplo, a aproximadamente 50º C hasta que se completa la hidrólisis.
La 4-amino-1- ( (2R, 3R, 4R, 5R) -3-fluoro-4-hidroxi-5-hidroximetil-3-metiltetrahidro-furan-2-il) -1H-pirimidin-2-ona de la fórmula IV se puede aislar siguiendo los procedimientos conocidos por los expertos en la materia.
En una realización adicional de la presente invención se ha desarrollado un procedimiento para la preparación del producto de partida, el (2R, 3R, 4R) -2- (aril) alcanoiloximetil-4-fluoro-4-metil-5-oxo-tetrahidro-furan-3-il éster del ácido (aril) alcanoico de fórmula II
en la que R es fenilo desarrollado.
El procedimiento comprende las etapas a1) transformar el éster etílico del ácido (E) -3- ( (S) -2, 2-dimetil-[1, 3]dioxolan-4-il) -2-metil-acrílico de fórmula V
en el éster etílico del ácido (2S, 3R) -3- ( (R) -2, 2-dimetill-[1, 3]dioxolan-4-il) -2, 3-dihidroxi-2-metil propiónico de fórmula VI
b1) convertir el éster etílico del ácido (2S, 3R) -3- ( (R) -2, 2-dimetil-[1, 3]dioxolan-4-il) -2, 3-dihidroxi-2-metilpropiónico de fórmula VI en el sulfito de fórmula VII
c1) hacer reaccionar adicionalmente el sulfito de fórmula VII con el sulfato de fórmula VIII
d1) transformar el sulfato de fórmula VIII en el sulfato de fluorohidrina de fórmula IX e1) descomponer el sulfato de fluorohidrina de fórmula IX en la lactona... [Seguir leyendo]
Reivindicaciones:
1. Un procedimiento de preparación de 4-amino-1- ( (2R, 3R, 4R, 5R) -3-fluoro-4-hidroxi-5-hidroximetil-3-metil-tetrahidrofuran-2-il) -1H-pirimidin-2-ona de fórmula que comprende a) trasformar un (2R, 3R, 4R) -2- (aril) alcanoiloximetil-4-fluoro-4-metil-5-oxo-tetrahidro-furan-3-il éster del ácido (aril) alcanoico de fórmula II
en la que R es arilo o alquilo en un (2R, 3R, 4R) -2- (aril) alcanoiloxi metil-5-cloro-4-fluoro-4-metil-tetrahidro-furan-3-il éster del ácido (aril) alcanoico de fórmula III
en la que R es arilo o alquilo; b) convertir el (2R, 3R, 4R) -2- (aril) alcanoiloxi metil-5-cloro-4-fluoro-4-metil-tetrahidro-furan-3-il éster del ácido (aril) alcanoico de fórmula III en un (2R, 3R, 4R, 5R) -3- (aril) alcanoiloxi-5- (4-benzoilamino-2-oxo-2H-pirimidin-1il) -4-fluoro-4-metil-tetrahidro-furan-2-ilmetil éster del ácido (aril) alcanoico de fórmula I en la que R es arilo o alquilo y Bz es benzoílo e c) hidrolizar el (2R, 3R, 4R, 5R) -3- (aril) alcanoiloxi-5- (4-benzoilamino-2-oxo-2H-pirimidin-1-il) -4-fluoro-4-metiltetrahidro-furan-2-ilmetill éster del ácido (aril) alcanoico de fórmula I para dar como resultado la 4-amino-1
( (2R, 3R, 4R, 5R) -3-fluoro-4-hidroxi-5-hidroximetil-3-metil-tetrahidro-furan-2-il) -1H-pirimidin-2-ona de fórmula IV.
2. Procedimiento de acuerdo con la reivindicación 1, caracterizado porque tiene el significado de fenilo.
3. Procedimiento de acuerdo con la reivindicación 1 o 2, caracterizado porque la trasformación de la etapa a)
comprende una reducción en presencia de un agente reductor y una posterior cloración en presencia de un agente 10 clorante.
4. Procedimiento de acuerdo con la reivindicación 3, caracterizado porque el agente reductor es hidruro de bis- (2metoxietoxi) (2, 2, 2-trifluoro-etoxi) aluminio y sodio
5. Procedimiento de acuerdo con la reivindicación 3 o 4, caracterizado porque el agente clorante está seleccionado entre cloruro de sulfurilo, cloruro de tionilo u oxicloruro de fósforo.
6. Procedimiento de acuerdo con la reivindicación 5, caracterizado porque el agente clorante es cloruro de sulfurilo en presencia de cantidades catalíticas de bromuro de tetrabutilamonio.
7. Procedimiento de acuerdo con una cualquiera de las reivindicaciones 1 a 6, caracterizado porque la conversión en la etapa b) comprende hacer reaccionar el (2R, 3R, 4R) -2- (aril) alcanoiloximetil-5-cloro-4-fluoro-4-metil-tetrahidrofuran-3-il éster del ácido (aril) alcanoico de fórmula III con O-trimetil silil-N4-benzoilcitosina en presencia de un ácido de Lewis.
8. Procedimiento de acuerdo con una cualquiera de las reivindicaciones 1 a 7, caracterizado porque la hidrólisis en la etapa c) se lleva a cabo en presencia de una base.
9. Procedimiento de acuerdo con la reivindicación 1, que comprende preparar un (2R, 3R, 4R) -2- (aril) alcanoiloximetil4-fluoro-4-metil-5-oxo-tetrahidro-furan-3-il éster del ácido (aril) alcanoico de fórmula II
en la que R es fenilo que comprende las etapas de a1) trasformar el éster etílico del ácido (E) -3- ( (S) -2, 2-dimetil-[1, 3]dioxolan-4-il) -2-metilacrílico de fórmula V
en el éster etílico del ácido (2S, 3R) -3- ( (R) -2, 2-dimetil-[1, 3]dioxolan-4-il) -2, 3-dihidroxi-2-metilpropiónico de fórmula VI
b1) convertir el éster etílico del ácido (2S, 3R) -3- ( (R) -2, 2-dimetil-[1, 3]dioxolan-4-il) -2, 3-dihidroxi-2-metilpropiónico de fórmula VI en el sulfito de fórmula VII
c1) hacer reaccionar de forma adicional el sulfito de fórmula VII con el sulfato de fórmula VIII
d1) trasformar el sulfato de fórmula VIII en el sulfato de fluorohidrina de fórmula IX
e1) descomponer el sulfato de fluorohidrina de fórmula IX a la lactona de fórmula X
y, finalmente f1) acilar la lactona de fórmula X para formar el producto final de fórmula II en el que R es fenilo.
10. Procedimiento de acuerdo con la reivindicación 9, caracterizado porque la trasformación de la etapa a1) se 10 lleva a cabo con permanganato de sodio en presencia de etilenglicol y bicarbonato de sodio.
11. Procedimiento de acuerdo con la reivindicación 9 o 10, caracterizado porque la trasformación de la etapa b1) se lleva a cabo con cloruro de tionilo.
12. Procedimiento de acuerdo con una cualquiera de las reivindicaciones 9 a 11, caracterizado porque la trasformación en la etapa c1) se lleva a cabo con hipoclorito de sodio.
13. Procedimiento de acuerdo con una cualquiera de las reivindicaciones 9 a 12, caracterizado porque la trasformación en la etapa d1) se lleva a cabo con una trialquilamina.
14. Procedimiento de acuerdo con la reivindicación 13, caracterizado porque se utiliza trialquilamina junto con trifluorhidrato de trietilamina.
15. Procedimiento de acuerdo con una cualquiera de las reivindicaciones 9 a 14, caracterizado porque la descomposición en la etapa e1) se lleva a cabo con cloruro de bario en agua.
16. Procedimiento de acuerdo con una cualquiera de las reivindicaciones 9 a 15, caracterizado porque la acilación 10 5 en la etapa f1) se lleva a cabo con anhídrido benzoico.
Patentes similares o relacionadas:
Derivados de 5-fluorouridina, del 1 de Julio de 2020, de B. BRAUN MELSUNGEN AG: Compuesto representado por la fórmula (I) **(Ver fórmula)** en donde X es un grupo de fórmula (III) **(Ver fórmula)** en donde R1 se selecciona entre H, **(Ver […]
Nucleótidos modificados para secuenciación de polinucleótidos, del 8 de Abril de 2020, de ILLUMINA CAMBRIDGE LIMITED: Una molécula de nucleótido que tiene una unidad estructural de azúcar ribosa o desoxirribosa y una base enlazada a un marcador detectable a través de […]
Nucleósidos sustituidos en 2',4' como agentes antivirales, del 25 de Marzo de 2020, de Gilead Pharmasset LLC: Un compuesto de la siguiente fórmula: **(Ver fórmula)** o una de sus sales farmacéuticamente aceptables, en donde: (a) R2 es F; (b) R es H, […]
Intermedios de D-ribonolactona con sustitución de 2-fluoro-2-alquilo, del 6 de Noviembre de 2019, de Gilead Pharmasset LLC: 2-desoxi-2-fluoro-2-C-metilo-D-ribono-g-lactona de la siguiente fórmula general (49B) y su L-isómero (49B-L): **Fórmula** en donde R3 y R5 pueden ser independientemente […]
Oligómeros polinucleotídicos de citosina modificados y métodos, del 23 de Octubre de 2019, de CEPHEID: Un oligómero polinucleotídico que comprende al menos una base modificada, en el que la al menos una base modificada se representa mediante la fórmula: **(Ver […]
Análogos de N-nucleósido de pirimidina 1-sustituidos para un tratamiento antiviral, del 12 de Junio de 2019, de GILEAD SCIENCES, INC.: Un Compuesto seleccionado de:**Fórmula** o una sal farmacéuticamente aceptable de los mismos.
Ruta sintética de 2-desoxi-2,2-difluorotetrahidrouridinas, del 16 de Mayo de 2019, de OTSUKA PHARMACEUTICAL CO., LTD.: Método de producción de compuesto 1:**Fórmula** o una sal del mismo, que comprende precipitar o cristalizar el compuesto 1 a partir de una solución de compuesto […]
Nucleósidos sustituidos, nucleótidos y sus análogos, del 25 de Abril de 2019, de Alios Biopharma, Inc: Un compuesto de Fórmula (I), o una de sus sales farmacéuticamente aceptable, para su uso en la mejora o el tratamiento de una infección vírica causada por un virus seleccionado […]