Análogos marcados de halobenzamidas como radiofármacos.
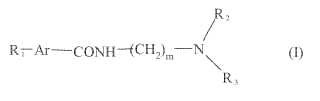
Compuesto de fórmula (I):
en la que
R1 representa un radionúclido,
Ar es un grupo heteroarílico,
m es un número entero que varía de 2 a 4,
R2 y R3 representan, independientemente entre sí, un átomo de hidrógeno, un grupo alquilo (C1-C6) o un grupo alquenilo (C1-C6), en el que el grupo heteroarilo es un anillo aromático de 5 ó 6 miembros, que comprende 1 ó 2 átomos de nitrógeno, o un núcleo aromático bi- o tricíclico que comprende de 1 a 4 átomos de nitrógeno o que comprende un átomo de azufre, presentando al menos uno de los anillos 6 miembros anulares, presentando el otro anillo o anillos condensados 5 ó 6 miembros anulares, siendo posible que dicho grupo heteroarílico esté monosustituido por:
- un átomo de halógeno opcionalmente marcado,
- un grupo alcoxi (C1-C4),
- un grupo alquilo (C1-C4),
- un grupo oxo, o
- un grupo anilino, el cual puede estar en sí mismo sustituido por entre 1 y 3 grupos, que se pueden seleccionar de entre un grupo alquilo (C1-C4) o un grupo alcoxi (C1-C4), un grupo hidroxilo, un átomo de halógeno o un grupo NHRe, en el que Re representa un hidrógeno, o un grupo CORa, un grupo COORa o un 20 grupo SO2Ra, en los que Ra representa un grupo arilo o un grupo alquilo (C1-C10) opcionalmente sustituido con un grupo oxo;
y en la que R1 está enlazado con el núcleo aromático como tal, o, cuando el sustituyente del núcleo aromático es un grupo anilino, R1 puede estar enlazado con el grupo fenilo del grupo anilino,
y en la que Ar se selecciona de entre un grupo piridilo, fenazinilo, naftiridinilo, indolilo, imidazopiridilo,
bencimidazolilo, quinolilo, quinolonilo, isoquinolilo, quinoxalinilo, benzotienilo, acridinilo o acridonilo, siendo posible que dicho grupo esté monosustituido por un grupo metilo, un grupo metoxi o un átomo de halógeno opcionalmente marcado, y un grupo acridinilo sustituido por un grupo anilino el cual puede estar en sí mismo sustituido por entre 1 y 3 grupos que se pueden seleccionar de entre un grupo alquilo (C1-C4) o alcoxi (C1-C4), un grupo hidroxilo, un átomo de halógeno o un grupo NHRc, en el que Re representa un hidrógeno, o un grupo CORa, un grupo COORa o un 30 grupo SO2Ra, en los que Ra representa un grupo arilo o un grupo alquilo (C1-C10) opcionalmente sustituido por un grupo oxo, y sus sales de adición con ácidos farmacéuticamente aceptables, para su uso en una composición radiofarmacéutica en el diagnóstico y/o el tratamiento del melanoma.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/IB2007/052992.
Solicitante: INSTITUT NATIONAL DE LA SANTE ET DE LA RECHERCHE MEDICALE (INSERM).
Nacionalidad solicitante: Francia.
Dirección: 101, RUE DE TOLBIAC 75013 PARIS FRANCIA.
Inventor/es: MADELMONT, JEAN-CLAUDE, CHEZAL,JEAN-MICHEL, CHAVIGNON,OLIVER, TEULADE,JEAN-CLAUDE, MOINS,NICOLE.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K31/165 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › teniendo ciclos aromáticos, p. ej. colchicina, atenolol, progabide.
- C07D209/42 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07D COMPUESTOS HETEROCICLICOS (Compuestos macromoleculares C08). › C07D 209/00 Compuestos heterocíclicos que contienen ciclos de cinco miembros, condensados con otros ciclos, con solamente un átomo de nitrógeno como heteroátomo. › Atomos de carbono que tienen tres enlaces a heteroátomos con a lo más un enlace a halógeno, p. ej. radicales éster o nitrilo.
- C07D215/54 C07D […] › C07D 215/00 Compuestos heterocíclicos que contienen quinoleína o quinoleína hidrogenada en el sistema cíclico. › unidos en posición 3.
- C07D217/26 C07D […] › C07D 217/00 Compuestos heterocíclicos que contienen isoquinoleína o isoquinoleína hidrogenada en el sistema cíclico. › Atomos de carbono que tienen tres enlaces a heteroátomos con a lo más un enlace a halógeno.
- C07D219/06 C07D […] › C07D 219/00 Compuestos heterocíclicos que contienen sistemas cíclicos de acridina o acridina hidrogenada. › Atomos de oxígeno.
- C07D233/62 C07D […] › C07D 233/00 Compuestos heterocíclicos que contienen ciclos de diazol-1,3 o diazol-1,3 hidrogenado, no condensados con otros ciclos. › con radicales de triarilmetil unidos a los átomos de nitrógeno del ciclo.
- C07D235/24 C07D […] › C07D 235/00 Compuestos heterocíclicos que contienen ciclos de diazol-1,3 o diazol-1,3 hidrogenado, condensados con otros ciclos. › con heteroátomos o con átomos de carbono que tienen tres enlaces a heteroátomos, con a lo sumo un enlace a halógeno, p. ej. radicales éster o nitrilo, unidos directamente en posición 2.
- C07D237/26 C07D […] › C07D 237/00 Compuestos heterocíclicos que contienen ciclos de diazina-1,2 o diazina-1,2 hidrogenada. › condensados con ciclos o sistemas cíclicos carbocíclicos.
- C07D333/68 C07D […] › C07D 333/00 Compuestos heterocíclicos que contienen ciclos de cinco miembros que tienen un átomo de azufre como único heteroátomo del ciclo. › Atomos de carbono que tienen tres enlaces a heteroátomos con a lo más un enlace a halógeno.
- C07D471/04 C07D […] › C07D 471/00 Compuestos heterocíclicos que contienen átomos de nitrógeno como únicos heteroátomos del sistema condensado, teniendo al menos un ciclo de seis miembros con un átomo de nitrógeno, no previstos en los grupos C07D 451/00 - C07D 463/00. › Sistemas condensados en orto.
PDF original: ES-2394274_T3.pdf
Fragmento de la descripción:
Análogos marcados de halobenzamidas como radiofármacos.
La presente invención se refiere al uso de análogos aromáticos y heteroaromáticos de halobenzamidas marcados con un isótopo radioactivo adecuado como radiofármaco para el diagnóstico médico por imágenes positrónicas y gamma escintigráficas, o para el tratamiento radioterapéutico interno de melanoma, y también a algunos nuevos análogos aromáticos y heteroaromáticos de halobenzamidas.
El melanoma es uno de los tumores de piel más peligrosos, con una incidencia lenta pero firmemente creciente. Específicamente, la incidencia actual de melanoma cutáneo está próxima a 10000 nuevos casos diagnosticados poraño en Francia. Éste es un cáncer altamente invasivo, cuyo desarrollo es rápidamente mortal en la fase metastásica. La supervivencia de 5 años no supera el 14%, excepto en el caso en el que el grosor del tumor es menor que 0, 76 mm. En el caso en el que la lesión supera este grosor, este tumor da metástasis de una manera silenciosa y no predecible. Esta es la razón por la que actualmente se está llevando a cabo una investigación en busca de un método de investigación que haga posible la evaluación temprana tanto de la extensión local como de la extensión distante del tumor.
Durante la última década, se han experimentado un número de productos radiofarmacéuticos, seleccionados en busca de su afinidad potencial por la melanina, pero muy pocos han tenido un desarrollo clínico satisfactorio.
Se debería explicar que los productos radiofarmacéuticos comprenden dos componentes fundamentales, siendo uno radioactivo y siendo el otro no radioactivo. El componente radioactivo hace posible la detección del producto en el contexto del diagnóstico, y constituye el agente activo en el caso de uso terapéutico. Está compuesto de un radionúclido con propiedades físicas apropiadas. El componente no radioactivo, por su parte, está compuesto de una molécula o trazador, opcionalmente biológico, destinado a acumularse en el órgano diana, en este caso, en el contexto de la presente invención, en el melanoma, y asegurar la absorción de radioactividad por este último. Este componente no radioactivo determina el comportamiento biológico del producto radiofarmacéutico en el cuerpo, en particular con respecto a la especificidad y el perfil farmacocinético.
Más particularmente, en el diagnóstico médico por la imagen, se han desarrollado anticuerpos monoclonales que seleccionan específicamente como diana al melanoma. Además, se han estudiado en el hombre diversas moléculas que presentan una afinidad por el melanoma, después de marcarlas con 123I: azul de metileno, N-[3- (4morfolino) propil]-N-metil-2-hidroxi-5-yodo-3-metilbencilamina (ERC9) y estructuras benzamídicas.
Además, el documento EP 458886 describe compuestos de uso en el diagnóstico y tratamiento de melanoma maligno. En particular, N- (2-dietilaminoetil) -4-yodobenzamida (BZA) forma el objeto de estudios más detallados, y también N- (2-dietilaminoetil) -2-yodobenzamida (BZA2) , en la aplicación del diagnóstico médico por la imagen, y más particularmente para la detección escintigráfica de melanoma ocular primario y metástasis de melanomas cutáneos y oculares.
La patente US nº 5.911.970, por su parte, describe, entre otros, otros compuestos derivados de benzamida que presentan una elevada especificidad y afinidad con respecto a la superficie de células cancerosas.
De este modo, por un lado, existe la necesidad de disponer de un trazador específico que haga posible, desde el momento del diagnóstico, llevar a cabo una evaluación de la extensión de la enfermedad y después, subsiguientemente, la monitorización. Tal trazador haría posible ventajosamente el diagnóstico diferencial de melanoma ocular, lesión primaria, que a menudo es difícil de identificar.
Por otro lado, los tratamientos siguen siendo derrotados con respecto a melanoma diseminado, y es esencial el desarrollo de nuevos enfoques terapéuticos específicos para el tratamiento de melanoma.
Esto es debido a que, mientras que el tratamiento quirúrgico de melanoma sigue siendo la mejor arma (tumores cutáneos primarios operables y sitios secundarios aislados) , la baja efectividad de los tratamientos proporcionados hasta la fecha con respecto a la enfermedad diseminada ilustra la necesidad de desarrollar un tratamiento de melanoma mediante radioterapia interna vectorizada. Hasta la fecha, los primeros resultados experimentales, llevados a cabo con un análogo -MSH, son muy preliminares, y todavía se ha de determinar el trazador ideal. De este modo, el objetivo de la presente invención es la selección como diana de lesiones melanóticas mediante el desarrollo de moléculas que, administradas al cuerpo, harán posible vectorizar un radioisótopo. Este objetivo da como resultado dos campos de aplicaciones, a saber, el diagnóstico médico por la imagen y la radioterapia.
De este modo, los compuestos según la invención son ventajosos tanto por su uso en diagnóstico médico por la imagen, a saber, para el diagnóstico de melanoma maligno, como en radioterapia interna vectorizada, seleccionando como dianas más particularmente a lesiones secundarias y lesiones oculares primarias. Una de las ventajas principales de los compuestos según la presente invención reside precisamente en su potencialidad mixta. En otras palabras, según las variaciones químicas bajo consideración, sus comportamientos respectivos en el cuerpo los destinan más particularmente para uso en el diagnóstico médico por la imagen, para su uso en radioterapia u otros, y esta categoría de compuestos puede ser particularmente atractiva para uso tanto el diagnóstico médico por la imagen como en radioterapia.
Los ejemplos dados más abajo ilustran claramente, para unos pocos compuestos, estos diversos comportamientos en términos de especificidad, de duración de radioactividad, o de eficacia antitumoral.
Finalmente, algunos compuestos que corresponden a la fórmula general de los compuestos según la invención, cuando no están marcados, también pueden mostrar una actividad antitumoral innata. De este modo, en este caso específico, esto equivale a decir que el componente no radioactivo definido anteriormente puede presentar, además de su papel de seleccionador de la diana del melanoma y/o de promover la absorción de radioactividad, un papel de agente citotóxico per se.
En consecuencia, esta categoría particular de compuestos, cuyo uso es la materia objeto de la presente invención, para algunos ya conocida por su actividad contra el cáncer cuando están desprovistos de radionúclidos, en particular vía el modo de acción de agentes intercalantes, puede mostrar la ventaja de hacer posible una aplicación radioterapéutica que se puede combinar con una aplicación en quimioterapia. La referencia es entonces a compuestos destinados a una aplicación en radioquimioterapia. Sin embargo, es claramente la actividad vía el
marcado mediante un isótopo radioactivo la que se selecciona como diana en la presente invención. En otras palabras, la posible actividad relacionada con el mecanismo de acción innata al compuesto no marcado sólo generalmente se ha de considerar como una ventaja adicional.
En particular, se puede hacer mención, entre compuestos no marcados que muestran una actividad citotóxica innata que se puede usar, tras el marcado, en la radioquimioterapia del melanoma, de ciertos compuestos descritos en los documentos WO93/24096, WO98/17649 o US 6821983 como análogos de acridinacarboxamida (“DACA”) . La selección como diana de melanoma no ha sido demostrada hasta ahora para estos compuestos. Las dos publicaciones siguientes:
-Osman, S., Rowlinson-Busza, G., Luthra, K. S., Aboagye, E. O., Brown, G. D., Brady, F., Myers, R., Gamage,
S. A., Denny, W. A., Baguley, B. C., Price, P. M., Cancer Res., 2001, 61, 2935-2944, y
- Saleem, A., Harte, R. J., Matthews, J. C., Osman, S., Brady, F., Luthra, S. K., Brown, G. D., Bleehen, N., Connors, T., Jones, T., Price, P. M., y Aboagye, E. O., J. Clin. Oncology, 2001, 19, 1421-1429,
describen la biodistribución de DACA marcada con 11C. Sin embargo, estos dos experimentos se refieren a tiempos cortos (< 1 h) , y no demuestran una fijación específica de DACA para los tumores melanóticos evaluados.
Los derivados de tipo fenazina se describen en particular en el documento WO 2005/118580 y en la publicación S.
A. Gamageet al., Bioorganic & Medicinal Chemistr y , 2006, 14, 1160-1168, por su actividad innata contra el cáncer. Sin embargo, nunca se ha demostrado el uso de tales derivados de fenazina para la selección como diana de melanoma.
Según un... [Seguir leyendo]
Reivindicaciones:
1. Compuesto de fórmula (I) :
en la que R1 representa un radionúclido,
Ar es un grupo heteroarílico,
m es un número entero que varía de 2 a 4,
R2 y R3 representan, independientemente entre sí, un átomo de hidrógeno, un grupo alquilo (C1-C6) o un grupo alquenilo (C1-C6) , en el que el grupo heteroarilo es un anillo aromático de 5 ó 6 miembros, que comprende 1 ó 2
átomos de nitrógeno, o un núcleo aromático bi- o tricíclico que comprende de 1 a 4 átomos de nitrógeno o que comprende un átomo de azufre, presentando al menos uno de los anillos 6 miembros anulares, presentando el otro anillo o anillos condensados 5 ó 6 miembros anulares, siendo posible que dicho grupo heteroarílico esté monosustituido por:
- un átomo de halógeno opcionalmente marcado,
- un grupo alcoxi (C1-C4) ,
- un grupo alquilo (C1-C4) ,
- un grupo oxo, o
- un grupo anilino, el cual puede estar en sí mismo sustituido por entre 1 y 3 grupos, que se pueden seleccionar de entre un grupo alquilo (C1-C4) o un grupo alcoxi (C1-C4) , un grupo hidroxilo, un átomo de
halógeno o un grupo NHRe, en el que Re representa un hidrógeno, o un grupo CORa, un grupo COORa o un grupo SO2Ra, en los que Ra representa un grupo arilo o un grupo alquilo (C1-C10) opcionalmente sustituido con un grupo oxo;
y en la que R1 está enlazado con el núcleo aromático como tal, o, cuando el sustituyente del núcleo aromático es un grupo anilino, R1 puede estar enlazado con el grupo fenilo del grupo anilino,
y en la que Ar se selecciona de entre un grupo piridilo, fenazinilo, naftiridinilo, indolilo, imidazopiridilo, bencimidazolilo, quinolilo, quinolonilo, isoquinolilo, quinoxalinilo, benzotienilo, acridinilo o acridonilo, siendo posible que dicho grupo esté monosustituido por un grupo metilo, un grupo metoxi o un átomo de halógeno opcionalmente marcado, y un grupo acridinilo sustituido por un grupo anilino el cual puede estar en sí mismo sustituido por entre 1 y 3 grupos que se pueden seleccionar de entre un grupo alquilo (C1-C4) o alcoxi (C1-C4) , un grupo hidroxilo, un átomo de halógeno o un grupo NHRc, en el que Re representa un hidrógeno, o un grupo CORa, un grupo COORa o un grupo SO2Ra, en los que Ra representa un grupo arilo o un grupo alquilo (C1-C10) opcionalmente sustituido por un grupo oxo,
y sus sales de adición con ácidos farmacéuticamente aceptables, para su uso en una composición radiofarmacéutica en el diagnóstico y/o el tratamiento del melanoma.
2. Compuesto para su uso según la reivindicación 1, caracterizado porque Ar es un núcleo aromático bi- o tricíclico, y el grupo R1 está enlazado con uno de estos anillos y el grupo está enlazado con el otro anillo o con uno de los otros anillos que constituyen el grupo bi- o tricíclico.
3. Compuesto para su uso según cualquiera de las reivindicaciones anteriores, caracterizado porque, alternativamente:
- el grupo R1 está en la posición para con respecto al grupo
cuando Ar comprende un solo anillo, y porque el grupo R1 está enlazado con uno de los anillos y el grupo está enlazado con el otro anillo o con uno de los otros anillos cuando Ar es bi- o tricíclico, o
- Ar es un heteroarilo bi- o tricíclico, y porque R1 está enlazado con el anillo, tomado aisladamente, que no comprende un heteroátomo o que comprende lo menos del mismo, y el grupo
está enlazado con otro anillo que comprende el mayor número de heteroátomos.
4. Compuesto de fórmula (I’)
en la que W se selecciona de entre un grupo fenazinilo, imidazopiridilo, quinolilo, quinoxalinilo, acridinilo y acridonilo, siendo posible que dicho grupo acridinilo sea sustituido por un grupo anilino sustituido él mismo por tres grupos,
- representando al menos uno de los sustituyentes el grupo alcoxi (C1-C4) ,
- siendo al menos uno de los sustituyentes seleccionado de entre un grupo NHRc, en el que Rc representa un
hidrógeno, o un grupo CORa, un grupo COORa o un grupo SO2Ra, en el que Ra representa un grupo arilo o un grupo alquilo (C1-C10) opcionalmente sustituido por un grupo oxo, y
- representando el sustituyente restante un átomo de hidrógeno o de halógeno, R1, R2, R3 y m tienen el mismo significado que el definido en cualquiera de las reivindicaciones 1 a 3, y
R8 representa un átomo de hidrógeno, un grupo alquilo (C1-C4) o alcoxi (C1-C4) , un átomo de halógeno opcionalmente marcado, un grupo –SH, un grupo –OH o un grupo –NR5R6, en el que R5 y R6 pueden representar independientemente un átomo de hidrógeno o un grupo alquilo (C1-C4) ,
para su uso en una composición en el tratamiento del melanoma.
5. Compuesto para su uso según cualquiera de las reivindicaciones anteriores, caracterizado porque el radionúclido es un radioisótopo seleccionado de entre 113I, 124I, 125I, 131I, 75Br, 76Br, 77Br, 18F, 210At o 211At, y es en particular 123I, 124I, 125I o 131I.
6. Compuesto de fórmula (II)
en la que R'1 representa un átomo de halógeno marcado, m tiene el mismo significado que el definido en la reivindicación 1, R2 y R3 representan, independientemente entre sí, un grupo alquilo (C1-C6) o un grupo alquenilo (C1-C6) , y Ar se selecciona de entre el grupo piridilo, indolilo, imidazopiridinilo, bencimidazolilo, quinolilo, quinolonilo,
isoquinolilo, quinoxalinilo, naftiridinilo y benzotienilo.
7. Compuesto de fórmula (I”)
en la que R2, R3 y m son tal como se definen en la reivindicación 1, R8 y W son tal como se definen en la reivindicación 4, y 20 siendo el átomo de yodo opcionalmente 123I, 124I, 125I o 131I.
8. Compuesto seleccionado de entre:
-Dihidrocloruro de N- (2-dietilaminoetil) -6-yodonicotinamida;
-Hidrocloruro de N- (2-dietilaminoetil) -5-yodoindol-2-carboxamida;
-Hidrocloruro de N- (2-dietilaminoetil) -4-yodobenzo[b]tiofen-2-carboxamida.
25. Dihidrocloruro de N- (2-dietilaminoetil) -3-yodoimidazo[1, 2-a]piridin-2-carboxamida;
-Dihidrocloruro de N- (2-dietilaminoetil) -6-yodoimidazo[1, 2-a]piridin-2-carboxamida;
-Dihidrocloruro de N- (2-dietilaminoetil) -5-yodobenzimidazol-2-carboxamida;
-Dihidrocloruro de N- (2-dietilaminoetil) -6-yodoquinolin-2-carboxamida;
-Hidrocloruro de N- (2-dietilaminoetil) -1, 4-dihidro-6-yodo-4-oxoquinolin-3-carboxamida.
30. Dihidrocloruro de N- (2-dietilaminoetil) -5-yodoisoquinolin-3-carboxamida;
-Dihidrocloruro de N- (2-dietilaminoetil) -6-yodoquinoxalin-2-carboxamida;
-Dihidrocloruro de N- (4-dipropilaminobutil) -6-yodoquinolin-2-carboxamida;
-Hidrocloruro de N- (2-dietillaminoetil) -9, 10-dihidro-1-yodo-9-oxacridin-4-carboxamida;
-Hidrocloruro de N- (2-dietilaminoetil) -9, 10-dihidro-2-yodo-9-oxoacridin-4-carboxamida;
-Hidrocloruro de N- (2-dietilaminoetil) -9, 10-dihidro-3-yodo-9-oxoacridin-4-carboxamida; 5 -Hidrocloruro de N- (2-dietilaminoetil) -9, 10-dihidro-5-yodo-9-oxoacridin-4-carboxamida;
-Hidrocloruro de N- (2-dietilaminoetil) -9, 10-dihidro-6-yodo-9-oxoacridin-4-carboxamida;
-Hidrocloruro de N- (2-dietilaminoetil) -9, 10-dihidro-7-yodo-9-oxoacridin-4-carboxamida;
-Hidrocloruro de N- (2-dietilaminoetil) -9, 10-dihidro-8-yodo-9-oxoacridin-4-carboxamida;
-Dihidrocloruro de N- (2-dietilaminoetil) -1-yodoacridin-4-carboxamida.
10. Dihidrocloruro de N- (2-dietilaminoetil) -2-yodoacridin-4-carboxamida;
-Dihidrocloruro de N- (2-dietilaminoetil) -3-yodoacridin-4-carboxamida;
-Dihidrocloruro de N- (2-dietilaminoetil) -5-yodoacridin-4-carboxamida;
-Dihidrocloruro de N- (2-dietilaminoetil) -6-yodoacridin-4-carboxamida;
-Dihidrocloruro de N- (2-dietilaminoetil) -7-yodoacridin-4-carboxamida.
15. Dihidrocloruro de N- (2-dietilaminoetil) -8-yodoacridin-4-carboxamida;
-Dihidrocloruro de N- (2-dietilaminoetil) -2-yodoacridin-9-carboxamida;
-Dihidrocloruro de N- (2-dietilaminoetil) -2, 7-diyodoacridin-9-carboxamida;
-Dihidrocloruro de N- (2-dietilaminoetil) -2-yodo-9- (4-metanosulfonamido-2-metoxianilino) acridin-4-carboxamida;
-Dihidrocloruro de N- (2-dietilaminoetil) -5-yodo-9- (4-metanosulfonamido-2-metoxianilino) acridin-4-carboxamida.
20. Dihidrocloruro de N- (2-dietilaminoetil) -7-yodo-9- (4-metanosulfonamido-2-metoxianilino) acridin-4-carboxamida;
-Dihidrocloruro de N- (2-dietilaminoetil) -9- (5-yodo-4-metanosulfonamido-2-metoxianilino) acridin-4-carboxamida;
-Dihidrocloruro de N- (2-dietilaminoetil) -8-yodo-1, 6-naftiridin-2-carboxamida;
-Dihidrocloruro de N- (4-dipropilaminobutil) -6-yodoquinoxalin-2-carboxamida;
-Dihidrocloruro de N- (2-dietilaminoetil) -7-yodofenazin-1-carboxamida.
25. y sus sales farmacéuticamente aceptables.
9. Procedimiento para la preparación del compuesto de fórmula (I”) según la reivindicación 7, o del compuesto de fórmula (II) según la reivindicación 6, caracterizado porque consiste en condensar un éster de fórmula (III)
con una diamina de fórmula (IV) H2N- (CH2) m-NR2R3 (IV) en la que R2 y R3, m y R1 son tal como se definen en la reivindicación 1 y R4 representa un grupo alquilo (C1-C6) , arilo o heteroarilo.
10. Compuesto de fórmula (VII) en la que Ar, m, R2 y R3 son tal como se definen en la reivindicación 1 a 3.
11. Composición radiofarmacéutica que comprende, como principio activo, un compuesto de fórmula (I) , en la que R2
y R3 representan, independientemente entre sí, un grupo alquilo (C1-C6) o un grupo alquenilo (C1-C6) , o de fórmula (I’) , (I”) o (II) , o una de sus sales farmacéuticamente aceptables tal como se define según cualquiera de las reivindicaciones 1 a 8.
12. Compuesto de fórmula (I”) tal como se define según la reivindicación 7 o compuesto de fórmula (II) o una de sus sales farmacéuticamente aceptables según la reivindicación 6, comprendiendo dicho compuesto un radionúclido, 10 para su uso en una composición radiofarmacéutica en el diagnóstico médico por la imagen.
13. Compuesto para su uso según la reivindicación 12, en el que la composición radiofarmacéutica está destinada al diagnóstico de melanomas.
14. Compuesto (I”) tal como se define según la reivindicación 7, o compuesto de fórmula (II) o una de sus sales
farmacéuticamente aceptables según la reivindicación 6, para su uso en una composición radiofarmacéutica en el 15 tratamiento de melanomas.
15. Procedimiento para la preparación de un compuesto de fórmula (VI) .
en la que R1 es un átomo de halógeno y R4 representa un grupo alquilo (C1-C4) , arilo o heteroarilo, de uso como intermedio sintético en la preparación de los compuestos de fórmula (I’) , siendo W un grupo acridonilo, caracterizado 20 porque comprende una etapa de reducción de la acridona de fórmula (IIIa)
en la que R1 y R4 son tal como se definen anteriormente, en presencia de un agente complejante.
Patentes similares o relacionadas:
Uso de principios activos refrescantes fisiológicos y agentes que contienen tales principios activos, del 17 de Junio de 2020, de Symrise AG: Procedimiento no terapéutico para la modulación in-vitro del receptor de mentol frío TRPM8, en el que se lleva a contacto el receptor con al menos un modulador, que se selecciona […]
Moléculas químicas que inhiben el mecanismo de corte para tratar enfermedades causadas por anomalías de empalme, del 17 de Junio de 2020, de CENTRE NATIONAL DE LA RECHERCHE SCIENTIFIQUE (C.N.R.S.): Un compuesto elegido entre el grupo que comprende: • N-(3-Dimetilamino-propil)-3-(4-trifluorometoxi-fenilamino)-benzamida; • 4-(4-Metoxi-fenilamino)-3-metil-N-(3-metil-butil)-benzamida; […]
Sales cristalinas de un profármaco de dextroanfetamina, del 6 de Mayo de 2020, de SANDOZ AG: Una sal cristalina de L-lisina-d-anfetamina representada por la estructura química como se representa en la fórmula (II) **(Ver fórmula)** […]
Composición farmacéutica inyectable estable de antagonista del receptor de neuroquinina-1 y procedimiento para su preparación, del 29 de Abril de 2020, de PHARMATHEN S.A.: Una composición farmacéutica de liberación controlada para administración intramuscular o subcutánea que comprende Aprepitant o Fosaprepitant […]
Combinaciones de moduladores duales de IRS/STAT3 y agentes anticancerígenos para el tratamiento del cáncer, del 29 de Abril de 2020, de TyrNovo Ltd: Una composición farmacéutica que comprende un inhibidor de EGFR y/o un anticuerpo EGFR en combinación con un compuesto representado por la estructura […]
Implantes intraoculares que contienen prostamida y métodos de uso de éstos, del 1 de Abril de 2020, de ALLERGAN, INC.: Implante intraocular biodegradable, comprendiendo el implante una matriz de polímero biodegradable, polietilen glicol 3350, y una prostamida como el […]
Formulaciones de 15-hidroxiestearato de macrogol, del 25 de Diciembre de 2019, de ALLERGAN, INC.: Composición oftálmica que comprende un principio activo farmacéutico en una cantidad suficiente para contribuir al tratamiento, la prevención o reducción […]
Inhibidores de benzimidazol del canal de sodio, del 18 de Diciembre de 2019, de Zalicus Pharmaceuticals Ltd: Un compuesto seleccionado del grupo que consiste en **(Ver fórmula)** o una sal o solvato farmacéuticamente aceptable del mismo.