Piridazinas anilladas para el tratamiento de tumores dirigidos por se;alización Hedgehog inapropiada.
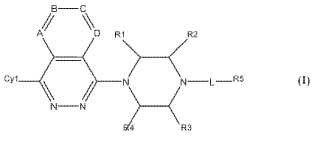
Compuesto de fórmula I
o una sal farmacéuticamente aceptable del mismo,
en el que
A, B, C y D se seleccionan independientemente de CH o N, siempre que al menos uno pero no más de dosde A, B, C y D sea N,
Cy1 es fenilo sustituido opcionalmente de manera independiente con 1-5 sustituyentes, en el que lossustituyentes se seleccionan del grupo que consiste en alquilo C1-8, alquenilo C1-8, alquinilo C1-8, haloalquiloC1-6, halógeno, ciano, hidroxilo, oxo, -ORc, -NRaRb, NRaC(≥O)Rb, -C(≥O)ORc, -RcOC(≥O)NRaRb, -RcOH, -C(≥O)NRaRb, -OC(≥O)NRaRb, -OC(≥O)Rc, -NRaC(≥O)Rc, -Rb(Ra)C(≥O)Rc, -RbN(Ra)C(≥O)ORc,-NRaS(≥O)mRc, -S(≥O)mNRaRb y S(≥O)mRc;
R1, R2, R3 y R4 se seleccionan independientemente cada uno de H, alquilo C1-6, cicloalquilo C1-6, haloalquiloC1-6, oxo, -C(≥O)ORa, -RcOH, -ORc, -NRaRb, NRaC(≥O)Rb, -C(≥O)ORc, -C(≥O)NRaRb, -OC(≥O)Rc,-NRaC(≥O)Rc, -NRaS(≥O)mRc, -S(≥O)mNRaRb y S(≥O)mRc, siempre que al menos uno de R1, R2, R3 y R4 nosea H;
Ra, Rb y Rc se seleccionan independientemente cada uno de H, alquilo C1-8, alquenilo C1-8, alquinilo C1-8,haloalquilo C1-6, heterociclilo, arilo y heteroarilo;
m es 1 ó 2;
L es -C(≥O)- o -S(≥O)m-;
R5 es -NRaRb o Cy2;
Cy2 es un anillo monocíclico de 6 miembros parcial o totalmente saturado o insaturado formado por átomosde carbono que incluye opcionalmente 1-3 heteroátomos, estando el anillo sustituido opcionalmente demanera independiente con 1-5 sustituyentes, en el que los sustituyentes se seleccionanindependientemente del grupo que consiste en alquilo C1-8, alquenilo C1-8, alquinilo C1-8, haloalquilo C1-6,halógeno, ciano, hidroxilo, oxo, -C(≥O)ORc, -RcOH, -ORc, -NRaRb, NRaC(≥O)Rb, -C(≥O)NRaRb, -OC(≥O)Rc,-NRaC(≥O)Rc, -NRaS(≥O)mRc, -S(≥O)mNRaRb y S(≥O)mRc.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2008/010498.
Solicitante: AMGEN INC..
Nacionalidad solicitante: Estados Unidos de América.
Dirección: ONE AMGEN CENTER DRIVE THOUSAND OAKS, CA 91320-1799 ESTADOS UNIDOS DE AMERICA.
Inventor/es: ZAMBONI, ROBERT, KAIZERMAN, JACOB, MCMINN,DUSTIN,L, LUCAS,BRIAN.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K31/5025 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › condensadas en orto o en peri con sistemas heterocíclicos.
- A61P35/00 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › Agentes antineoplásicos.
- C07D471/04 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07D COMPUESTOS HETEROCICLICOS (Compuestos macromoleculares C08). › C07D 471/00 Compuestos heterocíclicos que contienen átomos de nitrógeno como únicos heteroátomos del sistema condensado, teniendo al menos un ciclo de seis miembros con un átomo de nitrógeno, no previstos en los grupos C07D 451/00 - C07D 463/00. › Sistemas condensados en orto.
- C07D487/04 C07D […] › C07D 487/00 Compuestos heterocíclicos que contienen átomos de nitrógeno como únicos heteroátomos del ciclo en el sistema condensado, no previstos por los grupos C07D 451/00 - C07D 477/00. › Sistemas condensados en orto.
PDF original: ES-2392157_T3.pdf
Fragmento de la descripción:
Piridazinas anilladas para el tratamiento de tumores dirigidos por señalización Hedgehog inapropiada
Referencia cruzada a solicitud relacionada
Esta solicitud reivindica el beneficio de la solicitud estadounidense provisional n.º 60/967.859 presentada el 7 de septiembre de 2007.
Campo de la invención
Esta invención se refiere generalmente al campo de la medicina y, más específicamente, a compuestos y composiciones farmacéuticas que los comprenden, a usos y métodos para tratar el cáncer.
Antecedentes de la invención
Los miembros de la familia Hedgehog (Hh) de moléculas de señalización median muchos procesos importantes de formación de patrones de corto y largo alcance durante el desarrollo de invertebrados y vertebrados. La formación de patrones es la actividad mediante la cual las células embrionarias forman disposiciones espaciales ordenadas de tejidos diferenciados. Las proteínas Hedgehog se descubrieron por primera vez en Drosophila. Aunque existen algunas diferencias cruciales, los mecanismos de señalización generalmente están bien conservados entre Drosophila y organismos superiores. En la mosca, un único gen Hh regula el sistema de formación de patrones de discos segmentarios e imaginales. Por el contrario, en los vertebrados, una familia del gen Hh está implicada en el control de la asimetría izquierda-derecha, la polaridad en el SNC, somitas y extremidad, organogénesis, condrogénesis y espermatogénesis. Se han identificado tres homólogos de Hh en seres humanos: Sonic hedgehog (SHH) , Indian hedgehog (IHH) y Desert hedgehog (DHH) . La cascada de señalización Hh se inicia mediante la unión de Hh a las proteínas Patched (PTCH1 en seres humanos) en la célula diana. En ausencia del ligando Hh, PTCH1 reprime la actividad de Smoothened (SMO en seres humanos, Smo en ratón y smo en Drosophila) , una proteína similar a receptor acoplado a proteínas G (GPCR) . La señalización Hh en mamíferos requiere la presencia de cilios inmóviles en los que se ubican SMO y otros componentes de la ruta posterior para lograr la activación de los factores de transcripción GLI, los ortólogos de cubis interruptus (Ci) . Las formas del activador y represor de Ci en mamíferos están representados por tres proteínas de dedos de zinc independientes, funcionando GLI1 y GLI2 principalmente como activadores y GLI3 como represor. Para su revisión, véase Rubin L.L. et al. (2006) Nature Reviews, vol 5, 1026-1033. El mecanismo mediante el cual esta cascada de señalización regula la proliferación implica la activación de ciclinas y cinasas dependientes de ciclinas. El control de la diferenciación podría producirse mediante la producción de otras proteínas secretadas, incluyendo factores neurotróficos y angiogénicos.
Los esfuerzos de la química médica para identificar inhibidores de la ruta de Hh empezaron cuando Richard Keeler y colaboradores aislaron teratógenos a partir de Veratrum californicum en 1964. La investigación posterior estableció que el alcaloide conocido previamente, jervina, y el alcaloide descubierto recientemente, ciclopamina, podían inducir la ciclopía. Casi cuatro décadas después, se identificó el haz heptahelicoidal de Smo como el sitio de unión de ciclopamina usando su fotoafinidad y derivados fluorescentes. Chen, J. et al. (2002) Genes & Develop. 16: 2743-2748; Chen, J. et al. (2002) Proc. Natl. Acad. Sci. USA. 99: 14071-14076; Frank-Kamenetsky, M. et al. (2002)
J. Biol. 1, artículo 10. Se usan varios ensayos para seleccionar antagonistas para Smo in vitro. Uno de los ensayos para la selección de alto rendimiento examina la actividad global de la ruta de Hh en un contexto celular determinando el grado de actividad de la proteína GLI efectora posterior. Chen et al., citado anteriormente. Las líneas celulares de este tipo a menudo incorporan un indicador de luciferasa dependiente de GLI para la lectura del ensayo. La señal de luciferasa puede reforzarse mediante otras modificaciones mediante ingeniería genética, tales como la adición de Shh biológicamente activo, (por ejemplo, Shh con un resto octilo unido a su extremo N-terminal) ,
o la utilización de líneas celulares que carecen de la función PTCH1. Alternativamente, la unión directa a Smo puede medirse a través del desplazamiento de un derivado de ciclopamina fluorescente. Además, también pueden usarse modelos de xenoinjerto de tumor basándose en líneas SCLC, biliares, de próstata, pancreáticas y de meduloblastoma.
En los últimos años se estableció que la activación aberrante de la ruta de señalización de Hh puede conducir a cáncer. El síndrome de Gorlin (SG) , o síndrome de carcinoma basocelular nevoide, es una enfermedad genética autosómica dominante que se caracteriza por anomalías de desarrollo y la predisposición a tumores. Prácticamente todos los individuos con síndrome de Gorlin desarrollan carcinomas basocelulares (CBC) , habitualmente en múltiples sitios, y están predispuestos a otras clases de cáncer así como, especialmente meduloblastoma, un tumor de células progenitoras neuronales granulares cerebelosas, rabdomiosarcoma, un tumor muscular, así como fibromas y sarcomas de ovarios. Borzillo, G. et al. (2005) Curr. Topics en Med. Chem. 5: 147-157.
El CBC es el cáncer humano más común, siendo responsable de aproximadamente el 70% de los cánceres de piel en seres humanos, y representando al menos una tercera parte de todos los cánceres diagnosticados en los EE.UU. cada año. Más del 99% de los casos de CBC aparecen esporádicamente en la población, apareciendo sólo el 0, 5% de los casos en individuos con SG. El CBC casi nunca metastatiza, pero puede ser localmente agresivo y recurrente. Las mutaciones de inactivación en PTCH1 se producen de la manera más común en estos tumores. Un subconjunto de CBC se dirige mediante mutaciones en SMO, y estas mutaciones activan la ruta generando proteínas con una sensibilidad disminuida con respecto a la supresión de PTCH1.
El meduloblastoma (MB) es un tumor cerebral que se forma en el cerebelo de niños y adultos jóvenes, y puede ser el resultado final de defectos en la organogénesis cerebelosa. El MB, además del CBC, tiene una implicación bien reconocida en la ruta de Hh. El desenlace de este cáncer es casi invariablemente malo. La cirugía con radioterapia o
quimioterapia posterior aumenta la supervivencia hasta más del 50%, pero existe una grave morbimortalidad asociada con el tratamiento, incluyendo retraso mental. Se han sometido a prueba antagonistas de la ruta de Hh en cultivo celular y modelos de ratón de meduloblastoma. Se ha demostrado que una nueva clase de antagonistas de Hh de unión a SMO es muy potente. Berman C. M. et al. (2002) Science 297: 1559-1561.
Se ha implicado la ruta de Hh en muchos otros tipos de cáncer, incluyendo cáncer de páncreas, otros tumores del
tracto gastrointestinal (GI) y cáncer de próstata. Se ha mostrado de manera temprana la expresión anómala de SHH, PTCH1 y SMO en la formación de tumores de páncreas humanos. Thayer, S.P. et al. (2003) Nature 425: 313-317. Se encontró que varias líneas celulares de cáncer de páncreas eran positivas para PTCH1 y SMO y se inhibía su crecimiento in vitro por ciclopamina, sugiriendo un bucle autocrino activo a través del que las células tumorales tanto generan como responden al ligando de Hh. Además, el tratamiento sistémico con ciclopamina ralentizó el
crecimiento de tumores formados cuando se implantan estas líneas celulares en ratones inmunocomprometidos. Se realizaron observaciones similares para tumores de páncreas y otros tumores GI. Berman, D.M. et al. (2003) Nature
425: 846-851. También se proporcionaron datos similares para cáncer de próstata, incluyendo la sobreexpresión de SHH en biopsias tumorales, especialmente en tumores de grado Gleason superior, y efectos inhibidores in vitro e in vivo de ciclopamina sobre el crecimiento de líneas celulares de cáncer de próstata. La ruta de Hh se implicó además
en la metástasis de tumores de próstata, ya que la capacidad de las células AT6.3 para metastatizar al pulmón se suprimió completamente por la ciclopamina, y pudo inducirse la metástasis de AT2.1, un clon que casi nunca metastatiza, mediante la sobreexpresión de GLI1, de manera no sensible a ciclopamina.
Se ha demostrado recientemente que Hh puede estar implicado en el desarrollo de un subconjunto significativo de carcinoma de pulmón de células pequeñas (SCLC) . Watkins, D. N. et al. (2003)... [Seguir leyendo]
Reivindicaciones:
1. Compuesto de fórmula I
o una sal farmacéuticamente aceptable del mismo, en el que 5 A, B, C y D se seleccionan independientemente de CH o N, siempre que al menos uno pero no más de dos de A, B, C y D sea N, Cy1 es fenilo sustituido opcionalmente de manera independiente con 1-5 sustituyentes, en el que los 10 sustituyentes se seleccionan del grupo que consiste en alquilo C1-8, alquenilo C1-8, alquinilo C1-8, haloalquilo C1-6, halógeno, ciano, hidroxilo, oxo, -ORc, -NRaRb, NRaC (=O) Rb , -C (=O) ORc, -RcOC (=O) NRaRb, -RcOH, -C (=O) NRaRb , -OC (=O) NRaRb , -OC (=O) Rc , -NRaC (=O) Rc , -Rb (Ra) C (=O) Rc , -RbN (Ra) C (=O) ORc , -NRaS (=O) mRc, -S (=O) mNRaRb y S (=O) mRc; R1, R2, R3 y R4 se seleccionan independientemente cada uno de H, alquilo C1-6, cicloalquilo C1-6, haloalquilo C1-6, oxo, -C (=O) ORa, -RcOH, -ORc, -NRaRb, NRaC (=O) Rb , -C (=O) ORc , -C (=O) NRaRb , -OC (=O) Rc , -NRaC (=O) Rc, -NRaS (=O) mRc, -S (=O) mNRaRb y S (=O) mRc, siempre que al menos uno de R1, R2, R3 y R4 no 15 sea H; Ra, Rb y Rc se seleccionan independientemente cada uno de H, alquilo C1-8, alquenilo C1-8, alquinilo C1-8, haloalquilo C1-6, heterociclilo, arilo y heteroarilo; m es 1 ó 2; L es -C (=O) -o -S (=O) m-; 20 R5 es -NRaRb oCy2; Cy2 es un anillo monocíclico de 6 miembros parcial o totalmente saturado o insaturado formado por átomos de carbono que incluye opcionalmente 1-3 heteroátomos, estando el anillo sustituido opcionalmente de manera independiente con 1-5 sustituyentes, en el que los sustituyentes se seleccionan 25 independientemente del grupo que consiste en alquilo C1-8, alquenilo C1-8, alquinilo C1-8, haloalquilo C1-6, halógeno, ciano, hidroxilo, oxo, -C (=O) ORc, -RcOH, -ORc, -NRaRb, NRaC (=O) Rb, -C (=O) NRaRb, -OC (=O) Rc , -NRaC (=O) Rc, -NRaS (=O) mRc, -S (=O) mNRaRb y S (=O) mRc . 2. Compuesto según la reivindicación 1, representado por la fórmula IIo una sal farmacéuticamente del mismo.
3. Compuesto según la reivindicación 1, representado por la fórmula III
o una sal farmacéuticamente del mismo.
4. Compuesto según la reivindicación 1, representado por la fórmula IV
o una sal farmacéuticamente del mismo.
5. Compuesto según la reivindicación 1, representado por la fórmula V
o una sal farmacéuticamente del mismo.
6. Compuesto según la reivindicación 1, o una sal farmacéuticamente aceptable del mismo, en el que Cy1 es 10 fenilo no sustituido.
7. Compuesto según la reivindicación 1, o una sal farmacéuticamente aceptable del mismo, en el que Cy1 es fenilo sustituido independientemente con 1-5 sustituyentes, en el que los sustituyentes se seleccionan del grupo que consiste en alquilo C1-8, haloalquilo C1-6, halógeno, ciano, -ORc, -NRaRb, NRaC (=O) Rb, -C (=O) ORc, -RcOC (=O) NRaRb, -RcOH, -C (=O) NRaRb, -OC (=O) NRaRb, -OC (=O) Rc, -NRaC (=O) Rc,
- RbN (Ra) C (=O) Rc y-RbN (Ra) C (=O) ORc.
8. Compuesto según la reivindicación 1, o una sal farmacéuticamente aceptable del mismo, en el que R1, R2, R3 y R4 se seleccionan independientemente cada uno de H, alquilo C1-6 y haloalquilo C1-6, siempre que al menos uno de R1, R2, R3 y R4 no sea H.
9. Compuesto según la reivindicación 8, o una sal farmacéuticamente aceptable del mismo, en el que R1, R2, 20 R3 son cada uno H y R4 es alquilo C1-6.
10. Compuesto según la reivindicación 9, o una sal farmacéuticamente aceptable del mismo, en el que R4 is metilo.
11. Compuesto según la reivindicación 8, o una sal farmacéuticamente aceptable del mismo, en el que R1 yR3 son cada uno H, y R2 yR4 son cada uno independientemente alquilo C1-6.
12. Compuesto según la reivindicación 8, o una sal farmacéuticamente aceptable del mismo, en el que R2 yR4 son cada uno metilo.
13. Compuesto según la reivindicación 8, o una sal farmacéuticamente aceptable del mismo, en el que R1, R3 y R4 son cada uno H y R2 es alquilo C1-6
14. Compuesto según la reivindicación 8, o una sal farmacéuticamente aceptable del mismo, en el que R1, R2 y R4 son cada uno H y R3 es alquilo C1-6.
15. Compuesto según la reivindicación 8, o una sal farmacéuticamente aceptable del mismo, en el que R2, R3 y R4 son cada uno H y R1 es alquilo C1-6.
16. Compuesto según la reivindicación 8, o una sal farmacéuticamente aceptable del mismo, en el que R1 yR3 son cada uno independientemente alquilo C1-6, y R2 yR4 son cada uno H.
17. Compuesto según la reivindicación 1, o una sal farmacéuticamente aceptable del mismo, en el que L es -C (=O) -.
18. Compuesto según la reivindicación 1, o una sal farmacéuticamente aceptable del mismo, en el que L es -S (=O) 2-.
19. Compuesto según la reivindicación 1, o una sal farmacéuticamente aceptable del mismo, en el que L es -S (=O) -.
20. Compuesto según la reivindicación 1, o una sal farmacéuticamente aceptable del mismo, en el que R5 es Cy2.
21. Compuesto según la reivindicación 20, o una sal farmacéuticamente aceptable del mismo, en el que Cy2 es fenilo sustituido opcionalmente de manera independiente con 1-5 sustituyentes, en el que los sustituyentes se seleccionan del grupo que consiste en alquilo C1-8, alquenilo C1-8, alquinilo C1-8, haloalquilo C1-6, halógeno, ciano, hidroxilo, oxo, -C (=O) ORc, -RcOH, -ORc, -NRaRb, NRaC (=O) Rb, -C (=O) NRaRb, -OC (=O) Rc, -NRaC (=O) Rc, -NRaS (=O) mRc, -S (=O) mNRaRb y S (=O) mRc.
22. Compuesto según la reivindicación 21, o una sal farmacéuticamente aceptable del mismo, en el que Cy2 es fenilo no sustituido.
23. Compuesto según la reivindicación 20, o una sal farmacéuticamente aceptable del mismo, en el que Cy2 es ciclohexilo sustituido opcionalmente de manera independiente con 1-5 sustituyentes, en el que los sustituyentes se seleccionan del grupo que consiste en alquilo C1-8, alquenilo C1-8, alquinilo C1-8, haloalquilo C1-6, halógeno, ciano, hidroxilo, oxo, -C (=O) ORc, -RcOH, -ORc, -NRaRb, NRaC (=O) Rb, -C (=O) NRaRb, -OC (=O) Rc, -NRaC (=O) Rc, -NRaS (=O) mRc, -S (=O) mNRaRb y S (=O) mRc.
24. Compuesto según la reivindicación 20, o una sal farmacéuticamente aceptable del mismo, en el que Cy2 es piperidilo sustituido opcionalmente de manera independiente con 1-5 sustituyentes, en el que los sustituyentes se seleccionan del grupo que consiste en alquilo C1-8, alquenilo C1-8, alquinilo C1-8, haloalquilo C1-6, halógeno, ciano, hidroxilo, oxo, -C (=O) ORc, -RcOH, -ORc, -NRaRb, NRaC (=O) Rb, -C (=O) NRaRb, -OC (=O) Rc, -NRaC (=O) Rc, -NRaS (=O) mRc, -S (=O) mNRaRb y S (=O) mRc.
25. Compuesto según la reivindicación 24, o una sal farmacéuticamente aceptable del mismo, en el que el piperidilo no está sustituido.
26. Compuesto según la reivindicación 20, o una sal farmacéuticamente aceptable del mismo, en el que Cy2 es morfolinilo sustituido opcionalmente de manera independiente con 1-5 sustituyentes, en el que los sustituyentes se seleccionan del grupo que consiste en alquilo C1-8, alquenilo C1-8, alquinilo C1-8, haloalquilo C1-6, halógeno, ciano, hidroxilo, oxo, -C (=O) ORc, -RcOH, -ORc, -NRaRb, NRaC (=O) Rb, -C (=O) NRaRb, -OC (=O) Rc, -NRaC (=O) Rc, -NRaS (=O) mRc, -S (=O) mNRaRb y S (=O) mRc.
27. Compuesto según la reivindicación 20, o una sal farmacéuticamente aceptable del mismo, en el que Cy2 es tetrahidro-2H-piranilo sustituido opcionalmente de manera independiente con 1-5 sustituyentes, en el que los sustituyentes se seleccionan del grupo que consiste en alquilo C1-8, alquenilo C1-8, alquinilo C1-8, haloalquilo C1-6, halógeno, ciano, hidroxilo, oxo, -C (=O) ORc, -RcOH, -ORc, -NRaRb, NRaC (=O) Rb, -C (=O) NRaRb, -OC (=O) Rc, -NRaC (=O) Rc, -NRaS (=O) mRc, -S (=O) mNRaRb y S (=O) mRc.
28. Compuesto según la reivindicación 1, en el que el compuesto se selecciona del grupo que consiste en:
(S) - (2-metil-4- (1-fenilpirido[3, 4-d]piridazin-4-il) piperazin-1-il) (fenil) metanona, (S) - (2-metil-4- (1- (4- (trifluorometil) fenil) pirido[3, 4-d]piridazin-4-il) piperazin-1-il) (fenil) metanona, (S) - (2-metil-4- (1- (4- (trifluorometil) fenil) pirido[3, 4-d]piridazin-4-il) piperazin-1-il) (piperidin-1-il) metanona, (S) - (4- (1- (4- (hidroximetil) fenil) pirido[3, 4-d]piridazin-4-il) -2-metilpiperazin-1-il) (piperidin-1-il) metanona, Carbamato de (S) - (4- (4- (3-metil-4- (piperidin-1-carbonil) piperazin-1-il) pirido[3, 4-d]piridazin-1-il) fenil) metilo, ( (R) -4- (1- (4-cloro-2-fluorofenil) pirido[3, 4-d]piridazin-4-il) -3-metilpiperazin-1-il) (fenil) metanona, (R) - (4, 4-difluorociclohexil) (3-metil-4- (1-fenilpirido[3, 4-d]piridazin-4-il) piperazin-1-il) metanona, (R) -ciclohexil (3-metil-4- (1-fenilpirido[3, 4-d]piridazin-4-il) piperazin-1-il) metanona, ( (R) -4- (1- (4-cloro-2-fluorofenil) pirido[3, 4-d]piridazin-4-il) -3-metilpiperazin-1-il) (ciclohexil) metanona, (R) - (3-metil-4- (1- (4- (trifluorometil) fenil) pirido[3, 4-d]piridazin-4-il) piperazin-1-il) (fenil) metanona, (R) - (3-metil-4- (1-fenilpirido[3, 4-d]piridazin-4-il) piperazin-1-il) (fenil) metanona, ( (1S, 4S) -4-hidroxiciclohexil) ( (R) -3-metil-4- (1-fenilpirido[3, 4-d]piridazin-4-il) piperazin-1-il) metanona, ( (1R, 4R) -4-hidroxiciclohexil) ( (R) -3-metil-4- (1-fenilpirido[3, 4-d]piridazin-4-il) piperazin-1-il) metanona, (R) - (3-metil-4- (4-fenilpirido[4, 3-d]piridazin-1-il) piperazin-1-il) (fenil) metanona, (R) - (3-metil-4- (1-fenilpirido[4, 3-d]piridazin-4-il) piperazin-1-il) (tetrahidro-2H-piran-4-il) metanona, (S) - (3-metil-4- (1-fenilpirido[3, 4-d]piridazin-4-il) piperazin-1-il) (fenil) metanona, (S) - (4, 4-difluorociclohexil) (3-metil-4- (1-fenilpirido[3, 4-d]piridazin-4-il) piperazin-1-il) metanona, (R) - (3-metil-4- (1-fenilpirido[3, 4-d]piridazin-4-il) piperazin-1-il) (morfolino) metanona, (R) -N, 3-dimetil-N-fenil-4- (1-fenilpirido[3, 4-d]piridazin-4-il) piperazin-1-carboxamida, (R) - (3-metil-4- (1-fenilpirido[3, 4-d]piridazin-4-il) piperazin-1-il) (piperidin-1-il) metanona, (R) -N, N, 3-trimetil-4- (1-fenilpirido[3, 4-d]piridazin-4-il) piperazin-1-carboxamida, (R) - (4, 4-difluoropiperidin-1-il) (3-metil-4- (1-fenilpirido[3, 4-d]piridazin-4-il) piperazin-1-il) metanona, (4, 4-difluorociclohexil) ( (2S, 5R) -2, 5-dimetil-4- (1-fenilpirido[3, 4-d]piridazin-4-il) piperazin-1-il) metanona, (4, 4-difluorociclohexil) ( (2R, 5S) -2, 5-dimetil-4- (1-fenilpirido[3, 4-d]piridazin-4-il) piperazin-1-il) metanona, (S) - (4, 4-difluoropiperidin-1-il) (2-metil-4- (1- (4- (trifluorometil) fenil) pirido[3, 4-d]piridazin-4-il) piperazin-1-il)
metanona,
(4- (4- (4- (4, 4-difluorociclohexanocarbonil) -3-metilpiperazin-1-il) pirido[3, 4-d]piridazin-1-il) fenil) metilcarbamato de (S) -metilo, (S) -N- ( (4- (4- (4- (4, 4-difluorociclohexanocarbonil) -3-metilpiperazin-1-il) pirido[3, 4-d]piridazin-1-il) fenil) metil)
acetamida,
Carbamato de (S) - (4- (4- (4- (4, 4-difluorociclohexanocarbonil) -3-metilpiperazin-1-il) pirido[3, 4-d]piridazin-1-il) fenil) metilo, (R) - (4, 4-difluorociclohexil) (3-metil-4- (1- (4- (trifluorometil) fenil) pirido[3, 4-d]piridazin-4-il) piperazin-1-il)
metanona, (R) - (3-metil-4- (1- (4- (trifluorometoxi) fenil) pirido[3, 4-d]piridazin-4-il) piperazin-1-il) (fenil) metanona, (R) -4- (4- (4- (4, 4-difluorociclohexanocarbonil) -2-metilpiperazin-1-il) pirido[3, 4-d]piridazin-1-il) benzonitrilo, (R) -4- (4- (4-benzoil-2-metilpiperazin-1-il) pirido[3, 4-d]piridazin-1-il) benzonitrilo, (R) -4- (4- (4-benzoil-2-metilpiperazin-1-il) pirido[3, 4-d]piridazin-1-il) benzamida, (R) - (4- (1- (4-fluorofenil) pirido[3, 4-d]piridazin-4-il) -3-metilpiperazin-1-il) (fenil) metanona, (R) - (4- (1- (4- (hidroximetil) fenil) pirido[3, 4-d]piridazin-4-il) -3-metilpiperazin-1-il) (fenil) metanona, (S) - (2-metil-4- (5-fenilpirido[2, 3-d]piridazin-8-il) piperazin-1-il) (fenil) metanona, (R) - (3-metil-4- (5-fenilpirido[2, 3-d]piridazin-8-il) piperazin-1-il) (fenil) metanona, (R) - (3-metil-4- (8-fenilpirido[3, 2-d]piridazin-5-il) piperazin-1-il) (fenil) metanona, (R) - (4- (5- (4- (hidroximetil) fenil) pirido[2, 3-d]piridazin-8-il) -3-metilpiperazin-1-il) (fenil) metanona,
( (R) -4- (5- (4-cloro-2-fluorofenil) pirido[2, 3-d]piridazin-8-il) -3-metilpiperazin-1-il) (fenil) metanona, (R) - (3-metil-4- (5- (4- (trifluorometil) fenil) pirido[2, 3-d]piridazin-8-il) piperazin-1-il) (fenil) metanona, (R) -4- (8- (4-benzoil-2-metilpiperazin-1-il) pirido[2, 3-d]piridazin-5-il) benzonitrilo, y (R) - (3-metil-4- (8- (4- (trifluorometil) fenil) pirido[3, 2-d]piridazin-5-il) piperazin-1-il) (fenil) metanona,
o una sal farmacéuticamente aceptable de los mismos.
29. Composición farmacéutica que comprende un compuesto según la reivindicación 1 ó 28, o una sal farmacéuticamente aceptable del mismo y un vehículo farmacéuticamente aceptable.
30. Compuesto según la reivindicación 1, o una sal farmacéuticamente aceptable del mismo, para su uso en el tratamiento de cáncer o angiogénesis, o para su uso en la reducción del flujo sanguíneo en un tumor en un sujeto.
31. Uso de un compuesto según la reivindicación 1, o una sal farmacéuticamente aceptable del mismo, para la preparación de un medicamento para tratar cáncer o angiogénesis, o para reducir el flujo sanguíneo en un tumor en un sujeto.
32. Compuesto para su uso o uso según la reivindicación 30 ó 31, en el que el cáncer es cáncer de páncreas, carcinoma basocelular, meduloblastoma, síndrome de Gorlin, cáncer de próstata o carcinoma de pulmón.
Patentes similares o relacionadas:
Formas cristalinas de 6-((6,7-dimetoxiquinazolin-4-il)oxi)-N,2-dimetilbenzofuran-3-carboxamida, del 29 de Julio de 2020, de Hutchison Medipharma Limited: Forma I de 6-((6,7-dimetoxiquinazolin-4-il)oxi)-N,2-dimetilbenzofuran-3-carboxamida, en donde el difractograma de rayos X de polvo de la Forma […]
Compuestos y procedimientos de uso, del 29 de Julio de 2020, de Medivation Technologies LLC: Un compuesto de fórmula (Aa-1): **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, en la que: A representa H, halógeno, amino, […]
Complejos de agentes terapéuticos de base vírica y poli(beta-amino-ésteres) modificados, del 29 de Julio de 2020, de Sagetis Biotech, SL: Un complejo de un agente terapéutico de base vírica con un polímero de fórmula I: **(Ver fórmula)** donde cada L1 y L2 están seleccionados […]
Compuestos de alquinilbenceno heterocíclicos, y composiciones médicas y usos de los mismos, del 29 de Julio de 2020, de Guangzhou Healthquest Pharma Co., Ltd: Un compuesto de alquinilbenceno heterocíclico que tiene la fórmula (I) y una sal farmacéuticamente aceptable, o estereoisómero del mismo, **(Ver […]
 Composiciones y métodos para el tratamiento de trastornos de células plasmáticas y trastornos prolinfocíticos de células b, del 29 de Julio de 2020, de Knopp Biosciences LLC: Una composición que comprende una cantidad terapéuticamente eficaz de dexpramipexol para su uso en el tratamiento de un trastorno de células B caracterizado por niveles elevados […]
Composiciones y métodos para el tratamiento de trastornos de células plasmáticas y trastornos prolinfocíticos de células b, del 29 de Julio de 2020, de Knopp Biosciences LLC: Una composición que comprende una cantidad terapéuticamente eficaz de dexpramipexol para su uso en el tratamiento de un trastorno de células B caracterizado por niveles elevados […]
Derivados de piperidina 1,4 sustituidos, del 29 de Julio de 2020, de 89Bio Ltd: Un compuesto de acuerdo con la Fórmula I: **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, en donde: A se selecciona de […]
Profármacos de gemcitabina, del 29 de Julio de 2020, de NuCana plc: Una formulación farmacéutica que comprende gemcitabina-[fenil-benzoxi-L-alaninil)]-(S)-fosfato 3: **(Ver fórmula)** o una sal o solvato […]
Utilización de anticuerpos optimizados en ADCC para tratar a los pacientes con bajo nivel de respuesta, del 22 de Julio de 2020, de LABORATOIRE FRANCAIS DU FRACTIONNEMENT ET DES BIOTECHNOLOGIES: Utilización de una composición de anticuerpo monoclonal quimérico, humanizado o humano de isotipo IgG1 anti- Rhesus del glóbulo rojo humano cuya […]