PROCEDIMIENTO PARALA EXPANSION INDIFERENCIADA U ORIENTADA A LINAJE MIELOIDE DE CELULAS MADRE HEMATOPOYETICAS PROCEDENTES DE SANGRE DE CORDONUMBILICAL, SANGRE PERIFERICA MOVILIZADA O MEDULA OSEA.
Procedimiento para la expansión indiferenciada u orientada a linaje mieloide de células madre hematopoyéticas (CMH).
Más específicamente, la presente invención se refiere a un procedimiento de expansión de CMH a partir de la sangre del cordón umbilical, médula ósea o sangre periférica movilizada. Dicho procedimiento comprende las etapas de cultivo de expansión a volumen constante de las células CDS4+ purificadas, cultivo de expansión a volumen variable de dichas células y el acondicionamiento de las células CD34+ para el trasplante. Con este procedimiento se genera de forma reproducible, robusta y segura la dosis de CMH indiferenciadas u orientadas a linaje mieloide necesarias para su uso clínico
Tipo: Patente de Invención. Resumen de patente/invención. Número de Solicitud: P200930939.
Solicitante: BANC DE SANG I TEIXITS.
Nacionalidad solicitante: España.
Provincia: BARCELONA.
Inventor/es: CAIRO BADILLO,JORDI JOAN, GARCIA LOPEZ,JOAN, PLA CALVET,ARNAU, CASAMAYOR GENESCA,ALBA.
Fecha de Solicitud: 2 de Noviembre de 2009.
Fecha de Publicación: .
Fecha de Concesión: 11 de Enero de 2011.
Clasificación Internacional de Patentes:
- C12N5/06B11P
Clasificación PCT:
- C12N5/0789 QUIMICA; METALURGIA. › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › C12N 5/00 Células no diferenciadas humanas, animales o vegetales, p. ej. líneas celulares; Tejidos; Su cultivo o conservación; Medios de cultivo para este fin (reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00). › Células madre; Células progenitoras multipotentes.
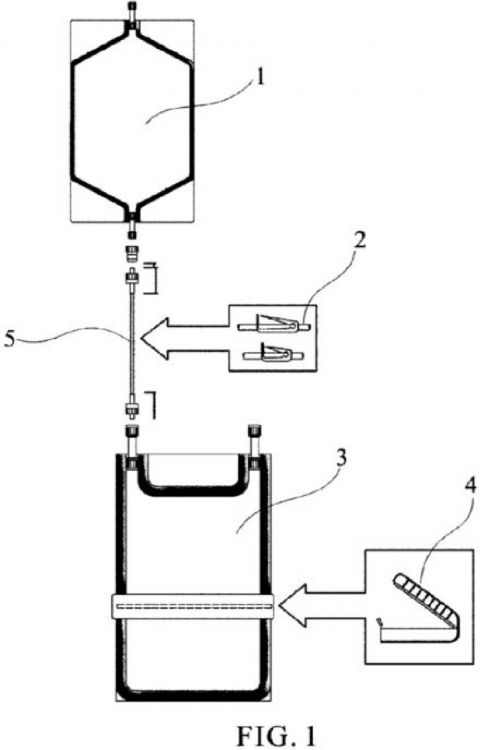
Fragmento de la descripción:
Procedimiento para la expansión indiferenciada u orientada a linaje mieloide de células madre hematopoyéticas procedentes de sangre de cordón umbilical, sangre periférica movilizada o médula ósea.
La presente invención se refiere a un procedimiento aplicable para la expansión in vitro indiferenciada u orientada a linaje mieloide de células madre hematopoyéticas (CMH). Dicho procedimiento comprende las etapas de expansión a volumen constante de las células madre purificadas, expansión a volumen variable de dichas células y el acondicionamiento de las células para el trasplante. Con este procedimiento es posible expandir de forma reproducible y robusta las CMH hasta alcanzar dosis clínicamente significativas o bien de células inmaduras u orientadas a linaje mieloide de una manera rápida y segura.
Las CMH son células multipotenciales capaces, mediante un complejo proceso de autorenovación y diferenciación, de mantener la homeostasis del órgano hematopoyético dando lugar, de forma exquisitamente regulada, a todos los linajes celulares de la sangre. Estos linajes se organizan en dos grandes grupos con funcionalidades distintas: mieloides y linfoides. Los mieloides agrupan a: monocitos, macrófagos, neutrófilos, basófilos, eosinófilos, que combaten las infecciones en el organismo; los megacariocitos (plaquetas), que participan del proceso de coagulación de la sangre, así como los eritrocitos, transportan el oxígeno a los tejidos. El otro gran grupo de células sanguíneas son las linfoides compuesto por: células B, células T y NK, que se ocupan de la vigilancia inmunológica.
El trasplante autólogo o alogénico de CMH representa una importante alternativa terapéutica para enfermedades hematológicas como las neoplasias, inmunodeficiencias primarias y desordenes metabólieos. Las principales fuentes para el trasplante terapéutico de CMH son: la médula ósea (MO), la sangre periférica movilizada (SPM) y la sangre de cordón umbilical (SCU). Históricamente, la médula ósea ha representado la fuente principal de células madre para el trasplante de pacientes pediátricos y adultos. No obstante, la dificultad de encontrar donantes compatibles y el riesgo de sufrir la enfermedad del injerto contra el huésped asociado al trasplante alogénico, ha limitado su aplicabilidad. Problemática que la MO comparte con la sangre periférica movilizada. En respuesta a esta problemática, y como fuentes alternativas a la MO y SPM, se pueden utilizar para transplante hematopoyético las CMH procedentes de sangre de cordón umbilical. Esta fuente de CMH presenta una serie de importantes ventajas con respecto a la MO y SPM, tales como el menor grado de correspondencia del complejo mayor histocompatibilidad de HLA donante-receptor necesario, la menor incidencia de la enfermedad del donante contra el huésped y la gran disponibilidad de unidades almacenadas en los bancos de cordón de todo el mundo, lo que facilita la rápida localización de potenciales donantes (Barker y otros Searching for unrelated donor hematopoietic stem cells: availability and speed of umbilical cord blood versus bone marrow. Biol Blood Marrow Trasplant. 2002; 8:257-260).
La mayor desventaja en el trasplante de SCU es la baja dosis celular disponible de CMH por unidad respecto a las disponibles en SMP y MO. Esta particularidad se traduce en un mayor riesgo de fallo del trasplante y elevados tiempos de aplasia mieloide, que dejan al paciente expuesto a contraer infecciones potencialmente mortales. Esta problemática limita la utilización de las CMH de SCU básicamente al trasplante pediátrico. La cantidad de CMH disponibles para el trasplante es, por tanto, un parámetro crítico. El mejor parámetro de predicción para la supervivencia y recuperación de los parámetros hematológicos normales en pacientes pediátricos y adultos es la dosis celular (Barker y otros Serious infections after unrelated donor trasplantation in 136 children: impact of stem cell source. Biol Blood Marrow Trasplant. 2005; 11:362-370).
Diversos estudios realizados con CMH de SPM y MO han permitido establecer una dosis mínima requerida en función de la fuente celular que se ha fijado en 2x106 células por kilo de paciente en MO y de 3-5x106 células por kilo de paciente para SMP (Heimfeld y otros HLA-identical stem cell transplantation: is there an optimal CD34 cell dose?. Bone Marrow Transplantation 2003; 31:839-845).
Estos resultados sugieren que las metodologías para expandir las células madre/progenitoras hematopoyéticas de SCU supondrían una mejora notable en las alternativas terapéuticas disponibles. Existen varias estrategias prometedoras disponibles para la expansión in vitro de las CMH con diferentes sistemas (Cabrita y otros, Hematopoietic stem cells from the bone to the reactor. Trends in Biotechnology 2003; 21:223-240) pero de momento en ensayos clínicos realizados estas metodologías no han demostrado mejoras destacables en las recuperaciones hematológicas respecto a las unidades de SCU no expandidas.
La principal limitación que presentan muchas de las expansiones in vitro es la escasa dosis obtenida de células madre/progenitoras con funcionalidad adecuada.
Uno de los principales problemas del cultivo in vitro de las CMH es el bloqueo de la capacidad de crecimiento de dichas células. Este bloqueo se produce como consecuencia de la acumulación en el medio de cultivo de biomoléculas liberadas por las propias CMH y las células maduras presentes en el cultivo. Estas biomoléculas producen la detención del ciclo de las CMH bloqueando la expansión o la diferenciación al hacerlas entrar en quiescencia.
La presente invención da a conocer un procedimiento de cultivo in vitro de CMH cuya estrategia se fundamenta en mantener la concentración de las biomoléculas solubles responsables de la detención del crecimiento de las CMH en la fase G0/G1 por debajo de su nivel de acción, a base de realizar adiciones puntuales de medio fresco. De esta forma, se puede inducir y mantener el crecimiento de CMH de sangre de cordón umbilical a un ritmo aproximadamente constante durante toda la duración del cultivo.
Esta particularidad permite controlar y manipular el factor de expansión (células finales/células iniciales) para la población de interés, lo que facilita adaptar dicho factor de expansión en función de la dosis celular requerida para la terapia.
Otro aspecto adicional del procedimiento de la presente invención es que dicha expansión no se produce a costa de agotar la subpoblación de CMH más primitivas, que son de gran interés terapéutico, ya que su número se mantiene constante a lo largo del procedimiento. Por otro lado, el procedimiento de la presente invención, variando los factores de crecimiento empleados, permite realizar una expansión madurativa de las CMH que facilita la obtención de productos destinados a terapia celular en base a células en distintos estadios de diferenciación de linajes mieloide. Dichas células son aplicables en deficiencias del sistema inmunológico.
Otras ventajas adicionales son que el procedimiento es robusto, reproducible y que es extremadamente sencillo, tanto en equipamiento como en manipulación. El procedimiento de la presente invención es aplicable a la expansión indiferenciada o madurativa de células CMH a partir de sangre del cordón umbilical, médula ósea y de sangre periférica movilizada.
Descripción detallada de la invención
En consecuencia, un objetivo de la presente invención es dar a conocer un procedimiento para la expansión in vitro indiferenciada u orientada a linaje mieloide de CMH a partir de sangre de cordón umbilical, médula ósea o sangre periférica movilizada. Este procedimiento está caracterizado porque comprende las etapas de:
a) Expansión a volumen constante, en la que se siembran células CD34+, anteriormente purificadas por técnicas estándares conocidas en el estado de la técnica, tales como la selección positiva mediante perlas paramagnéticas conjugadas con anticuerpos contra CD34+, en un medio de cultivo sintético adecuado disponible comercialmente en el mercado, suplementado con factores de crecimiento: TPO, FLT3, SCF, IL-6 en caso de expansión indiferenciada de CMH o bien SCF, IL3, G-CSF en caso de expansión madurativa a linaje mieloide durante 4 días. El volumen inicial de la etapa a volumen constante es función de la disponibilidad de células procedentes de la purificación inicial de las células CD34+. El volumen final en la etapa de expansión a volumen...
Reivindicaciones:
1. Procedimiento para la expansión indiferenciada u orientada a linaje mieloide de células madre hematopoyéticas procedentes de sangre de cordón umbilical, sangre periférica movilizada o médula ósea, caracterizado porque comprende las etapas de:
a) Expansión a volumen constante, en la que se siembran células CD34+, anteriormente purificadas por técnicas estándares conocidas en el estado de la técnica, tales como la selección positiva mediante perlas paramagnéticas conjugadas con anticuerpos contra CD34+, en un medio de cultivo sintético adecuado disponible comercialmente en el mercado, suplementado con factores de crecimiento: TPO, FLT3, SCF, IL-6 en caso de expansión indiferenciada de CMH o bien SCF, IL3, G-CSF en caso de expansión madurativa a linaje mieloide durante 4 días. El volumen inicial de la etapa a volumen constante es función de la disponibilidad de células procedentes de la purificación inicial de las células CD34+. El volumen final en la etapa de expansión a volumen constante también estará en dependencia de la densidad de siembra inicial.
b) Expansión a volumen variable: en el día 4 del cultivo se añade medio fresco suplementado con factores de crecimiento: TPO, FLT3, SCF y IL-6, en caso de expansión indiferenciada de CMH o bien SCF, IL-3 y G-CSF en caso de expansión madurativa a linaje mieloide a una concentración de entre 5 y 100 ng/ml a la bolsa de cultivo hasta duplicar el volumen anterior contenido en la bolsa. Se repite dicha operación los días 6, 8, 10, 12, 14, 16 y 18. El cultivo se detiene a los 20 días.
2. Procedimiento, según la reivindicación 1, en el que en la etapa de expansión a volumen constante se siembran de 100.000 a 1.000.000 de células CD34+ por mi de medio de cultivo.
3. Procedimiento, según las reivindicaciones 1 y 2, en el que la concentración de factores de crecimiento TPO, FLT3, SCF, IL-6 en el medio de cultivo es de entre 5 y 100 ng/ml.
4. Procedimiento, según cualquiera de las reivindicaciones anteriores, en el que a los 20 días de cultivo la tasa de expansión de la población CD34+ es de, como mínimo, 200 veces.
Patentes similares o relacionadas:
COMPOSICIONES PARA LA DERIVACIÓN CULTIVO IN VITRO DE LÍNEAS DE CÉLULAS MADRE EMBRIONARIAS (ES) CON CAPACIDAD DE TRANSMISIÓN DE LA LÍNEA GERMINAL Y PARA EL CULTIVO DE CÉLULAS MADRE ADULTAS, del 4 de Julio de 2011, de THROMBOGENICS N.V.: Un método para obtener, mantener o hacer crecer células madre embrionarias pluripotentes de roedor que comprenden la etapa de cultivar las células durante al menos […]
MEDIO DE CULTIVO CELULAR Y PROCEDIMIENTO DE CULTIVO DE CÉLULAS MADRE Y CÉLULAS PROGENITOR, del 15 de Febrero de 2011, de UNIVERSITÄT LEIPZIG: Utilización de un medio de cultivo celular que contiene menos de 500 mg/l de glucosa y menos de 500 µg/l de inositol, que comprende un medio basal suministrado como una solución […]
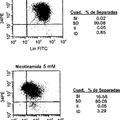 EXPANSION DE POBLACIONES DE CELULAS MADRE RENOVABLES, del 23 de Agosto de 2010, de GAMIDA CELL LTD: Un método de expansión de una población de células madre hematopoyéticas ex vivo, mientras al mismo tiempo, se inhibe sustancialmente la diferenciación de dichas […]
EXPANSION DE POBLACIONES DE CELULAS MADRE RENOVABLES, del 23 de Agosto de 2010, de GAMIDA CELL LTD: Un método de expansión de una población de células madre hematopoyéticas ex vivo, mientras al mismo tiempo, se inhibe sustancialmente la diferenciación de dichas […]
PROCEDIMIENTO DE OBTENCION DE CELULAS MADRE MESENQUIMALES CON CAPACIDAD PLURIPOTENTE, del 26 de Julio de 2010, de FUNDACION PROGRESO Y SALUD: El objeto de la presente invención es un procedimiento de obtención de células madre mesenquimales con capacidad pluripotente que utiliza sangre […]
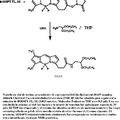 BODIPY AMINOACETALDEHIDO DIETIL ACETAL, del 26 de Julio de 2010, de DUKE UNIVERSITY: Compuesto de fórmula
BODIPY AMINOACETALDEHIDO DIETIL ACETAL, del 26 de Julio de 2010, de DUKE UNIVERSITY: Compuesto de fórmula
 POLIPEPTIDOS LIGANDOS PARA SELECTINA-E/SELECTINA-L DE LA CELULA HEMATOPOYETICA Y METODOS DE UTILIZACION DE LOS MISMOS, del 12 de Mayo de 2010, de THE BRIGHAM AND WOMEN'S HOSPITAL, INC.: Un polipéptido glucosilado sustancialmente purificado, dicho polipéptido glucosilado comprende un eje polipéptido CD44 en el que dicho polipéptido glucosilado […]
POLIPEPTIDOS LIGANDOS PARA SELECTINA-E/SELECTINA-L DE LA CELULA HEMATOPOYETICA Y METODOS DE UTILIZACION DE LOS MISMOS, del 12 de Mayo de 2010, de THE BRIGHAM AND WOMEN'S HOSPITAL, INC.: Un polipéptido glucosilado sustancialmente purificado, dicho polipéptido glucosilado comprende un eje polipéptido CD44 en el que dicho polipéptido glucosilado […]
 METODO Y APARATO PARA MANTENIMIENTO Y EXPASION DE CELULAS MADRE HEMOPOYETICAS Y/O CELULAS PROGENITORAS, del 7 de Mayo de 2010, de TECHNION RESEARCH & DEVELOPMENT FOUNDATION LTD.: Un método para expandir/mantener ex-vivo células madre hemopoyéticas no diferenciadas o células progenitoras, comprendiendo el método las etapas de:
(a) cultivar en […]
METODO Y APARATO PARA MANTENIMIENTO Y EXPASION DE CELULAS MADRE HEMOPOYETICAS Y/O CELULAS PROGENITORAS, del 7 de Mayo de 2010, de TECHNION RESEARCH & DEVELOPMENT FOUNDATION LTD.: Un método para expandir/mantener ex-vivo células madre hemopoyéticas no diferenciadas o células progenitoras, comprendiendo el método las etapas de:
(a) cultivar en […]
Espumas de fibroína de seda inyectables y usos de la misma, del 1 de Abril de 2020, de TRUSTEES OF TUFTS COLLEGE: Un aplicador de inyección que comprende una composición inyectable, la composición inyectable comprende una espuma de fibroína de seda comprimida que tiene […]