PROCEDIMIENTO PARA LA OBTENCION DE CELULAS MADRE MESENQUIMALES A PARTIR DE LA FRACCION MONONUCLEAR DE LA MEDULA OSEA HUMANA.
Procedimiento para la obtención de células madre mesenquimales a partir de la fracción mononuclear de la médula ósea humana.
La presente invención se refiere a un procedimiento de obtención de células madre mesenquimales a partir de la fracción mononuclear de células de médula ósea humana que utiliza como suplemento suero humano del tipo AB. Dicho procedimiento comprende las etapas de obtención de dicha fracción mononuclear de médula ósea, la etapa de recuperación y pre-expansión de las células madre mesenquimales, y la etapa de expansión de las células madres mesenquimales hasta la obtención de la dosis clínica necesaria para su uso terapéutico
Tipo: Patente de Invención. Resumen de patente/invención. Número de Solicitud: P200900005.
Solicitante: BANC DE SANG I TEIXITS.
Nacionalidad solicitante: España.
Provincia: BARCELONA.
Inventor/es: GODIA CASABLANCAS,FRANCESC, CAIRO BADILLO,JORDI JOAN, GARCIA LOPEZ,JOAN, RODRIGUEZ GOMEZ,LUCIANO, PLA CALVET,ARNAU.
Fecha de Solicitud: 2 de Enero de 2009.
Fecha de Publicación: .
Fecha de Concesión: 1 de Marzo de 2010.
Clasificación Internacional de Patentes:
- C12N5/06B21P
Clasificación PCT:
- C12N5/0775 QUIMICA; METALURGIA. › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › C12N 5/00 Células no diferenciadas humanas, animales o vegetales, p. ej. líneas celulares; Tejidos; Su cultivo o conservación; Medios de cultivo para este fin (reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00). › Células madre mesenquimales; Células madre derivadas de tejido adiposo.
Fragmento de la descripción:
Procedimiento para la obtención de células madre mesenquimales a partir de la fracción mononuclear de la médula ósea humana.
La presente invención se refiere a un procedimiento para la obtención de células madre mesenquimales. Más específicamente, la presente invención se refiere a un procedimiento de obtención de células madre mesenquimales a partir de la fracción mononuclear de células de médula ósea humana. Dicho procedimiento comprende las etapas de obtención de dicha fracción mononuclear de médula ósea, la etapa de recuperación y pre-expansión de las células madre mesenquimales, y la etapa de expansión de las células madres mesenquimales hasta la obtención de la dosis clínica necesaria para su posible uso terapéutico.
Las células madre mesenquimales (CMM) son células multipotentes, que han mostrado su eficacia en el tratamiento de lesiones musculoesqueléticas y en el mejoramiento de la función cardiaca en enfermedades cardiovasculares (Le Blanc K., Pittenger M. Mesenchymal stem cells: progress toward promise. Cytotherapy 2005;7:36-45). Las CMM pueden ser aisladas de varios tejidos de adultos, entre los que se encuentran la médula ósea, tejido adiposo y sangre del cordón umbilical. Además, dichas células pueden ser expandidas ex vivo.
La fracción de mononuclear médula ósea (CMN) se obtiene mediante una operación de separación basada en la centrifugación de sangre proveniente de la médula ósea. La CMN es un conjunto heterogéneo de células, entre las que se pueden encontrar, además de las células madre mesenquimales, las células hematopoyéticas progenitoras. Estas dos poblaciones se encuentran en una concentración muy baja respecto a las células hematopoyéticas maduras, también presentes en las CMN.
Fridenshtein y otros (Fridenshtein A. J., Deriglazova U. F., Kulagina N. N. et al. Precursors for fibroblasts in different populations of hematopoietic cells as detected by the in vitro colony assay method. Exp. Hematol. 1974 Vol. 2. P. 83-92) obtuvieron por primera vez células madre mesenquimales a partir de médula ósea, basándose en la capacidad de las células madre mesenquimales para adherirse a superficies plásticas, propiedad que no poseen la mayoría de las células hematopoyéticas. La desventaja de este método es el bajo rendimiento obtenido en la recuperación de células mesenquimales atribuible a la baja prevalencia de este tipo celular en la médula ósea, que se estima entre el 0,001 al 0,01% (Alhadlag A and Mao J. Mesenchymal Stem Cells: Isolation and Therapeutics. Stem Cells and Development. 2004. 13: 436-448 (3). Sin embargo, la adhesión a plásticos se ha establecido como punto de partida para seguir mejorando los métodos de obtención de células madre mesenquimales.
Heynesworth y otros han logrado obtener células madre mesenquimales con una alta capacidad de adherencia, elevada tasa de proliferación y el mantenimiento de la multipotencialidad durante un período de tiempo largo (Heynesworth S. E., Goshima J., Goldberg V. M., Calplan A. I. Characterization of cells with osteogenic potential from the human bone marrow//Bone. 1995. Vol. 13. P. 81-85.) utilizando suero fetal bovino como suplemento del medio de cultivo. La desventaja de este método consiste en que el hecho de que la búsqueda de un lote adecuado para el cultivo de las células y el análisis correspondiente del suero fetal bovino conlleva mucho tiempo y es muy trabajoso. Además, debido a la gran variación lote a lote que presenta el suero fetal bovino, no es posible garantizar la reproducibilidad de los resultados.
Otra desventaja de este método es que para obtener las cantidades suficientes de células madres mesenquimales para su uso clínico, las células deben ser cultivadas entre 4 y 6 semanas, e incluso en algunas circunstancias, tales como en pacientes con enfermedades del metabolismo óseo, el tiempo de cultivo puede ser superior. La razón por la que se necesitan estos tiempos tan elevados de cultivo, como se ha mencionado anteriormente, es la poca cantidad de células mesenquimales que es posible obtener de la médula ósea.
Un periodo largo de cultivo celular puede aumentar el riesgo de contaminación y aumenta considerablemente los costes de mantenimiento del cultivo. Además, a medida que aumenta el número de duplicaciones se corre el riesgo de que las células pierdan multipotencialidad o entren en senescencia, lo que compromete su capacidad terapéutica.
La metodología utilizada habitualmente para buscar una disminución de los tiempos de cultivo de células mesenquimales centra su atención en factores tales como los suplementos del medio de cultivo, el tipo de superficie plástica, la dosis de siembra y los medios de cultivo empleados (Sotiropolou PA, Pérez SA, Salagianni M, Baxevanis CN, Papamichail M. Characterization of the optimal culture conditions for clinical scale production of human mesenchymal stem cells. Stem Cells 2006; 24: 462-471).
Un objetivo de la presente invención es dar a conocer un procedimiento de cultivo ex vivo de células madre mesenquimales a partir de médula ósea humana en el que se reduce el tiempo y el número de duplicaciones necesarias para la obtención de la dosis clínica de células madres mesenquimales, cuando se compara con los métodos tradicionales. Este procedimiento se basa en el efecto sinérgico a partir de combinar unas condiciones muy específicas de aislamiento de células mesenquimales a partir de la fracción mononuclear de médula ósea, con la utilización de suero humano del grupo sanguíneo AB como suplemento del medio de cultivo. Este se usa en sustitución de costoso y poco reproducible suero fetal bovino. Además, el suero AB humano presenta las ventajas de ser más económico y tener mayor reproducibilidad que el suero fetal bovino. A su vez, las condiciones de aislamiento propuestas facilitan la recuperación de un mayor número de células mesenquimales de la fracción mononuclear con respecto a las condiciones utilizadas en las estrategias convencionales. Este hecho es de especial relevancia si se tiene en cuenta que cuando más elevado sea el número inicial de células mesenquimales aisladas disponibles menor es el tiempo y recursos necesarios para la obtención de la dosis clínica requerida.
Dichas condiciones de aislamiento se han obtenido mediante el estudio sistemático de la influencia sobre la recuperación de células mesenquimales a partir del inóculo y el tiempo de lavado de las células mononucleares de médula ósea en medios de cultivo suplementados con suero humano AB.
Otro objetivo de la presente invención es proporcionar un procedimiento que permita disponer de una copia idéntica de seguridad de las células madres mesenquimales, que poseen las mismas características de las células madre mesenquimales iniciales en cuanto a capacidad de proliferación y diferenciación.
El procedimiento de la presente invención puede ser aplicado para la obtención de células mesenquimales provenientes de otras fuentes, tales como tejido adiposo, páncreas, hígado, músculo esquelético, dermis, membrana sinovial, hueso trabecular, sangre de cordón umbilical, tejido pulmonar, pulpa dental y ligamento periodontal. En el caso que la fuente de células mesenquimales sea diferente a la médula ósea, el tratamiento inicial de la muestra será diferente, adecuándose para cada tipo celular que se utilice como fuente.
Descripción detallada de la invención
En consecuencia, un objetivo de la presente invención es dar a conocer un procedimiento para la obtención de células madre mesenquimales a partir de la fracción mononuclear de médula ósea humana, obtenida mediante centrifugación en gradiente de densidad, caracterizado porque comprende las etapas de:
a) Recuperación y pre expansión de las células madre mesenquimales, mediante un cultivo primario, en el que las células mononucleares de médula ósea se siembran en medio de cultivo DMEM suplementado con suero AB humano (10%) siguiendo el siguiente esquema de cultivo:
b) Cultivo secundario: resiembra de las células mononucleares lavadas en (a) en medio de cultivo suplementado...
Reivindicaciones:
1. Procedimiento para la obtención de células madre mesenquimales a partir de la fracción mononuclear de médula ósea humana obtenida mediante centrifugación en gradiente de densidad, caracterizado porque comprende las etapas de:
a) Recuperación y pre expansión de las células madre mesenquimales, mediante un cultivo primario, en el que las células mononucleares de médula ósea se siembran en medio de cultivo DMEM suplementado con suero AB humano (10%) siguiendo el siguiente esquema de cultivo:
b) Cultivo secundario: resiembra de las células mononucleares lavadas en (a) en medio de cultivo suplementado con suero AB humano (10%) siguiendo el siguiente esquema de cultivo:
c) Cultivo de expansión: expansión de las células mesenquimales asiladas en (a) a los 12 días. Se resiembran y expanden estas células en medio de cultivo suplementado con suero AB humano (10%) siguiendo el siguiente esquema de cultivo:
2. Procedimiento, según cualquiera de las reivindicaciones anteriores, en el que la cantidad de células mononucleares de médula ósea inoculadas en la etapa (a) es de entre 200 000 y 400 000 células por centímetro cuadrado de superficie.
3. Procedimiento, según cualquiera de las reivindicaciones anteriores, en el que la cantidad de células madre mesenquimales inoculadas en la etapa (b) es de entre 3 000 y 5 000 células por centímetro cuadrado de superficie.
4. Procedimiento, según cualquiera de las reivindicaciones anteriores, en el que en el cultivo primario de la etapa (a) se obtienen entre 15.106 y 20.106 células madre mesenquimales.
5. Procedimiento, según cualquiera de las reivindicaciones anteriores, en el que en el cultivo secundario (etapa (b)) se obtienen entre 3.106 y 6.106 células madre mesenquimales.
6. Procedimiento, según cualquiera de las reivindicaciones anteriores, en el que la pureza de las células madre mesenquimales obtenidas en el cultivo primario de la etapa (a) es de 80%.
7. Procedimiento, según cualquiera de las reivindicaciones anteriores, en el que la pureza de las células madre mesenquimales obtenidas en el cultivo secundario (etapa (b)) es de 65%.
8. Procedimiento, según cualquiera de las reivindicaciones anteriores, en el que en la etapa (c) se obtienen entre 40.106 y 50.106 de células madre mesenquimales.
9. Procedimiento, según cualquiera de las reivindicaciones anteriores, en el que el número de duplicaciones celulares se encuentra entre 6 y 8.
10. Procedimiento, según cualquiera de las reivindicaciones anteriores, en el que el tiempo total de obtención de las células madre mesenquimales no sobrepasa los 21 días.
11. Procedimiento, según cualquiera de las reivindicaciones anteriores, en el que el cultivo secundario (etapa (b)) se congela y se mantiene como copia de seguridad.
12. Uso del suero humano AB como suplemento del medio de cultivo en la obtención de células madre mesenquimales para uso terapéutico.
Patentes similares o relacionadas:
MICROCÁPSULAS ESFÉRICAS O NO ESFÉRICAS QUE COMPRENDEN PÉPTIDOS GLP-1, SU PRODUCCIÓN Y SU USO, del 17 de Agosto de 2011, de BIOCOMPATIBLES UK LIMITED: Microcápsula esférica que comprende como mínimo un revestimiento superficial y un núcleo, en la que el como mínimo un revestimiento superficial comprende […]
CÉLULAS PROGENITORAS PROCEDENTES DE LA GELATINA DE WHARTON DE CORDÓN UMBILICAL HUMANO, del 3 de Febrero de 2011, de DAVIES, JOHN E. SARUGASER, RAHUL BAKSH, DOLORES HOSSEINI, MORRIS LICKORISH, ANTONY DAVID SUTTON: Un procedimiento para obtener una población de células progenitoras humanas, que comprende la etapa de extraer dicha población de la gelatina de Wharton
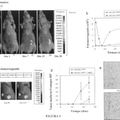 MODELO ANIMAL DE ANGIOGENESIS HUMANA Y SUS APLICACIONES, del 2 de Febrero de 2011, de UNIVERSIDAD AUTONOMA DE MADRID: La presente invención se relaciona con un modelo animal de angiogénesis humana para la monitorización cuantitativa y no invasiva de dicho proceso de angiogénesis in vivo mediante […]
MODELO ANIMAL DE ANGIOGENESIS HUMANA Y SUS APLICACIONES, del 2 de Febrero de 2011, de UNIVERSIDAD AUTONOMA DE MADRID: La presente invención se relaciona con un modelo animal de angiogénesis humana para la monitorización cuantitativa y no invasiva de dicho proceso de angiogénesis in vivo mediante […]
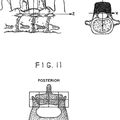 REGENERACION E INCREMENTO DE HUESO UTILIZANDO CELULAS MADRE MESENQUIMALES, del 2 de Diciembre de 2009, de OSIRIS THERAPEUTICS, INC.: SE PRESENTAN COMPOSICIONES Y METODOS PARA ACRECENTAR LA FORMACION DE HUESOS A BASE DE ADMINISTRAR CELULAS MADRE MESENQUIMATOSAS HUMANAS AISLADAS (HMSCS) CON UN MATERIAL […]
REGENERACION E INCREMENTO DE HUESO UTILIZANDO CELULAS MADRE MESENQUIMALES, del 2 de Diciembre de 2009, de OSIRIS THERAPEUTICS, INC.: SE PRESENTAN COMPOSICIONES Y METODOS PARA ACRECENTAR LA FORMACION DE HUESOS A BASE DE ADMINISTRAR CELULAS MADRE MESENQUIMATOSAS HUMANAS AISLADAS (HMSCS) CON UN MATERIAL […]
 CELULAS MADRE MESENQUIMALES COMO VEHICULOS PARA LA TRANSFERENCIA DE CANALES IONICOS EN ESTRUCTURAS SINCITIALES, del 30 de Noviembre de 2009, de THE TRUSTEES OF COLUMBIA UNIVERSITY IN THE CITY OF NEW YORK
THE RESEARCH FOUNDATION OF STATE UNIVERSITY OF NEW YORK: Una composición que comprende una célula madre mesenquimal en la que se ha introducido un ácido nucleico que codifica un canal de HCN en una cantidad suficiente […]
CELULAS MADRE MESENQUIMALES COMO VEHICULOS PARA LA TRANSFERENCIA DE CANALES IONICOS EN ESTRUCTURAS SINCITIALES, del 30 de Noviembre de 2009, de THE TRUSTEES OF COLUMBIA UNIVERSITY IN THE CITY OF NEW YORK
THE RESEARCH FOUNDATION OF STATE UNIVERSITY OF NEW YORK: Una composición que comprende una célula madre mesenquimal en la que se ha introducido un ácido nucleico que codifica un canal de HCN en una cantidad suficiente […]
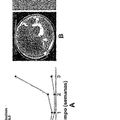 POBLACIONES DE CELULAS PROGENITORAS, EXPANSION DE LAS MISMAS Y CRECIMIENTO DE TIPOS DE CELULAS NO HEMATOPOYETICAS Y TEJIDOS PROVENIENTES DE LAS MISMAS, del 13 de Noviembre de 2009, de BAKSH, DOLORES
DAVIES, JOHN E.
ZANDSTRA, PETER: Método para expandir células progenitoras no hematopoyéticas humanas, comprendiendo dicho método la etapa de someter una población de células […]
POBLACIONES DE CELULAS PROGENITORAS, EXPANSION DE LAS MISMAS Y CRECIMIENTO DE TIPOS DE CELULAS NO HEMATOPOYETICAS Y TEJIDOS PROVENIENTES DE LAS MISMAS, del 13 de Noviembre de 2009, de BAKSH, DOLORES
DAVIES, JOHN E.
ZANDSTRA, PETER: Método para expandir células progenitoras no hematopoyéticas humanas, comprendiendo dicho método la etapa de someter una población de células […]
Función promotora del crecimiento del cabello de células madre de tamaño pequeño y uso de las mismas, del 6 de Mayo de 2020, de MEDIPOST, CO., LTD.: Una composición para su uso en la terapia de pérdida de cabello para prevenir la pérdida de cabello y estimular el crecimiento del cabello, que comprende: células […]
Terapia con células madre basada en células madre procedentes de tejido adiposo, del 6 de Mayo de 2020, de RIGSHOSPITALET: Una composición que comprende una suspensión de una población sustancialmente homogénea e inmunosupresora de células madre procedentes de tejido adiposo (ASC) humanas adultas […]