PREPARACIÓN PARA MARCAR POR TIEMPO LIMITADO LOS SITIOS DE BIOPSIA.
Uso de un material que se puede eliminar de un sitio en el interior del cuerpo de una paciente de mama de la cual se ha extraído una muestra de tejido y caracterizado por:
(i) permanecer presente en el sitio en una cantidad suficiente para permitir la detección y localización del sitio durante al menos 2 semanas después de su introducción, y (ii) eliminarse suficientemente del sitio como para no interferir con la visualización en diagnóstico por imágenes del tejido adyacente del sitio de cinco a ocho meses después de la introducción del mismo, como un marcador detectable para marcar dicho sitio en el interior del cuerpo de la paciente de mama
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2000/002004.
Solicitante: SENORX, INC..
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 3 MORGAN IRVINE, CA 92618 ESTADOS UNIDOS DE AMERICA.
Inventor/es: LUBOCK, PAUL, BURBANK, FRED, H., JONES, MICHAEL, L., FORCIER, NANCY.
Fecha de Publicación: .
Fecha Solicitud PCT: 26 de Enero de 2000.
Fecha Concesión Europea: 13 de Octubre de 2010.
Clasificación Internacional de Patentes:
- A61B19/00R
- A61K49/00P8
- A61M37/04
Clasificación PCT:
- A61K49/00 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › Preparaciones para examen in vivo.
Clasificación antigua:
- A61K49/00 A61K […] › Preparaciones para examen in vivo.
Países PCT: Austria, Bélgica, Suiza, Alemania, Dinamarca, España, Francia, Reino Unido, Grecia, Italia, Liechtensein, Luxemburgo, Países Bajos, Suecia, Mónaco, Portugal, Irlanda, Eslovenia, Finlandia, Rumania, Chipre, Lituania, Letonia, Ex República Yugoslava de Macedonia, Albania.
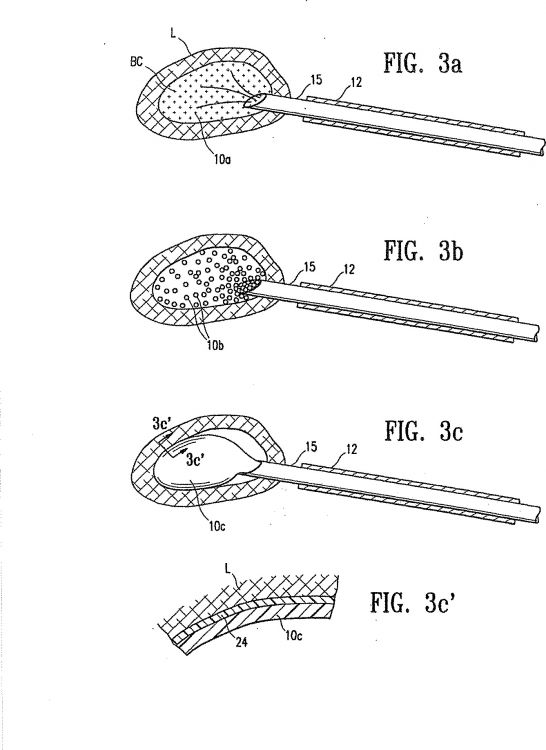
Fragmento de la descripción:
CAMPO DE LA INVENCIÓN
La presente invención pertenece de forma general al campo de la medicina y de la cirugía, y más particularmente a un material que puede utilizarse para marcar la ubicación desde la cual se ha extraído una muestra de tejido, de forma tal que puedan llevarse a cabo tratamientos posteriores (por ejemplo, extirpación quirúrgica, radioterapia, terapia con drogas, etc.) de forma precisa en esa ubicación.
ANTECEDENTES DE LA INVENCIÓN
A. Uso de biopsias de tejido en la medicina y cirugía moderna
En la práctica médica moderna, a menudo se extraen pequeñas muestras de tejido, conocidas como muestras de biopsia, de tumores, lesiones, órganos, músculos y otros tejidos del cuerpo. Tal extracción de muestras de tejido puede llevarse a cabo mediante técnicas de cirugía abierta (es decir, extracción de una pequeña muestra de tejido a través de una pequeña incisión quirúrgica utilizando una anestesia local), o a través del uso de un instrumento de biopsia especializado, tal como una aguja de biopsia. Después de la extracción de las muestras de tejido, éstas son sometidas de manera típica a pruebas o exámenes de diagnóstico tales como: a) examen macroscópico y microscópico para determinar la citología y / o histología, b) análisis bioquímicos para determinar la presencia o ausencia de sustancias químicas que indican ciertos estados de enfermedad, c) cultivo microbiológico para determinar la presencia de bacterias u otros microbios, y / o d) otros procedimientos diagnósticos. La información obtenida a partir de estas pruebas y / o exámenes diagnósticos puede utilizarse entonces para realizar o confirmar un diagnóstico y/o para formular planes de tratamiento para el paciente.
B. Consideraciones especiales en relación con la biopsia de cánceres de mama
Aproximadamente una de cada nueve mujeres en América desarrollará cáncer de mama en algún momento de su vida. En la actualidad, el cáncer de mama es el cáncer más común en las mujeres, y es la segunda causa de muerte por cáncer en las mujeres. El examen físico periódico de las mamas es importante para la detección precoz de lesiones potencialmente cancerosas. Adicionalmente, los estudios especializados con rayos X, conocidos como mamografías, son una herramienta comprobada para el diagnóstico del cáncer de mama en mujeres de más de 40 años de edad. La mamografía también es considerada por muchos profesionales médicos como beneficiosa para el diagnóstico en mujeres más jóvenes. En la mamografía, la mama es comprimida entre dos placas mientras se toman imágenes especializadas con rayos X.
Si se encuentra una masa anormal en la mama mediante examen físico o mamografía, puede utilizarse el ultrasonido para determinar si la masa es un tumor sólido o un quiste lleno de fluido. Las lesiones quísticas generalmente son benignas y el diagnóstico de una lesión quística se confirma a menudo mediante aspiración con una aguja del fluido procedente del interior del quiste. (Debería notarse, sin embargo, que la aspiración con aguja de lesiones quísticas es diferente a la “biopsia con aguja” de masas sólidas, como se plantea de aquí en adelante). Sin embargo, las masas sólidas normalmente son sometidas a algún tipo de biopsia de tejido para determinar si la masa es cancerosa.
Si una masa o lesión sólida es suficientemente grande como para ser palpable (es decir, detectada mediante exploración con la yema de los dedos) puede extraerse de la masa una muestra de tejido mediante una variedad de técnicas, incluyendo, pero no limitada a, biopsia por cirugía abierta o una técnica conocida como Biopsia por Aspiración con Aguja Fina (BAAF). En la biopsia por cirugía abierta se hace una incisión y se extrae una cantidad de tejido de la masa para un subsiguiente examen histopatológico. En el procedimiento BAAF se aspira una pequeña muestra de células de la masa a través de una aguja y las células aspiradas son sometidas después a examen citológico.
Si una masa sólida de la mama es pequeña y no palpable (por ejemplo, del tipo encontrado de manera típica por medio de mamografía), puede utilizarse un procedimiento de biopsia relativamente nuevo conocido como “biopsia estereotáctica con aguja”. En la ejecución de una biopsia estereotáctica con aguja de una mama, la paciente yace sobre una mesa de biopsia especial con su mama comprimida entre las placas de un aparato de mamografía y se toman dos imágenes con rayos X digitales separadas desde dos puntos de vista ligeramente diferentes. Un ordenador calcula la posición exacta de la lesión en coordenadas X e Y así como la profundidad de la lesión en el interior de la mama. Después de esto, se programa un aparato mecánico estereotáctico con la información de coordenadas y profundidad calculadas por el ordenador, y se utiliza dicho aparato para avanzar la aguja de biopsia de forma precisa hacia la pequeña lesión. Dependiendo del tipo de aguja(s) de biopsia utilizada(s), esta técnica estereotáctica puede utilizarse para obtener muestras citológicas (obtenidas por medio de BAAF) y / o muestras histológicas (obtenidas mediante biopsia central con aguja). Normalmente se obtienen por lo menos cinco muestras de biopsia separadas de ubicaciones alrededor de la pequeña lesión así como una del centro de la lesión.
1) tiempo de demora potencial entre la biopsia y el comienzo de la cirugía u otro tratamiento
Para algunos tipos de biopsia (diferentes de las lesiones de mama), pueden ser preparadas “secciones congeladas” de las muestras de biopsia por un patólogo y tales secciones congeladas pueden utilizarse para llegar a un diagnóstico razonablemente exacto en unos minutos desde la extracción de la muestra de biopsia. Tales secciones congeladas son preparadas congelando rápidamente el tejido, cortando el tejido en secciones de espesor aproximadamente mayor que 10 micrómetros y montando las secciones sobre portaobjetos de vidrio para un examen microscópico inmediato por parte de un patólogo. Las secciones congeladas de este tipo no son utilizadas de manera típica para biopsias de lesiones de mama debido a que la sección congelada habitual es demasiado gruesa para una visualización y diagnosis definitiva de los tipos de células encontrados en tumores de mama. En cambio, las muestras de biopsia de mama son preparadas normalmente para un examen histopatológico mediante una técnica sin congelación más tradicional en la cual la muestra de tejido es sumergida en una solución fijadora química (por ejemplo, formol, glutaraldehído, etc.) durante un período de tiempo suficiente para producir una unión cruzada de las proteínas del tejido conectivo presentes en el tejido, el tejido fijado es cortado en secciones delgadas de aproximadamente 8 micrómetros de espesor, las secciones de tejido son colocadas sobre portaobjetos y se aplican tinturas histológicas selectivas de células para teñir el tejido antes del examen microscópico. Esta técnica de preparación del tejido sin congelación requiere de manera típica por lo menos 24 – 48 horas para completarse y, como consecuencia, el diagnóstico del patólogo de la lesión de mama puede no estar disponible hasta 24 a 72 horas después de que la muestra de biopsia ha sido extraída de la mama. De este modo, por estas razones, el examen y diagnóstico histopatológico de las lesiones de mama puede consumir mucho más tiempo que el examen y diagnóstico histopatológico de otro tipo de lesiones. Después de esto, si una lesión de mama ha sido diagnosticada como cancerosa, la paciente puede requerir algún tiempo (por ejemplo, de varios días a más de una semana) para considerar cada una de las opciones quirúrgicas disponibles para ella, buscar segundas opiniones y tomar una decisión sobre el tratamiento. Las opciones quirúrgicas disponibles para las lesiones cancerosas de la mama incluyen varios grados de mastectomía o lumpectomía. Más aún, en algunos casos, dependiendo de la histología (tipo de cáncer), grado (cuán agresivo parece bajo el microscopio), estadio (cuán grande es el cáncer y cuán lejos se ha extendido), y pronósticos o información predictiva adicionales, los médicos pueden recomendar que se realice alguna terapia de radiación
o quimioterapia antes de proceder con la lumpectomía quirúrgica.
2) Marca de los sitios de biopsia para facilitar la subsiguiente ubicación y tratamiento de la lesión
Con el fin de dirigir al oncólogo cirujano o radiólogo en el tratamiento quirúrgico
Reivindicaciones:
1. Uso de un material que se puede eliminar de un sitio en el interior del cuerpo de una paciente de mama de la cual se ha extraído una muestra de tejido y caracterizado por:
(i) permanecer presente en el sitio en una cantidad suficiente para permitir la detección y localización del sitio durante al menos 2 semanas después de su introducción, y
(ii) eliminarse suficientemente del sitio como para no interferir con la visualización en diagnóstico por imágenes del tejido adyacente del sitio de cinco a ocho meses después de la introducción del mismo, como un marcador detectable para marcar dicho sitio en el interior del cuerpo de la paciente de mama.
2. El uso de la Reivindicación 1, en el cual el marcador es inicialmente un marcador visible en diagnóstico por imágenes y permanece visible en diagnóstico por imágenes en el sitio durante por lo menos dos semanas, pero se elimina suficientemente del sitio después del período de dos semanas, de forma tal que el marcador no interfiere con el diagnóstico por imágenes del tejido adyacente al sitio de cinco a ocho meses después de la introducción del mismo.
3. El uso de la Reivindicación 2, en el cual el marcador es detectable mediante métodos de diagnóstico por imágenes elegidos de un grupo consistente en rayos X, fluoroscopia, mamografía, tomografía computarizada, imagen por resonancia magnética, ultrasonidos, Doppler, detector de radiación y combinaciones de los mismos, durante por lo menos dos semanas desde su introducción.
4. El uso de la Reivindicación 1, en el cual el marcador es detectable visualmente.
5. El uso de la Reivindicación 4, en el cual el marcador detectable visualmente es una sustancia coloreada elegida del grupo consistente en una tinta, un colorante, partículas colorantes, carbón y combinaciones de los mismos.
6. El uso de la Reivindicación 1, en el cual el marcador se elimina del sitio por disolución, biodistribución, biodegradación y / o metabolismo local.
7. El uso de la Reivindicación 1, en el cual el marcador detectable comprende un material detectable que interferirá con el diagnóstico por imágenes de los tejidos adyacentes al mismo y que permanecerá presente en el sitio en una cantidad suficiente para permitir la localización del sitio mediante diagnóstico por imágenes hasta dicho primer momento de tiempo, pero que se eliminará suficientemente del sitio como para no interferir con el diagnóstico por imágenes del tejido adyacente al sitio en dicho segundo momento de tiempo.
8. El uso de la Reivindicación 1, en el cual el marcador detectable comprende una cantidad de material detectable que, si se introduce solo en el sitio, se eliminará del sitio de forma tal que ya no estará presente en el sitio una cantidad detectable del marcador a las dos semanas después de la introducción de dicho marcador detectable; y un recubrimiento retardador de la eliminación sobre el material detectable que retarda la eliminación de dicho material desde el sitio, de forma tal que
(i) permanece presente en el sitio una cantidad detectable de dicho material durante por lo menos dos semanas desde la introducción en el sitio, y (ii) dicho material se elimina suficientemente del sitio como para permitir el diagnóstico por imágenes del tejido adyacente al sitio sin interferencia de dicho marcador detectable en cinco a ocho meses desde la introducción en el sitio.
9. El uso de la Reivindicación 8, en el cual el material detectable es un compuesto químico que tiene una constante de solubilidad de menos de 1x10-3 gramos cada 100 centímetros cúbicos de agua.
10. El uso de la Reivindicación 9, en el cual dicho compuesto químico es elegido del grupo consistente en AgCl, AgI; BaCO3; BaSO4; K; CaCO3; ZnO; Al2O3, y combinaciones de los mismos.
11. El uso de la Reivindicación 8, en el cual el material detectable es elegido del grupo consistente en AgNO3, sales de amoníaco, sales de sodio, sales de potasio, aceite etiodizado, iohexol, isopamidol, gas, lípidos, aceite, y combinaciones de los mismos.
12. El uso de la Reivindicación 8, en el cual el recubrimiento de retardo de eliminación es elegido entre el ácido poliláctico, el ácido poliglicólico, la policaprolactona, un material encapsulante colágeno, colágeno renaturalizado, gelatina, gelatina renaturalizada y gelatina con los enlaces cruzados.
13. El uso de la Reivindicación 1, en el cual el marcador detectable comprende un material que es detectable por medios radiográficos de diagnóstico por imágenes, por medios sonográficos de diagnóstico por imágenes o por medios magnéticos de diagnóstico por imágenes.
14. El uso de la Reivindicación 1, en el cual el marcador detectable comprende un polvo seco, una esponja, una suspensión o una lechada.
15. El uso de la Reivindicación 1, en el cual el marcador detectable comprende un material colagenoso o gelatinoso que tiene materia visible en diagnóstico por imágenes de forma radiográfica unida al mismo.
16. El uso de la Reivindicación 15, en el cual el material colagenoso o gelatinoso del marcador comprende colágeno o gelatina renaturalizados.
17. El uso de la Reivindicación 16, en el cual el material colagenoso o gelatinoso también tiene los enlaces cruzados de forma covalente.
18. El uso de la Reivindicación 15, en el cual la materia visible en diagnóstico por imágenes de forma radiográfica comprende iones de metal o un gas.
19. El uso de la Reivindicación 15, en el cual el material colagenoso o gelatinoso del marcador comprende colágeno o gelatina renaturalizados y la materia visible en diagnóstico por imágenes de forma radiográfica del marcador comprende iones de metal que son unidos a dicho colágeno o gelatina renaturalizados.
20. El uso de la Reivindicación 19, en el cual los iones de metal son iones de plata. 21. El uso de la Reivindicación 19, mediante un proceso que comprende: en el cual el marcador es preparado 5 a) la obtención de una cantidad de material colagenoso desnaturalizado; b) la renaturalización del material colagenoso o gelatinoso; y c) la unión de los iones de metal al material colagenoso renaturalizado. o o gelatinoso gelatinoso 10 22. El uso de la Reivindicación 18, mediante un proceso que comprende: en el cual el marcador es preparado 15 a) la obtención de una cantidad de material colagenoso o desnaturalizado; b) la renaturalización del material colagenoso o gelatinoso; y c) la dispersión de un gas a través del material colagenoso o renaturalizado. gelatinoso gelatinoso
Patentes similares o relacionadas:
DISPOSITIVO DE CANULA PARA REALIZAR UN IMPLANTE, del 8 de Agosto de 2011, de Acino AG: 1. Dispositivo de cánula para realizar un implante caracterizado porque comprende:un extremo proximal que está previsto para introducirse en […]
DISPOSITIVO PARA LA ADMINISTRACION DE PREPARACIONES SOLIDAS., del 1 de Julio de 1996, de SUMITOMO PHARMACEUTICALS COMPANY, LIMITED NISSHO CORPORATION: SE PRESENTA UN DISPOSITIVO PARA LA ADMINISTRACION DE PREPARACIONES SOLIDAS O SEMISOLIDAS A UN ORGANISMO DE FORMA SUBCUTANEA. EL EQUIPO COMPRENDE UNA JERINGUILLA […]
DISPOSITIVO PARA INSERTAR ELEMENTOS IMPLANTABLES EN ANIMALES A EFECTOS DE INTRODUCIR MEDICAMENTOS EN SUS CUERPOS., del 31 de Enero de 1984, de ELI LILLY AND COMPANY: DISPOSITIVO PARA INSERTAR ELEMENTOS IMPLANTABLES EN ANIMALES, A EFECTOS DE INTRODUCIR MEDICAMENTOS EN SUS CUERPOS. COMPRENDE UN RECIPIENTE DE ELEMENTOS […]
"PERFECCIONAMIENTOS EN DISPOSITIVOS IMPLANTADORES CON CARGADOR DE IMPLANTES PARA ANIMALES"., del 1 de Junio de 1983, de SYNTEX INC.: DISPOSITIVO INTRODUCTOR DE FARMACOS EN LOS ANIMALES. CONSTA DE UN ALOJAMIENTO CON UNA PARTE ANTERIOR , POSICION POSTERIOR Y PARTE INTERMEDIA […]
PERFECCIONAMIENTOS EN APARATOS IMPLANTADORES DE MASAS SOLIDAS DE MATERIAL PARA EL TRATAMIENTO DE ANIMALES., del 1 de Octubre de 1978, de AMERICAN CYANAMID COMPANY: Perfeccionamientos en aparatos implantadores de masas sólidas de material para el tratamiento de animales, cuyas masas de forma cilíndrica, para implantar al menos […]
MÉTODO Y APARATO PARA LA FABRICACIÓN DE FÉRULAS QUIRÚRGICAS ORTOGNÁTICAS, del 1 de Diciembre de 2011, de BOARD OF REGENTS THE UNIVERSITY OF TEXAS SYSTEM: Un método para la formación de un modelo compuesto computarizado de la estructura ósea y la dentición de un paciente, caracterizado por: colocar una pluralidad […]
CABEZAL DE DETECCIÓN PREOPERATORIO ADECUADO PARA SER ACOPLADO A UNA HERRAMIENTA DE EXÉRESIS, del 31 de Agosto de 2011, de CENTRE NATIONAL DE LA RECHERCHE SCIENTIFIQUE: Sonda peroperatoria para guiar una herramienta de exéresis, que comprende un cabezal de detección , comprendiendo dicho cabezal de detección: […]
 DISPOSITIVO MEJORADO PARA MARCAR TEJIDOS CON PRECISIÓN, del 4 de Abril de 2011, de FOGARTY, THOMAS J.: Un dispositivo de localización de tejido que comprende: al menos un elemento localizador adaptado para penetrar en el tejido, teniendo el elemento localizador […]
DISPOSITIVO MEJORADO PARA MARCAR TEJIDOS CON PRECISIÓN, del 4 de Abril de 2011, de FOGARTY, THOMAS J.: Un dispositivo de localización de tejido que comprende: al menos un elemento localizador adaptado para penetrar en el tejido, teniendo el elemento localizador […]