MODULACIÓN DE NIVELES DE EXPRESIÓN DE TRPV.
Uso de una dosis farmacéuticamente eficaz de ANsi dirigido frente a TRPV1 en la preparación de un fármaco para su uso en el tratamiento de un estado ocular caracterizado por un aumento de la expresión y/o actividad de TRPV1,
en el que dicho fármaco se administra por vía tópica a la superficie de la córnea
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/GB2006/050342.
Solicitante: SYLENTIS S.A.U.
Nacionalidad solicitante: España.
Inventor/es: BELMONTE MARTINEZ,CARLOS, GALLAR MARTINEZ,JUANA, ACOSTA BOJ,Maria del Carmen, SESTO YAGUE,Angela, JIMÉNEZ GÓMEZ,Maria Concepción, JIMÉNEZ ANTÓN,Ana Isabel.
Fecha de Publicación: .
Fecha Solicitud PCT: 20 de Octubre de 2006.
Clasificación Internacional de Patentes:
- A61K31/713 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › Acidos nucleicos u oligonucleótidos con estructura en doble hélice.
- C12N15/113E
Clasificación PCT:
- A61K31/713 A61K 31/00 […] › Acidos nucleicos u oligonucleótidos con estructura en doble hélice.
- A61P17/14 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › A61P 17/00 Medicamentos para el tratamiento de problemas dermatológicos. › para la calvicie o para la alopecia.
- A61P27/02 A61P […] › A61P 27/00 Medicamentos para tratar los trastornos de los sentidos. › Agentes oftálmicos.
- C12N15/11 QUIMICA; METALURGIA. › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › C12N 15/00 Técnicas de mutación o de ingeniería genética; ADN o ARN relacionado con la ingeniería genética, vectores, p. ej. plásmidos, o su aislamiento, su preparación o su purificación; Utilización de huéspedes para ello (mutantes o microorganismos modificados por ingeniería genética C12N 1/00, C12N 5/00, C12N 7/00; nuevas plantas en sí A01H; reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00; nuevas razas animales en sí A01K 67/00; utilización de preparaciones medicinales que contienen material genético que es introducido en células del cuerpo humano para tratar enfermedades genéticas, terapia génica A61K 48/00; péptidos en general C07K). › Fragmentos de ADN o de ARN; sus formas modificadas (ADN o ARN no empleado en tecnología de recombinación C07H 21/00).
Países PCT: Austria, Bélgica, Suiza, Alemania, Dinamarca, España, Francia, Reino Unido, Grecia, Italia, Liechtensein, Luxemburgo, Países Bajos, Suecia, Mónaco, Portugal, Irlanda, Eslovenia, Finlandia, Rumania, Chipre, Lituania, Letonia.
PDF original: ES-2358538_T3.pdf
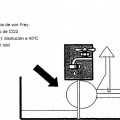




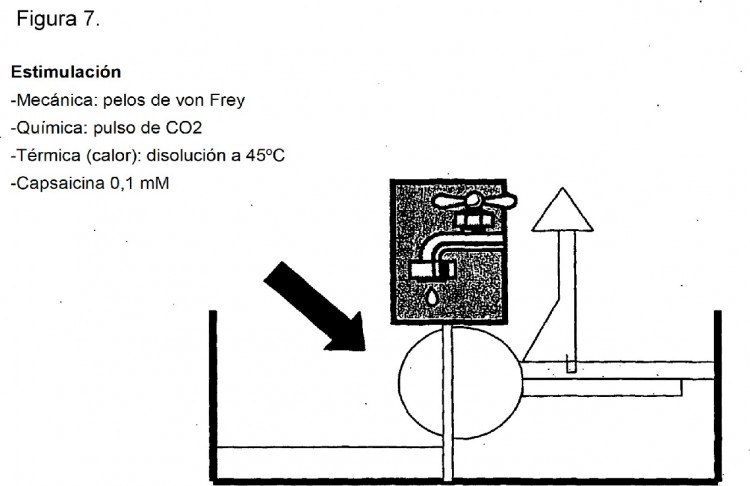
Fragmento de la descripción:
Campo de la invención
La presente invención se refiere a composiciones para el tratamiento y/o la prevención de estados relacionados con altos niveles de expresión y/o actividad del potencial receptor transitorio de vaniloide-1 (TRPV1). Van a mitigarse, entre otros, estados oculares tales como molestia y sensibilidad alterada de la córnea tras cirugía refractiva, uso de lentes de contacto, ojos secos y retinopatía diabética.
También se proporcionan procedimientos y composiciones para el tratamiento y/o la prevención de estados anómalos de la piel y el folículo piloso mediados por altos niveles de expresión y/o actividad de TRPV1, tales como alopecia. La invención proporciona el uso de la tecnología de ARNi para regular por disminución la expresión de TRPV1.
Antecedentes de la invención
La interferencia de ARN se refiere al procedimiento de silenciamiento génico postranscripcional específico de secuencia mediado por ARN pequeños de interferencia (ARNsi). Tras el descubrimiento del fenómeno en plantas en los primeros años 1990, Andy Fire y Craig Mello demostraron que el ARN bicatenario (ARNds) inhibía de manera específica y selectiva la expresión génica de manera extremadamente eficaz en Caenorhabditis elegans (Fire et al., 1998, Potent and specific genetic interference by double stranded RNA in Caenorhabditis elegans. Nature, 391:806). La secuencia de la primera cadena (ARN sentido) coincidía con la de la región correspondiente del ARN mensajero (ARNm) diana. La segunda cadena (ARN antisentido) era complementaria al ARNm. El ARNds resultante resultó ser varios ordenes de magnitud más eficaz que las correspondientes moléculas de ARN monocatenarias (en particular, ARN antisentido).
El procedimiento de ARNi comienza cuando la enzima, DICER, encuentra ARNds y lo corta en trozos denominados ARN pequeños de interferencia (ARNsi). Esta proteína pertenece a la familia de nucleasas RNasa III. Un complejo de proteínas reúne estos residuos de ARN y usa su código como guía para buscar y destruir cualquier ARN en la célula con una secuencia de apareamiento, tal como ARNm diana (véase Bosher & Labouesse, 2000, RNA interference: genetic wand and genetic watchdog. Nat Cell Biol, 2000, 2 (2):E31, y Akashi et al., 2001, Suppression of gene expression by RNA interference in cultured plant cells. Antisense Nucleic Acid Drug Dev, 11(6):359).
En intentos de utilizar ARNi para el silenciamiento génico se reconoció que las células de mamífero han desarrollado diversos mecanismos protectores contra infecciones virales que podrían dificultar el uso de este enfoque. De hecho, la presencia de niveles extremadamente bajos de ARNds viral provoca una respuesta de interferón, dando como resultado una supresión de la traducción no específica global, lo que a su vez provoca apoptosis (Williams, 1997, Role of the double-stranded RNA-activated protein kinase (PKR) in cell regulation. Biochem Soc Trans, 25(2):509; Gil & Esteban, 2000, Induction of apoptosis by the dsRNA-dependent protein kinase (PKR): mechanism of action. Apoptosis, 5(2): 107-14).
En 2000 se notificó que ARNds inhibía específicamente 3 genes en el ovocito de ratón y embrión temprano. La detención de la traducción, y por tanto una respuesta de PKR, no se observó cuando los embriones continuaron desarrollándose (Wianny & Zernicka-Goetz, 2000, Specific interference with gene function by double-stranded RNA in early mouse development. Nat Cell Biol, 2(2):70). La investigación en Ribopharma AG (Kulmbach, Alemania) demostró que la funcionalidad de ARNi en células de mamífero, usando ARNds pequeño (20-24 pares de bases) interrumpía genes en células humanas sin iniciar la respuesta de fase aguda. Estos resultados se confirmaron por experimentos similares llevados a cabo por otros grupos de investigación. (Elbashir et al., 2001, RNA interference is mediated by 21-and 22-nucleotide RNAs. Genes Dev, 15(2): 188; Caplen et al., 2001, Specific inhibition of gene expression by small double stranded RNAs in invertebrate and vertebrate systems. Proc. Natl. Acad. Sci. USA, 98: 9742). Sometido a prueba en una variedad de líneas de células de ratón y humanas de cáncer y normales, se determinó que el ARN de horquilla pequeña (ARNsh) puede silenciar genes de manera tan eficaz como sus homólogos de ARNsi (Paddison et al., 2002, Short hairpin RNAs (shRNAs) induce sequence-specific silencing in mammalian cells. Genes Dev, 16(8):948). Recientemente, se demostró que otro grupo de ARN pequeños (21-25 pares de bases) mediaban la regulación por disminución de la expresión génica. Estos ARN, ARN pequeños regulados temporalmente (ARNst), regulan la sincronización de la expresión génica durante el desarrollo en Caenorhabditis elegans (para revisión véase Banerjee & Slack, Control of developmental timing by small temporal RNAs: a paradigm for RNA-mediated regulation of gene expression. Bioessays, 2002, 24(2): 119-29 y Grosshans & Slack, 2002, Micro-RNAs: small is plentiful. J Cell Biol, 156(1):17).
Los científicos han usado ARNi en varios sistema, incluyendo Caenorhabditis elegans, Drosophila, trypanosomas y otros invertebrados. Varios grupos han presentado recientemente la supresión específica de la biosíntesis de proteínas en diferentes líneas de células de mamífero (específicamente en células HeLa) demostrando que ARNi es un procedimiento que puede aplicarse ampliamente para el silenciamiento génico in vitro. Basándose en estos resultados, ARNi se ha convertido rápidamente en una herramienta bien reconocida para validar (identificar y asignar) la función génica. El ARNi que emplea oligonucleótidos de ARNds pequeños proporcionará un entendimiento de la función de genes que están secuenciados sólo parcialmente.
El potencial receptor transitorio de vaniloide-1 (TRPV1), también denominado receptor de vaniloide 1 (VR-1), es un canal catiónico dependiente de ligando sensible a capsaicina, que se descubrió por primera vez en 1997 (Caterina et al. The capsaicin receptor: a heat-activated ion channel in the pain pathway. Nature. 23 de octubre de 1997;389(6653):816-24). TRPV1 se expresa principalmente en neuronas sensoriales y sirve como detector molecular de calor, capsaicina, protones y endovaniloides (Caterina MJ & Julius D. The vanilloid receptor: a molecular gateway to the pain pathway. Annu Rev Neurosci., 2001;24:487-517; Montell et al. Short hairpin RNAs (shRNAs) induce sequence-specific silencing in mammalian cells. Genes Dev., 2002, 16(8): 948-58.; Baumann TK & Martenson ME. Extracellular protons both increase the activity and reduce the conductance of capsaicin-gated channels. J Neurosci. 2000; 20:RC80).
Cuando TRPV1 se activa por agonistas tales como capsaicina y otros factores tales como calor, acidosis, productos de lipoxigenasa o anandamida, el calcio entra en la célula y se inician señales de dolor. La activación del canal induce la liberación de neuropéptidos desde terminales nerviosas sensoriales centrales y periféricas, dando como resultado la sensación de dolor, inflamación neurogénica, y a veces, contracción del músculo liso y tos. Las pruebas recientes sugieren un papel de TRPV1 en el dolor, tos, asma e incontinencia urinaria (Jia et al., TRPV1 receptor: a target for the treatment of pain, cough, airway disease and urinary incontinence. Drug News Perspect. Abril 2005;18(3): 165-71).
Debido al hecho de que tanto la sensibilidad como la densidad de expresión de TRPV1 se potencian durante estados inflamatorios (Di Marzo et al., Endovanilloid signaling in pain. Curr Opin Neurobiol. Agosto 2002;12(4): 3729), la regulación por disminución de la expresión y/o actividad de TRPV1 es una estrategia terapéutica prometedora para fármacos analgésicos novedosos. A decir verdad, la administración intraperitoneal de bloqueadores de TRPV1 selectivos en ratones demostró atenuar la nocicepción química y térmica y la hiperalgesia (Garcia-Martinez et al., Attenuation of thermal nociception and hyperalgesia by VR1 blockers. Proc Natl Acad Sci USA. 19 de febrero 2002;99(4):2374-9).
La función del canal de TRPV1 está regulada por incremento por varios mediadores endógenos presentes en estados inflamatorios, que reducen el umbral para la activación del canal. Por tanto, se ha demostrado recientemente que el comportamiento relacionado con el dolor agudo provocado mediante la fuerza iónica elevada se suprime en ratones sin TRPV1 y se inhibe mediante yodoresiniferatoxina, un potente antagonista de TRPV1 (Ahern et al., Extracellular cations sensitize and gate capsaicin receptor TRPV1 modulating pain signaling. J Neurosci. 25 de mayo de 2005 ;25(21):5109-16).... [Seguir leyendo]
Reivindicaciones:
1. Uso de una dosis farmacéuticamente eficaz de ANsi dirigido frente a TRPV1 en la preparación de un fármaco para su uso en el tratamiento de un estado ocular caracterizado por un aumento de la expresión y/o actividad de TRPV1, en el que dicho fármaco se administra por vía tópica a la superficie de la córnea.
2. El uso de acuerdo con la reivindicación 1, en el que la administración es mediante el uso de gotas oculares.
3. El uso de acuerdo con la reivindicación 1 o reivindicación 2, en el que el estado ocular se selecciona del grupo que comprende molestia y sensibilidad alterada de la córnea tras cirugía refractiva, uso de lentes de contacto, ojos secos, retinopatía diabética y otras patologías oculares.
4. El uso de acuerdo con cualquier reivindicación anterior, en el que el ANsi es ARNsi.
5. El uso de acuerdo con la reivindicación 4, en el que el ARNsi es ARNds o ARNsh.
6. El uso de acuerdo con cualquier reivindicación anterior, en el que el ANsi comprende un oligonucleótido modificado en el que dicha modificación se selecciona de enlaces internucleotídicos de fosforotioato, 2'-Ometilrribonucleótidos, 2'-desoxi-fluororribonucleótidos, 2'-desoxirribonucleótidos, nucleótidos de “base universal”, 5C-metilnucleótidos, incorporación desoxiabásica invertida, entrecruzamiento químico entre las dos cadenas complementarias de un ARNsi, modificación química de un extremo terminal en 3' o 5' de una cadena de un ARNsi, modificaciones de azúcares, modificaciones de nucleobases y/o modificaciones de la estructura principal, ribonucleótidos 2'-fluoro-modificados y 2'-desoxirribonucleótidos, sustitución de un nucleótido de pirimidina no modificada por una 2-tio, 5-alquinil, 5-metil o 5-propinilpirimidina o sustitución de una purina no modificada por una 7desaza, 7-alquil o 7-alquenilpurina.
7. El uso de acuerdo con cualquiera de las reivindicaciones anteriores, en el que se usa una pluralidad de especies de ANsi.
8. El uso de acuerdo con la reivindicación 7, en el que dicha pluralidad de especies selecciona como diana a la misma especie de ARNm.
9. El uso de acuerdo con cualquiera de las reivindicaciones anteriores, en el que el ANsi selecciona como diana a una secuencia seleccionada de SEC ID Nos 1 a SEC ID Nos 81 o a una secuencia que comprende una secuencia seleccionada de SEC ID Nos 1 a SEC ID Nos 81.
10. El uso de acuerdo con cualquier reivindicación anterior, en el que las moléculas de ANsi de la invención comprenden secuencias de nucleótidos seleccionadas del grupo de SEC ID Nos 82 a SEC ID Nos 162.
11. El uso de acuerdo con la reivindicación 10, en el que moléculas de ANsi contienen proyecciones en 3'.
12. ANsi dirigido frente a TRPV1 para su uso en el tratamiento de un estado ocular caracterizado por un aumento de la expresión y/o actividad de TRPV1, en el que se administra dicho ANsi, en el que dicho fármaco se administra por vía tópica a la superficie de la córnea.
13. Un compuesto de ANsi que selecciona como diana a TRPV1 que comprende una secuencia de nucleótidos complementaria a la secuencia de nucleótidos de SEC ID Nº: 65.
14. Un compuesto de ANsi de acuerdo con la reivindicación 13 que comprende la secuencia de nucleótidos descrita en SEC ID Nº: 146.
15. Un compuesto de ANsi de acuerdo con la reivindicación 14 que comprende la SEC ID Nº 146 con proyecciones en ambos extremos en 3', en el que ambas proyecciones son dTdT.
16. El ANsi de acuerdo con cualquiera de las reivindicaciones 13 a 15, en el que el ANsi es ARNsi.
17. El ANsi de acuerdo con la reivindicación 16, en el que el ARNsi es ARNds o ARNsh.
18. El ANsi de acuerdo con cualquiera de las reivindicaciones 13 a 17, en el que el ANsi comprende un oligonucleótido modificado en el que dicha modificación se selecciona de enlaces internucleotídicos de fosforotioato, 2'-O-metilrribonucleótidos, 2'-desoxi-fluororribonucleótidos, 2'-desoxirribonucleótidos, nucleótidos de “base universal”, 5-C-metilnucleótidos, incorporación desoxiabásica invertida, entrecruzamiento químico entre las dos cadenas complementarias de un ARNsi, modificación química de un extremo terminal en 3' o 5' de una cadena de un ARNsi, modificaciones de azúcares, modificaciones de nucleobases y/o modificaciones de la estructura principal, ribonucleótidos 2'-fluoro-modificados y 2'-desoxirribonucleótidos, sustitución de un nucleótido de pirimidina no modificada por una 2-tio, 5-alquinil, 5-metil o 5-propinilpirimidina o sustitución de una purina no modificada por una 7desaza, 7-alquil o 7-alquenilpurina.
19. Un ANsi de acuerdo con cualquiera de las reivindicaciones 13 a 18 para su uso como fármaco.
20. El uso de una dosis farmacéuticamente eficaz de ANsi de acuerdo con cualquiera de las reivindicaciones 13 a 18 en la preparación de un fármaco para su uso en un procedimiento de tratamiento de un estado ocular caracterizado por un aumento de la expresión y/o actividad de TRPV1, en el que dicho fármaco se administra por vía tópica a la
5 superficie de la córnea.
21. Un ANsi de acuerdo con cualquiera de las reivindicaciones 13 a 18 para su uso en el tratamiento de un estado ocular caracterizado por un aumento de la expresión y/o actividad de TRPV1, en el que dicho ANsi se administra por vía tópica a la superficie de la córnea.
22. Una composición farmacéutica que comprende un compuesto de acuerdo con cualquiera de las reivindicaciones 10 13a18.
Patentes similares o relacionadas:
 Compuestos que modulan la actividad de señalización de las interleucinas 17 y 23, del 29 de Julio de 2020, de Sarepta Therapeutics, Inc: Un método ex vivo de modulación de la actividad de señalización de IL-17 en una célula, que comprende poner en contacto la célula con un oligómero antisentido de morfolino […]
Compuestos que modulan la actividad de señalización de las interleucinas 17 y 23, del 29 de Julio de 2020, de Sarepta Therapeutics, Inc: Un método ex vivo de modulación de la actividad de señalización de IL-17 en una célula, que comprende poner en contacto la célula con un oligómero antisentido de morfolino […]
Método para producir inmunoconjugados de anticuerpo-SN-38 con un enlazador CL2A, del 22 de Julio de 2020, de IMMUNOMEDICS, INC.: Un método para producir un compuesto, CL2A-SN-38, que presenta la estructura, **(Ver fórmula)** que comprende realizar un esquema de reacción como el que se muestra: **(Ver […]
Composiciones para modular la expresión de SOD-1, del 24 de Junio de 2020, de Biogen MA Inc: Un compuesto antisentido según la siguiente fórmula: mCes Aeo Ges Geo Aes Tds Ads mCds Ads Tds Tds Tds mCds Tds Ads mCeo Aes Geo mCes Te (secuencia […]
Terapia mediada por ARN interferente para enfermedades neurodegenerativas, del 24 de Junio de 2020, de Università Degli Studi Di Trento: Agente terapéutico para su uso en el tratamiento de enfermedades neurodegenerativas asociadas con anomalías de la proteína tau codificada […]
Compuestos oligonucleotídicos dirigidos a ARNm de huntingtina, del 3 de Junio de 2020, de UNIVERSITY OF MASSACHUSETTS: Una molécula de ARN que tiene una longitud entre 15 y 35 bases, que comprende una región de complementariedad que es completamente complementaria a 5' CAGUAAAGAGAUUAA 3' […]
Lípido catiónico, del 29 de Abril de 2020, de TAKEDA PHARMACEUTICAL COMPANY LIMITED: Un compuesto representado por la fórmula: **(Ver fórmula)** donde, W denota la fórmula -NR1R2 o la fórmula -N+R3R4R 5(Z-); R1 y R2 denotan, cada uno de forma independiente, […]
Oligonucleótidos TGF-beta modificados, del 29 de Abril de 2020, de ISARNA Therapeutics GmbH: Oligonucleótido que consiste en CAAAGTATTTGGTCTCC (SEQ ID NO. 46), en el que los nucleótidos en negrita son oligonucleótidos modificados con LNA, complementarios […]
Agente de direccionamiento para células cancerosas o fibroblastos asociados con cáncer, del 29 de Abril de 2020, de NITTO DENKO CORPORATION: Composición para su uso en el tratamiento de cáncer en el que están implicados fibroblastos asociados con cáncer, caracterizada porque la composición comprende un portador […]