DERIVADOS DE TRIAZA-BENZO(E)AZULENO PARA EL TRATAMIENTO DE TUMORES.
Compuestos de la fórmula I en la queR1significa H, A, OH, OA,
NO2, NH2, NHA, NA2, Hal, CN, A-COO, COOH, COOA o CONR4R5, R2, R3 significan respectivamente, de manera independiente entre sí, H, A, alquenilo con 2 hasta 6 átomos de carbono, alquinilo con 2 hasta 6 átomos de carbono o Hal,R4, R5 significan respectivamente, de manera independiente entre sí, H o A,Asignifica alquilo no ramificado o ramificado con 1, con 2, con 3, con 4, con 5, con 6, con 7, con 8, con 9 o con 10 átomos de carbono, pudiendo estar reemplazados desde 1 hasta 7 átomos de H por F, Halsignifica F, Cl, Br o I, así como sus derivados, sus solvatos, sus sales, sus tautómeros y sus estereoisómeros farmacéuticamente empleables, con inclusión de sus mezclas en todas las proporciones
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/EP2007/008494.
Solicitante: MERCK PATENT GMBH.
Nacionalidad solicitante: Alemania.
Dirección: FRANKFURTER STRASSE 250 64293 DARMSTADT ALEMANIA.
Inventor/es: GREINER, HARTMUT, HOELZEMANN,GUENTER, AMENDT,CHRISTIANE.
Fecha de Publicación: .
Fecha Solicitud PCT: 29 de Septiembre de 2007.
Clasificación Internacional de Patentes:
- C07D487/04 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07D COMPUESTOS HETEROCICLICOS (Compuestos macromoleculares C08). › C07D 487/00 Compuestos heterocíclicos que contienen átomos de nitrógeno como únicos heteroátomos del ciclo en el sistema condensado, no previstos por los grupos C07D 451/00 - C07D 477/00. › Sistemas condensados en orto.
Clasificación PCT:
- A61K31/55 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › que tienen ciclos con siete eslabones, p. ej. azelastina, pentilentetrazol.
- A61P35/00 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › Agentes antineoplásicos.
- C07D487/04 C07D 487/00 […] › Sistemas condensados en orto.
Países PCT: Austria, Bélgica, Suiza, Alemania, Dinamarca, España, Francia, Reino Unido, Grecia, Italia, Liechtensein, Luxemburgo, Países Bajos, Suecia, Mónaco, Portugal, Irlanda, Eslovenia, Finlandia, Rumania, Chipre, Lituania, Letonia.
Fragmento de la descripción:
Derivados de triaza-benzo[e]azuleno para el tratamiento de tumores.
Fundamento de la invención
La invención tenía como tarea encontrar nuevos compuestos con propiedades valiosas, de manera especial aquellos que pudieran ser empleados para la fabricación de medicamentos.
La presente invención se refiere a compuestos y al empleo de los compuestos, en los que juega un papel la inhibición, la regulación y/o la modulación de la transducción de las señales de las cinasas, de manera especial de las cinasas del receptor TGF-beta, así mismo la invención se refiere a composiciones farmacéuticas, que contienen estos compuestos, así como al empleo de los compuestos para llevar a cabo el tratamiento de enfermedades condicionadas por las cinasas.
El factor beta de transformación celular (transforming growth factor beta) es el prototipo de la superfamilia TGF-beta, una familia de factores del crecimiento pleitrópico, altamente conservada, que ejerce importantes funciones tanto durante el desarrolle embrionario así como, también, en el organismo adulto. En los mamíferos han sido identificadas tres isoformas del TGF-beta (TGF-beta 1, 2 y 3), representando el TGF-beta 1, la isoforma mas frecuente (Kingsley (1994) Genes Deva 8: 133-146). El TGF-beta 3 es expresado, por ejemplo, únicamente en células mesenquimales mientras que, por el contrario, el TGF-beta 1 se encuentra en las células mesenquimales y epiteliales. El TGF-beta es sintetizado como preproteína y es segregado en forma inactiva en la matriz extracelular (Derynck (1985) Nature 316: 701-705; Bottinger (1996) PNAS 93: 5877-5882). De la misma manera, puede estar enlazada una de las 4 isoformas de las proteínas de enlace TRGF-beta latentes (Latent TGF-beta Binding Proteins (LTBP 1-4)) sobre el TGF-beta (Gentry (1988) Mol Cell Biol 8: 4162-4168, Munger (1997) Kindey Int 51: 1376-1382), además de la prorregión disociada, que se denomina también péptido asociado latente (Latency Associated Peptide (LAP)) y que permanece asociada con la región madura. Todavía no ha sido aclarada por completo la activación de los complejos inactivos, que es necesaria para llevar a cabo el despliegue del efecto biológico del TGF-beta. Desde luego se requiere, con seguridad, un procesamiento proteolítico, por ejemplo por medio de plasmina, de transglutaminasa del plasma o de trombospondina (Munger (1997) Kindey Int 51: 1376-1382). El ligando TGF-beta activado induce su efecto biológico a través de tres receptores TGF-beta, que están situados en la membrana, los receptores de tipo I y de tipo II, que son expresados de forma ubicua, y los receptores de tipo III constituidos por el betaglicano y por la endoglina, siendo expresado esta último solamente en las células del endotelio (Gougos (1990) J Biol Chem 264: 8361-8364, Lopes-Casillas (1994) J Cell Biol 124: 557-568). Ninguno de los dos receptores TGF-beta de tipo III tiene dominios de cinasa intracelulares, que posibiliten una retransmisión de las señales hasta la célula. Puesto que los receptores TGF-beta de tipo III enlazan a las tres isoformas del TGF-beta con elevada afinidad y, así mismo, el receptor TGF-beta de tipo II tiene una elevada afinidad para los ligandos, que están enlazados sobre el receptor de tipo III, probablemente la función biológica consiste en la regulación de la disponibilidad de los ligandos para los receptores TGF-beta de tipo I y de tipo II (Lastres (1996) J Cell Biol 133: 1109-1121; Lopes-Casillas (1993) Cell 73: 1435-1344). Los receptores de tipo I y de tipo II, que están estrechamente emparentados desde el punto de vista estructural, tienen una la región citoplasmática un dominio de serina/treonina-cinasa, que es responsable de la retransmisión de las señales. El receptor TGF-beta de tipo II enlaza el TGF-beta, después de lo cual es recrutado el receptor TGF-beta de tipo I para formar este complejo retransmisor de las señales. El dominio de serina/treonina-cinasa del receptor de tipo II es constituyentemente activo y puede llevar a cabo la fosforilación en este complejo de los restos serilo en el dominio denominado GS del receptor de tipo I. Esta fosforilación lleva a cabo la activación de la cinasa del receptor de tipo I que, por su parte, puede llevar a cabo, ahora, la fosforilación de los mediadores de las señales intracelulares, la proteína SMAD y, de este modo, puede llevar a cabo la iniciación de la retransmisión intracelular de las señales (resumido en la publicación de Derynck (1997) Biochim Biophys Acta 1333: F105-F150). Las proteínas de la familia SMAD sirven como substratos para todas las cinasas del receptor de las familias TGF-beta. Hasta el presente han sido identificadas 8 proteínas SMAD, que se subdividen en 3 grupos: (1) las SMADs asociadas con el receptor (R-SMADs) son substratos directos de las cinasas del receptor TGF-β (SMAD1, 2, 3, 5, 8); (2) las co-SMADs, que se asocian con las R-SMADs durante la cascada de señales (SMAD4); y (3) las SMADs inhibidoras (SMAD6, 7), que inhiben la actividad de las proteínas SMAD, que han sido citadas más arriba. Entre las diversas R-SMADs, la SMAD2 y la SMAD3 son los mediadores de las señales específicos del TGF-beta. Por lo tanto, en la cascada de señales del TGF-beta, las SMAD2/SMAD3 llevarán a cabo la fosforilación del receptor TGF-beta de tipo I, por lo que pueden ser asociadas a la SMAD4. El complejo formado, que está constituido por SMAD2/SMAD3 y por SMAD4, puede ser translocalizado ahora hasta el núcleo de la célula puede llevar a cabo en el mismo, de manera directa o a través de otra proteína, la transcripción del gen regulado por el TGF-beta (resumido en la publicación Itoh (2000) Eur J Biochem 267: 6954-6967; Shi (2003) Cell 113: 685-700).
El espectro de las funciones del TGF-beta presenta un amplio abanico y depende del tipo celular y del estado de diferenciación (Roberts (1990) Handbook of Experimental Pharmacology: 419-472). A las funciones celulares, que son influenciadas por el TGF-beta, pertenecen: la apoptosis, la proliferación, la diferenciación, la movilidad y la adherencia celular. Por lo tanto el TGF-beta juega un papel importante en los procesos biológicos más diversos. Durante el desarrollo embrional son expresados en los lugares de la morfogérnesis y, de manera especial, en los puntos con interacción epitelial mesenquimal y son inducidos en dichos puntos importantes procesos de diferenciación (Pelton (1991) J Cell Biol 115: 1091-1105). El TGF-beta ejerce también una punción clave en la autonutrición y en el mantenimiento de un estado indiferenciado de las células madre (Mishra (2005) Science 310: 68-71). Por otra parte, el TGF-beta también cumple una función importante en la regulación del sistema inmune. En general, actúa de forma inmunosupresora, puesto que, entre otras cosas inhibe la proliferación de los linfocitos y limita la actividad de los macrófagos tisulares. De este modo, el TGF-beta permite que las reacciones inflamatorias remitan de nuevo y ayuda de este modo a evitar reacciones inmunes en exceso (Bogdan (1993) Ann NY Acad Sci 685: 713-739, resumido en la publicación Letterio (1998) Annu Rev Immunol 16: 137-161). Otra función del TGF-beta consiste en la regulación de la proliferación celular. El TGF-beta inhibe el crecimiento de las células de origen endotelial, epitelial y hematopoyético, pero fomenta el crecimiento de las células de origen mesenquimal (Tucker (1984) Science 226: 705-707, Shipley (1986) Cancer Res 46: 2068-2071, Shipley (1985) PNAS 82: 4147-4151). Otra función importante del TGF-beta consiste en la regulación de la adherencia celular y de las interacciones de célula a célula. El TGF-beta fomenta la formación de la matriz extracelular por medio de la inducción de proteínas de la matriz extracelular tales como, por ejemplo, la fibronectina y el colágeno. De manera adicional, el TGF-beta reduce la expresión de las metaloproteasas degradadotas de la matriz y los inhibidores de las metaloproteasas (Roberts (1990) Ann NY Acad Sci 580: 225-232; Ignotz (1986) J Biol Chem 261: 4337-4345; Overall (1989) J Biol Chem 264: 1860-1869); Edwards (1987) EMBO J 6: 1899-1904).
El amplio espectro de actividad del TGF-beta implica, que el TGF-beta juega un papel importante en muchos supuestos fisiológicos, tales como la curación de las heridas y en los procesos patológicos, tales como el cáncer y la fibrosis.
El TGF-beta es una de los factores clave del crecimiento en la curación de las heridas (resumido en O'Kane (1997) Int J Biochem Cell Biol 29: 79-89). Durante la fase de granulación, es liberado el TGF-beta en el lugar de la herida a partir de las plaquetas sanguíneas. Por lo tanto, el TGF-beta regula su propia producción...
Reivindicaciones:
1. Compuestos de la fórmula I
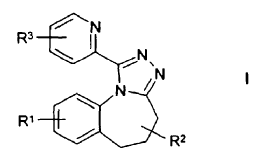
en la que
R2, R3 significan respectivamente, de manera independiente entre sí, H, A, alquenilo con 2 hasta 6 átomos de carbono, alquinilo con 2 hasta 6 átomos de carbono o Hal,
R4, R5 significan respectivamente, de manera independiente entre sí, H o A,
así como sus derivados, sus solvatos, sus sales, sus tautómeros y sus estereoisómeros farmacéuticamente empleables, con inclusión de sus mezclas en todas las proporciones.
2. Compuestos según la reivindicación 1, en los que
así como sus derivados, sus solvatos, sus sales y sus estereoisómeros farmacéuticamente empleables, con inclusión de sus mezclas en todas las proporciones.
3. Compuestos según la reivindicación 1 o 2, en los que
así como sus derivados, sus solvatos, sus sales y sus estereoisómeros farmacéuticamente empleables, con inclusión de sus mezclas en todas las proporciones.
4. Compuestos según la reivindicación 1, 2 o 3, en la que
así como sus derivados, sus solvatos, sus sales y sus estereoisómeros farmacéuticamente empleables, con inclusión de sus mezclas en todas las proporciones.
5. Compuestos según una o varias de las reivindicaciones 1 a 4, en los que
así como sus derivados, sus solvatos, sus sales y sus estereoisómeros farmacéuticamente empleables, con inclusión de sus mezclas en todas las proporciones.
6. Compuestos según una o varias de las reivindicaciones 1 a 5, en los que
así como sus derivados, sus solvatos, sus sales y sus estereoisómeros farmacéuticamente empleables, con inclusión de sus mezclas en todas las proporciones.
7. Compuestos según la reivindicación 1 elegidos entre el grupo constituido por

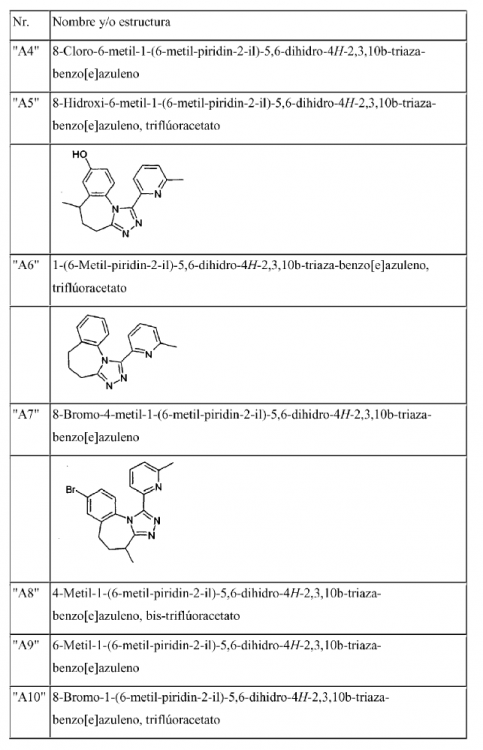
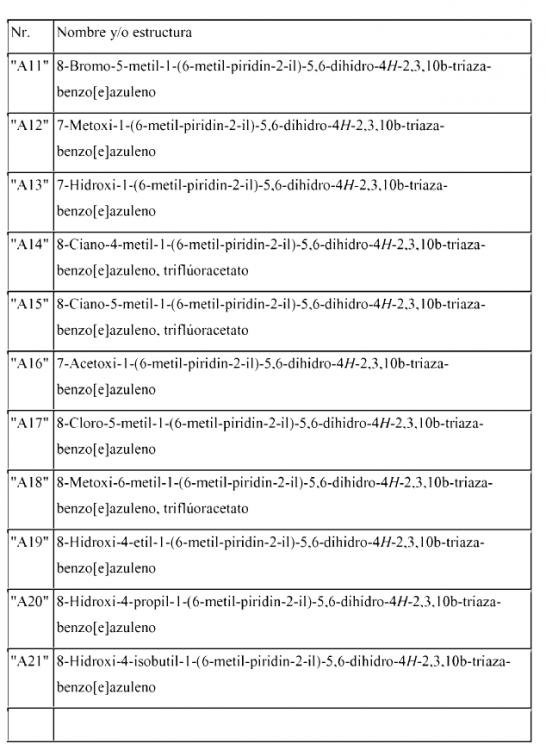
así como sus derivados, sus solvatos, sus sales y sus estereoisómeros farmacéuticamente empleables, con inclusión de sus mezclas en todas las proporciones.
8. Procedimiento para la obtención de compuestos de la fórmula I según las reivindicaciones 1 a 7 así como de sus derivados, sus sales, sus solvatos, sus tautómeros y sus estereoisómeros farmacéuticamente empleables, caracterizado porque
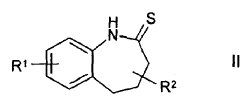
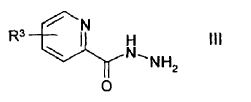
9. Medicamento que contiene, al menos, un compuesto de la fórmula I según una o varias de las reivindicaciones 1 a 7 y/o sus derivados, sus solvatos, sus sales y sus estereoisómeros farmacéuticamente empleables, con inclusión de sus mezclas en todas las proporciones, así como, en caso dado, excipientes y/o productos auxiliares.
10. Empleo de los compuestos según una o varias de las reivindicaciones 1 a 7 así como de sus derivados, sus sales, sus solvatos, sus tautómeros y sus estereoisómeros, farmacéuticamente empleables, para la fabricación de un medicamento para llevar a cabo el tratamiento y/o a para combatir el cáncer, el crecimiento de los tumores, el crecimiento de las metástasis, la fibrosis, la restenosis, la infección por HIV, el Alzheimer, la aterosclerosis, y/o para fomentar la curación de las heridas.
11. Empleo según la reivindicación 10, en el que el tumor se elige entre el grupo de los tumores del epitelio plano, de la vejiga, del estómago, de los riñones, de la cabeza, del cuello, del esófago, del cuello de la matriz, de la glándula tiroides, del intestino, del hígado, del cerebro, de la próstata, del tracto urogenital, del sistema linfático, del estómago, de la laringe, del pulmón, el adenocarcinoma de pulmón, el carcinoma de pulmón microcelular, el cáncer del páncreas, el gliobastoma, el carcinoma de colon, el carcinoma de mama, del sistema sanguíneo y del sistema inmune, la leucemia mielitica aguda, la leucemia mielítica crónica, la leucemia linfática aguda, la leucemia linfática crónica.
12. Empleo de los compuestos según la reivindicación 10 y/o de sus sales y sus solvatos, fisiológicamente aceptables, para la fabricación de un medicamento para llevar a cabo el tratamiento de tumores sólidos, llevándose a cabo la administración de una cantidad terapéuticamente activa de un compuesto de la fórmula I en combinación con un compuesto del grupo 1) modulador del receptor de los estrógenos, 2) modulador del receptor de los andrógenos, 3) modulador del receptor de retinoide, 4) citotóxico, 5) agente antiproliferante, 6) inhibidor de la prenil-proteínatransferasa, 7) inhibidor de la HMG-CoA-reductasa, 8) inhibidor de la HIV-proteasa, 9) inhibidor de la transcriptasa inversa así como 10) otro inhibidor de la angiogénesis.
13. Empleo de los compuestos según la reivindicación 10 y/o de sus sales y sus solvatos, fisiológicamente aceptables, para la fabricación de un medicamento para llevar a cabo el tratamiento de tumores sólidos, llevándose a cabo la administración de una cantidad terapéuticamente activa de un compuesto de la fórmula I en combinación con radioterapia y de un compuesto del grupo 1) modulador del receptor de los estrógenos, 2) modulador del receptor de los andrógenos, 3) modulador del receptor de retinoide, 4) citotóxico, 5) agente antiproliferante, 6) inhibidor de la prenil-proteínatransferasa, 7) inhibidor de la HMG-CoA-reductasa, 8) inhibidor de la HIV-proteasa, 9) inhibidor de la transcriptasa inversa así como 10) otro inhibidor de la angiogénesis.
14. Medicamento que contiene, al menos, un compuesto de la fórmula I según una o varias de las reivindicaciones 1 a 7 y/o sus derivados, sus solvatos y sus estereoisómeros farmacéuticamente empleables, con inclusión de sus mezclas en todas las proporciones y, al menos, otro principio activo para medicamentos.
Patentes similares o relacionadas:
Compuestos de heteroaril carboxamida como inhibidores de RIPK2, del 29 de Julio de 2020, de BOEHRINGER INGELHEIM INTERNATIONAL GMBH: Un compuesto de fórmula (I): **(Ver fórmula)** o sus sales farmacéuticamente aceptables, en la que: X es N y Y es CH; o X es CH y Y es N; […]
Compuestos de alquinilbenceno heterocíclicos, y composiciones médicas y usos de los mismos, del 29 de Julio de 2020, de Guangzhou Healthquest Pharma Co., Ltd: Un compuesto de alquinilbenceno heterocíclico que tiene la fórmula (I) y una sal farmacéuticamente aceptable, o estereoisómero del mismo, **(Ver […]
1,5-Dihidro-4H-pirazolo[3,4-d]pirimidin-4-onas y 1,5-dihidro-4H-pirazolo[4,3-c]piridin-4-onas como inhibidores de la PDE1, del 29 de Julio de 2020, de H. LUNDBECK A/S: Un compuesto de fórmula (I) **(Ver fórmula)** en donde Y es N o CH; R1 se selecciona del grupo que consiste en alquilo C2-C8 lineal o ramificado, cicloalquilo […]
Compuestos y procedimientos de uso, del 29 de Julio de 2020, de Medivation Technologies LLC: Un compuesto de fórmula (Aa-1): **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, en la que: A representa H, halógeno, amino, […]
Ureas cíclicas como inhibidores de ROCK, del 22 de Julio de 2020, de BRISTOL-MYERS SQUIBB COMPANY: Un compuesto de acuerdo con la Fórmula (I): **(Ver fórmula)** o un enantiómero, un diastereómero, un estereoisómero, un tautómero, una sal farmacéuticamente aceptable […]
Derivado heteroarilo o sal farmacéuticamente aceptable del mismo, método de preparación del mismo y composición farmacéutica para prevenir o tratar enfermedades asociadas con PI3 quinasas, que contiene el mismo como principio activo, del 22 de Julio de 2020, de KOREA RESEARCH INSTITUTE OF CHEMICAL TECHNOLOGY: Un compuesto representado por la fórmula 1, un isómero óptico del mismo o una sal farmacéuticamente aceptable del mismo: **(Ver fórmula)** en la fórmula […]
Derivados de 5-[2-(piridin-2-ilamino)-1,3-tiazol-5-il]-2,3-dihidro-1H-isoindol-1-ona y su uso como inhibidores dobles de fosfatidilinositol··3-cinasa delta y gamma, del 15 de Julio de 2020, de ASTRAZENECA AB: Compuesto de formula (I) **(Ver fórmula)** donde X es C(O) o SO2; Y es SO2NHR5 o SO2R6; R1 se selecciona de alquilo C1-4, […]
Antagonistas del receptor de dopamina D3 que tienen una unidad estructural biciclo, del 15 de Julio de 2020, de Indivior UK Limited: Un compuesto, o una sal farmacéuticamente aceptable del mismo, que tiene la fórmula: **(Ver fórmula)** en donde; A y B juntos tienen la fórmula: **(Ver […]