CICLOPÉPTIDO CON ACTIVIDAD ANTICANCERÍGENA DERIVADO DEL COLÁGENO DE TIPO IV.
Ciclopéptido seleccionado de entre: a) un ciclopéptido homodético,
caracterizado porque comprende la secuencia YSNS; y b) un ciclopéptido, cuyo ciclo comprende la secuencia YSNS y tiene un número de residuos de aminoácidos comprendido entre 4 y 6
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/FR2007/000487.
Solicitante: UNIVERSITE DE REIMS CHAMPAGNE-ARDENNE.
Nacionalidad solicitante: Francia.
Dirección: VILLA DOUCE, 9, BOULEVARD DE LA PAIX 51097 REIMS CEDEX FRANCIA.
Inventor/es: MONBOISSE,JEAN-CLAUDE,PAUL,LOUIS, FLOQUET,NICOLAS,JOSEPH,GILBERT, THEVENARD,JESSICA,ANDREE,MIREILLE, RAMONT,LAURENT,GABRIEL,EMILE, BRASSART,SYLVIE,ANNE,YVONNE.
Fecha de Publicación: .
Fecha Solicitud PCT: 22 de Marzo de 2007.
Clasificación Internacional de Patentes:
- C07K5/12B
- C07K7/64 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 7/00 Péptidos con 5 a 20 aminoácidos en una secuencia totalmente determinada; Sus derivados. › Péptidos cíclicos que contienen solamente enlaces peptídicos normales.
Clasificación PCT:
- A61K38/12 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 38/00 Preparaciones medicinales que contienen péptidos (péptidos que contienen ciclos beta-lactama A61K 31/00; dipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina 2,5-dionas, A61K 31/00; péptidos basados en la ergolina A61K 31/48; que contienen compuestos macromoleculares que tienen unidades aminoácido repartidas estadísticamente A61K 31/74; preparaciones medicinales que contienen antígenos o anticuerpos A61K 39/00; preparaciones medicinales caracterizadas por los ingredientes no activos, p. ej. péptidos como soportes de fármacos, A61K 47/00). › Péptidos cíclicos.
- C07K5/12 C07K […] › C07K 5/00 Péptidos con hasta cuatro aminoácidos en una secuencia totalmente determinada; Sus derivados. › Péptidos cíclicos.
- C07K7/64 C07K 7/00 […] › Péptidos cíclicos que contienen solamente enlaces peptídicos normales.
Países PCT: Austria, Bélgica, Suiza, Alemania, Dinamarca, España, Francia, Reino Unido, Grecia, Italia, Liechtensein, Luxemburgo, Países Bajos, Suecia, Mónaco, Portugal, Irlanda, Eslovenia, Finlandia, Rumania, Chipre, Lituania, Letonia, Ex República Yugoslava de Macedonia, Albania.
PDF original: ES-2360004_T3.pdf
Fragmento de la descripción:
La presente invención se refiere a un ciclopéptido homodético. Es decir, que el ciclo se realiza mediante la ciclización de los grupos amina y carboxilo de los aminoácidos N- y C-terminales, formando así un péptido cíclico unido por un enlace amida, caracterizado porque comprende la secuencia YSNS; o un ciclopéptido, cuyo ciclo comprende la secuencia YSNS y tiene un número de residuos de aminoácidos comprendido entre 4 y 6. De manera particular, el 5 ciclopéptido es un pentapéptido, que forma una estructura en codo a nivel de los aminoácidos YSNS, y susceptible de ser obtenido mediante la formación de una unión peptídica entre los dos aminoácidos de los extremos del pentapéptido representado linealmente. En un modo de realización preferido, el ciclopéptido de la invención es capaz de fijarse a la integrina V3.
La utilización de un ciclopéptido tal como se ha definido anteriormente en el tratamiento del cáncer, y más 10 particularmente en el tratamiento de las diferentes formas (o estados) del melanoma, así como en la fabricación de un medicamento para tratar el cáncer, forma parte asimismo de la invención. El ciclopéptido está particularmente adaptado a la administración de una composición que lo contiene, por vía oral.
El melanoma es el segundo cáncer en el ser humano en términos de número de años de vidas perdidos. Durante los diez últimos años, su incidencia ha aumentado de manera más importante (3 a 5% por año) que los demás tipos de 15 cáncer, con la excepción del cáncer bronquial en la mujer. En el año 2000, se estimaba que uno de cada 100 individuos desarrollaría un melanoma a lo largo de su vida, y que uno de cada 2 pacientes tendría menos de 50 años. Este tipo de cáncer se vuelve ineludiblemente un problema principal de salud pública. El melanoma es un tumor maligno de muy mal pronóstico con un riesgo elevado de metástasis ganglionares y viscerales.
Durante los últimos años, se ha estudiado el mecanismo tumoral y se han explicado poco a poco los mecanismos subtendentes a la progresión tumoral. Así, durante la progresión tumoral, las células cancerígenas dejan el tumor primario, atraviesan las membranas vasculares y migran en el seno de la matriz extracelular cercana.
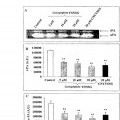
El conjunto de estos fenómenos implica la secreción y después la activación de enzimas proteolíticas, tal como las metaloproteinasas matriciales (MMP) o el sistema de activación del plasminógeno (Hornebeck W. et al.). El perfil de expresión de estas enzimas proteolíticas, estudiado en diversas líneas de células de melanoma humano o de ratón, 25 revela un aumento muy elevado de la expresión de diversas MMP, de manera correlacionada con el fenotipo invasivo de estas células (Egeblad M et al.). La expresión en la superficie celular de MMP-2, funcionalmente activa, influye directamente en la adhesión y en la extensión de las células sobre los componentes de la matriz extracelular y de las membranas basales, y favorece la migración y la invasión de estas células.
La activación de la MMP-2 requiere la formación de complejos con su inhibidor, el TIMP-2, y otra MMP 30 transmembranaria, la MT1-MMP o MMP-14 (Egeblad M et al.). Requiere asimismo la presencia de la integrina Vβ3 cuya expresión aumenta con el grado de invasión de las células de melanoma. Esta integrina sirve de receptor membranario de la MMP-2, favorece su activación y focaliza la forma activa de la MMP-2 a los lamelipodios, que inducen la progresión de la célula cancerígena en el seno de la matriz extracelular (Settor REB et al.; Deryugina EI et al.). Además, durante la progresión tumoral, intervienen numerosos fenómenos inflamatorios que implican la activación 35 de células inflamatorias (polinucleares, neutrófilos, monocitos, macrófagos, etc.) que desembocan en la liberación de diversas citocinas y factores de crecimiento, pero también de MMP, tal como la MMP-9.
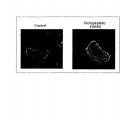
El aumento del volumen tumoral provoca una hipoxia y una falta de aportación de los nutrientes para las células tumorales. Los efectos se superan mediante la angiogénesis tumoral, mecanismo de neovascularización que nace en el seno de los tumores a partir de una red capilar preexistente. Es indispensable para el crecimiento de los tumores y el 40 desarrollo de las metástasis, debido a que restablece la aportación de oxígeno y de nutrientes. La activación de las células endoteliales, inducida por la hipoxia y los protooncogenes en el seno de los tumores, conduce a la degradación de la membrana basal y de la matriz extracelular cercana poniendo en juego las cascadas proteolíticas implicadas en la progresión tumoral. La migración orientada de las células endoteliales está seguida de una fase proliferativa. Las células se organizan en una estructura de tipo capilar para formar la red vascular intratumoral. La angiogénesis es un 45 factor pronóstico en diversos canceres, incluyendo el melanoma.
La única función de soporte mecánico se debió durante mucho tiempo a las macromoléculas de la matriz extracelular. Se ha demostrado, desde hace varios años, que ciertos dominios proteicos constitutivos de estas macromoléculas podían asimismo controlar diversos eventos fisiopatológicos tales como la diferenciación celular, la apoptosis o la expresión de los genes. Las matrikinas son unos péptidos procedentes de la proteolisis parcial de las macromoléculas 50 de la matriz extracelular capaces de regular la actividad biológica de numerosos tipos celulares (Maquart FX et al.). Las moléculas de la matriz extracelular, y más particularmente los diversos constituyentes de las membranas basales (colágeno de tipo IV, XV y XVIII, lamininas, proteoglicanos, etc.) pueden regular la adhesión y la migración de las células cancerígenas, por medio de ciertas matrikinas (Pasco S et al. (2004); Ortega N et al.). Asimismo, estas últimas pueden asegurar un control de la expresión y/o de la activación de las proteasas puestas en juego durante la 55 progresión tumoral.
Entre las macromoléculas de las membranas basales, el colágeno de tipo IV que es el principal constituyente de éstos, desempeña una función preponderante en este control por medio del dominio no colagénico (NC1) de sus diferentes cadenas. Está constituido por la asociación en triple hélice de tres cadenas polipeptídicas (IV), entre 6 posibles,
1(IV) a 6(IV), cada una codificada por un gen diferente (Kalluri R.). La asociación más frecuente corresponde a [1(IV)2; 2(IV)]; se encuentra en el conjunto de las membranas basales. Otras asociaciones, menos determinadas, contienen las cadenas 3(IV) a 6(IV), denominadas menores debido a su baja expresión. La cadena 3(IV) presenta una distribución tisular muy especializada (alvéolo pulmonar, glomérulo renal, cápsula del cristalino, etc.) (Kalluri R). Unas matrikinas derivadas de los dominios NC1 de las cadenas (IV) del colágeno de tipo IV, o de su dominio 5 helicoidal, introducen la adhesión de las células cancerígenas y controlan sus propiedades invasivas (Pasco S et al. (2004); Ortega N et al.; Kalluri R).
Los estudios anteriores se han concentrado en el dominio C-terminal de la cadena 3(IV) (aminoácidos 1438 a 1670 de la secuencia NP_000082; Número de registro NCBI) denominado dominio NC1 (noncollagenous domain) que resultó extremadamente interesante a la vista de los resultados siguientes: 10
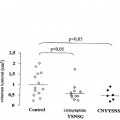
- el dominio NC1 de la cadena 3(IV) posee una actividad inhibidora sobre la proliferación y las propiedades invasivas de diversas líneas de células cancerígenas. Más particularmente, un péptido constituido por los aminoácidos 185 a 203 del dominio NC 13(IV) (CNYYSNSYSFWLASLNPER) puede inhibir la proliferación de estas diversas líneas celulares. Por el contrario, los péptidos constituidos por las secuencias homólogas de las demás cadenas (IV) no tienen ningún efecto sobre estas mismas líneas (Han J et al.; Shanan S et al.). 15
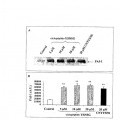
- por otra parte, unos péptidos de secuencia [NC1 3(IV) 185-203] inhiben la migración de células de melanomas o de fibrosarcoma in vitro. Esta inhibición de la migración de las células tumorales parece ser explicada por el efecto inhibidor de la secuencia [NC1 3(IV) 185-203] sobre la fijación de la MMP-2 a la membrana plásmica pero también por el efecto inhibidor sobre la activación de la MMP-2 (Pasco S et al. (2000a)). Se han obtenido unos resultados comparables con unas células cancerígenas bronquiales (Martinella-Catusse et al., 2001). 20
Reivindicaciones:
1. Ciclopéptido seleccionado de entre:
a) un ciclopéptido homodético, caracterizado porque comprende la secuencia YSNS; y
b) un ciclopéptido, cuyo ciclo comprende la secuencia YSNS y tiene un número de residuos de aminoácidos comprendido entre 4 y 6.
2. Ciclopéptido según la reivindicación 1, caracterizado porque el ciclo está constituido por la secuencia YSNS. 5
3. Ciclopéptido según la reivindicación 1 ó 2, caracterizado porque su tamaño es superior o igual a 4 aminoácidos e inferior a 10 aminoácidos, y preferentemente porque su tamaño es de 4 a 6 aminoácidos.
4. Ciclopéptido según cualquiera de las reivindicaciones 1 a 3, caracterizado porque es capaz de fijarse a la integrina V3.
5. Ciclopéptido según cualquiera de las reivindicaciones 1 a 4, caracterizado porque forma un codo a nivel de los 10 aminoácidos YSNS.
6. Ciclopéptido según cualquiera de las reivindicaciones 1 a 5, caracterizado porque su secuencia de aminoácidos consiste en YSNS.
7. Ciclopentapéptido homodético que consiste en la secuencia YSNSX y representado por la fórmula siguiente:
15
en la que X es cualquier aminoácido que permite la ciclización del péptido lineal de misma secuencia.
8. Ciclopéptido según la reivindicación 7, en el que X es un aminoácido de bajo volumen y/o es un aminoácido poco cargado o neutro.
9. Ciclopéptido según cualquiera de las reivindicaciones 7 a 8, caracterizado porque es capaz de fijarse a la integrina V3. 20
10. Ciclopentapéptido cuya secuencia de aminoácidos consiste en YSNSG, representada por la fórmula siguiente:
11. Ciclopéptido según cualquiera de las reivindicaciones 7 a 10, caracterizado porque todos los enlaces peptídicos están en trans, y opcionalmente porque tiene la estructura tridimensional representada en la figura 4.
12. Ciclopéptido según cualquiera de las reivindicaciones 1 a 11, caracterizado porque posee unas propiedades anti-25 tumorales.
13. Composición caracterizada porque comprende un ciclopéptido según cualquiera de las reivindicaciones 1 a 12, y opcionalmente una molécula biológicamente activa en el tratamiento del cáncer.
14. Composición según la reivindicación 13, caracterizada porque la molécula biológicamente activa se selecciona de entre por lo menos una de las moléculas siguientes:
a. un agente quimioterapéutico;
b. un epítopo tumoral específicamente asociado a las células tumorales;
c. un antígeno de diferenciación celular; y 5
d. la interleuquina 2 y/o el interferón .
15. Ciclopéptido según cualquiera de las reivindicaciones 1 a 12, o composición según cualquiera de las reivindicaciones 13 a 14, para su utilización como medicamento.
16. Ciclopéptido según cualquiera de las reivindicaciones 1 a 12, o composición según cualquiera de las reivindicaciones 13 a 14, para su utilización en el tratamiento del cáncer, en particular en el tratamiento del melanoma o 10 en el tratamiento del cáncer bronquial, del cáncer de mama o del cáncer de próstata, o en particular en el tratamiento de un cáncer cuyas células tumorales expresan la molécula integrina V3.
17. Ciclopéptido según cualquiera de las reivindicaciones 1 a 12, o composición según cualquiera de las reivindicaciones 13 a 14, para su utilización en la inhibición o en la reducción de la angiogénesis, preferentemente en el seno de tumores. 15
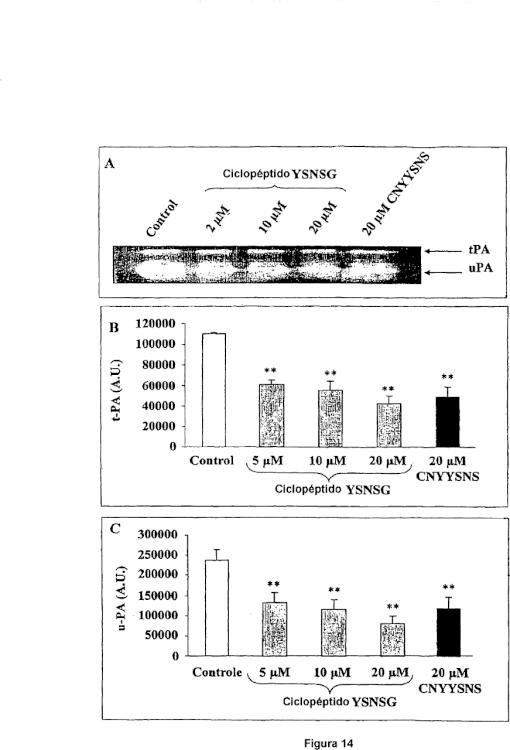
18. Ciclopéptido según cualquiera de las reivindicaciones 1 a 12, o composición según cualquiera de las reivindicaciones 13 a 14, para su utilización en la disminución de la cascada proteolítica asociada a proMMP-2 o del sistema de activación del plasminógeno (uPA).
19. Kit que comprende una composición según cualquiera de las reivindicaciones 13 a 14, en particular formulada para una administración parenteral, oral, sub-cutánea o intravenosa. 20
Patentes similares o relacionadas:
Péptidos de unión beta amiloide y sus usos para el tratamiento y el diagnóstico de la demencia de Alzheimer, del 17 de Junio de 2020, de Priavoid GmbH: Péptido que contiene al menos una secuencia de aminoácidos que se une a especies beta amiloides y en el que la carga negativa del grupo carboxilo presente […]
Péptidos cíclicos de localización en NTCP y sus usos como inhibidores de entrada, del 6 de Mayo de 2020, de Ruprecht-Karls-Universität Heidelberg: Un péptido cíclico de la fórmula general Ia cyclo[(X)m-P-(Y)n] (Ia) en el que P es la secuencia de aminoácidos NPLGFXaaP (SEQ. ID NÚM.: […]
Inmunomoduladores, del 8 de Abril de 2020, de BRISTOL-MYERS SQUIBB COMPANY: Un compuesto de fórmula (I) **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, en la que: A se selecciona entre; **(Ver fórmula)** […]
Análogos de compstatina con propiedades farmacocinéticas mejoradas, del 23 de Octubre de 2019, de THE TRUSTEES OF THE UNIVERSITY OF PENNSYLVANIA: Un compuesto que comprende un péptido de compstatina modificado (ICVVQDWGHHRCT (C2-C12 cíclico; SEQ ID NO:1), en donde la modificación comprende un componente […]
Peptidomiméticos en horquilla beta, del 24 de Julio de 2019, de Polyphor AG: Compuesto de fórmula general (I), Ciclo[P1-P2-P3-P4-P5-P6-P7-P8-P9-P10-P11-P12-T1-T2] (I) en la que los elementos individuales T o P están conectados en […]
Usos de bremelanotida en una terapia para la disfunción sexual femenina, del 22 de Febrero de 2019, de PALATIN TECHNOLOGIES, INC.: Una composición que comprende bremelanotida o una sal farmacéuticamente aceptable de la misma para usar en un método para tratar la disfunción sexual femenina en una paciente […]
Peptidomiméticos en horquilla beta, del 29 de Noviembre de 2018, de Polyphor AG: Un compuesto de la fórmula general (I), ciclo[P1-P2-P3-P4-P5-P6-P7-P8-P9-P10-P11-P12-T1-T2] (I) en donde los elementos individuales T o P están conectados […]
Péptido antagonista de la unión entre el CD47 y una proteína perteneciente a la familia de las trombospondinas, del 13 de Septiembre de 2018, de UNIVERSITE DE REIMS CHAMPAGNE-ARDENNE: Péptido antagonista de la unión entre un receptor CD47 y una proteína perteneciente a la familia de las trombospondinas, o TSP, caracterizado porque presenta la siguiente […]