PROCESO PARA LA PREPARACION DE ASENAPINA Y PRODUCTOS INTERMEDIOS USADOS EN DICHO PROCESO.
Un proceso para preparar la asenapina de Fórmula I, ** ver fórmula** o una sal farmacéuticamente aceptable de la misma,
caracterizado por que un derivado de E-estilbeno de Fórmula II. ** ver fórmula** se hace reaccionar con un iluro de azometino para proporcionar un derivado de trans-pirrolidina de Fórmula III, ** ver fórmula** del que se retira el grupo protector, cuando está presente, y que se trata posteriormente en condiciones que efectúan una reacción de cierre intramolecular del anillo para producir el compuesto de Fórmula I y opcionalmente convertir el compuesto de Fórmula I en una sal farmacéuticamente aceptable del mismo, en la que R1 es F, Br o I; R2 y R3 son diferentes y cada uno se selecciona entre H y Cl; y R4 es H o un grupo protector de hidroxilo
Tipo: Resumen de patente/invención. Número de Solicitud: W07005876EP.
Solicitante: N. V. ORGANON.
Nacionalidad solicitante: Países Bajos.
Dirección: P.O. BOX 20 KLOOSTERSTRAAT 6,5349 AB OSS.
Inventor/es: STUK,TIMOTHY LEE, KEMPERMAN,GERARDUS,JOHANNES, LINDEN,VAN DER,JACOBUS,JOHANNES,MARIA.
Fecha de Publicación: .
Fecha Concesión Europea: 14 de Octubre de 2009.
Clasificación Internacional de Patentes:
- C07C39/24 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07C COMPUESTOS ACICLICOS O CARBOCICLICOS (compuestos macromoleculares C08; producción de compuestos orgánicos por electrolisiso electroforesis C25B 3/00, C25B 7/00). › C07C 39/00 Compuestos que tienen al menos un grupo hidroxilo u O-metal unido a un átomo de carbono de un ciclo aromático de seis miembros. › Derivados halogenados.
- C07C69/017 C07C […] › C07C 69/00 Esteres de ácidos carboxílicos; Esteres del ácido carbónico o del ácido halofórmico. › Esteres de compuestos hidroxilados cuyo grupo hidroxilo esterificado está unido a un átomo de carbono de un ciclo aromático de seis miembros.
- C07D207/08 C07 […] › C07D COMPUESTOS HETEROCICLICOS (Compuestos macromoleculares C08). › C07D 207/00 Compuestos heterocíclicos que contienen ciclos de cinco miembros no condensados con otros ciclos, con solamente un átomo de nitrógeno como heteroátomo. › con radicales hidrocarbonados, sustituidos por heteroátomos, unidos a los átomos de carbono del ciclo.
- C07D491/04 C07D […] › C07D 491/00 Compuestos heterocíclicos que contienen en el sistema cíclico condensado, a la vez uno o más ciclos que tienen átomos de oxígeno como únicos heteroátomos del ciclo, y uno o más ciclos que tienen átomos de nitrógeno como únicos heteroátomos del ciclo, no previstos en los grupos C07D 451/00 - C07D 459/00, C07D 463/00, C07D 477/00 ó C07D 489/00. › Sistemas orto-condensados.
- C07F7/08C6D
Clasificación PCT:
- C07C39/21 C07C 39/00 […] › estando al menos un grupo hidroxilo unido a un ciclo no condensado.
- C07C69/017 C07C 69/00 […] › Esteres de compuestos hidroxilados cuyo grupo hidroxilo esterificado está unido a un átomo de carbono de un ciclo aromático de seis miembros.
- C07D207/08 C07D 207/00 […] › con radicales hidrocarbonados, sustituidos por heteroátomos, unidos a los átomos de carbono del ciclo.
- C07D491/04 C07D 491/00 […] › Sistemas orto-condensados.
- C07F7/10 C07 […] › C07F COMPUESTOS ACICLICOS, CARBOCICLICOS O HETEROCICLICOS QUE CONTIENEN ELEMENTOS DISTINTOS DEL CARBONO, HIDROGENO, HALOGENOS, OXIGENO, NITROGENO, AZUFRE, SELENIO O TELURO (porfirinas que contienen metal C07D 487/22; compuestos macromoleculares C08). › C07F 7/00 Compuestos que contienen elementos de los grupos 4 o 14 del sistema periódico. › que contienen nitrógeno.
Fragmento de la descripción:
Proceso para la preparación de asenapina y productos intermedios usados en dicho proceso.
Esta presente invención se refiere a un proceso novedoso para la preparación de trans-5-cloro-2-metil-2,3,3a,12b-tetrahidro-1H-dibenz[2,3:6,7]oxepino[4,5-c]pirrol, así como a productos intermedios novedosos para uso en dicho proceso.
El trans-5-cloro-2-metil-2,3,3a,12b-tetrahidro-1H-dibenz[2,3:6,7]oxepino[4,5-c]-pirrol, que se conoce comúnmente como asenapina, es un compuesto que tiene actividad depresora del SNC y que tiene actividades de antihistamina y antiserotonina (Patente de Estados Unidos 4.145.434 para van den Burg). Se han revisado el perfil farmacológico de la asenapina, su cinética y metabolismo y sus primeros estudios de seguridad y eficacia en voluntarios humanos y en pacientes de esquizofrenia (De Boer et al., Drugs of the Future, 18(12), 1117-1123, 1993). Se ha establecido que la sal maleato de asenapina, conocida como Org 5222, es un antagonista de amplio espectro y alta potencia de serotonina, noradrenalina y dopamina.
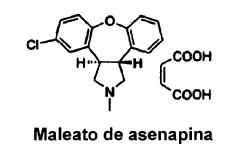
La asenapina muestra actividad potencialmente antipsicótica y puede ser útil en el tratamiento de la depresión (véase la Solicitud de Patente Internacional WO 99/32108). En la Solicitud de Patente Internacional WO 95/23600 (Akzo Nobel N.V.) se ha descrito una preparación farmacéutica adecuada para la administración sublingual o bucal de maleato de asenapina. El maleato de asenapina es ahora el objeto de estudios clínicos, haciendo necesaria la síntesis a gran escala de la sustancia farmacológica.
En la Patente de Estados Unidos Nº 4.145.434 se describe una metodología general para la preparación de asenapina. Se han presentado las propiedades físico-químicas de la sustancia farmacológica Org 5222 (Funke et al. Arzneim.-Forsch/Drug.Res. 40, 536-539, 1990). También se han descrito los métodos sintéticos adicionales para la preparación de Org 5222 y derivados radiomarcados de los mismos (Vader et al., J. Labelled Comp. Radiopharm. 34, 845-869, 1994).
Existe una necesidad de procedimientos sintéticos para la preparación de asenapina que se puedan realizar fácilmente a una escala industrial.
La presente invención proporciona un proceso para la preparación de trans-5-cloro-2-metil-2,3,3a,12b-tetrahidro-1H-dibenz[2,3:6,7]oxepino[4,5-c]pirrol (Fórmula I)
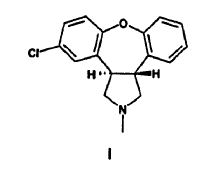
caracterizado por que un derivado de E-estilbeno de Fórmula II
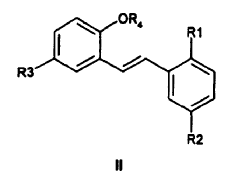
se hace reaccionar con un iluro de azometino para proporcionar un derivado de trans-pirrolidina de Fórmula III
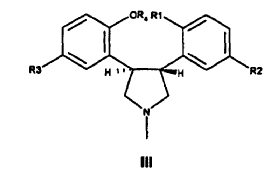
En la Fórmula II y la Fórmula III, R1 es F, Br o I;
R2 y R3 son diferentes y cada uno se selecciona entre H y Cl; y
R4 es H o un grupo protector de hidroxilo. La retirada posterior del grupo protector, cuando está presente, y el tratamiento en condiciones que efectúan un cierre intramolecular del anillo producen el compuesto de Fórmula I.
En la definición de la Fórmula II, R4 puede ser un grupo protector de hidroxi que es estable en las condiciones de reacción que conducen al derivado de trans-pirrolidina de la Fórmula III. Son ejemplos de dichos grupos protectores el grupo tetrahidropiranilo, un grupo protector de sililo o un grupo acilo. En la técnica se conocen ejemplos adicionales. Véase, por ejemplo, Wuts, P.G.M. y Greene, T.W.: Protective Groups in Organic Synthesis, Tercera Edición, Wiley, New York, 1999. Un grupo protector preferido es el grupo acilo, especialmente el grupo acetilo.
A lo largo de esta descripción, los compuestos representados mediante fórmulas estructurales que tienen un par de enlaces en cuña discontinua y en negrita, como se muestra, por ejemplo, en la fórmula de los compuestos (I) y (III), se refieren al diastereoisómero "trans". Cada uno de los compuestos puede existir como un enantiómero simple que tiene la configuración estereoquímica absoluta de los enlaces en cuña o que tiene la configuración absoluta opuesta o como una mezcla de enantiómeros (por ejemplo, racemato) que tiene la configuración estereoquímica relativa indicada mediante los enlaces en cuña.
En una primera etapa de reacción del proceso de la invención, un derivado de E-estilbeno de Fórmula II se hace reaccionar en una reacción de cicloadición dipolar [3+2] con un iluro de azometino generado in situ para proporcionar un derivado de trans-pirrolidina de Fórmula III. Se piensa que la reacción produce de una manera coordinada en la que todos los enlaces se crean simultáneamente. Por consiguiente, se conserva la estereoquímica en el producto. Cuando la reacción se inicia con un derivado de E-estilbeno, se forma exclusivamente el anillo de trans pirrolidina. La estereoselectividad de la etapa de adición dipolar en el proceso de la invención representa una gran ventaja con respecto al buen rendimiento total del proceso.
El iluro de azometino requerido que se puede representar mediante la siguiente estructura bipolar
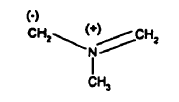
se puede generar, por ejemplo, in situ a partir de N-óxido de trimetilamina dihidrato (TMNO2H2O), N-óxido de trimetilamina anhidrato (TMNO) con diisopropilamida de litio (LDA) o tetrametilpiperidida de litio. La reacción de adición dipolar puede realizarse mediante la adición de LDA a una mezcla de un E-estilbeno de Fórmula II y TMNO en un disolvente aprótico tal como tetrahidrofurano. Preferiblemente, se añade lentamente LDA para controlar la temperatura de reacción, preferiblemente por debajo de 30ºC y para efectuar la disolución del N-óxido de trimetilamina.
Cuando R1 es Br o I en la Fórmula II, la adición dipolar usando TMNO produjo la pirrolidina de Fórmula III con un buen rendimiento y pureza y se demostró que era posible cristalizar los derivados de la pirrolidina resultante de Fórmula III directamente a partir de una mezcla de n-pentano/acetato de etilo o una mezcla de etanol/agua.
En un proceso preferido, el iluro de azometino requerido se genera in situ a partir de N-metoximetil-N-trimetil-sililmetil-N-metilamina (Fórmula 3, a continuación) mediante la activación con ácido trifluoroacético o fluoruro de cesio (Hosomi, A. et al. Chem. Lett. 1117-1120, 1984).
El aminometil éter novedoso (3) se puede preparar a partir de la alquilación de metilamina mediante (clorometil)trimetilsilano (1) para producir la amina secundaria (2) que se puede tratar posteriormente con formaldehído en solución de metanol:
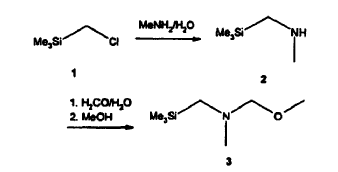
El uso del reactivo (3) ofrece muchas ventajas. Por ejemplo, el proceso de la invención puede realizarse con rendimientos más altos porque el reactivo aminometil éter permite el uso de volúmenes más pequeños de disolvente. Además, el uso del reactivo (3) proporciona un método más seguro porque el proceso de generación del iluro de azometino es mucho menos exotérmico en comparación con el proceso que usa N-óxido de trimetilamina. Además, el reactivo (3) no reacciona en ninguna proporción apreciable con el derivado de Z-estilbeno de manera que la síntesis puede tolerar más cantidad del isómero Z.
En una realización preferida, la reacción de adición dipolar se realiza usando derivados de estilbeno de Fórmula II en la que R4 representa un grupo protector. El grupo protector, tal como un grupo acetilo, desactiva el grupo hidroxi-fenilo para reacciones de sustitución aromática que pueden competir con la reacción de adición dipolar que conduce a la pirrolidina de Fórmula II. Como resultado se puede minimizar la aparición de productos secundarios.
En una segunda etapa del proceso, un derivado de trans-pirrolidina de Fórmula IIIA,
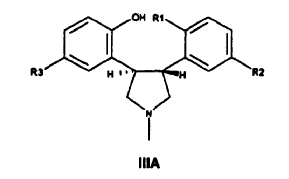
Reivindicaciones:
1. Un proceso para preparar la asenapina de Fórmula I,
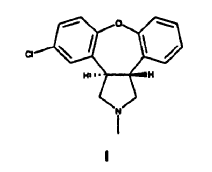
o una sal farmacéuticamente aceptable de la misma, caracterizado por que un derivado de E-estilbeno de Fórmula II.
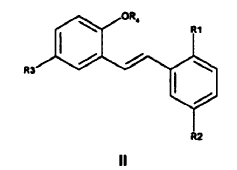
se hace reaccionar con un iluro de azometino para proporcionar un derivado de trans-pirrolidina de Fórmula III,
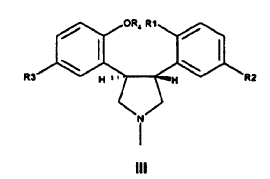
del que se retira el grupo protector, cuando está presente, y que se trata posteriormente en condiciones que efectúan una reacción de cierre intramolecular del anillo para producir el compuesto de Fórmula I y opcionalmente convertir el compuesto de Fórmula I en una sal farmacéuticamente aceptable del mismo, en la que
R1 es F, Br o I;
R2 y R3 son diferentes y cada uno se selecciona entre H y Cl; y
R4 es H o un grupo protector de hidroxilo.
2. El proceso de la reivindicación 1, en el que R1 es Br o I.
3. El proceso de la reivindicación 2, en el que R1, es Br, R2 es H y R3 es Cl.
4. El proceso de una cualquiera de las reivindicaciones 1-3, en el que el iluro de azometino se genera in situ a partir de N-óxido de trimetilamina o a partir de N-metoximetil-N-trimetilsililmetil-N-metilamina.
5. El proceso de la reivindicación 4, en el que el iluro de azometino se genera in situ a partir de N-óxido de trimetilamina junto con di-isopropilamida de litio o tetrametilpiperidida de litio.
6. El proceso de la reivindicación 4, en el que el iluro de azometino se genera a partir de N-metoximetil-N-trimetilsililmetil-N-metilamina con la ayuda de ácido trifluoroacético.
7. Un proceso para preparar el compuesto de Fórmula I,
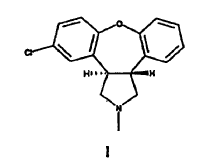
o una sal farmacéuticamente aceptable del mismo, en el que se hace reaccionar acetato de (E)-2-(2-bromoestiril)-4-clorofenilo,
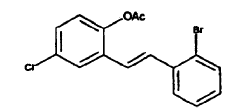
en un disolvente inerte con un iluro de azometino generado in situ a partir de N-metoximetil-N-trimetilsililmetil-N-metilamina con la ayuda de ácido trifluoroacético para proporcionar trans-N-metil-2-bromofenil-3-(2-acetoxi-5-clorofenil)-pirrolidina,
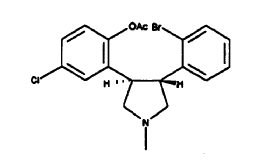
cuyo derivado de pirrolidina se trata para retirar el grupo acetilo y que se trata posteriormente en condiciones de Ullman con la ayuda de la sal de cobre (I) para efectuar el cierre intramolecular del anillo para dar el compuesto de Fórmula I y opcionalmente convertir el compuesto de Fórmula I en una sal farmacéuticamente aceptable del mismo.
8. El derivado de trans-pirrolidina de Fórmula IIIA,
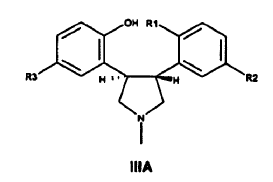
o una sal del mismo,
en la que R1 es F, Br o I y
R2 y R3 son diferentes y cada uno se selecciona entre H y Cl.
9. El derivado de trans-pirrolidina de la reivindicación 8, que es trans-N-metil-2-bromofenil-3-(2-hidroxi-5-clorofenil)-pirrolidina.
10. El derivado de E-estilbeno de Fórmula II,
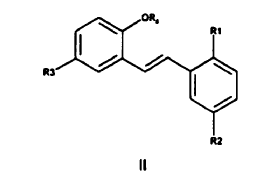
en el que
R1 es F, Br o I;
R2 y R3 son diferentes y cada uno se selecciona entre H y Cl; y
R4 es H o un grupo protector hidroxilo.
11. El compuesto N-metoximetil-N-trimetilsililmetil-N-metilamina.
Patentes similares o relacionadas:
Imidazopirazinas tricíclicas fusionadas como moduladores de la actividad de TNF, del 27 de Mayo de 2020, de UCB Biopharma SPRL: Un compuesto de fórmula (I) o un N-óxido del mismo, o una sal o un solvato farmacéuticamente aceptable del mismo: **(Ver fórmula)** en donde n representa un número […]
Nuevos compuestos antibacterianos, del 1 de Abril de 2020, de AZIENDE CHIMICHE RIUNITE ANGELINI FRANCESCO A.C.R.A.F. S.P.A.: Compuesto de fórmula: : A-L1-Y-L2-R-B en el que: A es un grupo cíclico que presenta la fórmula (II) siguiente: **(Ver fórmula)** […]
Derivados de quinazolinona como inhibidores de fosfatidilinositol 3-quinasa, del 9 de Octubre de 2019, de GILEAD SCIENCES, INC.: Un compuesto que tiene la estructura de Fórmula (I):**Fórmula** en donde: X, Y y Z se seleccionan independientemente de C(R') y N, en donde al menos uno […]
Derivados tetracíclicos activos como plaguicidas con sustituyentes que contienen azufre, del 18 de Septiembre de 2019, de SYNGENTA PARTICIPATIONS AG: Un compuesto de fórmula I,**Fórmula** en donde A1 representa S, O o NCH3; A2, A3, A4 y A5, independientemente entre sí, representan CR3 o N; […]
6H-isocromeno[3,4-c]piridinas y benzo[c][1,7]naftiridin-6-(5H)-onas como inhibidores de la cinasa asociada a adaptador 1 (AAK1), del 22 de Mayo de 2019, de BRISTOL-MYERS SQUIBB COMPANY: Un compuesto de fórmula (I)**Fórmula** o una sal farmacéuticamente aceptable del mismo, en donde: X se selecciona entre O y NR5; R1 y R2 se seleccionan independientemente […]
Proceso para la producción de compuestos de triprenilfenol, del 8 de Mayo de 2019, de TMS Co., Ltd: Un método de producción de un compuesto de triprenilfenol de Stachybotrys microspora, comprendiendo el método: en primer lugar, cultivar un hongo filamentoso usando un medio […]
Derivados de heterociclil-butanamida, del 22 de Febrero de 2019, de MERCK PATENT GMBH: Los compuestos de la fórmula I**Fórmula** en la que W representa**Fórmula** en la que * indica el punto de unión al resto propileno, X […]
Formas cristalinas de 2-((4S)-6-(4-clorofenil)-1-metil-4H-benzo[c]isoxazolo[4,5-e]azepin-4-il)acetamida, del 13 de Febrero de 2019, de Constellation Pharmaceuticals, Inc: Forma A monohidrato cristalina de 2-((4S)-6-(4-clorofenil)-1-metil-4H-benzo[c]isoxazolo[4,5-e]azepin- 4-il)acetamida, en la que la forma cristalina está caracterizada […]