ESTRUCTURA CRISTALIZADA DE PROTEINA AURORA-2 Y SUS BOLSILLOS DE UNION.
Un cristal perteneciente al grupo espacial P3221 y que tiene parámetros de celda unitaria de a=b=87 ± 2Å,
c=76 ±2 Å; a,ß=90º y ?=120º, que comprende una molécula o complejo molecular que comprende los residuos de aminoácidos 107-403 de la SEQ ID NO:1 de una proteína quinasa Aurora -2 no fosforilada de acuerdo con la Figura 1, 2, 3 o 4, donde la desviación cuadrática media de los átomos del esqueleto entre los residuos de aminoácidos de dicha molécula o complejo molecular y dichos residuos de aminoácidos de Aurora-2 no es mayor que 5 Å
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US03/13605.
Solicitante: VERTEX PHARMACEUTICALS INCORPORATED.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 130 WAVERLY STREET,CAMBRIDGE, MA 02139-4242.
Inventor/es: KNEGTEL, RONALD, WEBER, PETER, CHEETHAM,GRAHAM, SWENSON,LOVORKA, COLL,JOYCE,T, RENWICK,SUZANNE.
Fecha de Publicación: .
Fecha Concesión Europea: 17 de Febrero de 2010.
Clasificación Internacional de Patentes:
- C12N9/12B1
Clasificación PCT:
- A61K31/517 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › condensadas en orto o en peri con sistemas carbocíclicos, p. ej. quinazolina, perimidina.
- C07D401/14 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07D COMPUESTOS HETEROCICLICOS (Compuestos macromoleculares C08). › C07D 401/00 Compuestos heterocíclicos que contienen dos o más heterociclos, que tienen átomos de nitrógeno como únicos heteroátomos del ciclo, siendo al menos un ciclo de seis miembros con solamente un átomo de nitrógeno. › que contienen tres o más heterociclos.
- C07D403/12 C07D […] › C07D 403/00 Compuestos heterocíclicos que contienen dos o más heterociclos, que tienen átomos de nitrógeno como únicos heteroátomos del ciclo, no previstos por el grupo C07D 401/00. › unidos por una cadena que contiene heteroátomos como enlaces de cadena.
- C07D417/12 C07D […] › C07D 417/00 Compuestos heterocíclicos que contienen dos o más heterociclos, teniendo al menos un ciclo átomos de nitrógeno y azufre como únicos heteroátomos del ciclo, no previstos por el C07D 415/00. › unidos por una cadena que contiene heteroátomos como enlaces de cadena.
Clasificación antigua:
- A61K31/517 A61K 31/00 […] › condensadas en orto o en peri con sistemas carbocíclicos, p. ej. quinazolina, perimidina.
- C07D401/14 C07D 401/00 […] › que contienen tres o más heterociclos.
- C07D403/12 C07D 403/00 […] › unidos por una cadena que contiene heteroátomos como enlaces de cadena.
- C07D417/12 C07D 417/00 […] › unidos por una cadena que contiene heteroátomos como enlaces de cadena.
Fragmento de la descripción:
Estructura cristalina de proteína Aurora-2 y sus bolsillos de unión.
Esta solicitud reivindica el beneficio de la solicitud provisional de Estados Unidos Núm. 60/377.510, presentada el 1 de mayo de 2002, cuya descripción se incorpora en la presente por referencia.
Campo técnico de la invención
La presente invención describe moléculas o complejos moleculares cristalinos que comprenden bolsillos de unión de Aurora-2 o sus homólogas. La presente invención también se refiere a cristales que comprenden Aurora-2. En el contexto de la presente invención también se divulgan métodos para utilizar las coordenadas estructurales para resolver la estructura de proteínas homólogas o complejos de proteínas. Además, se divulgan métodos de uso de coordenadas estructurales para diseñar compuestos, que incluyen compuestos inhibidores y anticuerpos, que se unen a Aurora-2 o sus homólogas en el contexto de la presente invención.
Antecedentes de la invención
Las proteína quinasas median la transducción de señales intracelulares al producir una transferencia de fosforilo de un nucleósido trifosfato a una proteína aceptora involucrada en una vía de señalización. Existen numerosas quinasas y vías a través de las cuales estímulos extracelulares y otros determinan que una variedad de respuestas celulares ocurran en el interior de la célula. Ejemplos de tales estímulos incluyen señales de estrés ambientales y químicos (por ejemplo, shock osmótico, shock térmico, radiación ultravioleta, endotoxinas bacterianas, H2O2), citoquinas (por ejemplo, interleuquina-1 (IL-I) y factor de necrosis tumoral a (TNF-a)), factores de crecimiento (por ejemplo, factor estimulante de colonias de granulocitos-macrófagos (GM-CSF) y factor de crecimiento de fibroblastos (FGF). Un estímulo extracelular puede afectar a una o más respuestas celulares relacionadas con el crecimiento, migración y diferenciación celular, secreción de hormonas, factores de activación de transcripción, contracción muscular, metabolismo de la glucosa, control de síntesis de proteínas y regulación del ciclo celular.
Muchos estados de enfermedad se asocian con respuestas celulares anormales desencadenadas por eventos mediados por proteína quinasas. Estas enfermedades incluyen enfermedades autoinmunes, enfermedades inflamatorias, enfermedades neurológicas y neurodegenerativas, cáncer, enfermedades cardiovasculares, alergias y asma, enfermedad de Alzheimer y enfermedades relacionadas con hormonas. En consecuencia, una comprensión de la estructura, función e inhibición de la actividad de quinasa podría conducir a terapias humanas útiles.
Entre las quinasas de importancia medicinal se hallan las serina/treonina quinasas. La familia de serina treonina quinasas incluye las proteína quinasas activadas por mitógenos de mamíferos (MAP). Las quinasas MAP se activan por fosforilación dual de treonina y tirosina en el segmento Thr-X-Tyr del bucle de activación. Los miembros de la familia de quinasas MAP también comparten semejanza de secuencia y dominios estructurales conservados, e incluyen las quinasas reguladas por señales extracelulares (ERK), quinasas Jun N-terminales (aNKs) y quinasas p38. Las quinasas MAP también fosforilan varios sustratos que incluyen los factores de transcripción, que a su vez regulan la expresión de conjuntos de genes específicos y median una respuesta específica al estímulo.
Otro grupo importante de la familia de serina/treonina quinasas incluye un subgrupo de tres proteína quinasas de serina/treonina estrechamente relacionadas, las quinasas Aurora. Las quinasas Aurora cumplen un papel clave en los eventos de fosforilación de proteínas que regulan la fase mitótica del ciclo celular. La Aurora-2, por ejemplo, se regula por aumento durante la fase M del ciclo celular y se localiza en el polo del huso durante la mitosis, lo que sugiere una posible participación en las funciones del centrosoma. Las quinasas Aurora comparten una estructura común, que incluye un dominio catalítico altamente conservado, y un dominio N-terminal muy corto que varía en tamaño (R. Giet y C. Prigent, J. Cell Sci., 112, pp. 3591-3601 (1999)). Los dominios N-terminales no comparten ninguna semejanza de secuencia. Las quinasas Aurora se sobreexpresan en varios tipos de cáncer, tales como colon, mama y otros tumores sólidos (para una revisión, véase T. M. Goepfert y B. R. Brinkley, Curr. Tap. Dev. Biol., 49, pp. 331-342 (2000)). Más importante aún, ambos genes de Aurora-1 y 2 se amplifican en cánceres de mama y colorrectal mientras que el gen de Aurora-3 se ubica en una región que está reordenada o suprimida en varias células cancerosas. La sobreexpresión de Aurora-2 en fibroblastos de roedores induce la transformación, lo que indica que Aurora-2 es oncogénica. Recientemente, la expresión de ARNm de Aurora-2 se ha vinculado con la inestabilidad cromosómica en cánceres de mama humanos (Y. Miyoshi et al., Int. J. Cancer, 92, pp. 370-373 (2001)).
Por consiguiente, ha habido interés en hallar inhibidores de Aurora-1, Aurora-2 o Aurora-3 que sean efectivos como agentes terapéuticos. Ha sido un desafío hallar inhibidores de proteína quinasas que actúen de modo selectivo para las quinasas de la familia Aurora. Debido a que existen numerosas proteína quinasas involucradas en una variedad de respuestas celulares, los inhibidores no selectivos pueden producir efectos secundarios no deseables. En este aspecto, la estructura tridimensional de la quinasa debe contribuir al diseño racional de los inhibidores. La determinación de los residuos de aminoácidos en los bolsillos de unión de Aurora-2 y la determinación de la forma de esos bolsillos de unión permitiría diseñar inhibidores selectivos que se unan favorablemente a esta clase de enzimas. La determinación de los residuos de aminoácidos en los bolsillos de unión de Aurora-2 y la determinación de la forma de estos bolsillos de unión también permitiría diseñar inhibidores que puedan unirse selectivamente a Aurora-1, Aurora-2 o Aurora-3, o a cualquiera de sus combinaciones.
A pesar del hecho de que se han aislado genes para varias Aurora-1, Aurora-2 y Aurora-3 y se conocen las secuencias de aminoácidos de Aurora-1, Aurora-2 y Aurora-3, la información de coordenadas estructurales del cristal por rayos X de la proteína Aurora-1, Aurora-2 o Aurora-3 aún no ha sido descrita. Dicha información sería útil para identificar y diseñar inhibidores terapéuticos de las quinasas Aurora o sus homólogas.
Sumario de la invención
La presente invención se refiere a los siguientes aspectos:
1. Un cristal perteneciente al grupo espacial P3221 y que tiene parámetros de celda unitaria de a=b=87
2. El cristal de acuerdo con el aspecto 1, donde dicho cristal además comprende una entidad química, en el que la entidad química se selecciona del grupo que consiste en (5-metil-2H-pirazol-3-il)-(2-(piridin-3-ilmetilamino)-quinazolin-4-il)-amina, (5-ciclopropil-2H-pirazol-3-il)-(2-fenil-quinazolin-4-il)-amina, (5-metiltiazol-2-il)-(2-fenil-quinazolin-4-il)-amina, adenosina, ATP, un análogo de ATP y un nucleótido trifosfato.
3. El cristal de acuerdo con el aspecto 2, en el que dicha entidad química se selecciona del grupo que consiste en (5-metil-2H-pirazol-3-il)-(2-(piridin-3- ilmetilamino)-quinazolin-4-il)-amina, (5-ciclopropil-2H-pirazol-3-il)-(2-fenil-quinazolin-4-il)-amina, (5-metiltiazol-2-il)-(2-fenil-quinazolin-4-il)-amina y adenosina.
4. El cristal de acuerdo con el aspecto 1, donde dicho cristal además comprende un bolsillo de unión definido por las coordenadas estructurales de un conjunto de residuos de aminoácidos que corresponden a los residuos de aminoácidos de Aurora-2 L139, L194, L210, E211, A213, L263 y W277 de acuerdo con cualquiera de las Figuras 1-4, donde la desviación cuadrática media de los átomos del esqueleto entre los residuos de aminoácidos de dicha molécula o complejo molecular y dichos residuos de aminoácidos de Aurora-2 no es mayor que aproximadamente 3 Å.
5. El cristal de acuerdo con el aspecto 1, donde dicho cristal además...
Reivindicaciones:
1. Un cristal perteneciente al grupo espacial P3221 y que tiene parámetros de celda unitaria de a=b=87
2. El cristal de acuerdo con la reivindicación 1, donde dicho cristal además comprende una entidad química, donde la entidad química se selecciona del grupo que consiste en (5-metil-2H-pirazol-3-il)-(2-(piridin-3-ilmetilamino)-quinazolin-4-il)-amina, (5-ciclopropil-2-pirazol-3-il)-(2-fenil-quinazolin-4-il)-amina, (5-metiltiazol-2-il)-(2-fenil-quinazolin-4-il)-amina, adenosina, ATP, un análogo de ATP y un nucleótido trifosfato.
3. El cristal de acuerdo con la reivindicación 2, en el que dicha entidad química se selecciona del grupo que consiste en (5-metil-2H-pirazol-3-il)-(2-(piridin-3-ilmetilamino)-quinazolin-4-il)-amina, (5-ciclopropil-2H-pirazol-3-il)-(2-fenil-quinazolin-4-il)-amina, (5-metiltiazol-2-il)-(2-fenil-quinazolin-4-il)-amina y adenosina.
4. El cristal de acuerdo con la reivindicación 1, donde dicho cristal además comprende un bolsillo de unión definido por las coordenadas estructurales de un conjunto de residuos de aminoácidos que corresponden a los residuos de aminoácidos de Aurora-2 L139, L194, L210, E211, A213, L263 y V277 de acuerdo con una cualquiera de las Figuras 1-4, donde la desviación cuadrática media de los átomos del esqueleto entre los residuos de aminoácidos de dicha molécula o complejo molecular y dichos residuos de aminoácidos de Aurora-2 no es mayor que aproximadamente 3 Å.
5. El cristal de acuerdo con la reivindicación 1, donde dicho cristal además comprende un bolsillo de unión definido por las coordenadas estructurales de un conjunto de residuos de aminoácidos que corresponden a los residuos de aminoácidos de Aurora-2 L139, G140, F144, V147, A160, K162, L194, L210, E211, Y212, A213, P214, L215, T217, 8220, L263, A273 y W277 de acuerdo con la Figura 3, donde la desviación cuadrática media de los átomos del esqueleto entre los residuos de aminoácidos de dicha molécula o complejo molecular y dichos residuos de aminoácidos de Aurora-2 no es mayor que aproximadamente 3 Å.
6. El cristal de acuerdo con la reivindicación 1, donde dicho cristal además comprende un bolsillo de unión definido por las coordenadas estructurales de un conjunto de residuos de aminoácidos que corresponden a los residuos de aminoácidos de Aurora-2 L139, G140, F144, V147, A160, K162, L194, L210, E211, Y212, A213, P214, L215, T217, R220, L263, A273, W277 y S278 de acuerdo con la Figura 1 o 4, donde la desviación cuadrática media de los átomos del esqueleto entre los residuos de aminoácidos de dicha molécula o complejo molecular y dichos residuos de aminoácidos de Aurora-2 no es mayor que aproximadamente 3 Å.
7. El cristal de acuerdo con la reivindicación 1, donde dicho cristal además comprende un bolsillo de unión definido por las coordenadas estructurales de un conjunto de residuos de aminoácidos que corresponden a los residuos de aminoácidos de Aurora-2 L139, G140, F144, V147, A160, K162, L194, L210, E211, Y212, A213, P214, L215, T217, R220, L263, A273, W277, S278 y V279 de acuerdo con la Figura 2, donde la desviación cuadrática media de los átomos del esqueleto entre los residuos de aminoácidos de dicha molécula o complejo molecular y dichos residuos de aminoácidos de Aurora-2 no es mayor que aproximadamente 3 Å.
8. El cristal de acuerdo con la reivindicación 1, donde dicho cristal además comprende un bolsillo de unión definido por las coordenadas estructurales de un conjunto de residuos de aminoácidos que corresponden a los residuos de aminoácidos de Aurora-2 R137, L139, G140, 6142, F144, 6145, N146, V147, Y148, L149, I158, L159, A160, L161, K162, L194, R195, L208, I209, L210, E211, Y212, A213, P214, L215, T217, V218, Y219, 1220, E260, N261, L262, L263, L264, K271, I272, A273, D274, F275 y W277 de acuerdo con la Figura 3, donde la desviación cuadrática media de los átomos del esqueleto entre los residuos de aminoácidos de dicha molécula o complejo molecular y dichos residuos de aminoácidos de Aurora-2 no es mayor que aproximadamente 3 Å.
9. El cristal de acuerdo con la reivindicación 1, donde dicho cristal además comprende un bolsillo de unión definido por las coordenadas estructurales de un conjunto de residuos de aminoácidos que corresponden a los residuos de aminoácidos de Aurora-2 R137, L139, G140, G142, F144, G145, N146, V147, Y148, L149, I158, L159, A160, L161, K162, L194, R195, L208, I209, L210, E211, Y212, A213, P214, L215, T217, V218, Y219, R220, E260, N261, L262, L263, L264, K271, I272, A273, D274, F275, W277 y S278 de acuerdo con la Figura 1 o 4, donde la desviación cuadrática media de los átomos del esqueleto entre los residuos de aminoácidos de dicha molécula o complejo molecular y dichos residuos de aminoácidos de Aurora-2 no es mayor que aproximadamente 3 Å.
10. El cristal de acuerdo con la reivindicación 1, donde dicho cristal además comprende un bolsillo de unión definido por las coordenadas estructurales de un conjunto de residuos de aminoácidos que corresponden a los residuos de aminoácidos de Aurora-2 R137, L139, G140, G142, F144, G145, N146, VI47, Y148, L149, I158, L159, A160, L161, K162, L194, R195, L208, I209, I210, E211, Y212, A213, P214, L215, T217, V218, Y219, R220, E260, N261, L262, L263, L264, K271, I272, A273, D274, F275, W277, S278 y V279 de acuerdo con la Figura 2, donde la desviación cuadrática media de los átomos del esqueleto entre los residuos de aminoácidos de dicha molécula o complejo molecular y dichos residuos de aminoácidos de Aurora-2 no es mayor que aproximadamente 3 Å.
11. El cristal de acuerdo con la reivindicación 1, donde dicho cristal además comprende un bolsillo de unión definido por las coordenadas estructurales de un conjunto de residuos de aminoácidos que corresponden a los residuos de aminoácidos de Aurora-2 F133, I135, G136, R137, P144, N146, V147, Y148, L149, A150, R151, E152, I158, L159, A160, L161, K162, V163, V182, E183, Q185, H190, N192, I193, L194, 8195, L196, Y197, G198, Y199, F200, V206, Y207, L208, I209, L210, E211, Y212, A213, P214, L215, T217, V218, Y719, R220, E221, D229, E230, Q231, R232, T233, A234, T235, Y236, I237, T238, E239, L240, A241, N242, A243, L244, S245, Y246, C247, H248, S249, K250, R251, V252, I253, H254, R255, D256, L257, K258, P259, E260, N261, L262, L263, L264, G265, S266, G268, E269, L270, K271, I272, A273, D274, F275 y W277 de acuerdo con la Figura 3, donde la desviación cuadrática media de los átomos del esqueleto entre los residuos de aminoácidos de dicha molécula o complejo molecular y dichos residuos de aminoácidos de Aurora-2 no es mayor que aproximadamente 3 Å.
12. El cristal de acuerdo con la reivindicación 1, donde dicho cristal además comprende un bolsillo de unión definido por las coordenadas estructurales de un conjunto de residuos de aminoácidos que corresponden a los residuos de aminoácidos de Aurora-2 F133, I135, G136, R137, F144, N146, V147, Y148, L149, A150, R151, E152, I158, L159, A160, L161, K162, V163, V182, E183, Q185, H190, N192, I193, L194, R195, L196, Y197, G198, Y199, F200, V206, Y207, L208, I209, L210, E211, Y212, A213, P2I4, L215, T217, V218, Y219, R220, E221, D229, E230, Q231, R232, T233, A234, T235, Y236, I237, T238, E239, L240, A241, N242, A243, L244, S245, Y246, C247, H248, S249, K250, R251, V252, I253, H254, R255, D256, I257, K258, P259, E260, N261, L262, L263, L264, G265, S266, G268, E269, L270, K271, I272, A273, D274, F275, W277 y S278 de acuerdo con la Figura 1 o 4, donde la desviación cuadrática media de los átomos del esqueleto entre los residuos de aminoácidos de dicha molécula o complejo molecular y dichos residuos de aminoácidos de Aurora-2 no es mayor que aproximadamente 3 Å.
13. El cristal de acuerdo con la reivindicación 1, donde dicho cristal además comprende un bolsillo de unión definido por las coordenadas estructurales de un conjunto de residuos de aminoácidos que corresponden a los residuos de aminoácidos de Aurora-2 F133, I135, G136, R137, F144, N146, V147, Y148, L149, A150, R151, E152, I158, LI59, A160, L161, K162, V163, V182, E183, Q185, H190, N192, I193, L194, R195, L196, Y197, G198, Y199, F200, V206, Y207, L208, I209, L210, E211, Y212, A213, P214, L215, T217, V218, Y219, R220, E221, D229, E230, Q231, R232, T233, A234, T235, Y236, I237, T238, E239, L240, A241, N242, A243, L244, S245, Y246, C247, H248, S249, K250, R251, V252, I253, H254, R255, D256, I257, K258, P259, E260, N261, L262, L263, L264, G265, S266, K258, E269, L270, K271, I272, A273, D274, F275, W277, S278 y V279 de acuerdo con la Figura 2, donde la desviación cuadrática media de los átomos del esqueleto entre los residuos de aminoácidos de dicha molécula o complejo molecular y dichos residuos de aminoácidos de Aurora-2 no es mayor que aproximadamente 3 Å.
14. Un método para diseñar, seleccionar y/u optimizar una entidad química que se une a todo o parte del bolsillo de unión o proteína de acuerdo con una cualquiera de las reivindicaciones 1-13, que comprende las etapas de:
(a) proporcionar las coordenadas estructurales de dicho bolsillo de unión o proteína, de acuerdo con la Figura 1, 2, 3 o 4, en un ordenador que comprende el medio para generar la información de la estructura tridimensional a partir de dichas coordenadas estructurales; y
(b) diseñar, seleccionar y/u optimizar dicha entidad química realizando una operación de ajuste entre dicha entidad química y dicha información de la estructura tridimensional de todo o parte de dicho bolsillo de unión o proteína.
15. Un método para evaluar la capacidad de una entidad química para asociarse con todo o parte del bolsillo de unión o proteína de acuerdo con una cualquiera de las reivindicaciones 4-13, que comprende las etapas de:
(a) proporcionar las coordenadas estructurales de dicho bolsillo de unión o proteína, de acuerdo con la Figura. 1, 2, 3 o 4, en un ordenador que comprende el medio para generar información de la estructura tridimensional a partir de dichas coordenadas estructurales;
(b) emplear un medio computacional para realizar una operación de ajuste entre la entidad química y todo o parte del bolsillo de unión o proteína; y
(c) analizar los resultados de dicha operación de ajuste para cuantificar la asociación entre la entidad química y todo o parte del bolsillo de unión o proteína.
16. El método de acuerdo con la reivindicación 15, que además comprende generar una representación gráfica tridimensional de todo o parte del bolsillo de unión o proteína antes de la etapa (b).
17. Un método para identificar un agonista o antagonista de una molécula o complejo molecular de acuerdo con una cualquiera de las reivindicaciones 4-13, que comprende las etapas de:
(a) utilizar una estructura tridimensional del bolsillo de unión o proteína, de acuerdo con la Figura 1, 2, 3 o 4, de la molécula o complejo molecular para diseñar o seleccionar una entidad química;
(b) poner en contacto la entidad química con la molécula o el complejo molecular;
(c) controlar la actividad catalítica de la molécula o el complejo molecular; y
(d) clasificar la entidad química como agonista o antagonista sobre la base del efecto de la entidad química sobre la actividad catalítica de la molécula o el complejo molecular.
18. Un método para diseñar un compuesto o complejo que se asocia con todo o parte del bolsillo de unión de acuerdo con una cualquiera de las reivindicaciones 4-13:
(a) proporcionar las coordenadas estructurales de dicho bolsillo de unión o proteína, de acuerdo con la Figura 1, 2, 3 o 4, en una computadora que comprende el medio para generar información de la estructura tridimensional a partir de dichas coordenadas estructurales; y
(b) utilizar el ordenador para realizar una operación de ajuste para asociar una primera entidad química con todo o parte del bolsillo de unión;
(c) realizar una operación de ajuste para asociar al menos una segunda entidad química con todo o parte del bolsillo de unión;
(d) cuantificar la asociación entre la primera y la segunda entidad química y todo o parte del bolsillo de unión;
(e) opcionalmente repetir las etapas b) a d) con otra primera y segunda entidad química, seleccionar una primera y una segunda entidad sobre la base de dicha asociación cuantificada del total de dichas primera y segunda entidad química;
(f) opcionalmente, inspeccionar en forma visual la relación de la primera y la segunda entidad química entre sí en relación con el bolsillo de unión en una pantalla de ordenador usando la representación gráfica tridimensional del bolsillo de unión y dicha primera y segunda entidad química; y
(g) ensamblar la primera y la segunda entidad química en un compuesto o complejo que se asocia con todo o parte de dicho bolsillo de unión por construcción modelada.
19. Un método de utilización del reemplazo molecular para obtener información estructural acerca de una molécula o un complejo molecular de estructura desconocida, que comprende las etapas de:
(a) cristalizar dicha molécula o complejo molecular;
(b) generar un patrón de difracción de rayos X a partir de dicha molécula o complejo molecular cristalizado; y
(c) aplicar al menos una porción de las coordenadas estructurales de un cristal de acuerdo con una cualquiera de las reivindicaciones 1-13, como se expone en la Figura 1, 2, 3 o 4, o un modelo de homología del mismo, al patrón de difracción de rayos X para generar un mapa de densidad electrónica tridimensional de al menos una porción de la molécula o el complejo molecular cuya estructura es desconocida.
20. El método de acuerdo con la reivindicación 19, en el que la molécula es una proteína Aurora-2 u homóloga.
21. El método de acuerdo con la reivindicación 19, en el que el complejo molecular se selecciona del grupo que consiste en un complejo de la proteína Aurora-2 o un complejo de una homóloga de Aurora-2.
Patentes similares o relacionadas:
COMPOSICIONES Y MÉTODOS QUE UTILIZAN INTERFERENCIA DE ARN DE TIPO CDPK PARA EL CONTROL DE NEMÁTODOS, del 7 de Febrero de 2012, de BASF PLANT SCIENCE GMBH: Un método para conferir resistencia a los nematodos a una planta, comprendiendo dicho método las etapas de: a) preparar un ácido nucleico que codifica una […]
HOMÓLOGO HUMANO DE LA PROTEÍNA "FUSED" DE DROSOPHILA, del 10 de Enero de 2012, de GENENTECH, INC.: Ácido nucleico aislado que comprende ADN que codifica: (i) un polipéptido fused de vertebrado que tiene por lo menos un 80% de identidad en la secuencia de aminoácidos […]
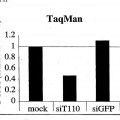 COMPOSICIONES Y MÉTODOS PARA EL DIAGNÓSTICO Y EL TRATAMIENTO DE TUMORES, del 18 de Mayo de 2011, de GENENTECH, INC.: Antagonista de TASK110 para utilizar en un método de inhibición del crecimiento de una célula de cáncer pancreático que expresa un polipéptido que tiene por lo […]
COMPOSICIONES Y MÉTODOS PARA EL DIAGNÓSTICO Y EL TRATAMIENTO DE TUMORES, del 18 de Mayo de 2011, de GENENTECH, INC.: Antagonista de TASK110 para utilizar en un método de inhibición del crecimiento de una célula de cáncer pancreático que expresa un polipéptido que tiene por lo […]
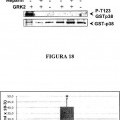 NUEVO SITIO DE FOSFORILACIÓN DE PROTEINAS QUINASAS ACTIVADAS POR MITÓGENO, PROTEÍNAS FOSFORILADAS Y APLICACIONES, del 28 de Abril de 2011, de UNIVERSIDAD AUTONOMA DE MADRID: Una proteína MAPK, donde dicha proteína MAPK is una proteína p38, seleccionada entre: a) una proteína MAPK que comprende un resto fosforilado en un sitio de […]
NUEVO SITIO DE FOSFORILACIÓN DE PROTEINAS QUINASAS ACTIVADAS POR MITÓGENO, PROTEÍNAS FOSFORILADAS Y APLICACIONES, del 28 de Abril de 2011, de UNIVERSIDAD AUTONOMA DE MADRID: Una proteína MAPK, donde dicha proteína MAPK is una proteína p38, seleccionada entre: a) una proteína MAPK que comprende un resto fosforilado en un sitio de […]
PROTEÍNAS DEL FACTOR DE TRANSCRIPCIÓN RELACIONADAS CON EL ESTRÉS Y MÉTODOS DE USO EN PLANTAS, del 16 de Marzo de 2011, de BASF PLANT SCIENCE GMBH: Una planta transgénica transformada por medio de un ácido nucleico que codifica una proteína del factor de transcripción relacionada con el estrés (TFSRP), […]
UN MIEMBRO DE LA FAMILIA DE LAS PROTEÍNA QUINASAS HUMANAS Y USOS DE LA MISMA, del 18 de Enero de 2011, de MILLENNIUM PHARMACEUTICALS, INC.: Un método para identificar un compuesto capaz de tratar un trastorno respiratorio que comprende analizar la capacidad del compuesto o agente […]
PROTEINAS PROTEINA-QUINASA RELACIONADAS CON EL ESTRES Y METODOS DE UTILIZACION EN LAS PLANTAS, del 4 de Octubre de 2010, de BASF PLANT SCIENCE GMBH: Una célula de planta de una monocotiledónea o una dicotiledónea que comprende una casete de expresión que comprende un ácido nucleico codificante de una proteína […]
PLANTAS QUE TIENEN CARACTERISTICAS DE CRECIMIENTO MEJORADAS Y METODO PARA SU ELABORACION, del 3 de Agosto de 2010, de CROPDESIGN N.V.: Método para mejorar las características de crecimiento de las plantas con relación a las correspondientes plantas de control, que comprende: - […]