BIOMARCADORES POLIPEPTIDICOS PARA DIAGNOSTICAR ENFERMEDAD DE ALZHEIMER.
Un péptido que tiene la secuencia de SEQ ID Nº: 4, SEQ ID Nº: 5 o SEQ ID Nº: 6
Tipo: Patente Europea. Resumen de patente/invención. Número de Solicitud: E08002793.
Solicitante: BAYER SCHERING PHARMA AKTIENGESELLSCHAFT.
Nacionalidad solicitante: Alemania.
Dirección: MULLERSTRASSE 178 13353 BERLIN ALEMANIA.
Inventor/es: KONIG, GERHARD, CARRETTE,ODILE, HOCHSTRASSER,DENIS FRANCOIS,PROF. DR, SANCHEZ,JEAN-CHARLES,DR. C/O BIOMEDICAL PROTEOMICS RESEARCH GROUP, YALKINOGLU,OZKAN A.,DR.
Fecha de Publicación: .
Fecha Solicitud PCT: 11 de Agosto de 2003.
Fecha Concesión Europea: 28 de Julio de 2010.
Clasificación Internacional de Patentes:
- C07K14/805 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 14/00 Péptidos con más de 20 aminoácidos; Gastrinas; Somatostatinas; Melanotropinas; Sus derivados. › Hemoglobinas; Mioglobinas.
- C07K14/81B2
- G01N33/68V2
Clasificación PCT:
- G01N33/68 FISICA. › G01 METROLOGIA; ENSAYOS. › G01N INVESTIGACION O ANALISIS DE MATERIALES POR DETERMINACION DE SUS PROPIEDADES QUIMICAS O FISICAS (procedimientos de medida, de investigación o de análisis diferentes de los ensayos inmunológicos, en los que intervienen enzimas o microorganismos C12M, C12Q). › G01N 33/00 Investigación o análisis de materiales por métodos específicos no cubiertos por los grupos G01N 1/00 - G01N 31/00. › en los que intervienen proteínas, péptidos o aminoácidos.
Países PCT: Austria, Bélgica, Suiza, Alemania, Dinamarca, España, Francia, Reino Unido, Grecia, Italia, Liechtensein, Luxemburgo, Países Bajos, Suecia, Mónaco, Portugal, Irlanda, Eslovenia, Finlandia, Rumania, Chipre.
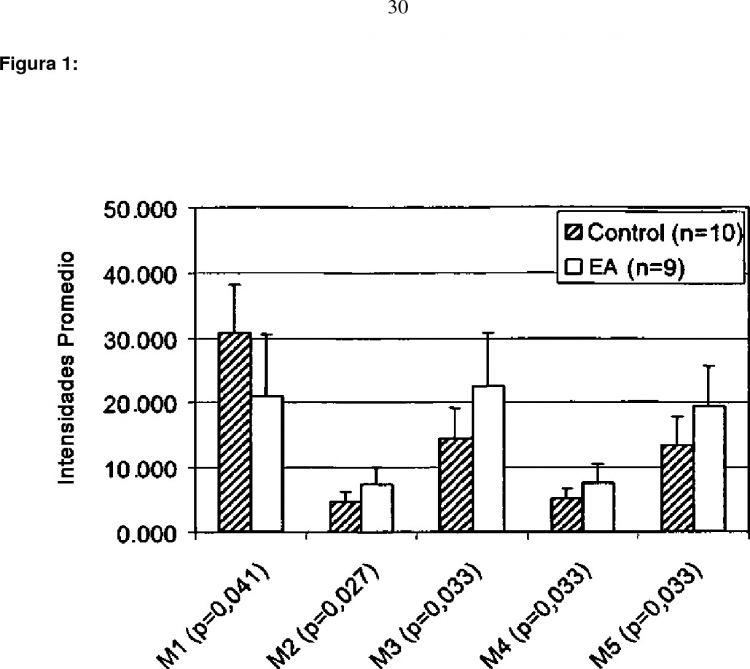
Fragmento de la descripción:
Campo de la invención
La invención está en el campo de los diagnósticos. Más específicamente, la invención está en el campo de evaluar el estrado de la enfermedad de Alzheimer en sujetos por detección de polipéptidos marcadores específicos de la enfermedad de Alzheimer.
Antecedentes de la invención Enfermedad de Alzheimer
La enfermedad de Alzheimer es una forma crecientemente prevalente de neurodegeneración que da cuenta de aproximadamente el 50-60 % de los casos generales de demencia entre la gente por encima de los 65 años de edad. Patológicamente, la neurodegeneración de la enfermedad de Alzheimer se caracteriza por atrofia prominente de estructuras corticolímbicas con muerte neuronal y pérdida de sinapsis neuronales, formación de marañas neurofibrilares, (NFT) y la formación de placas seniles que contienen depósitos de agregados de ß1-42 amiloide (Aß42) en el cerebro [Francis PT 1999]. La duración del declive cognitivo progresivo es aproximadamente 7 años desde la aparición de los primeros signos hasta la muerte. Se asume que la fase clínica está precedida por un periodo preclínico de 15-30 años de deposición continua de placas amiloides y marañas neurofibrilares. La edad de aparición y la progresión de la enfermedad están grandemente determinadas por las mutaciones de los genes causantes y por factores genéticos de susceptibilidad. Se pueden añadir varios factores de riesgo ambientales a los factores de riesgo genéticos individuales. Los factores genéticos conocidos por estar implicados en la forma familiar de enfermedad de Alzheimer con aparición temprana de la enfermedad son: mutaciones en genes de presenilina I (PS1), presenilina 2 (PS2) y proteína precursora amiloide (APP) y la presencia del alelo E4 de la apolipoproteína E4. Sin embargo, la mayoría (95 %) de los casos de enfermedad de Alzheimer son esporádicos y heterogéneos. Actualmente, la diagnosis clínica de la enfermedad de Alzheimer solo puede establecerse en fases más tardías de la enfermedad, cuando la actuación cognitiva está significativamente disminuida por alteraciones estructurales del cerebro. El tratamiento diagnóstico clínico requiere un historial medico cuidadoso; examen físico y neurológico; exámenes de sangre, orina y fluido cerebroespinal (CSF) para excluir estados morbosos metabólicos y médicos que puedan pasar por enfermedad de Alzheimer; exámenes psicométricos detallados para valorar el estado mental y la actuación cognitiva y técnicas de formación de imágenes tales como formación de imágenes de exploración tomográfica computerizada o formación de imágenes de resonancia magnética del cerebro. Las evaluaciones diagnósticas en centros de expertos alcanzan una seguridad de aproximadamente el 80-85 %. Debido al hecho de que estas pruebas son caras y llevan mucho tiempo y son particularmente incómodas para los pacientes, hay una necesidad creciente de marcadores biomoleculares diagnósticos específicos fácilmente accesibles, que puedan medirse en fluidos corporales, tales como CSF, sangre u orina y que tengan un valor predictivo positivo alto para diagnosis de enfermedad de Alzheimer, o que ayudarían a distinguir la enfermedad de Alzheimer de otras formas de demencia. Además, los marcadores fiables sensibles a la progresión de la enfermedad pueden constituir parámetros sustitutos, un prerrequisito principal para la evaluación y el desarrollo de nuevas estrategias terapéuticas orientadas a las causas y modificadoras de la enfermedad en la enfermedad de Alzheimer. Dado que el CSF rodea directamente el cerebro, los cambios en su composición proteica pueden reflejar con la mayor seguridad afecciones patológicas que están asociadas con alteraciones específicas de los patrones de expresión proteicos. Durante la última década, se ha comunicado un número de anormalidades biológicas en el fluido cerebroespinal (CSF) de pacientes de enfermedad de Alzheimer, en particular niveles alterados del fragmento Aß1-42 de la proteína precursora amiloide y niveles alterados de la proteína tau hiperfosforilada. La sensibilidad y especificidad de estos marcadores, sin embargo, es baja o solo modesta [El Ronald and Nancy Reagan Research Institute of the Alzheimer's Association y el National Institute on Aging Working Group, 1998, Robles A 1998, Teunissen CE y col., 2002]. Así, hay una necesidad de biomarcadores novedosos con suficiente sensibilidad y especificidad para (i) detectar enfermedad de Alzheimer tan pronto como sea posible y (ii) permitir la diferenciación de la enfermedad de otros tipos de demencia o enfermedades neurodegenerativas y (iii) realizar seguimiento de eficacia terapéutica como parámetro sustituto, por ejemplo en desarrollo de fármacos clínicos e iniciar farmacoterapia tan pronto como sea posible y posponer pérdida de memoria y progresión de la enfermedad.
Tecnología de Chip Proteico
Una tecnología de chip proteico llamada desorción por láser potenciada de superficie/espectrometría de masas de dispersión de ionización (EM de SELDI-TOF) se ha desarrollado recientemente para facilitar la elaboración de perfiles proteicos de mezclas biológicas completas [Davies HA 2000, Fung ET 2001, Merchant M 2000]. La espectrometría de masas de chip de proteínas se ha usado ya por varios grupos para detectar biomarcadores potencialmente novedosos de próstata y vejiga [Adam BL 2001] o cáncer de mama [Wulfkuhle JD 2001] en suero, plasma seminal, fluido del pezón, orina o extractos celulares. Para una revisión de la búsqueda de biomarcadores usando EM de SELDI-TOF, véase [Issaq HJ 2002].
Cistatina C
Descrita inicialmente en 1961 en el fluido cerebroespinal (CSF), la cistatina C (traza de γ
globulina o post-γ-globulina, nº de acceso P01034) es un inhibidor de proteínasa de cisteína pequeño presente en todos los fluidos corporales humanos a concentraciones fisiológicamente relevantes. El papel fisiológico de cistatina C es probablemente regular actividad proteasa de cisteína extracelular, que resulta de invasión microbiana o de liberación de proteinasas lisosomales a partir de células moribundas o enfermas. La cistatina C colocaliza con ß-amiloide (Aß) en las paredes de las arteriolas en los cerebros de enfermedad de Alzheimer y de angiopatía amiloide cerebral [Levy E 2001]. Hay dos haplotipos comunes del gen CST3 que codifican para cistatina C (A y B) que difieren el uno del otro en tres sitios: dos cambios de pares de bases únicos en la región promotora y uno en el dominio de péptido señal que causan una sustitución de aminoácido (alanina a treonina). Recientemente, los estudios control de casos encontraron asociaciones de CST3 con riesgo incrementado para enfermedad de Alzheimer de aparición tardía [Crawford FC 2000, Finckh U 2000, Beyer K 2001]. La hemorragia cerebral hereditaria con amiloidosis, tipo Islandés (HCHWA-I), también llamada angiopatía amiloide de cistatina C hereditaria (HCCAA), es una forma autonómica dominante de angiopatía amiloide cerebral (CAA). El amiloide depositado en las paredes de los vasos del cerebro está compuesto principalmente de una variante de cistatina C caracterizada por la presencia de sustitución Leu68-GIn [Cohen 1983, Ghiso 1986]. Esta patología está acoplada también a una concentración disminuida de este inhibidor de proteínasa de cisteína principal en el fluido cerebroespinal y conduce a su deposición amiloide en el cerebro [Grubb AO 1984]. Leung-Tack y col. han purificado también dos isoformas truncadas N-terminales de cistatina C en orina a partir de un paciente quien había recibido transplante renal. De acuerdo con sus datos, la cistatina C (des1-4) tiene un efecto inhibidor sobre dos funciones de células mononucleares periféricas humanas (PMN): liberación de O2 y fagocitosis, que pueden deberse a la secuencia N-terminal 'KPPR'. Sus datos respaldan un papel potencialmente importante para cistatina C como un posible inmunomodulador durante inflamación. La evidencia que se acumulan indican que el daño mediado por radicales libres incrementado a la función celular contribuye al proceso de envejecimiento y a los trastornos neurodegenerativos relacionados con la edad. El estrés oxidativo puede jugar un papel en la enfermedad de Alzheimer, la enfermedad de Parkinson, la esclerosis lateral amiotrófica (ALS). Aunque el daño de los radicales libres a neuronas puede no ser el evento principal que inicie estas enfermedades, parece que el daño de los radicales libres está implicado en la cascada patogenética de estos trastornos.
Beta-2-microglobulina
La beta-2-microglobulina (nº de acceso P01884) constituye el componente constante pequeño del complejo principal de histocompatibilidad (CMH)...
Reivindicaciones:
1. Un péptido que tiene la secuencia de SEQ ID Nº: 4, SEQ ID Nº: 5 o SEQ ID Nº: 6.
2. Un procedimiento de evaluar el estado de la enfermedad de Alzheimer en un sujeto, que comprende la detección de un polipéptido seleccionado del grupo constituido por la secuencia de SEQ ID Nº: 3, SEQ ID Nº: 4, SEQ ID Nº: 5 o SEQ ID Nº: 6 en una muestra del sujeto.
3. Procedimiento de evaluar el estado de la enfermedad de Alzheimer según la reivindicación 2, en el que se detecta al menos un polipéptido adicional seleccionado del grupo constituido por polipéptidos que comprenden SEQ ID Nº: 1, SEQ ID Nº: 2, SEQ ID Nº: 7, SEQ ID Nº: 8, SEQ ID Nº: 9, SEQ ID Nº: 10, SEQ ID Nº: 11, SEQ ID Nº: 12, SEQ ID Nº: 13, SEQ ID Nº: 14, SEQ ID Nº: 15, SEQ ID Nº: 16, SEQ ID Nº: 17 o seleccionado del grupo constituido por cistatina C humana, beta-2-microglobulina humana, el homólogo de 7,7 kD de mioglobina humana, proteína VGF neurosecretora, un fragmento de al menos 5 aminoácidos de cistatina C humana, un fragmento de al menos 5 aminoácidos de beta-2-microglobulina humana, un fragmento de al menos 5 aminoácidos del homólogo de 7,7 kD de mioglobina humana y un fragmento de al menos 5 aminoácidos de proteína VGF neurosecretora.
4. Procedimiento de investigar la progresión de la enfermedad de Alzheimer en un sujeto caracterizado porque se lleva a cabo un procedimiento de la reivindicación 2 ó de la reivindicación 3 con al menos dos muestras distintas extraídas del mismo sujeto.
5. Procedimiento de cualquiera de las reivindicaciones 2 a 4, en el que la detección de dicho(s) polipéptido(s) es por EM de SELDI-TOF.
6. Procedimiento de cualquiera de las reivindicaciones 2 a 5, en el que anticuerpos específicos o anticuerpos que reconocen dichos polipéptidos se usan para la detección de dicho(s) polipéptido(s).
7. Procedimiento de cualquiera de las reivindicaciones 2 a 6, en el que la detección es en una muestra que comprende CSF, sangre, suero, plasma, orina, plasma seminal, fluido del pezón, y/o extractos celulares de dicho paciente.
8. Un kit para evaluar el estado de la enfermedad de Alzheimer que comprende un polipéptido seleccionado del grupo constituido por SEQ ID Nº: 4, SEQ ID Nº: 5 o SEQ ID Nº: 6.
Patentes similares o relacionadas:
Procedimientos y composiciones para el tratamiento de una afección genética, del 24 de Junio de 2020, de Sangamo Therapeutics, Inc: Una célula precursora de glóbulos rojos genomanipulada caracterizada por una modificación genómica dentro del exón 2 o el exón 4 de BCL11A o dentro de BCL11A-XL […]
Solución conservante para hemoproteína, y procedimiento de estabilización de hemoproteína, del 29 de Abril de 2020, de EIKEN KAGAKU KABUSHIKI KAISHA: Un procedimiento de estabilización de una hemoproteína, en el que se hace coexistir un ácido disulfónico o una de sus sales en una muestra que comprende una […]
MEDICAMENTO ÚTIL COMO SUSTITUTO SANGUÍNEO PARA TRATAR, A LA VEZ, LA ANEMIA AGUDA POR PÉRDIDA DE SANGRE Y LA INFECCIÓN BACTERIANA EN MAMÍFEROS, del 27 de Febrero de 2020, de UNIVERSIDAD AUSTRAL DE CHILE: La presente invención se refiere al uso de la hemoglobina extracelular aislada de purificada de un anélido nativo de Chile, preferentemente de la especie […]
Secreción de polipéptidos que contienen hemo, del 19 de Febrero de 2020, de Impossible Foods Inc: Método de producción de un polipéptido que contiene hemo seleccionado del grupo que consiste en una leghemoglobina, una eritrocruorina, una hemoglobina no simbiótica, […]
Elementos reguladores distales de bcl11a como dianas para la reinducción de la hemoglobina fetal, del 12 de Abril de 2019, de THE CHILDREN'S MEDICAL CENTER CORPORATION: Un método para producir una célula progenitora hematopoyética que tiene disminución del ARNm o la expresión proteica de BCL11A, el método comprende […]
Procedimiento para retirar hemoglobina no modificada de soluciones de hemoglobina reticulada que incluyen hemoglobina polimérica con aparato de tratamiento térmico de corta duración a altas temperaturas, del 21 de Febrero de 2018, de Billion King International Limited: Un procedimiento para la preparación de una composición farmacéutica que contenga un portador de oxígeno altamente purificado y termoestable, incluyendo […]
Composiciones hemoactivas y procedimientos para su fabricación y uso, del 10 de Enero de 2018, de FUSION MEDICAL TECHNOLOGIES, INC.: Material hemoactivo seco que comprende: un polímero biológicamente compatible reticulado que forma un hidrogel cuando se expone a la sangre; y un polímero […]
Composiciones de hemoglobina y métodos de uso, del 12 de Abril de 2017, de Boston Therapeutics, Inc: Un método para producir una molécula híbrida de hemoglobina, útil para formar un sustituto de sangre estable, a partir de hemoglobina contenida en una solución […]