FORMA DE DOSIFICACIÓN OSMÓTICA DE LIBERACIÓN PROLONGADA.
Un comprimido con forma de dosificación que comprende una capa de fármaco,
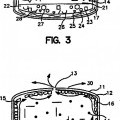
así como una pared interna en contacto con la capa de fármaco, y esta pared comprende una mezcla del 40% al 99% en peso de etilcelulosa y del 1% al 60% en peso de hidroxialquilcelulosa, con un peso total de la mezcla de la composición igual al 100% en peso, y una pared externa en contacto con la pared interna, y la pared externa comprende acetato de celulosa y al menos una salida que conecta el entorno exterior con la capa de fármaco, y dicha capa de fármaco comprende un analgésico opioide y opcionalmente un analgésico no opioide
Tipo: Patente Europea. Resumen de patente/invención. Número de Solicitud: E05075190.
Solicitante: ALZA CORPORATION.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 1900 CHARLESTON ROAD MOUNTAIN VIEW, CA 94043 ESTADOS UNIDOS DE AMERICA.
Inventor/es: WONG, PATRICK, S.- L., EDGREN, DAVID, E., LI, SHU, BHATTI, GURDISH, K., SKLUZACEK, ROBERT, R.
Fecha de Publicación: .
Fecha Solicitud PCT: 26 de Febrero de 1999.
Clasificación Internacional de Patentes:
- A61K9/00L4
- A61K9/20H6D
Clasificación PCT:
- A61K9/24 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 9/00 Preparaciones medicinales caracterizadas por un aspecto particular. › en dosis unitarias constituidas por capas u hojas.
- A61K9/36 A61K 9/00 […] › que contienen hidratos de carbono o sus derivados (A61K 9/34 tiene prioridad).
Clasificación antigua:
Países PCT: Austria, Bélgica, Suiza, Alemania, Dinamarca, España, Francia, Reino Unido, Grecia, Italia, Liechtensein, Luxemburgo, Países Bajos, Suecia, Portugal, Irlanda, Finlandia, Chipre.
PDF original: ES-2357412_T3.pdf

Fragmento de la descripción:
ÁMBITO DE LA INVENCIÓN
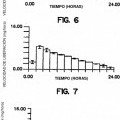
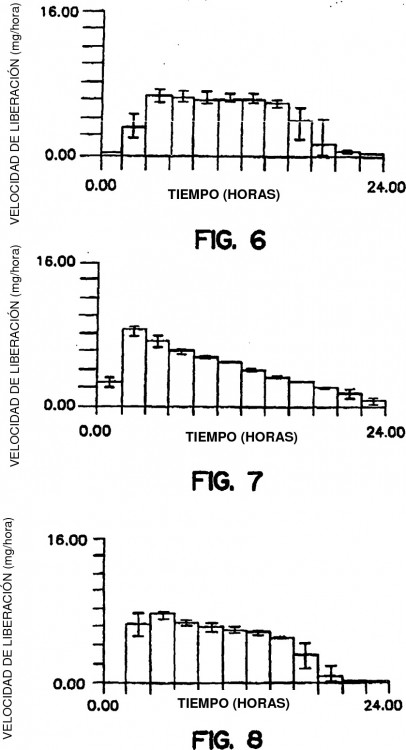
Esta invención se refiere a una forma de dosificación novedosa y terapéuticamente útil. Más en concreto, la invención se refiere a una forma de dosificación que administra una dosis de fármaco de manera prolongada y con liberación lineal para un tratamiento indicado. Específicamente, la invención se refiere a una forma de dosificación que comprende una 5 formulación medicamentosa envuelta por dos paredes, actuando la formulación y las paredes conjuntamente para brindar las características de administración del fármaco, a saber: de manera prolongada y con liberación lineal no descendente. Además, la invención se refiere a un método de administración de la forma de dosificación a fin de brindar una dosis de medicamento o fármaco para tratamiento.
ANTECEDENTES DE LA INVENCIÓN 10
Con el fin de aumentar la eficacia del tratamiento farmacológico y de reducir los posibles efectos secundarios sistémicos, se han realizado muchos intentos de suministrar fármacos de manera controlada a pacientes humanos. Las ventajas de las formas de dosificación con liberación controlada son bien conocidas en el ámbito de las ciencias farmacéuticas y médicas. Los beneficios terapéuticos de la liberación controlada incluyen la capacidad farmacocinética de mantener un nivel preplanificado de un fármaco en sangre, siendo administrado dicho fármaco a lo largo de un 15 período de tiempo comparativamente más largo. Los beneficios terapéuticos incluyen asimismo un aumento simultáneo del cumplimiento del tratamiento por parte del paciente y una reducción del número de dosis de fármaco que se administran a dicho paciente.
Las técnicas conocidas hasta ahora en este campo del conocimiento ponían a la disposición del ser humano una dosificación con liberación controlada cuyo objetivo era proporcionar una velocidad de liberación de fármacos que se 20 adecuaba a los requisitos fisiológicos y cronofarmacológicos de la sangre que imponía el tratamiento. Por ejemplo, en la patente estadounidense núm. 3.845.770 concedida a los solicitantes Theeuwes e Higuchi y en la patente estadounidense núm. 3.916.899 concedida a los mismos solicitantes se presenta una forma de dosificación osmótica para la administración de diversos fármacos en un entorno de uso del paciente. Las formas de dosificación descritas en dichas patentes se fabrican comprendiendo una pared que rodea a un compartimento que comprende un fármaco, con 25 una salida en la pared para administrar el fármaco a un paciente. En las patentes estadounidenses núm. 4.008.719, 4.014.334, 4.058.122, 4.116.241 y 4.160.452, los solicitantes de patente Theeuwes y Ayer describieron formas de dosificación que comprenden una pared interna y una pared externa hechas de poli(acilato de celulosa), para la administración de una dosis de un fármaco a un paciente que lo necesite.
La historia de las formas de dosificación conocidas hasta ahora en este campo indica que existe una necesidad 30 importante de una forma de dosificación novedosa y útil que brinde un avance inesperado en la ciencia de las formas de dosificación. Por ejemplo, las formas de dosificación conocidas anteriormente en este campo carecían de la presente capacidad de enmascarar un sabor desagradable, no mantenían la estabilidad de una formulación medicamentosa y no protegían al medicamento frente a la oxidación. Asimismo, la formulación medicamentosa de la forma de dosificación permitía que la liberación del fármaco disminuyese con el tiempo, con lo que se llegaba a administrar una dosis no 35 terapéutica del mismo. Las paredes de las formas de dosificación expuestas al tracto gastrointestinal eran lipófilas, absorbían las grasas endógenas y, por consiguiente, evidenciaban una reducción de su integridad estructural, como la que se observa en las grietas o fisuras de una pared. Además, la pared de las formas de dosificación y la formulación medicamentosa que contenían no actuaban conjuntamente a fin de brindar unas características de administración lineal controlada del fármaco a lo largo de un período de tiempo extenso. Igualmente, las formas de dosificación conocidas 40 hasta ahora estaban formuladas con componentes lixiviables en agua dentro de la membrana, a fin de controlar la velocidad de administración del fármaco; dicho fármaco era difundido desde la membrana por los componentes lixiviables en agua en sentido opuesto al del flujo osmótico del agua, lo que dificultaba la reproducibilidad y el control de las velocidades de administración, como se observa en la patente estadounidense núm. 5.160.744.
De la presentación realizada hasta aquí se desprende que hace mucho que existe una necesidad palpable de una 45 forma de dosificación que comprenda una estructura con paredes y una formulación medicamentosa que funcionen juntos para la administración oral de un medicamento, de manera tal que se obtenga una liberación controlada y sostenida en el tiempo. Existe la necesidad de una forma de dosificación para administrar un fármaco de manera lineal para tratar enfermedades infecciosas, respiratorias, el sistema cardiovascular, la sangre, el bazo, el aparato digestivo, los trastornos metabólicos, el sistema endocrino, el tracto genitourinario, las enfermedades sexualmente transmisibles, 50 el sistema nervioso, el aparato locomotor y los trastornos psiquiátricos, y también, para proporcionar alivio sintomático. Se necesita una forma de dosificación que sustituya a las formas de dosificación de liberación inmediata, que desaprovechan los fármacos, que se administran tres o cuatro veces al día. Hay motivos importantes para intentar obtener una forma de dosificación que sustituya a las formas de dosificación de liberación inmediata, y son, entre otros: obtener una manera de reducir los episodios de niveles máximos en sangre seguidos de una caída drástica de dichos 55 niveles; obtener una manera de reducir los efectos secundarios; obtener una manera de fabricar la integridad estructural de la forma de dosificación; y obtener una manera de reducir la cantidad de solventes empleados para fabricar la forma de dosificación.
OBJETOS DE LA INVENCIÓN
Por lo tanto, en vista de la presentación realizada, constituye un objeto inmediato de esta invención proporcionar una forma de dosificación novedosa y útil con la que se superen o solventen las desventajas asociadas a las técnicas conocidas hasta ahora en este campo del conocimiento.
Otro objeto de la presente invención es dar respuesta a una necesidad largamente arrastrada, para lo cual, se 5 proporciona una forma de dosificación que administra un fármaco de manera lineal a lo largo del tiempo.
Otro objeto de la presente invención es proporcionar una forma de dosificación que comprenda una formulación que comprenda un fármaco y una primera y segunda paredes y que dicha formulación y paredes funcionen juntas a fin de administrar un fármaco de manera lineal a lo largo de un período de tiempo extenso.
Otro objeto de la presente invención es proporcionar una forma de dosificación que comprenda una pared interna y una 10 pared externa, de manera tal que la pared externa proteja a la pared interna del entorno del tracto gastrointestinal.
Otro objeto de la presente invención es proporcionar una bicapa de paredes que mantenga su integridad física y química durante la administración de un fármaco.
Otro objeto de la presente invención es proporcionar una forma de dosificación fabricada, como dispositivo de administración osmótica de fármacos, mediante procedimientos de fabricación estándar, en tamaños, formas y 15 estructuras que representen un avance en el campo de la administración de fármacos.
Otro objeto de la invención es proporcionar una forma de dosificación que comprenda una pared externa bioprotectora que blinde a la forma de dosificación contra daños o contra su destrucción en un entorno gastrointestinal.
Otro objeto de la invención es proporcionar una forma de dosificación que comprenda etilcelulosa y una pared de hidroxialquilcelulosa formada a partir de un sistema de un único solvente. 20
Otro objeto de la invención es proporcionar una forma de dosificación que comprenda una pared interna que comprenda una etilcelulosa y una hidroxipropilalquilcelulosa blindadas por una pared externa que comprenda un poli(acilato de celulosa) y otros ingredientes conformadores de la pared.
Otro objeto de esta invención es proporcionar una forma de dosificación que comprenda una pared interna que comprenda... [Seguir leyendo]
Reivindicaciones:
1. Un comprimido con forma de dosificación que comprende una capa de fármaco, así como una pared interna en contacto con la capa de fármaco, y esta pared comprende una mezcla del 40% al 99% en peso de etilcelulosa y del 1% al 60% en peso de hidroxialquilcelulosa, con un peso total de la mezcla de la composición igual al 100% en peso, y una pared externa en contacto con la pared interna, y la pared externa comprende acetato de celulosa y al menos una salida que conecta el entorno exterior con la capa de fármaco, y dicha capa de fármaco comprende un analgésico opioide y 5 opcionalmente un analgésico no opioide.
2. Un comprimido con forma de dosificación conforme con la reivindicación 1, en el que la capa de fármaco comprende una sustancia seleccionada del grupo que consta de hidromorfona y las sales farmacéuticamente aceptables de la hidromorfona, acetaminofeno, y un excipiente basado en óxido de polietileno farmacéuticamente aceptable.
3. Un comprimido con forma de dosificación conforme con la reivindicación 1, en el que el analgésico opioide 10 comprende de 0,1 mg a 1000 mg de un sustancia seleccionada del grupo que consta de hidromorfona y sus sales farmacéuticamente aceptables, el analgésico no opioide comprende de 1 mg a 1000 mg de una sustancia seleccionada del grupo que consta de aspirina, flurbiprofeno, ibuprofeno, indoprofeno, benoxaprofeno, propoxifeno, salicilamida, zenazocina y zomepirac, y al menos un excipiente polimérico de los analgésicos opioide y no opioide se selecciona de entre una cantidad de 10 mg a 500 mg de un excipiente basado en poli(óxido de alquileno) farmacéuticamente 15 aceptable y un excipiente basado en carboxialquilcelulosa farmacéuticamente aceptable.
4. Un comprimido con forma de dosificación conforme con la reivindicación 1, en el que la capa de fármaco comprende un primer analgésico seleccionado del grupo que consta de morfina y sus sales farmacéuticamente aceptables, así como un segundo analgésico seleccionado del grupo que consta de acetaminofeno, aspirina, benoxaprofeno, flurbiprofeno, ibuprofeno, indoprofeno, propoxifeno, salicilamida, zenazocina y zomepirac, y un excipiente basado en 20 poli(óxido de alquileno) farmacéuticamente aceptable.
5. Un comprimido con forma de dosificación conforme con la reivindicación 4, en el que la capa de fármaco comprende de 1 mg a 1000 mg del primer analgésico y de 1 mg a 1000 mg del segundo analgésico.
6. Un comprimido con forma de dosificación conforme con la reivindicación 1, en el que la capa de fármaco comprende un 35% en peso de sulfato pentahidrato de morfina, un 58,50% en peso de poli(óxido de etileno), un 6% en peso de 25 poli(vinilpirrolidina), un 0,45% en peso de estearato de magnesio, y un 0,05% en peso de hidroxitolueno butilado.
7. Un comprimido con forma de dosificación conforme con la reivindicación 1, en el que la capa de fármaco comprende un 35% en peso de sulfato pentahidrato de morfina, un 58,50% en peso de poli(óxido de etileno), un 6% en peso de poli(vinilpirrolidina), un 0,45% en peso de estearato de magnesio, y un 0,05% en peso de hidroxitolueno butilado; y además, el comprimido comprende una capa de empuje-desplazamiento que comprende un 93,97% en peso de óxido 30 de polietileno, un 5% en peso de hidroxipropilmetilcelulosa, un 1% en peso de verde óxido férrico, un 0,25% en peso de estearato de magnesio, y un 0,08% en peso de hidroxitolueno butilado; además, la mencionada pared interna comprende polivinilpirrolidona; y la mencionada capa externa comprende un surfactante.
8. Un comprimido con forma de dosificación conforme con la reivindicación 1, en el que el analgésico opioide es hidrocodona o una sal terapéuticamente aceptable de la hidrocodona. 35
Patentes similares o relacionadas:
PROCEDIMIENTO PARA LA PREPARACIÓN DE UNA FORMA DE DOSIFICACIÓN SÓLIDA A PRUEBA DE ABUSO, del 10 de Noviembre de 2011, de GRUNENTHAL GMBH: Procedimiento para la preparación de una forma de dosificación sólida a prueba de abuso que contiene al menos un principio activo susceptible de abuso […]
ELASTÓMEROS DE POLIURETANO, del 12 de Agosto de 2011, de CONTROLLED THERAPEUTICS (SCOTLAND) LTD: Una composición de liberación controlada, que comprende un polímero lineal que puede obtenerse haciendo reaccionar juntos (a) un polietilenglicol o polipropilenglicol; […]
FORMAS DE DOSIFICACIÓN FARMACÉUTICAS ORALES RESISTENTES A MANIPULACIONES QUE INCLUYE UN ANALGÉSICO OPIOIDE, del 21 de Junio de 2011, de PURDUE PHARMA LP: Forma posológica farmacéutica oral sólida de liberación prolongada que comprende una formulación de matriz de liberación prolongada, comprendiendo la formulación […]
PREPARACIONES DE LIBERACIÓN CONTROLADA DE OXCARBAZEPINA QUE TIENEN PERFIL DE LIBERACIÓN SIGMOIDAL, del 3 de Junio de 2011, de SUPERNUS PHARMACEUTICALS, INC.: Una formulación farmacéutica para administración una vez al día de oxcarbazepina constituida esencialmente por una matriz homogénea que comprende: (a) una oxcarbazepina; […]
 FORMAS FARMACÉUTICAS DE DOSIFICACIÓN ORAL RESISTENTES A LA MANIPULACIÓN INDEBIDA QUE COMPRENDEN UN ANALGÉSICO OPIOIDE, del 5 de Mayo de 2011, de PURDUE PHARMA LP: Forma farmacéutica sólida de dosificación oral y liberación prolongada que comprende una formulación matricial de liberación prolongada, comprendiendo la formulación matricial […]
FORMAS FARMACÉUTICAS DE DOSIFICACIÓN ORAL RESISTENTES A LA MANIPULACIÓN INDEBIDA QUE COMPRENDEN UN ANALGÉSICO OPIOIDE, del 5 de Mayo de 2011, de PURDUE PHARMA LP: Forma farmacéutica sólida de dosificación oral y liberación prolongada que comprende una formulación matricial de liberación prolongada, comprendiendo la formulación matricial […]
 FORMAS FARMACÉUTICAS DE DOSIFICACIÓN ORAL RESISTENTES A LA MANIPULACIÓN INDEBIDA QUE COMPRENDEN UN ANALGÉSICO OPIOIDE, del 25 de Abril de 2011, de PURDUE PHARMA LP: Forma farmacéutica sólida de dosificación oral y liberación prolongada que comprende una formulación matricial de liberación prolongada, comprendiendo la formulación matricial […]
FORMAS FARMACÉUTICAS DE DOSIFICACIÓN ORAL RESISTENTES A LA MANIPULACIÓN INDEBIDA QUE COMPRENDEN UN ANALGÉSICO OPIOIDE, del 25 de Abril de 2011, de PURDUE PHARMA LP: Forma farmacéutica sólida de dosificación oral y liberación prolongada que comprende una formulación matricial de liberación prolongada, comprendiendo la formulación matricial […]
 FORMULACIÓN EN COMPRIMIDOS DE LIBERACIÓN EXTENDIDA QUE CONTIENE PRAMIPEXOL O UNA DE SUS SALES FARMACÉUTICAMENTE ACEPTABLES, MÉTODO PARA SU FABRICACIÓN Y SU USO, del 30 de Marzo de 2011, de BOEHRINGER INGELHEIM INTERNATIONAL GMBH: Una formulación en comprimidos de liberación extendida que comprende pramipexol, o su sal farmacéuticamente aceptable, en una matriz que comprende al menos […]
FORMULACIÓN EN COMPRIMIDOS DE LIBERACIÓN EXTENDIDA QUE CONTIENE PRAMIPEXOL O UNA DE SUS SALES FARMACÉUTICAMENTE ACEPTABLES, MÉTODO PARA SU FABRICACIÓN Y SU USO, del 30 de Marzo de 2011, de BOEHRINGER INGELHEIM INTERNATIONAL GMBH: Una formulación en comprimidos de liberación extendida que comprende pramipexol, o su sal farmacéuticamente aceptable, en una matriz que comprende al menos […]
 FORMAS DE DOSIFICACIÓN DE LIBERACIÓN MODIFICADA CON DOS NÚCLEOS Y UNA ABERTURA, del 24 de Marzo de 2011, de MCNEIL-PPC, INC.: Una forma de dosificación que comprende al menos un ingrediente activo, un primer núcleo, y un segundo núcleo, estando cada uno de dichos primer y segundo núcleos rodeados […]
FORMAS DE DOSIFICACIÓN DE LIBERACIÓN MODIFICADA CON DOS NÚCLEOS Y UNA ABERTURA, del 24 de Marzo de 2011, de MCNEIL-PPC, INC.: Una forma de dosificación que comprende al menos un ingrediente activo, un primer núcleo, y un segundo núcleo, estando cada uno de dichos primer y segundo núcleos rodeados […]