DISPOSICION DE MICROSALIENTES QUE PRESENTA UN REVESTIMIENTO QUE CONTIENE UN AGENTE BENEFICIOSO.
Dispositivo (5) para suministrar un agente beneficioso a través de la capa córnea,
comprendiendo el dispositivo:
una pluralidad de microsalientes de perforación de la capa córnea (10) que presentan un ancho y un grosor de aproximadamente 5 micras hasta aproximadamente 50 micras; y
un revestimiento sólido (50) dispuesto sobre por lo menos una parte de dicho microsaliente que presenta un grosor de aproximadamente desde 1 hasta aproximadamente 50 micras, en el que
dicho revestimiento sólido incluye por lo menos un agente beneficioso y por lo menos un portador biocompatible soluble en agua; y
dicho revestimiento está adaptado para ser colocado en contacto con el fluido corporal después de que los microsalientes hayan perforado la capa córnea,
en el que el revestimiento (50) dispuesto sobre por lo menos una parte de dicho microsaliente (10) es una composición que comprende un agente beneficioso y un portador biocompatible, en el que dicha composición se puede aplicar a los microsalientes en forma líquida y está adaptada para formar un revestimiento sólido en dicha disposición de microsaliente, y en el que el revestimiento sólido está adaptado para permitir la liberación del agente beneficioso a partir del revestimiento durante la hidratación del revestimiento
Tipo: Resumen de patente/invención. Número de Solicitud: W0212730US.
Solicitante: ALZA CORPORATION.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 1010 JOAQUIN ROAD,MOUNTAIN VIEW, CA 94043.
Inventor/es: YOUNG, WENDY, A., DADDONA, PETER, E., JOHNSON,JUANITA,A, CORMIER,MICHEL,J.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61B17/20B
- A61K47/42 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 47/00 Preparaciones medicinales caracterizadas por los ingredientes no activos utilizados, p. ej. portadores o aditivos inertes; Agentes de direccionamiento o agentes modificadores enlazados químicamente al ingrediente activo. › Proteínas; Polipéptidos; Sus productos de degradación; Sus derivados, p. ej. albúmina, gelatina or zeína (oligopéptidos que contienen hasta cinco aminoácidos A61K 47/18; poliaminoácidos A61K 47/34).
- A61K9/00M3
- A61K9/00M5B
- A61M37/00 A61 […] › A61M DISPOSITIVOS PARA INTRODUCIR AGENTES EN EL CUERPO O PARA DEPOSITARLOS SOBRE EL MISMO (introducción de remedios en o sobre el cuerpo de animales A61D 7/00; medios para la inserción de tampones A61F 13/26; dispositivos para la administración vía oral de alimentos o medicinas A61J; recipientes para la recogida, almacenamiento o administración de sangre o de fluidos médicos A61J 1/05 ); DISPOSITIVOS PARA HACER CIRCULAR LOS AGENTES POR EL CUERPO O PARA SU EXTRACCION (cirugía A61B; aspectos químicos de los artículos quirúrgicos A61L; magnetoterapia utilizando elementos magnéticos colocados dentro del cuerpo A61N 2/10 ); DISPOSITIVOS PARA INDUCIR UN ESTADO DE SUEÑO O LETARGIA O PARA PONERLE FIN. › Otros aparatos para introducir agentes en el cuerpo (para la reproducción o la fertilización A61B 17/425; aparatos para iontoforesis o cataforesis A61N 1/30 ); Percutanización, es decir, introducción de medicamentos en el cuerpo por difusión a través de la piel (baños de sales A61H 33/04).
Clasificación PCT:
- A61M37/00 A61M […] › Otros aparatos para introducir agentes en el cuerpo (para la reproducción o la fertilización A61B 17/425; aparatos para iontoforesis o cataforesis A61N 1/30 ); Percutanización, es decir, introducción de medicamentos en el cuerpo por difusión a través de la piel (baños de sales A61H 33/04).
Clasificación antigua:
- A61M37/00 A61M […] › Otros aparatos para introducir agentes en el cuerpo (para la reproducción o la fertilización A61B 17/425; aparatos para iontoforesis o cataforesis A61N 1/30 ); Percutanización, es decir, introducción de medicamentos en el cuerpo por difusión a través de la piel (baños de sales A61H 33/04).
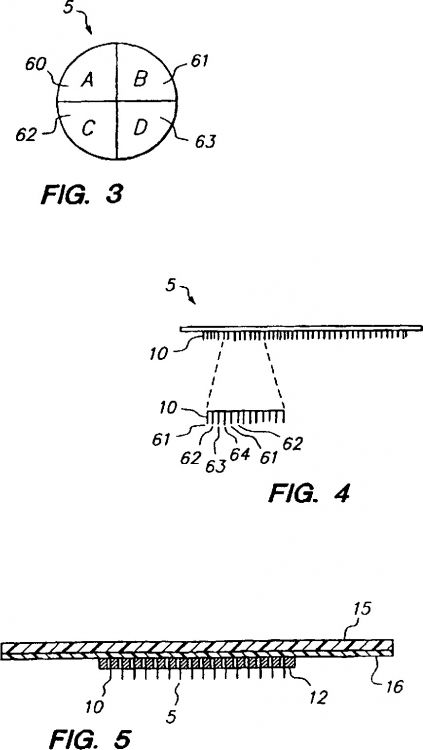
Fragmento de la descripción:
Disposición de microsalientes que presenta un revestimiento que contiene un agente beneficioso.
Campo técnico
La presente invención se refiere a la administración y al suministro transdérmico mejorados de un agente a través de la piel. Más particularmente, la invención se refiere a un sistema de suministro de una medicina para la administración de un agente biológicamente activo a través de la capa córnea utilizando microsalientes para perforar la piel, las cuales tienen un revestimiento sustancialmente seco dispuesto sobre las mismas, en el que un agente beneficioso está contenido en el interior del revestimiento. Los microsalientes perforan la piel únicamente hasta una profundidad muy poco profunda, preferentemente lo suficientemente poco profunda como para alcanzar los capilares que transportan la sangre. El suministro del agente se consigue cuando los microsalientes perforan la capa más exterior de la piel de un paciente y liberan el agente activo contenido en el revestimiento dentro del tejido de la piel del paciente.
Antecedentes de la técnica
De la forma más convencional las medicinas se administran tanto oralmente como mediante inyección. Desgraciadamente, muchos medicamentos son completamente ineficaces o de un rendimiento radicalmente reducido cuando se administran oralmente puesto que tanto dejan de ser absorbidos como se ven afectados adversamente antes de entrar en la corriente sanguínea y por lo tanto no posen la actividad deseada. El suministro transdérmico cuando se compara con el suministro oral evita los rigurosos entornos del tubo digestivo, se desvía del metabolismo gastrointestinal de la medicina, reduce los efectos del primer paso y evita la posible desactivación por las enzimas digestivas y del hígado. Por el contrario, el tubo digestivo no está sometido a la medicina durante la administración transdérmica. Por otra parte, la inyección directa del medicamento dentro de la corriente sanguínea, mientras asegura que el medicamento no se modifica en la administración, es un proceso difícil, inconveniente, doloroso e inconfortable, resultando algunas veces de poca conformidad por parte del paciente. Esto es particularmente cierto para la vacunación de los niños, a los que las vacunas se deben suministrar intramuscularmente en una serie de inyecciones.
Por lo tanto, en principio, el suministro transdérmico proporciona un procedimiento para administrar medicinas que de otro modo sería necesario que fueran suministradas a través de una inyección hipodérmica o una infusión intravenosa.
La palabra "transdérmica" se utiliza en la presente memoria para significar el suministro de un agente (por ejemplo, un agente terapéutico tal como una medicina) dentro o a través de la piel para una terapia local o sistemática. El suministro transdérmico del agente incluye el suministro a través de una difusión pasiva así como mediante otras fuentes de energías externas incluyendo electricidad (por ejemplo, iontoforesis) y ultrasonidos (por ejemplo, fonoforesis). Mientras las medicinas se difunden a través de la capa córnea y la epidermis, la velocidad de difusión a través de la capa córnea intacta es a menudo la etapa limitadora. Muchos compuestos requieren velocidades de suministro más elevadas que las que se pueden conseguir mediante una difusión transdérmica pasiva simple. Cuando se compara con las inyecciones, el suministro transdérmico del agente elimina el dolor asociado y reduce la posibilidad de infección. Teóricamente, el recorrido transdérmico de administración del agente puede ser ventajoso en el suministro de muchas proteínas terapéuticas, porque las proteínas son susceptibles de degradación gastrointestinal y presentan una pobre aceptación gastrointestinal. Además los dispositivos transdérmicos son más aceptables para los pacientes que las inyecciones. Sin embargo, el flujo transdérmico de péptidos y proteínas médicamente útiles a menudo es insuficiente para que sea terapéuticamente eficaz debido al gran tamaño y peso molecular de estas moléculas. A menudo la velocidad de suministro o el flujo es insuficiente para producir el efecto deseado o en el agente se degrada antes de alcanzar el lugar objetivo, por ejemplo la corriente sanguínea del paciente.
Los sistemas de suministro de medicinas transdérmicos pasivos generalmente se basan en una difusión pasiva para administrar la medicina mientras los sistemas de suministro de medicinas transdérmicos activos se basan en una fuente de energía exterior (por ejemplo, electricidad) para suministrar la medicina. Los sistemas de suministro de medicinas transdérmicos pasivos son más comunes. Los sistemas transdérmicos pasivos presentan un receptáculo para la medicina que contiene una elevada concentración de medicina adaptada para entrar en contacto con la piel en la que la medicina se difunde a través de la piel y dentro de los tejidos del cuerpo o de la corriente sanguínea del paciente. El flujo transdérmico de la medicina depende del estado de la piel, tamaño y las propiedades físicas y químicas de la molécula de la medicina y del gradiente de concentración a través de la piel. Debido a la baja permeabilidad de la piel a muchas medicinas, el suministro transdérmico ha tenido limitadas aplicaciones. Esta baja permeabilidad se atribuye principalmente a la capa córnea, la capa más exterior de la piel la cual consiste en unas células planas muertas llenas con fibras de queratina (queratinocitos) rodeadas por dobles capas de lípidos. La estructura altamente ordenada de las capas dobles de lípidos confiere el carácter relativamente impermeable de la capa córnea.
Un procedimiento común para incrementar el flujo de difusión transdérmico pasivo de la medicina implica el tratamiento previo, o suministrándolo conjuntamente con la medicina, con un intensificador de la permeabilidad de la piel. Un intensificador de la permeabilidad, cuando se aplica a una superficie del cuerpo a través de la cual se suministra la medicina, mejora el flujo de la medicina a través de la misma. Sin embargo, el rendimiento de estos procedimientos en intensificar el transporte transdérmico de proteínas ha sido limitado, por lo menos para las proteínas más grandes, debido a su tamaño. Los sistemas de transporte activos utilizan una fuente de energía exterior para ayudar al flujo de la medicina a través de la capa córnea. Un intensificador de este tipo para el suministro transdérmico de medicinas es referido como "electro transporte". Este mecanismo utiliza un potencial eléctrico, el cual resulta de la aplicación de corriente eléctrica para ayudar en el transporte del agente a través de la superficie del cuerpo, tal como por ejemplo la piel. Otros sistemas de transporte activos utilizan ultrasonidos (fonoforesis) o calor como la fuente exterior de energía.
Han existido también muchos intentos en penetrar o alterar mecánicamente las capas más externas de la piel, creando así trayectorias dentro de la piel a fin de intensificar la cantidad de agente que está siendo suministrado transdérmicamente. Recientes dispositivos de vacunación conocidos como escarificadores generalmente tienen una pluralidad de púas o agujas, las cuales se aplican a la piel para rascarla o hacer pequeños cortes en el área de aplicación. La vacuna se aplica entonces tópicamente sobre la piel, tal como se describe en la patente US nº 5.847.726 a favor de Rabenau, o alternativamente, como un líquido humedecido que puede ser aplicado a las púas del escarificador como se representa y describe en la patente US nº 4.453.926 a favor de Galy, o en la patente US nº 4.109.655 a favor de Charcornac, o la patente US nº 3.136.314 a favor de Kravitz. Los escarificadores han sido sugeridos para suministrar vacunas intradérmicas en parte porque únicamente cantidades muy pequeñas de la vacuna necesitan ser suministradas dentro de la piel para que sea eficaz en la inmunización del paciente. Además, la cantidad de vacuna suministrada no es particularmente crítica puesto que una mínima cantidad consigue una inmunización satisfactoria al igual que una cantidad en exceso. Sin embargo, una desventaja seria en la utilización de un escarificador para suministrar una medicina es la dificultad en la determinación del flujo transdérmico de la medicina y la dosificación resultante suministrada porque no se puede determinar si ha sido suministrada la cantidad mínima. Por ejemplo, en muchos casos, el agente dispuesto sobre las púas para perforar la piel de un dispositivo de vacunación intradérmica es empujado fuera de las púas durante la perforación de la piel. Además, muchos agentes beneficiosos no tienen unas buenas características de adherencia, después de ser recubiertos...
Reivindicaciones:
1. Dispositivo (5) para suministrar un agente beneficioso a través de la capa córnea, comprendiendo el dispositivo:
una pluralidad de microsalientes de perforación de la capa córnea (10) que presentan un ancho y un grosor de aproximadamente 5 micras hasta aproximadamente 50 micras; y
un revestimiento sólido (50) dispuesto sobre por lo menos una parte de dicho microsaliente que presenta un grosor de aproximadamente desde 1 hasta aproximadamente 50 micras, en el que
dicho revestimiento sólido incluye por lo menos un agente beneficioso y por lo menos un portador biocompatible soluble en agua; y
dicho revestimiento está adaptado para ser colocado en contacto con el fluido corporal después de que los microsalientes hayan perforado la capa córnea,
en el que el revestimiento (50) dispuesto sobre por lo menos una parte de dicho microsaliente (10) es una composición que comprende un agente beneficioso y un portador biocompatible, en el que dicha composición se puede aplicar a los microsalientes en forma líquida y está adaptada para formar un revestimiento sólido en dicha disposición de microsaliente, y en el que el revestimiento sólido está adaptado para permitir la liberación del agente beneficioso a partir del revestimiento durante la hidratación del revestimiento.
2. Dispositivo según la reivindicación 1, en el que el portador biocompatible incluye ácido poliamínico, polisacárido y/o oligosacárido.
3. Dispositivo según cualquiera de las reivindicaciones anteriores, en el que el portador biocompatible es albúmina humana, dextrán sulfato, polisulfato de pentosán, ácido poliglutámico, ácido poliaspártico, polihistidina y/o un azúcar no reductor.
4. Dispositivo según la reivindicación 1 ó 2, en el que el portador biocompatible es un ácido poliamínico.
5. Dispositivo según la reivindicación 4, en el que el ácido poliamínico es albúmina humana o albúmina humana creada por bioingeniería.
6. Dispositivo según cualquiera de las reivindicaciones anteriores, en el que el agente beneficioso está suspendido en el portador biocompatible.
7. Dispositivo según cualquiera de las reivindicaciones anteriores, en el que el agente beneficioso es una proteína, glicoproteína, péptido, polisacárido, oligosacárido, oligonucleótido y/o ADN.
8. Dispositivo según cualquiera de las reivindicaciones anteriores, en el que el agente beneficioso es una vacuna o un agente desensibilizante.
9. Dispositivo según la reivindicación 1, en el que la composición está en forma de una solución o suspensión acuosa.
10. Dispositivo según la reivindicación 1, en el que la composición está adaptada para formar un revestimiento que presenta una forma vítrea amorfa.
11. Dispositivo según cualquiera de las reivindicaciones anteriores, en el que la relación de todos los portadores biocompatibles con respecto a todos los agentes beneficiosos está comprendida entre 0,2:1 y 5:1 peso/peso, preferentemente entre 0,5:1 y 2:1 peso/peso.
12. Dispositivo según cualquiera de las reivindicaciones anteriores, en el que el portador biocompatible está adaptado para funcionar como un adhesivo para el agente beneficioso sobre los microsalientes.
13. Dispositivo según cualquiera de las reivindicaciones anteriores, en el que la composición puede estar formada como un revestimiento que presenta un grosor entre 1,0 micras y 10 micras.
14. Dispositivo según cualquiera de las reivindicaciones anteriores, en el que el portador biocompatible estabiliza al agente beneficioso.
15. Dispositivo según la reivindicación 1, en el que la composición puede formar un revestimiento que es soluble en el fluido corporal.
16. Dispositivo según cualquiera de las reivindicaciones anteriores, en el que el revestimiento sólido está adaptado para permitir la disolución del agente beneficioso a partir del revestimiento.
17. Dispositivo según cualquiera de las reivindicaciones anteriores, para la utilización en terapia.
Patentes similares o relacionadas:
Preparaciones ácidas de insulina con estabilidad mejorada, del 15 de Julio de 2020, de SANOFI-AVENTIS DEUTSCHLAND GMBH: Formulación farmacéutica que contiene insulina humana Gly(A21),Arg(B31),Arg(B32) y un tensioactivo, elegido de un grupo que contiene Tween 20® y Tween 80®; siendo […]
Marcador molecular para células madre cancerosas, del 29 de Abril de 2020, de Sapporo Medical University: Un péptido seleccionado del grupo que consiste en: DNAJB8 : AFMEAFSSF (SEQ ID NO: 71); DNAJB8 : AYRKLALRW (SEQ ID NO: 68); y DNAJB8 : […]
Variantes de clorotoxina, conjugados y métodos para su utilización, del 8 de Abril de 2020, de FRED HUTCHINSON CANCER RESEARCH CENTER: Conjugado de clorotoxina que comprende un péptido de clorotoxina acoplado covalentemente a un marcador fluorescente seleccionado del grupo que consiste […]
Composición que contiene coenzima Q10, del 25 de Marzo de 2020, de KANEKA CORPORATION: Una composición que contiene coenzima Q10, que comprende 1-70% en peso de coenzima Q10 (A), 15-94% en peso de caseína (B) y al menos 5% en peso de un sacárido […]
Composiciones y métodos para la embolización viral, del 19 de Febrero de 2020, de Sillajen, Inc: Una composición que comprende un virus oncolítico Poxviridae o Herpesviridae y una micropartícula biocompatible o un agente de gel de polímero […]
Cápsulas blandas llenas de líquido, del 12 de Febrero de 2020, de Patheon Softgels Inc: Una composición farmacéutica que comprende una forma de dosificación blanda que comprende un revestimiento que encapsula una matriz líquida, […]
Partículas que contienen un factor de crecimiento y usos de las mismas, del 8 de Enero de 2020, de INSTITUT NATIONAL DE LA SANTE ET DE LA RECHERCHE MEDICALE: Partícula que contiene al menos un polisacárido reticulado covalentemente y al menos un factor de crecimiento, comprendiendo además dicha […]
Un polipéptido de dímero CCL20 bloqueado modificado por ingeniería, del 8 de Enero de 2020, de The Medical College of Wisconsin, Inc: Un polipéptido de dímero CCL20 bloqueado, en donde el dímero comprende dos monómeros unidos covalentemente entre sí, en donde los dos monómeros […]