ARN de interferencia para el tratamiento del Síndrome Linfoproliferativo Autoinmune de tipo la.
ARN de interferencia para el tratamiento del Síndrome Linfoproliferativo Autoinmune de tipo Ia.
La presente invención se refiere a un ARN de interferencia específico del alelo mutado del gen FAS y su uso en el tratamiento del Síndrome Linfoproliferativo Autoinmune de tipo Ia.
Tipo: Patente de Invención. Resumen de patente/invención. Número de Solicitud: P201430504.
Solicitante: FUNDACIÓN PARA LA INVESTIGACIÓN BIOMÉDICA DEL HOSPITAL 12 DE OCTUBRE.
Nacionalidad solicitante: España.
Inventor/es: PAZ ARTAL,Estela, MANCEBO SIERRA,Esther.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K31/7105 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › Acidos ribonucleicos naturales, es decir conteniendo unicamente ribosas unidas a la adenina, la guanina, la citosina, o el uracilo y teniendo enlaces 3'-5' fosfodiester.
- A61P37/00 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › Medicamentos para el tratamiento de problemas inmunológicos o alérgicos.
PDF original: ES-2547471_A1.pdf

Fragmento de la descripción:
La presente invención se refiere a un ARN de interferencia especifico del alelo mutado del gen FAS y su uso en el tratamiento del Sindrome Linfoproliferativo Autoinmune de tipo la. Por lo tanto, la presente invención pertenece al campo de la medicina, en concreto del tratamiento terapéutico de enfermedades autoinmunes.
ESTADO DE LA TÉCNICA El Síndrome Linfoproliferativo Autoinmune (SLPA) es una patología congénita de la apoptosis (muerte celular programada) linfocitaria que causa linfoproliferación y autoinmunidad. La enfermedad se caracteriza por linfadenopatía crónica,
esplenomegalia, citopenias autoinmunes y una expansión anómala de linfocitos T aj3+ CD3+CD4-C08- (a~ dobles negativos) .
Los individuos con SLPA tienen defectos en la vía de apoptosis mediada por el receptor FAS, cuyo funcionamiento es crítico para mantener la tolerancia y 20 homeostasis linfocitarias. Aproximadamente dos tercios de los pacientes con SLPA (correspondientes al denominado tipo la) presentan una mutación germinal en heterocigosis en el gen de FAS (también llamado AP01 , TNFRSF6 Ó CD95) que suele localizarse en la porción intracelular del receptor FAS conocida como dominio de muerte (DO) . La correcta función de este dominio proteico es necesaria para el 25 reclutamiento de la molécula intracelular FADO y la activación de las caspasas que conduce finalmente a la apoptosis. Las mutaciones que afectan al DO actúan en forma "dominante negativa". Esto significa que en individuos heterocigotos y por tanto con un 50% de proteína FAS anómala, las cadenas aberrantes de FAS se incorporan en la mayoría de los homotrímeros FAS (se calcula que esto sucede en 7 de 8 30 homotrímeros) impidiendo la transducción de una señal de muerte eficaz en los linfocitos. Las mutaciones en el DO se asocian con formas severas de la enfermedad y alta penetrancia de los síntomas clínicos. Además , los pacientes con mutaciones germinales en FAS presentan un riesgo relativo 51 veces superior que la población normal de sufrir linfoma de Hodgkin y 14 veces superior de sufrir linfomas no Hodgkin.
Aunque en los últimos años ha mejorado considerablemente, el tratamiento del SLPA no es curativo ni completamente satisfactorio. El cuidado de los pacientes con SLPA incluye consejo genético familiar, vigilancia ante la potencial aparición de linfomas y fármacos inmunosupresores dirigidos principalmente al tratamiento de las citopenias. 5 La prednisona (sola o en combinación con inmunoglobulinas intravenosas) suele administrarse al principio pero sus importantes efectos secundarios, especialmente en niños, impiden un uso continuado. Los pacientes refractarios a corticoides con importantes esplenomegalia e hiperesplenismo pueden beneficiarse del tratamiento con micofenolato mofetilo (MMF) , pero este fármaco no mejora la linfoproliferación ni 10 reduce el número de células dobles negativas y presenta toxicidades como diarrea y neutropenia. La terapia con sirolimus (Rapamicina) , particularmente útil en la recuperación de las células sanguíneas y la reducción de la linfoproliferación, las adenomegalias, esplenomegalia y células dobles negativas, puede causar hipercolesterolemia, hipertensión y alteración de las funciones hepática y renal, y
requiere la cuantificación regular de niveles sanguíneos para asegurar márgenes terapéuticos adecuados. Por último, la administración de rituximab y la esplenectomía se asocian con toxicidades específicas en el SLPA que incluyen profundas y duraderas hipogammaglobulinemias y sepsis mortales respectivamente, por lo que sólo se utilizan en casos muy seleccionados.
La interferencia de RNA es un método ampliamente utilizado para disminuir la abundancia de productos génicos específicos. Este proceso de silenciamiento de la expresión génica, post-transcripcional y específico de secuencia, tiene un gran potencial como herramienta terapéutica en enfermedades en las que teóricamente la inhibición génica puede ser beneficiosa.
Desde hace algún tiempo se viene demostrando la posibilidad de sintetizar moléculas de siRNA capaces de suprimir la expresión del alelo patogénico con preservación de la expresión del alelo normal (wild type) por discriminación de un solo nucleótido.
DESCRIPCiÓN DE LA INVENCiÓN
Los autores de la presente invención han descubierto que la inhibición alelo-específica de las mutaciones en el gen FAS con siRNAs provoca la recuperación de la actividad
funcional de la vía FAS lo que deriva en la muerte celular por apoptosis. Por lo tanto, el proceso de silenciamiento específico en mutaciones del gen FAS permite el tratamiento de sujetos que padecen el Síndrome Linfoproliferativo Autoinmune (SLPA) de tipo la de herencia dominante negativa.
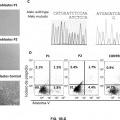
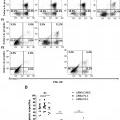
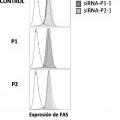
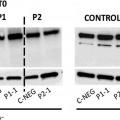
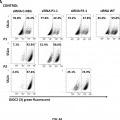
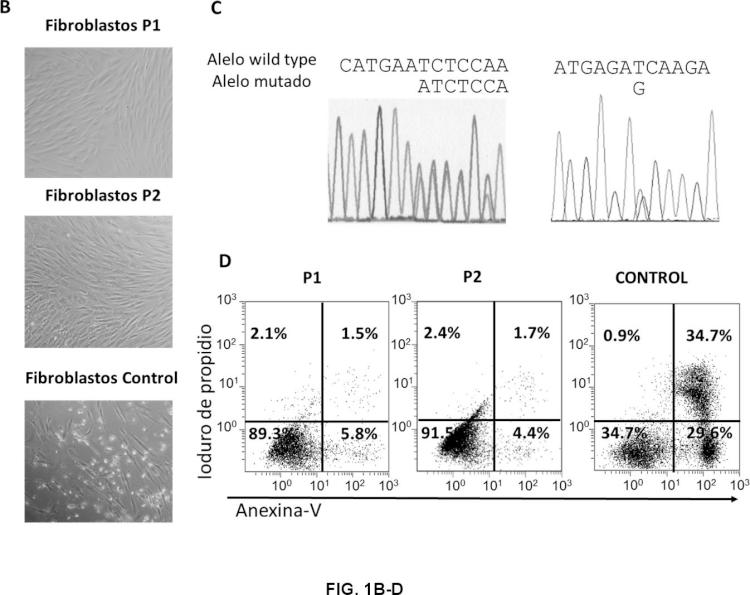
Para ello, se diseñaron varios siRNA dirigidos a mutaciones en el gen FAS en dos pacientes que padecen SLPA de tipo la y se transfectaron los fibroblastos de dichos pacientes con los siRNA diseñados. El tratamiento de los fibroblastos de los pacientes con sus siRNA específicos de los alelas FAS mutados permitió la recuperación de la apoptosis celular, no afectando a fibroblastos control, lo que demostró que efectivamente el silenciamiento afecta sólo a las formas mutadas de FAS y preserva la expresión de moléculas FAS wild type (silvestres) . Sin querer estar vinculados a ninguna teoría, se piensa que esto ocurre por generar mayor cantidad de trímeros FAS funcionales en la superficie celular, logrando incrementar la activación de las caspasas y la desorganización de las mitocondrias, pasos previos a la muerte celular por apoptosis. Por lo tanto, tras la transfección de los fibroblastos se observó una recuperación significativa de la muerte celular respecto a células no transfectadas o células transfectadas con un siRNA control (ver Ejemplo 1) .
ARN de interferencia de la invención La presente invención requiere el diseño de un ARN de interferencia (ARNi o en inglés, iRNA) dirigido a un alelo mutado del gen FAS que, al entrar en la célula, suprime la expresión del alelo patógeno, por lo que la proporción de proteína del alelo silvestre (wild type) se ve aumentada, permitiendo que la vía de señalización de FAS sea funcional.
Por lo tanto, en un aspecto, la presente invención se relaciona con un ARNi específico de un alelo mutado del gen FAS asociado al SLPA de tipo la, de aquí en adelante "ARNi de la invención", en el que dicho ARNi inhibe la expresión de dicho alelo mutado.
En la presente invención se entiende por "ARN de interferencia" (ARNi o iRNA) a la molécula de ácido ribonucleico, de entre 15 a 40 nucleótidos, que suprime la expresión de genes específicos mediante mecanismos conocidos globalmente como ribointerferencia o interferencia por ARN. De entre los tipos de ARNi que existen en el
estado de la técnica, los más adecuados para poner en práctica la presente invención son los siARN y shARN. En una realización particular, el ARNi es un siARN o un shARN.
El acrónimo siARN proviene del inglés small interfering RNA: en español, ARN
interferente pequeño. Son moléculas de ARN bicatenario perfectamente complementarias con 2 nucleótidos desemparejados en cada extremo 3'. Cada hebra de ARN tiene un grupo fosfato 5' y un grupo hidroxilo (-OH) 3'.
Un shARN es una pequeña horquilla de ARN codificada por un AON , de tal forma que cuando se realiza la transcripción (generación del ARN) se genera un ARN autocomplementario que se pliega como una horquilla y que será reconocido por la maquinaria celular como un iARN. Se puede, por tanto, utilizar para silenciar la expresión del gen diana a través de la interferencia de ARN. La expresión de shRNA en las células se realiza típicamente mediante la introducción de plásmidos, que codifican para la formación de shARN, a través de vectores virales.
En el contexto de la presente invención, el ARNi tiene que ser diseñado para que sea específico del alelo mutado del gen FAS
En la presente invención se entiende por "alelo" a la forma alternativa de un gen que se halla en el mismo locus de cromosomas homólogos. Cada individuo presenta dos alelas para un mismo gen, cada uno procedente de uno de sus progenitores. Se entiende por "alelo mutado" al alelo que presenta un cambio en su secuencia de nucleótidos desencadenante de la enfermedad.
En la presente invención se entiende por "alelo mutado del gen FAS" a aquel cambio en la secuencia de nucleótidos del gen FAS que afecta únicamente a uno de sus alelas y que se asocia con el Síndrome Linfoproliferativo Autoinmune (SLPA) de tipo la.
El gen FAS (también llamado AP01, TNFRSF6 o C095) codifica para la proteína FAS
o receptor FAS, una proteína de superficie de 36 kOa... [Seguir leyendo]
Reivindicaciones:
1. Usode -un ARNi específico de un alelo mutado del gen FAS asociado al síndrome 5 Linfoproliferativo Autoinmune (SLPA) de tipo la, en el que dicho ARNi inhibe la
expresión de dicho alelo mutado, -una secuencia de nucleótidos que codifica para dicho ARNi
- un vector que comprende dicha secuencia de nucleótidos, -una célula que comprende dicha secuencia de nucleótidos o dicho vector,
en la elaboración de una composición farmacéutica para el tratamiento del Síndrome Linfoproliferativo Autoinmune (SLPA) de tipo la.
2. Uso según la reivindicación 1, en el que dicho alelo mutado del gen FAS asociado al SLPA de tipo la es:
-la mutación c.979>G de la secuencia de nucleótidos con número de acceso a GeneBank AY495076 (SEO ID NO: 2) , o
-la mutación c.827dupA de la secuencia de nucleótidos con número de acceso a GeneBank EU481974.2 (SEO ID NO: 3) .
3. Uso según la reivindicación 1 ó 2, en el que el ARNi es un siARN o un shARN.
4. Uso según cualquiera de las reivindicaciones 1 a 3, en el que el ARNi comprende: -una primera cadena sentido que comprende una longitud de entre 16 y 30 nucleótidos homólogos a la región del gen FAS que comprende el alelo mutado y la posición nucleotídica mutada de dicho alelo, y -una segunda cadena antisentido que comprende de entre 16 y 30 nucleótidos complementarios a la primera cadena.
5. Uso según la reivindicación 4, en el que la primera cadena sentido comprende la secuencia SEO ID NO: 4 dirigida al alelo mutado del gen FAS portador de la mutación c.979T>G, o la secuencia SEO ID NO: 5 dirigida al alelo mutado del gen FAS portador de la mutación c.827dupA.
6. Método in vitro para determinar si un ARNi es útil en el tratamiento de un sujeto que 35 padece SLPA de tipo la, que comprende: a) poner en contacto un ARNi específico de una mutación en un alelo del gen FAS con un cultivo celular procedente de dicho sujeto, y b) evaluar la apoptosis celular en el cultivo celular procedente del sujeto, en donde un incremento de la apoptosis estadísticamente significativo en el cultivo celular procedente del sujeto con respecto a la apoptosis de un cultivo celular procedente del mismo sujeto tratado con un ARNi control negativo, es indicativo de que el ARNi es útil en el tratamiento del sujeto que padece SLPA de tipo la.
7. Método según la reivindicación 6, en el que previamente a la etapa a) , se determina en una muestra biológica del sujeto la mutación en el alelo del gen FAS y se diseña un ARNi especifico dicha mutación.
8. Método la reivindicación 6 ó 7, en el que la mutación en el alelo del gen FAS se selecciona del grupo que consiste en:
-mutación c.979>G de la secuencia de nucleótidos con número de acceso a GeneBank AY495076 (SEO ID NO: 2) , y -la mutación c.827dupA de la secuencia de nucleótidos con número de acceso a GeneBank EU4819742 (SEO ID NO: 3)
9. Método según cualquiera de las reivindicaciones 6 a 8, en el que el ARNi es un siARN o un shARN.
10. Método según cualquiera de las reivindicaciones 6 a 9, en el que el ARNi comprende:
-una primera cadena sentido que comprende una longitud de entre 16 y 30 nucleótidos homólogos a la región del gen FAS que comprende el alelo mutado y la posición nucleotídica mutada de dicho alelo, y -una segunda cadena antisentido que comprende de entre 16 y 30 nucleótidos complementarios a la primera cadena.
11. Método según la reivindicación 10, en el que la cadena sentido del ARNi comprende la secuencia SEQ ID NO: 4 específica del alelo mutado del gen FAS portador de la mutación c.979T>G, o la secuencia SEQ ID NO: 5 específica del alelo mutado del gen FAS portador de la mutación c.827dupA.
Patentes similares o relacionadas:
Compuestos de heteroaril carboxamida como inhibidores de RIPK2, del 29 de Julio de 2020, de BOEHRINGER INGELHEIM INTERNATIONAL GMBH: Un compuesto de fórmula (I): **(Ver fórmula)** o sus sales farmacéuticamente aceptables, en la que: X es N y Y es CH; o X es CH y Y es N; […]
Derivado heteroarilo o sal farmacéuticamente aceptable del mismo, método de preparación del mismo y composición farmacéutica para prevenir o tratar enfermedades asociadas con PI3 quinasas, que contiene el mismo como principio activo, del 22 de Julio de 2020, de KOREA RESEARCH INSTITUTE OF CHEMICAL TECHNOLOGY: Un compuesto representado por la fórmula 1, un isómero óptico del mismo o una sal farmacéuticamente aceptable del mismo: **(Ver fórmula)** en la fórmula […]
Composición de anticuerpos monoclonales dirigidos contra BDCA-2, del 22 de Julio de 2020, de LABORATOIRE FRANCAIS DU FRACTIONNEMENT ET DES BIOTECHNOLOGIES: Composición de anticuerpos monoclonales dirigidos contra la proteína BDCA-2, presentando dichos anticuerpos un porcentaje de fucosilación inferior al 60% […]
Isotopólogos de 3-(5-amino-2-metil-4-oxoquinazolin-3(4H)-il) piperidina-2-6-diona y métodos de preparación de los mismos, del 15 de Julio de 2020, de CELGENE CORPORATION: Un compuesto de la fórmula: **(Ver fórmula)** o una sal farmacéuticamente aceptable, solvato o hidrato del mismo, en donde: por lo menos uno de Y1,Y2 e Y5 es […]
PTPRS y proteoglicanos en enfermedad autoinmune, del 15 de Julio de 2020, de LA JOLLA INSTITUTE FOR ALLERGY AND IMMUNOLOGY: Una proteína recombinante no enzimática que comprende una secuencia de aminoácidos de un dominio extracelular de PTPRS, donde la proteína comprende tanto el dominio 1 (Ig1) […]
Combinación de anticuerpo anti-CD20 e inhibidor selectivo de PI3 quinasa, del 15 de Julio de 2020, de TG Therapeutics Inc: Un metodo in vitro para inhibir la proliferacion de una poblacion celular que comprende poner en contacto la poblacion con una combinacion que comprende […]
Macrocíclico y composición que comprende el mismo, del 8 de Julio de 2020, de Shenzhen TargetRx, Inc: Un compuesto macrocíclico sustituido, que es un compuesto macrocíclico representado por la fórmula (I), o una forma cristalina, una sal farmacéuticamente […]
Composición farmacéutica que comprende un complejo de carga portador polimérico y al menos un antígeno proteínico o peptídico, del 1 de Julio de 2020, de CureVac AG: Composición farmacéutica que incluye: (A) un complejo de carga portador polimérico, que comprende: a) un portador polimérico que comprende componentes catiónicos reticulados […]