Uso de la cepa CECT 7426 para provocar quorum quenching de la señal autoinductor-2 (AI-2).
Uso de la cepa CECT 7426 para provocar quorum quenching de la señal Autoinductor-2 (AI-2).
La invención se refiere al uso de una cepa bacteriana de la especie Tenacibaculum discolor, del extracto celular crudo o del sobrenadante de sus cultivos, para provocar quorum quenching en bacterias a través de la inhibición de señales tipo AI-2, y más concretamente para el tratamiento y/o prevención de enfermedades infecciosas y para inhibir la formación de biofilms, producidos por dichas bacterias.
Tipo: Patente de Invención. Resumen de patente/invención. Número de Solicitud: P201231552.
Solicitante: UNIVERSIDADE DE SANTIAGO DE COMPOSTELA.
Nacionalidad solicitante: España.
Inventor/es: ROMERO BERNARDEZ,MANUEL, OTERO CASAL,ANA MARIA.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K35/74 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 35/00 Preparaciones medicinales que contienen sustancias de constitución indeterminada o sus productos de reacción. › Bacterias (uso terapéutico de una proteína de la bacteria A61K 38/00).
- A61P31/04 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › A61P 31/00 Antiinfecciosos, es decir antibióticos, antisépticos, quimioterápicos. › Agentes antibacterianos.
PDF original: ES-2482666_A1.pdf
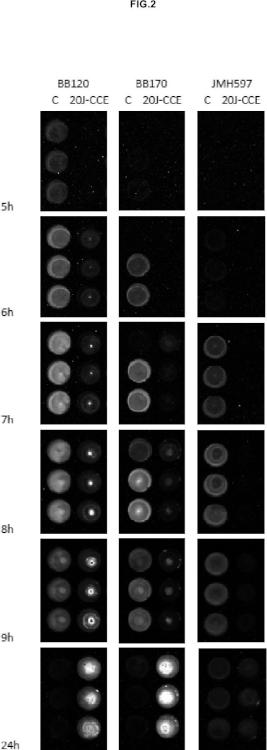
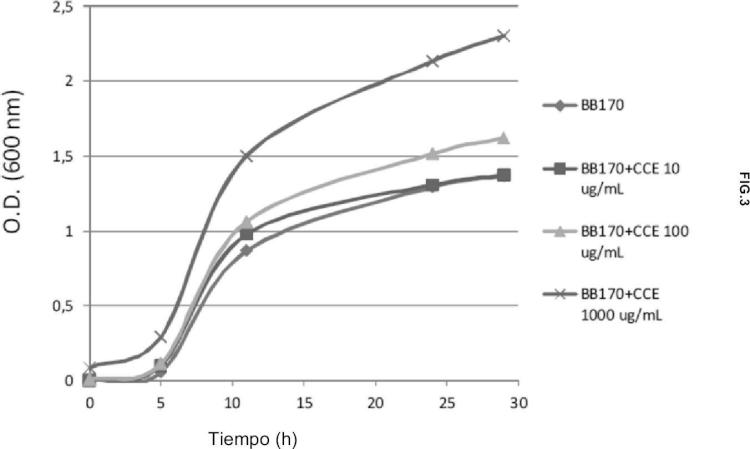
Fragmento de la descripción:
La presente invención se refiere al uso de una cepa bacteriana de la especie Tenacibaculum discolor para el control de enfermedades infecciosas y para inhibir la formación de biofilms producidos por bacterias, a través de la inhibición de las señales de quorum sensing tipo Autoinductor-2 (AI-2). Por tanto, la invención se podría encuadrar en el campo de la biología molecular.
ESTADO DE LA TÉCNICA ANTERIOR
Numerosas especies bacterianas usan un mecanismo de regulación genética coordinada dependiente de la densidad celular. Este mecanismo, conocido como quorum sensincf (QS), consiste en la producción y liberación de moléculas señal al medio, donde se acumulan controlando la expresión de múltiples genes. Mediante la comunicación por QS las poblaciones bacterianas pueden coordinarse para ejecutar importantes funciones biológicas, muchas de ellas implicadas en la virulencia de importantes patógenos, como: movilidad, swarming, agregación, luminiscencia, biosíntesis de antibióticos, expresión de factores de virulencia, simbiosis, formación y diferenciación de biofilms, o transferencia de plásmidos por conjugación, entre otros.
En bacterias Gram negativas, las señales de QS más estudiadas y conocidas son las N-acil-homoserin lactonas (AHLs), mientras que las bacterias Gram positivas usan varias moléculas de naturaleza peptídica. Mientras que los receptores de AHLs suelen ser citoplasmáticos, los receptores de los oligopéptidos presentes en Gram positivos suelen estar en la membrana, por lo que la transducción de señales ocurre mediante una cascada de fosforilación. Existe un tercer tipo de señal de QS, el autoinductor denominado Autoinductor-2 (AI-2). Éste consiste en realidad en una familia de moléculas de estructura similar al diéster furanosil borato descrito por primera vez para Vibrio harveyi, que se encuentra tanto en bacterias Gram positivas como Gram negativas y que son sintetizadas por la proteína LuxS. Por ello, se ha propuesto que AI-2 podría actuar como el lenguaje químico interespecífico más universal (Federle y Bassler, 2003. Journal ofClinical Investigation. 112(9):1291-1299). Para V. harveyi, AI-2 es un (2S,4S)-2-metil-2,3,3,4-tetrahidroxitetrahidrofurano-borato, mientras que el de S. typhimurium es un (2R,4S)-2-metil-2,3,3,4-tetrahidroxitetrahidrofurano. La proteína sintetizadora de AI-2 es LuxS y la búsqueda en bases de datos muestra que este gen está muy extendido, estando presente en aproximadamente 60 especies (Williams et al., 2007. Philosophical Transactions ofthe Royal Society B: Biological Sciences 362: 1119-1134). En algunas de estas bacterias, los sistemas de QS mediados por AI-2 controlan importantes funciones, incluyendo factores de virulencia y formación de biopelículas (Zhang y Dong, 2004. Molecular Microbiology 53; 1563-1571). Así, por ejemplo, se ha mostrado que la deleción del gen luxS en S. mutans afecta a la formación del biofilm (Merritt et al., 2003. Infection and Immunity 71(4): 1972-1979).
Dentro de las bacterias en las que se ha descrito la presencia de señales AI-2, existen distintos patógenos, tanto Gram-positivos como Gram-negativos, en los que además ya se ha demostrado un efecto fisiológico de AI-2 y/o de la mutación de su sintetasa (LuxS), tales como: Borrella burgdorferl, Campilobacter jejuni, Clostridium perfringens, Escherichia coli, Helicobacter pilón, Nelsserla menlngltldls, Salmonella entérica, Serraba marcescens, Shigella flexneri, Streptococcus pneumonlae, Streptococcus pyogenes, Streptococcus suis, Streptococcus anginosus, Streptococcus intermedias, Vibrio choierae, Vibrio vulnificus, Proteus mirabilis, Listeria monocytogenes, Eikenella corrodens, Staphyiococcus epidermidis, Staphyiococcus aureus, Bacilllus subtilis, Klebsiella pneumonlae, Photorhabdus luminescens, Bacteroides sps, Aeromonas hydrophila y Haemophilus influenzae. Otras bacterias no patógenas pero con importancia biotecnológica en las que también se ha demostrado dicho efecto fisiológico de AI-2 y/o de la mutación de su sintetasa LuxS son Lactobacillus rhamnosus y Lactobacillus reuteri (Vendeviile, A. et al. 2005. Nature Reviews Microbiology 3:383-396; Hardie, K.R. and Heurlier, K. 2008. Nature Reviews Microbiology 6:635-643). En concreto, en Staphyiococcus epidermidis y Streptococcus suis, se ha demostrado que las señales AI-2 juegan un papel esencial tanto en la formación de biofilms como en la virulencia de estas bacterias (Xu L, et al. 2006. Infection and Immunity 74(1): 488-96). A pesar de que algunos estudios no pudieron demostrar el papel de AI-2 en la expresión de factores de virulencia de S. aureus, estudios más recientes demuestran que esta molécula interviene en la formación de polisacáridos capsulares, que constituyen la base para la formación de biopelículas (Zhao, L. et al., 2010. Infection and immunity 78 (8): 3506-3515). Además, en Streptococcus mutans, S. oralis o S. gordonii, que poseen homólogos de luxS, una mutación de este gen produce biofilms de estructura alterada, demostrándose que las señales AI-2 regulan el proceso de producción de biopelículas en estos patógenos (Yoshida, A; et al. 2005. Applied and Environmentai Microbiology 71 (5): 2372-2380). Adicionalmente, se ha descrito el
gen luxS en otras bacterias orales tales como Actinobacillus antinomycetemcomitans, con lo que potencialmente deberían producir la señal AI-2.
Como las poblaciones de especies bacterianas coordinadas por QS obtienen importantes ventajas competitivas en sus múltiples interacciones con otros procariotas y eucariotas, sus competidores han desarrollado mecanismos para interferir con su comunicación por sistemas QS. A estos mecanismos se
les conoce como quorum quenching (QQ).
El documento de patente ES2342807B2 describe el uso de bacterias del género Tenacibaculum, y en concreto de la cepa CECT 7426, para provocar QQ a través de la degradación de AHLs, las señales de QS típicas de bacterias Gram negativas, y por tanto sugiere su uso para el tratamiento de enfermedades infecciosas bacterianas y la inhibición de la formación de biofilms en bacterias Gram negativas que utilicen AHLs como mecanismo de coordinación de su virulencia o como mecanismo para la formación de biofilms.
Se han descrito también estrategias de QQ dirigidas a bacterias Gram positivas cuyo objetivo es el bloqueo del regulador agr (accesory gene regulation) o del gen luxS, que está asociado con la síntesis de AI-2 (Voung ef al., 2003. The Journal of Infectious Diseases 188: 706-718; Merritt et al., 2003. Infection and Immunity 71(4): 1972-1979).
Una de las actividades bacterianas de mayor importancia clínica y ecológica en la que intervienen los procesos de quorum sensing es la formación de biofilms, que requiere la producción, por parte de los microorganismos, de estas moléculas señal difusibles.
Los biofilms son películas biológicas que se desarrollan y persisten en las superficies, y que suelen ser estables y difíciles de eliminar debido a la naturaleza protectora de la matriz de polisacárido en la que están embebidos los microorganismos. Pueden definirse como una población bacteriana encerrada dentro de una matriz de polisacárido que se adhiere a las superficies. Se encuentran generalmente en las superficies de los equipamientos industriales que procesan o transportan líquidos, o en las superficies adyacentes a tales equipamientos. A menudo se encuentran en la superficie de los implantes médicos o en los dispositivos insertados en el organismo. También se pueden formar en áreas del cuerpo que están expuestas al aire; en particular en heridas y en la pleura. Uno de los biofilms biológicos que presenta mayor complejidad y de mayor relevancia clínica es la placa dental.
Los medicamentos convencionales, como por ejemplo, los antibióticos, son poco eficaces en infecciones que cursan a través de la formación de biofilms, debido a las barreras de difusión o al estado metabólico de los microorganismos en el biofilm.
Por tanto, mecanismos de interferencia del QS, es decir el QQ, solos o en combinación con antibióticos, constituyen una estrategia interesante en la inhibición de la formación de biofilms, así como en el tratamiento de enfermedades infecciosas por patógenos multirresistentes (March & Bentley, 2004. Current Opinión in Biotechnology 15:495-502). Por ejemplo, se ha propuesto que puede ser útil en el tratamiento de enfermedades, tanto en los animales como en las plantas, provocadas por los géneros Staphylococcus, Pseudomonas, Borrelia, Salmonella, Burkholderia, Serraba, Chromobacteríum, Pectobacterium, Erwinia, Agrobacteríum, o por otras enterobacterias.
Además, el interés de las estrategias de QQ para el tratamiento de enfermedades infecciosas es que, al no afectar directamente a la supervivencia del... [Seguir leyendo]
Reivindicaciones:
1. Uso de una composición que comprende un elemento seleccionado de la lista que consiste en:
a. una cepa bacteriana de Tenacibaculum discolor depositada en la Colección Española de Cultivos Tipo con número de depósito CECT 7426,
b. el extracto celular crudo de un cultivo de la cepa bacteriana de a),
c. el sobrenadante de un cultivo de la cepa bacteriana de a),
o cualquiera de sus combinaciones, para provocar quorum quenching en bacterias productoras de la señal AI-2.
2. Uso según la reivindicación 1 donde la composición es para la elaboración de un medicamento para el tratamiento y/o prevención de infecciones provocadas por bacterias productoras de la señal AI-2.
3. Uso según cualquiera de las reivindicaciones 1 ó 2, donde las bacterias productoras de la señal AI-2 son Gram positivas.
4. Uso según la reivindicación 3, donde las bacterias Gram positivas se seleccionan de la lista que
consiste en: Actinomyces georgiae, Actinomyces odontolyticus, Actinomyces sp., Aerococcus viridans, Alkaliphilus oremlandii, Arthrobacter arilaitensis, Bacillus cellulosilyticus, Bacillus coagulaos, Badilus macauensis, Bacillus selenitireducens, Bacillus smithii, Bacillus subtilis, Bifidobacterium longum, Bifidobacterium breve, Brachybacteríum faecium, Corynebacteríum accoíens,
Corynebacteríum ammonlagenes, Corynebacteríum aurimucosum, Corynebacteríum casei, Corynebacteríum glucuronolyticum, Corynebacteríum glutamicum, Corynebacteríum kroppenstedtii, Corynebacteríum pseudogenitalium, Corynebacteríum striatum, Corynebacteríum tuberculostearicum, Clostridium botulinum, Clostridium cellulovorans, Clostrídium perfríngens, Clostridium sporogenes, Enterococcus faecium, Gemella haemolysans, Gemella morblllorum, Gemella sanguinis, Gordonia polyisoprenivorans, Kurthia sp., Lactobacillus amylovorus, Lactobacillus buchneri, Lactobacillus crispatus, Lactobacillus farciminis, Lactobacillus gasserí, Lactobacillus helveticus, Lactobacillus johnsonii, Lactobacillus kefiranofaciens, Lactobacillus mucosae, Lactobacillus rhamnosus, Lactobacillus reuteri, Lactobacillus ultunensls, Lactobacillus versmoldensis, Lentibacillus sp., Listeria monocytogenes, Mycobacterium sp., Mycobacterium intracellulare, Oenococcus oeni, Omithinibacillus scapharcae, Paenibacillus alvei, Pediococcus pentosaceus, Planococcus antarcticus, Ptanococcus donghaensis, Propionibacterium acnés, Ruminococcus flavefaciens, Solibacillus silvestris, Sporosarcina newyorkensis, Staphylococcus arlettae, Staphylococcus aureus, Staphylococcus capitis, Staphylococcus caprae, Staphylococcus carnosus, Staphylococcus epidermidis, Staphylococcus haemolyticus, Staphylococcus hominis, Staphylococcus lugdunensls, Staphylococcus pettenkoferi, Staphylococcus pseudintermedius, Staphylococcus saprophytlcus, Staphylococcus simiae, Staphylococcus warneri, Streptococcus anginosus, Streptococcus crícetl, Streptococcus cristatus, Streptococcus gordonii, Streptococcus intermedius, Streptococcus mutans, Streptococcus oralis, Streptococcus parasanguinis, Streptococcus pneumoniae, Streptococcus pyogenes, Streptococcus ratti, Streptococcus sanguinis, Streptococcus suis, Thermoanaerobacteríum saccharolyticum, Thermoanaerobacteríum thermosaccharolyticum.
5. Uso según la reivindicación 4, donde las bacterias Gram positivas son Staphylococcus aureus o Streptococcus mutans.
6. Uso según cualquiera de las reivindicaciones 2 a 5, donde las infecciones provocadas por bacterias productoras de la señal AI-2 son debidas a la formación de biofilms.
7. Uso según la reivindicación 6, donde el biofilm es placa dental.
8. Uso según la reivindicación 1 donde la composición es para inhibir la formación ex vivo de biofilms producidos por bacterias productoras de la señal AI-2.
9. Uso según la reivindicación 8, donde las bacterias productoras de la señal AI-2 son Gram positivas.
10. Uso según la reivindicación 9, donde las bacterias Gram positivas se seleccionan de la lista que consiste en: Actinomyces georgiae, Actinomyces odontolyticus, Actinomyces sp., Aerococcus viridans, Alkaliphilus oremlandii, Arthrobacter arilaitensis, Bacillus cellulosilyticus, Bacillus coagulaos, Bacillus macauensis, Bacillus selenitireducens, Bacillus smithii, Bacillus subtilis, Bifidobacterium longum, Bifidobacterium breve, Brachybacteríum faecium, Corynebacteríum accoíens, Corynebacteríum ammonlagenes, Corynebacteríum aurimucosum, Corynebacteríum casei, Corynebacteríum glucuronolyticum, Corynebacteríum glutamicum, Corynebacteríum kroppenstedtii,
Corynebacterium pseudogenitalium, Corynebacterium striatum, Corynebacterium tuberculostearicum, Clostrídium botulinum, Clostridium cellulovorans, Clostridium perfringens, Clostridium sporogenes, Enterococcus faecium, Gemella haemolysans, Gemella morbillorum, Gemella sanguinis, Gordonia polyisoprenivorans, Kurthia sp., Lactobacillus amylovorus, Lactobacillus buchnerí, Lactobacillus crispatus, Lactobacillus farcimlnls, Lactobacillus gasserl, Lactobacillus helveticus, Lactobacillus johnsonü, Lactobacillus kefiranofaclens, Lactobacillus mucosae, Lactobacillus rhamnosus, Lactobacillus reuteri, Lactobacillus ultunensls, Lactobacillus versmoldensis, Lentibacillus sp., Listeria monocytogenes, Mycobacterium sp., Mycobacterlum ¡ntracellulare, Oenococcus oeni, Ornithinibacillus scapharcae, Paenibacillus alvei, Pedlococcus pentosaceus, Planococcus antarcticus, Planococcus donghaensls, Propionibacterium acnés, Rumlnococcus flavefaciens, Solibacillus silvestris, Sporosarcina newyorkensis, Staphylococcus arlettae, Staphylococcus aureus, Staphylococcus capltls, Staphylococcus caprae, Staphylococcus carnosus, Staphylococcus epidermidis, Staphylococcus haemolyticus, Staphylococcus hominis, Staphylococcus lugdunensis, Staphylococcus pettenkoferi, Staphylococcus pseudlntermedius, Staphylococcus saprophyticus, Staphylococcus simiae, Staphylococcus warnerí, Streptococcus anginosus, Streptococcus cricetl, Streptococcus cristatus, Streptococcus gordonii, Streptococcus intermedius, Streptococcus mutans, Streptococcus oralis, Streptococcus parasangulnls, Streptococcus pneumoniae, Streptococcus pyogenes, Streptococcus ratti, Streptococcus sanguinis, Streptococcus suis, Thermoanaerobacterium sacchamlyticum, Thermoanaerobacterium thermosacchamlyticum.
11. Uso según la reivindicación 10, donde las bacterias Gram positivas son Staphylococcus aureus o Streptococcus mutans.
12. Uso según cualquiera de las reivindicaciones 1 a 11, donde la composición además comprende al menos un antibiótico u otro agente antibacteriano.
13. Uso según la reivindicación 1 donde la composición es un aditivo para alimentación animal.
14. Uso según la reivindicación 13 donde el aditivo para alimentación animal es un probiótico.
Patentes similares o relacionadas:
Composiciones que comprenden cepas bacterianas, del 15 de Julio de 2020, de 4D Pharma Research Limited: Una composición que comprende una cepa bacteriana de la especie Eubacterium contortum, en donde la composición no contiene ninguna otra cepa o especie […]
Cepa de Faecaslibacterium Prausnitzii CNCM I-4573 para el tratamiento y la prevención de una inflamación gastrointestinal, del 15 de Julio de 2020, de Institut national de recherche pour l'agriculture, l'alimentation et l'environnement: Cepa bacteriana de la especie Faecalibacterium prausnitzii depositada en la CNCM bajo el número de acceso CNCM I-4573, para su utilización en el tratamiento y/o la prevención […]
BACTERIA DE HOLDEMANELLA SP. Y USO DE LA MISMA, del 2 de Julio de 2020, de CONSEJO SUPERIOR DE INVESTIGACIONES CIENTIFICAS (CSIC): La presente invención se refiere a la cepa de Holdemanella biformis la cepa H. biformis CECT 9752 a sus componentes celulares, metabolitos, […]
Bacteria de Holdemanella sp. y uso de la misma, del 26 de Junio de 2020, de CONSEJO SUPERIOR DE INVESTIGACIONES CIENTIFICAS (CSIC): Bacteria de Holdemanella sp. y uso de la misma. La presente invención se refiere a la cepa de Holdemanella biformis la cepa H. biformis CECT 9752 a […]
COMPOSICIONES HOMEOPÁTICAS A BASE DE VIBRIO PARAHAEMOLYTICUS Y VIBRIO ALGINOLYTICUS Y SU USO COMO INMUNOESTIMULANTES EN EL CULTIVO DE ESPECIES ACUÁTICAS, del 25 de Junio de 2020, de CENTRO DE INVESTIGACIONES BIOLOGICAS DEL NOROESTE, S.C: La presente invención se refiere a composiciones homeopáticas a base de Vibrio parahaemolyticus y Vibrio Alginolyticus para uso inmunoestimulante en acuicultura, […]
Preparación de aceite microbiano que contiene ácidos grasos poliinsaturados, del 10 de Junio de 2020, de DSM IP ASSETS B.V.: Un aceite microbiano que comprende al menos el 50% de ácido araquidónico (ARA) basado en el aceite y que tiene un contenido en triglicéridos de al menos el 90%.
Procedimientos para el tratamiento dietético del síndrome del intestino irritable y la malabsorción de carbohidratos, del 3 de Junio de 2020, de GANEDEN BIOTECH, INC.: Uso de esporas de Bacillus coagulans Hammer en la fabricación de un medicamento para reducir los síntomas del síndrome del intestino irritable (SII) […]
Composiciones farmacéuticas y alimenticias basadas en Hafnia alvei para inducir saciedad y prolongar la saciedad, del 27 de Mayo de 2020, de INSERM (INSTITUT NATIONAL DE LA SANTE ET DE LA RECHERCHE MEDICALE): Un método cosmético no terapéutico para inducir saciedad en un sujeto que lo necesita que comprende administrar oralmente al sujeto una cantidad […]