Formulación de 3-(2-dimetilaminometil-ciclohexil)fenol de efecto retardado.
Forma de dosificación para la liberación controlada del principio activo 3-(2-dimetilaminometilciclohexil)fenol o de una de sus sales farmacéuticamente compatibles,
que
- libera in vitro, medido de acuerdo con la Farmacopea Europea con un aparato agitador de paletas entampón de pH 6,8, una temperatura de 37ºC y a 75 rpm,
- después de 0,5 horas del 9,0 al 31% en peso,
- después de 1 hora del 20 al 48% en peso,
- después de 2 horas del 31 al 65% en peso,
- después de 3 horas del 42 al 76% en peso,
- después de 4 horas del 50 al 83% en peso,
- después de 6 horas del 60 al 94% en peso,
- después de 8 horas del 71 al 99% en peso,
- después de 12 horas más del 79% en peso,
del principio activo contenido originalmente en la forma de dosificación,
- incluye una matriz polimérica basada en un éter o éster de celulosa, que en una concentración del 2,0% enpeso en solución acuosa a 20ºC presenta una viscosidad entre 3.000 y 150.000 mPa·s,estando encapsulada al menos una parte del principio activo en la matriz polimérica,siendo la proporción en peso de la matriz polimérica del 5 al 85% en peso con respecto al peso total de laforma de dosificación, y
seleccionándose el éter o éster de celulosa de entre el grupo consistente en metilcelulosa, etilcelulosa,hidroxietilcelulosa, hidroxipropilcelulosa, carboximetilcelulosa e hidroxipropilmetilcelulosa.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/EP2006/008988.
Solicitante: GRUNENTHAL GMBH.
Nacionalidad solicitante: Alemania.
Dirección: ZIEGLERSTRASSE 6 52078 AACHEN ALEMANIA.
Inventor/es: BARTHOLOMAUS, JOHANNES, JUNG,TOBIAS.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K31/00 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › Preparaciones medicinales que contienen ingredientes orgánicos activos.
- A61K31/133 A61K […] › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › que tienen grupos hidroxilo,p. ej. esfingosina.
- A61K47/38 A61K […] › A61K 47/00 Preparaciones medicinales caracterizadas por los ingredientes no activos utilizados, p. ej. portadores o aditivos inertes; Agentes de direccionamiento o agentes modificadores enlazados químicamente al ingrediente activo. › Celulosa; Sus derivados.
- A61K9/20 A61K […] › A61K 9/00 Preparaciones medicinales caracterizadas por un aspecto particular. › Píldoras, pastillas o comprimidos.
- A61K9/28 A61K 9/00 […] › Grageas; Píldoras o comprimidos con revestimientos.
PDF original: ES-2402206_T3.pdf
Fragmento de la descripción:
Formulación de 3- (2-dimetilaminometil-ciclohexil) fenol de efecto retardado La invención se refiere a una forma de dosificación farmacéutica de liberación controlada de 3- (2-dimetilaminometilciclohexil) fenol, preferentemente de sus estereoisómeros (1R, 2R) , o de una de sus sales farmacéuticamente compatibles.
El 3- (2-dimetilaminometil-ciclohexil) fenol es conocido en el estado actual de la técnica. Se trata de un fármaco de efecto analgésico de administración vía oral (véanse, por ejemplo, los documentos DE-A 195 25 137, WO 02/43712, WO 02/67916 y WO 02/067651) .
Los documentos WO 2005/009329, US 5.601.842 y DE 43 29 794 dan a conocer formas de dosificación farmacéuticas para la liberación retardada de principios activos que están encapsulados por polimerización.
Debido a los dos centros quirales, el 3- (2-dimetilaminometil-ciclohexil) fenol se presenta en forma de cuatro estereoisómeros (dos pares de enantiómeros) , a saber: (1R, 2R) -, (1S, 2S) -, (1R, 2S) -y (1S, 2R) -3- (2dimetilaminometil-ciclohexil) fenol. Estos cuatro estereoisómeros tienen la siguiente estructura:
Las formas de dosificación usuales para la administración oral de 3- (2-dimetilaminometil-ciclohexil) fenol conducen a una liberación rápida de toda la dosis del principio activo en el tracto gastrointestinal, de modo que el efecto analgésico se produce con rapidez. Por ello, hasta la fecha, el tratamiento de dolores crónicos fuertes con 3- (2dimetilaminometil-ciclohexil) fenol requiere la administración del medicamento a intervalos de tiempo relativamente cortos, por ejemplo cuatro a seis veces al día, para asegurar así una concentración suficiente de principio activo en el plasma sanguíneo del paciente durante un período de 24 horas.
La necesidad de una dosificación frecuente conduce con facilidad a errores en la toma y a fluctuaciones no deseadas de la concentración en plasma, lo que resulta perjudicial para el seguimiento del tratamiento por el paciente y a la utilidad terapéutica, sobre todo en caso de tratamientos frente estados de dolor crónico. Además, es sabido que con las formas de dosificación usuales, la administración oral de 3- (2-dimetilaminometil-ciclohexil) fenol puede provocar efectos secundarios, en particular náuseas y vómitos.
Ya es conocida la preparación de formas de dosificación de liberación retardada de los principios activos contenidos en las mismas para asegurar una liberación continua del principio activo durante un período de tiempo más largo.
En el estado actual de la técnica se conocen formulaciones de efecto retardado para una gran cantidad de principios activos. Normalmente, el retardo se consigue mediante revestimientos adecuados y/o encapsulando el principio activo en una matriz de liberación controlada.
En retardo mediante revestimiento, un núcleo que contiene el principio activo se provee de un revestimiento de polímeros hidrófilos y/o hidrófobos que retrasa la liberación del principio activo. En el caso de matrices, el principio activo está encapsulado en una matriz polimérica que controla su liberación.
Sin embargo, para obtener un perfil de liberación determinado para un principio activo no es posible partir sin más de una composición conocida del estado actual de la técnica con el perfil de liberación deseado y sustituir simplemente el principio activo contenido en la misma. Por el contrario, en cada caso independiente se han de considerar las propiedades físicas y químicas individuales del principio activo correspondiente. Numerosas propiedades individuales de un principio activo pueden tener una considerable influencia en su perfil de liberación. Este comportamiento de liberación específico del principio activo puede depender, por ejemplo, de la dosis a ser administrada, del tamaño de partícula, de la forma de la partícula, su dureza, grado de higroscopicidad, solubilidad, dependencia de la solubilidad del pH, carácter hidrófilo/lipófilo, acidez/alcalinidad, etc.
La invención tiene por objeto proporcionar una formulación farmacéutica de 3- (2-dimetilaminometil-ciclohexil) fenol, preferentemente de sus estereoisómeros (1R, 2R) , o de una de sus sales farmacéuticamente compatibles, que presente ventajas con respecto a las formulaciones del estado actual de la técnica.
La forma de dosificación farmacéutica debería asegurar concentraciones en plasma para el principio activo 3- (2
dimetilaminometil-ciclohexil) fenol farmacológicamente eficaces durante un período de tiempo más largo (liberación controlada) , preferentemente durante al menos 12 h, y además se debería caracterizar por el menor espectro de efectos secundarios posible, en particular en lo que respecta a náuseas y vómitos. Además, el comportamiento farmacocinético se debe diferenciar en gran medida del comportamiento farmacocinético de una formulación comparativa sin liberación controlada (solución de principio activo, jugo, immediate release - liberación inmediata) .
Este objeto se resuelve de acuerdo con las reivindicaciones.
Sorprendentemente se ha comprobado que se puede producir una forma de dosificación del principio activo 3- (2dimetilaminometil-ciclohexil) fenol, o de una de sus sales farmacéuticamente compatibles, que libera el principio activo de forma controlada y presenta ventajas frente a las formas farmacéuticas del estado actual de la técnica.
La invención se refiere a una forma de dosificación para la liberación controlada del principio activo 3- (215 dimetilaminometil-ciclohexil) fenol o de una de sus sales farmacéuticamente compatibles que
- libera in vitro, medido según la Farmacopea Europea con un aparato agitador de paletas en tampón a pH 6, 8, a
una temperatura de 37ºC y a 75 rpm, -después de 0, 5 horas del 9, 0 al 31% en peso, -después de 1 hora del 20 al 48% en peso
-después de 2 horas del 31 al 65% en peso, -después de 3 horas del 42 al 76% en peso, -después de 4 horas del 50 al 83% en peso, -después de 6 horas del 60 al 94% en peso, -después de 8 horas del 71 al 99% en peso,
-después de 12 horas más del 79% en peso, del principio activo contenido originalmente en la forma de dosificación,
-incluye una matriz polimérica basada en un éter o éster de celulosa que, en una concentración del 2, 0% en peso en solución acuosa a 20ºC, presenta una viscosidad de entre 3.000 y 150.000 mPa·s,
estando encapsulada al menos una parte del principio activo en la matriz polimérica,
siendo la proporción en peso de la matriz polimérica del 5 al 85% en peso con respecto al peso total de la forma de dosificación, y
seleccionándose el éter o éster de celulosa de entre el grupo consistente en metilcelulosa, etilcelulosa, hidroxietilcelulosa, hidroxipropilcelulosa, carboximetilcelulosa e hidroxipropilmetilcelulosa.
La siguiente tabla muestra perfiles de liberación especialmente preferentes de la forma de dosificación según la 35 invención (nº 1 a nº 4) :
Después de 1 2 3 4
[h] % en peso % en peso % en peso % en peso
0, 5 11-30 13-30 15-29 17-28
1 22-46 24-44 27-42 30-40
2 33-62 36-60 39-58 42-56
3 45-73 48-71 50-69 52-67
4 53-81 55-79 58-77 60-75
6 63-92 66-90 69-88 72-86
8 74-98 76-98 78-97 80-97
12 >82 >84 >86 >88
La forma de dosificación según la invención libera el principio activo 3- (2-dimetilaminometil-ciclohexil) fenol de forma retardada, preferentemente después de una administración oral, y, por tanto, es adecuada para una administración a intervalos de al menos 12 horas. Por consiguiente, la forma farmacéutica según la invención posibilita una terapia del dolor durante la cual el principio activo 3- (2-dimetilaminometil-ciclohexil) fenol ya sólo se administra una vez al día, por ejemplo a intervalos de 24 horas, o dos veces al día, preferentemente a intervalos de 12 horas, para asegurar una concentración suficiente de principio activo en plasma.
En este contexto se ha comprobado sorprendentemente que es posible reducir significativamente los efectos secundarios, en particular las náuseas y/o vómitos, en comparación con las formas de dosificación convencionales para la administración de 3- (2-dimetilaminometil-ciclohexil) fenol. Esto tiene la ventaja de aumentar el margen terapéutico (relación entre la dosis de principio activo terapéutica y la dosis tóxica) del 3- (2-dimetilaminometilciclohexil) fenol, lo que permite, entre otras cosas, incrementar la dosis de principio activo y con ello también la eficacia terapéutica.
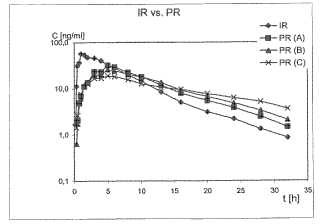
La Figura 1 muestra concentraciones en plasma medias del principio activo 3- (2-dimetilaminometil-ciclohexil) fenol después de... [Seguir leyendo]
Reivindicaciones:
1. Forma de dosificación para la liberación controlada del principio activo 3- (2-dimetilaminometilciclohexil) fenol o de una de sus sales farmacéuticamente compatibles, que
- libera in vitro, medido de acuerdo con la Farmacopea Europea con un aparato agitador de paletas en tampón de pH 6, 8, una temperatura de 37ºC y a 75 rpm,
-después de 0, 5 horas del 9, 0 al 31% en peso,
-después de 1 hora del 20 al 48% en peso,
-después de 2 horas del 31 al 65% en peso,
-después de 3 horas del 42 al 76% en peso,
-después de 4 horas del 50 al 83% en peso,
-después de 6 horas del 60 al 94% en peso,
-después de 8 horas del 71 al 99% en peso,
-después de 12 horas más del 79% en peso,
del principio activo contenido originalmente en la forma de dosificación,
-incluye una matriz polimérica basada en un éter o éster de celulosa, que en una concentración del 2, 0% en peso en solución acuosa a 20ºC presenta una viscosidad entre 3.000 y 150.000 mPa·s,
estando encapsulada al menos una parte del principio activo en la matriz polimérica,
siendo la proporción en peso de la matriz polimérica del 5 al 85% en peso con respecto al peso total de la forma de dosificación, y
seleccionándose el éter o éster de celulosa de entre el grupo consistente en metilcelulosa, etilcelulosa, hidroxietilcelulosa, hidroxipropilcelulosa, carboximetilcelulosa e hidroxipropilmetilcelulosa.
2. Forma de dosificación según la reivindicación 1, caracterizada porque el principio activo es (1R, 2R) -3- (2dimetilaminometil-ciclohexil) fenol o una de sus sales farmacéuticamente compatibles.
3. Forma de dosificación según la reivindicación 1 o 2, caracterizada porque se proporciona en forma de pastilla.
4. Utilización del principio activo 3- (2-dimetilaminometil-ciclohexil) fenol o de una de sus sales farmacéuticamente compatibles para producir una forma de dosificación según una de las reivindicaciones 1 a 3 para el tratamiento del dolor.
5. Utilización según la reivindicación 4, caracterizada porque la administración se lleva a cabo vía oral.
FIGURA 1A
FIGURA 1B
Patentes similares o relacionadas:
Uso de inhibidores de la PDE4 para la profilaxis y/o la terapia de la dislipoproteinemia y trastornos relacionados, del 27 de Mayo de 2020, de Albert-Ludwigs-Universität Freiburg: Inhibidor específico de la fosfodiesterasa 4 (PDE 4) para uso en el tratamiento profiláctico o terapéutico de la dislipoproteinemia, en donde el inhibidor […]
Métodos y composiciones para trastornos relacionados con la proliferación celular, del 27 de Mayo de 2020, de Agios Pharmaceuticals, Inc: Un método in vitro para diagnosticar a un sujeto que tiene un trastorno relacionado con la proliferación celular o que se sospecha que tiene un trastorno relacionado con […]
Un canal catiónico no selectivo en células neurales y compuestos que bloquean el canal para su uso en el tratamiento de la inflamación del cerebro, del 6 de Mayo de 2020, de UNIVERSITY OF MARYLAND, BALTIMORE: Un antagonista de SUR1 que bloquea el canal de NCCa-ATP para su uso en (a) la prevención o el tratamiento de la inflamación de las células neurales […]
Inhibidores de ERK y sus usos, del 8 de Abril de 2020, de Celgene CAR LLC: Un compuesto de fórmula VIII: **(Ver fórmula)** o una de sus sales farmacéuticamente aceptables, en donde: el anillo A se selecciona de **(Ver fórmula)** […]
Procedimiento de uso de inmunoconjugados anti-CD79b, del 8 de Abril de 2020, de F. HOFFMANN-LA ROCHE AG: Un inmunoconjugado que comprende un anticuerpo anti-CD79b unido a un agente citotóxico para su uso en un procedimiento para tratar un trastorno proliferativo […]
IMIPRAMINA PARA USO COMO INHIBIDOR DE LA SOBREXPRESIÓN DE LA FASCINA 1, del 2 de Abril de 2020, de FUNDACION UNIVERSITARIA SAN ANTONIO: La presente invención se refiere a imipramina para su uso como inhibidor de la sobreexpresión de la fascina 1, preferiblemente dicha sobreexpresión de la fascina 1 está asociada […]
Mutación novedosa del receptor de andrógenos, del 25 de Marzo de 2020, de NOVARTIS AG: Una composicion terapeutica para su uso en el tratamiento de un paciente que padece cancer de prostata o de mama, asociado con una mutacion del receptor de […]
Composiciones y métodos para la distribución de moléculas en células vivas, del 25 de Marzo de 2020, de THE TEXAS A & M UNIVERSITY SYSTEM: Un compuesto que tiene la fórmula: **(Ver fórmula)** En donde X es un resto de unión, Y es un residuo de aminoácido acoplado de forma covalente […]