Composición farmacéutica que comprende dapagliflozina y ciclodextrina.
Composición farmacéutica que comprende ciclodextrina y dapagliflozina.
Tipo: Patente Europea. Resumen de patente/invención. Número de Solicitud: E11004534.
Solicitante: RATIOPHARM GMBH.
Nacionalidad solicitante: Alemania.
Dirección: GRAF-ARCO-STRASSE 3 89079 ULM ALEMANIA.
Inventor/es: SZENTE, LAJOS, PUSKAS, ISTVAN.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K31/424 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › condensados con sistemas heterocíclicos, p. ej. ácido clavulánico.
- A61K31/7004 A61K 31/00 […] › Monosacáridos que tienen únicamente átomos de carbono, de hidrógeno y de oxígeno.
- A61K31/7034 A61K 31/00 […] › unidos a un compuesto carbocíclico, p. ej. floridzina.
- A61K47/48
- A61P3/10 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › A61P 3/00 Medicamentos para el tratamiento de trastornos del metabolismo (de la sangre o de fluido extracelular A61P 7/00). › para la hiperglucemia, p.ej. antidiabéticos.
PDF original: ES-2448398_T3.pdf
Fragmento de la descripción:
Composición farmacéutica que comprende dapagliflozina y ciclodextrina.
Antecedentes de la invención La presente invención se refiere a composiciones farmacéuticas que comprenden dapagliflozina y ciclodextrina, preferentemente como complejos de inclusión, más preferentemente a dapagliflozina dispersada molecularmente en una forma dispersada molecularmente de complejos de inclusión, que comprenden ciclodextrina, preferentemente (2-hidroxi) propil-1-ciclodextrina y dapagliflozina. La invención también se refiere a un proceso para producir dichas composiciones farmacéuticas a formas de dosificación que comprenden dichas composiciones farmacéuticas. Se indica que “dapagliflozina” es el nombre de la INN del compuesto C-aril glucósido (2S, 3R, 4R, 5S, 6R) -2-[4-cloro-3- (4etoxibencil) fenil]-6- (hidroximetil) -tetrahidro-2H-piran-3, 4, 5-triol y puede caracterizarse mediante la siguiente fórmula química:
Se indica que la dapagliflozina inhibe el subtipo 2 de las proteínas transportadoras de sodio-glucosa (SGLT2) , que es responsable de al menos el 90% de la reabsorción de glucosa en el riñón. El bloqueo de esta transportadora hace que la glucosa en sangre sea eliminada a través de de la orina. En particular, la dapagliflozina está indicada para el tratamiento de diabetes de tipo 1 y de tipo 2, en particular, diabetes de tipo 2.
La dapagliflozina y su síntesis se describen en el documento EP 1 506 211 B1. El documento WO 2004/063209 A2 se refiere a un proceso para preparar dapagliflozina e intermedios.
En la técnica, se conocen varias formulaciones de dapagliflozina. El documento EP 1 506 211 B1 menciona combinaciones de dapagliflozina con un agente antidiabético diferente del inhibidor de SGLT2, un agente para tratar las complicaciones de la diabetes, un agente antiobesidad, un agente antihipertensor, un agente antiplaquetas, un agente antiaterosclerótico, y/o un agente que rebaja los lípidos.
El documento WO 2008/116179 A1 parece desvelar una formulación de liberación inmediata que comprende hidrato de propilenglicol de dapagliflozina.
El documento WO 2008/116195 A2 se refiere al uso de un inhibidor de SLGT2 en el tratamiento de la obesidad, en el que la cantidad de dicho inhibidor de SGLT2 está por debajo de la cantidad eficaz para tratar la diabetes.
El documento WO 2011/060290 A2 desvela formulaciones de liberación inmediata que comprenden metformina y el inhibidor del transportador de glucosa dependiente de sodio (SGLT2) dapagliflozina o su hidrato de propilenglicol. Además, el documento D1 describe métodos de preparación de dichas formulaciones y métodos de tratamiento de enfermedades/trastornos asociados con la actividad de SGLT2 que emplean estas formulaciones.
El documento WO 2009/093264 A2 desvela combinaciones farmacéuticas que comprenden un agente antidiabético, en las que el agente antidiabético puede ser un inhibidor de SLGT2, tal como sergliflozina o dapagliflozina o una sal farmacéuticamente aceptable de las mismas.
El documento WO 2008/131149 A2 desvela combinaciones farmacéuticas que comprenden uno o más agente o agentes antidiabéticos seleccionados entre una pluralidad de agentes activos (inter alia, dapagliflozina) .
El documento EP 2 233 134 A1 se refiere a una forma de dosificación intra-oral de partes múltiples que comprende al menos un agente farmacéuticamente activo o agente beneficioso para la salud en la que al menos una parte comprende un componente para crear una sensación organoléptica perceptible. Además, el documento D4 se refiere a un compuesto farmacéuticamente con ciclodextrina en el que la ciclodextrina se selecciona entre a, 1, yciclodextrina.
La micronización de dapagliflozina, sin embargo, implica algunas desventajas. En primer lugar, la micronización en el ingrediente activo da como resultado una fluidez baja no deseada. Además, el ingrediente activo micronizado es más difícil de comprimir y ocasionalmente puede producirse una distribución irregular del ingrediente activo dentro de la formulación farmacéutica a comprimir. Causada por la gran extensión de la superficie durante la micronización, la tendencia del ingrediente activo a oxidarse se incrementa. Además, la dapagliflozina cuando se proporciona en forma cristalina es higroscópica. Por lo tanto, tiende a atraer moléculas de agua desde el entorno circundante a través de absorción, lo que conduce a difluencia de la sustancia activa, alterando de este modo las capacidades de procesamiento y la estabilidad en almacenamiento.
Por lo tanto, era un objeto de la presente invención superar los inconvenientes de las formulaciones mencionadas anteriormente.
En particular, la dapagliflozina debe proporcionarse en una forma que tenga solubilidad y capacidades de procesamiento superiores. Preferentemente, la dapagliflozina debe proporcionarse en una forma, que sea altamente soluble. Además, la dapagliflozina debe proporcionarse en una forma, que permita la aplicación oral independientemente de las comidas. El incremento de la solubilidad y la permeabilidad debe conseguirse particularmente sin una etapa de micronización y, preferentemente, sin el uso de excipientes o co-disolventes. Además, la dapagliflozina debe proporcionarse en una forma no higroscópica.
Además, era un objeto de la invención proporcionar dapagliflozina en una forma que tenga capacidades de almacenamiento superiores. Preferentemente, debe conseguirse una estabilidad en almacenamiento durante 12 meses a 40ºC y el 75% de humedad. Después del almacenamiento en dichas condiciones, las impurezas deben ser inferiores al 2% en peso, más preferentemente inferiores al 1% en peso.
Particularmente, los objetos mencionados anteriormente deben resolverse simultáneamente, eso significa que, la dapagliflozina debe proporcionarse en una forma no higroscópica que tenga elevada solubilidad, elevada permeabilidad y que muestre elevada estabilidad en almacenamiento.
Resumen de la invención Los objetos de la presente invención pueden resolverse mediante composiciones farmacéuticas que comprenden dapagliflozina y ciclodextrina, preferentemente como complejo de inclusión de dapagliflozina y ciclodextrina, más preferentemente como “genuinos” complejos de inclusión de dapagliflozina-ciclodextrina y un método para formar dichas composiciones farmacéuticas. Preferentemente, dicho complejo de inclusión preferido puede considerarse como un complejo de inclusión no covalente, supramolecular. El complejo de inclusión “genuino” preferido puede conducir a una nueva forma sólida de dapagliflozina, preferentemente a una forma de dispersividad molecular y, cuando se humedecen de nuevo, en una forma que tiene estructura amoría. La nueva forma sólida puede describirse como una forma sólida vítrea-amoría.
Un asunto de la presente invención puede ser, por lo tanto, una composición farmacéutica que comprende dapagliflozina y ciclodextrina, preferentemente como un complejo de inclusión.
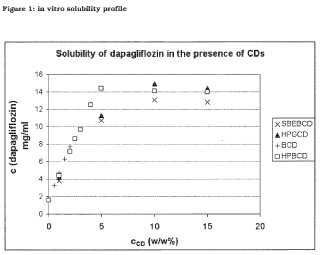
Un asunto preferido de la presente invención puede ser un complejo de inclusión que comprende (2-hidroxi) propil-1ciclodextrina (HPBCD) , sulfobutiléter-1-ciclodextrina (SBEBCD) y/o (2-hidroxi) -propil-y-ciclodextrina (HPGCD) , en particular (2-hidroxi) propil-1-ciclodextrina (HPBCD) y dapagliflozina.
Los asuntos ilustrados anteriormente de la presente invención son soluciones alternativas a los objetos perfilados anteriormente.
Además, la presente invención puede referirse a un proceso para producir una composición farmacéutica que comprende dapagliflozina y ciclodextrina - preferentemente en forma de un complejo de inclusión - que comprende las etapas de a) disolver y/o dispersar ciclodextrina en un disolvente;
b) añadir dapagliflozina;
c) someter a la mezcla resultante de la etapa (b) a un tratamiento mecánico; y
d) retirar el disolvente de la mezcla de reacción, preferentemente mediante liofilización o secado por pulverización.
En una realización adicional, la presente invención puede estar relacionada con el uso de ciclodextrina, preferentemente (2-hidroxi) propil-1-ciclodextrina, para producir una forma de dosificación que contiene dapagliflozina.
Finalmente, la presente invención puede referirse al método de purificación de dapagliflozina, que comprende las etapas de a) disolver y/o dispersar ciclodextrina en un disolvente;
b) añadir dapagliflozina impura; c) separar la dapagliflozina complejada de residuos no complejados.
Descripción detallada de la invención El término “dapagliflozina” tal como se usa en la presente solicitud se refiere a dapagliflozina en forma libre, así como a sus solvatos, hidratos, enantiómeros, polimorfos... [Seguir leyendo]
Reivindicaciones:
1. Composición farmacéutica que comprende ciclodextrina y dapagliflozina.
2. Composición farmacéutica de acuerdo con la reivindicación 1 en forma de un complejo de inclusión.
3. Composición farmacéutica de acuerdo con la reivindicación 1 ó 2, en la que la relación molar de ciclodextrina con respecto a dapagliflozina es de 0, 5:1 a 2:1, más preferentemente de 0, 8:1 a 1, 2:1, de la forma más preferente aproximadamente 1:1.
4. Composición farmacéutica de acuerdo con cualquiera de las reivindicaciones 1 a 3, en la que la ciclodextrina es (2-hidroxi) propil-1-ciclodextrina, sulfobutiléter-1-ciclodextrina o (2-hidroxi) propil-y-ciclodextrina, preferentemente 2hidroxi) propil-1-ciclodextrina.
5. Composición farmacéutica que comprende ciclodextrina y dapagliflozina de acuerdo con una cualquiera de las reivindicaciones 1 a 4, que forma una fase sólida que está esencialmente libre de estructura cristalina.
6. Proceso para producir una composición farmacéutica de acuerdo con las reivindicaciones 1 a 5, que comprende las etapas de a) disolver y/o dispersar ciclodextrina en un disolvente; b) añadir dapagliflozina;
c) someter a la mezcla resultante de la etapa b) a un tratamiento mecánico; y d) retirar el disolvente de la mezcla de reacción, preferentemente mediante liofilización o secado por pulverización.
7. Proceso de acuerdo con la reivindicación 6, en la que la ciclodextrina es (2-hidroxi) propil-1-ciclodextrina.
8. Proceso de acuerdo con la reivindicación 6 ó 7, en la que composición farmacéutica se forma en ausencia de excipientes y/o co-disolventes.
9. Una composición farmacéutica que puede obtenerse mediante un proceso de acuerdo con una cualquiera de las reivindicaciones 6 a 8.
10. Forma de dosificación que comprende una composición farmacéutica de acuerdo con una cualquiera de las reivindicaciones 1 a 5 ó 9, y opcionalmente uno o más excipientes farmacéuticos.
11. Forma de dosificación de acuerdo con la reivindicación 10, que está esencialmente libre de dapagliflozina cristalina.
12. Forma de dosificación de acuerdo con la reivindicación 10 u 11, en la que la forma de dosificación está adaptada a ser administrada por vía oral o por vía intravenosa.
13. Uso de ciclodextrina, preferentemente (2-hidroxi) propil-1-ciclodextrina, para producir una forma de dosificación que contiene dapagliflozina.
14. Método de purificación de dapagliflozina, que comprende las etapas de a) disolver o dispersar ciclodextrina en un disolvente; b) añadir dapagliflozina impura; c) separar la dapagliflozina complejada de residuos no complejados, preferentemente mediante filtración.
15. Una composición farmacéutica o forma de dosificación que comprende dapagliflozina caracterizada porque al introducirla en agua, dicha composición es capaz de formar una solución compuesta por no menos de 5 mg de dapagliflozina por ml de agua.
Patentes similares o relacionadas:
Derivativos del ácido siálico para la derivatización y conjugación de proteínas, del 20 de Diciembre de 2019, de LIPOXEN TECHNOLOGIES LIMITED: Un procedimiento de producción de un derivativo aldehído de un ácido siálico en el que un material de partida que tiene una unidad de ácido siálico en el […]
GELES DE QUITOSANO(A) CONTENIENDO NANOPARTICULAS METALICAS DE COBRE, PLATA Y ANTIBIOTICOS (CIPROFLOXACINO, CEFOTAXIME, GENTAMICINA Y CLOXACILINA), del 12 de Diciembre de 2019, de CARDENAS Y CIA LTDA: En la presente invención se describen geles de quitosano (poli-beta-glucosamina) con propiedades bactericidas y fungicidas en mezcla con nanopartículas […]
Compuestos de polímero de polialquileno y usos de los mismos, del 20 de Noviembre de 2019, de Biogen MA Inc: Una composición farmacéutica que comprende un conjugado y un vehículo, adyuvante, diluyente, conservante y/o solubilizante farmacéuticamente […]
Composiciones y métodos para la liberación dirigida de fármacos in vitro e in vivo a células de mamíferos mediante minicélulas intactas derivadas de bacterias, del 23 de Octubre de 2019, de ENGENEIC MOLECULAR DELIVERY PTY LTD: Una composición que comprende: (a) una pluralidad de minicélulas intactas derivadas de bacterias que tienen paredes celulares intactas, en donde la pluralidad […]
Moléculas con semividas prolongadas, composiciones y usos de las mismas, del 16 de Octubre de 2019, de MEDIMMUNE, LLC: Una molécula modificada que comprende una proteína o agente no de proteína y un dominio constante de IgG, en la que el dominio constante de IgG comprende un dominio CH3 humano […]
Método para la preparación de oligo etilenglicol monodisperso, del 19 de Junio de 2019, de NEKTAR THERAPEUTICS: Un método para preparar un oligo (etilenglicol) monodisperso, comprendiendo dicho método: (i) hacer reaccionar un oligo (etilenglicol) terminado […]
Construcciones de moléculas MHC y sus usos para el diagnóstico y terapia, del 29 de Mayo de 2019, de DAKO DENMARK A/S: Una construcción de moléculas MHC en forma soluble en un medio de solubilización o inmovilizada en un soporte sólido o semi-sólido, comprendiendo dicha construcción de moléculas […]
Usos terapéuticos de anticuerpos monoclonales frente al receptor de la angiotensina II tipo 1, del 17 de Mayo de 2019, de QUEEN MARY AND WESTFIELD COLLEGE: Un anticuerpo monoclonal o un fragmento del mismo que se une al péptido que consiste en la secuencia EDGIKRIQDD para su uso en el tratamiento de la proliferación […]