Co-cristales de pirrolidinonas.
Un co-cristal que comprende una pirrolidinona que bien es 2-[4-(2,
2-difluorovinil)-2-oxopirrolidinil]butanamida obien (2S)-2-(2-oxo-4-n-propil-1-pirrolidinil)butanamida y una sal elegida entre el grupo que consiste en MgCl2,MgSO4, MgBr2, Mg3(PO4)2, MgHPO4, Mg(H2PO4)2, MgCO3, Mg(HCO3)2, y sus hidratos.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/EP2007/005009.
Solicitante: UCB PHARMA, S.A..
Nacionalidad solicitante: Bélgica.
Dirección: ALLEE DE LA RECHERCHE 60 1070 BRUXELLES BELGICA.
Inventor/es: QUERE,LUC.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K31/4015 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › teniendo grupos oxo unidos directamente al heterociclo, p. ej. piracetam, etosuximida.
- A61P25/08 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › A61P 25/00 Medicamentos para el tratamiento de trastornos del sistema nervioso. › Antiepilépticos; Anticonvulsivos.
- C07D207/26 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07D COMPUESTOS HETEROCICLICOS (Compuestos macromoleculares C08). › C07D 207/00 Compuestos heterocíclicos que contienen ciclos de cinco miembros no condensados con otros ciclos, con solamente un átomo de nitrógeno como heteroátomo. › Pirrolidonas-2.
PDF original: ES-2444009_T3.pdf
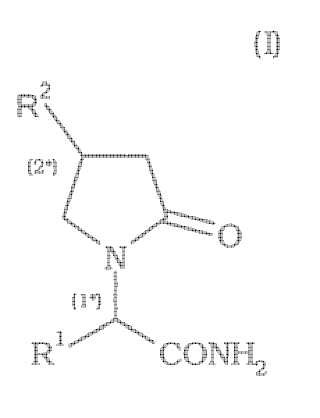
Fragmento de la descripción:
Co-cristales de pirrolidinonas Introducción Los ingredientes farmacéuticos activos (abreviado generalmente como API o APIs por sus iniciales en inglés: active pharmaceutical ingredients) en las composiciones farmacéuticas se pueden preparar de múltiples formas diferentes. Dichos APIs se pueden preparar de forma que tengan varias formas químicas diferentes, incluyendo los derivados químicos o sales. Dichos APIs también pueden prepararse para tener diferentes formas físicas. Los APIs pueden ser, por ejemplo, amorfos, pueden tener diferentes polimorfos cristalinos o pueden existir en diferentes estados de hidratación o de solvatación. Variando la forma de un API es posible variar sus propiedades físicas. Por ejemplo, los polimorfos cristalinos tienen generalmente, p. ej., diferentes solubilidades entre ellos de forma que un polimorfo más estable termodinámicamente es menos soluble que un polimorfo menos estable termodinámicamente a una temperatura dada. Los polimorfos farmacéuticos también pueden diferenciarse en propiedades tales como la durabilidad, biodisponibilidad, morfología, presión de vapor, densidad, color, viscosidad, punto de fusión y compresibilidad. Consecuentemente, la variación en el estado cristalino de un API es una de las formas en las que se pueden modular sus propiedades físicas.
Frecuentemente es necesaria una nueva forma de estos APIs que tenga propiedades mejoradas, en particular, en lo que se refiere a las formulaciones orales. Específicamente, puede ser adecuado identificar las formas mejoradas de APIs que presenten propiedades mejoradas significativamente, incluyendo solubilidad en agua, punto de fusión de la forma sólida así como estabilidad del API. Además, es adecuado mejorar la procesabilidad o la preparación de formulaciones farmacéuticas. Por ejemplo, las formas y hábitos cristalinos en forma de agujas de los APIs pueden producir agregación, incluso en composiciones en las que el API está mezclado con otras sustancias, de forma que se obtiene una mezcla no uniforme. También puede ser adecuado aumentar o disminuir la tasa de disolución en agua de las composiciones farmacéuticas que contienen el API, aumentar y proporcionar un inicio más rápido o más retrasado del efecto terapéutico o controlar la biodisponibilidad de las composiciones administradas oralmente con el fin de evitar cualquier absorción sistémica favoreciendo solo un efecto local. También es adecuado tener una forma del API que, cuando se administra a un sujeto, alcanza un nivel pico en el plasma más rápidamente o más despacio, tiene una concentración terapéutica en el plasma más duradera y mayor o menor exposición global cuando se compara con cantidades equivalentes del API en su forma actualmente conocida.
Finalmente, puede ser adecuado proporcionar una forma del API que tenga un punto de fusión de forma que puede formularse mejor como un producto disponible oralmente.
El documento WO 01/62726 se refiere a pirrolidinonas, su síntesis así como su uso médico en el tratamiento de varios trastornos del SNC como la epilepsia. El documento WO 01/62726 describe específicamente la síntesis de los dos diastereoisómeros de la 2-[4- (2, 2-difluorovinil) -2-oxopirrolidinil]-butanamida. También describe la síntesis de los dos diastereoisómeros de la (2S) -2- (2-oxo-4-n-propil-1-pirrolidinil) butanamida.
Sumario de la invención La presente invención se refiere a nuevos co-cristales de 2-[4- (2, 2-difluorovinil) -2-oxopirrolidinil]butanamida o (2S) (2-oxo-4-n-propil-1-pirrolidinil) butanamida. Además, la invención describe los obtenidos por cristalización con una sal elegida entre MgCl2, MgSO4, MgBr2, Mg3 (PO4) 2, MgHPO4, Mg (H2PO4) 2, MgCO3, Mg (HCO3) 2 y sus hidratos.
La invención también comprende una composición farmacéutica que contiene nuevos co-cristales así como un método para preparar dicha formulación, el uso de dicha formulación para el tratamiento de la epilepsia, epileptogénesis, trastornos convulsivos, convulsiones y otros trastornos neurológicos, incluyendo el trastorno bipolar, manía, depresión, ansiedad, migraña, neuralgia trigeminal y otras neuralgias, dolor crónico, dolor neuropático, isquemia cerebral, arritmia cardiaca, miotonía, abuso de la cocaína, ictus, mioclonia, temblor esencial y otros trastornos del movimiento, hemorragia cerebral neonatal, esclerosis lateral amiotrófica, espasticidad, enfermedad de Parkinson y otras enfermedades degenerativas, asma bronquial, estados asmáticos y bronquitis alérgica, síndrome asmático, hiperreactividad bronquial y síndromes broncoespásticos, así como rinitis alérgica y vasomotora y rinoconjuntivitis.
Los co-cristales del API de la presente invención tienen un punto de fusión significativamente mayor que los APIs descritos en el documento WO 01/62726.
Descripción de las figuras La figura 1 se refiere a un termograma de DSC de un co-cristal de (2S) -2-[ (4S) -4- (2, 2-difluorovinil) -2-oxopirrolidinil]butanamida:MgCl2:H2O (2:1:4) .
La figura 2 se refiere a un termograma de DSC de ( (2S) -2- ( (4R) -2-oxo-4-n-propil-1-pirrolidinil) butanamida:MgCl2:H2O (2:1:4) .
Descripción detallada de la invención En un modo de realización específico, la presente invención se refiere a nuevos co-cristales de 2-[4- (2, 2difluorovinil) -2-oxopirrolidinil]butanamida y bien MgCl2, MgSO4, MgBr2, Mg3 (PO4) 2, MgHPO4, Mg (H2PO4) 2, Mg (CO3)
o Mg (HCO3) 2 y sus hidratos.
Un segundo aspecto de la presente invención se refiere a una composición farmacéutica que comprende los cocristales de 2-[4- (2, 2-difluorovinil) -2-oxopirrolidinil]butanamida y bien MgCl2, MgSO4, MgBr2, Mg3 (PO4) 2, MgHPO4, Mg (H2PO4) 2, MgCO3 o Mg (HCO3) 2 y sus hidratos.
Otro aspecto de la presente invención proporciona un procedimiento para la preparación de una composición farmacéutica, cuyo procedimiento comprende la etapa de proporcionar un co-cristal de 2-[4- (2, 2-difluorovinil) -2ºxopirrolidinil]butanamida y bien MgCl2, MgSO4, MgBr2, Mg3 (PO4) 2, MgHPO4, Mg (H2PO4) 2, MgCO3 o Mg (CO3) 2 y sus hidratos.
En un modo de realización preferido, el API es el diastereómero específico que está en desarrollo clínico que tiene la DCI seletracetam, es decir la (2S) -2-[ (4S) -4- (2, 2-difluorovinil) -2-oxo-pirrolidinil]butanamida.
En un modo de realización adicional, la presente invención se refiere a un API específico que es la (2S) -2- (2-oxo-4n-propil-1-pirrolidinil) butanamida.
Consecuentemente, en un cuarto aspecto la presente invención se refiere a un co-cristal de (2S) -2- (2-oxo-4-n-propil1-pirrolidinil) butanamida y bien MgCl2, MgSO4, MgBr2, Mg3 (PO4) 2, MgHPO4, Mg (H2PO4) 2, MgCO3 o Mg (HCO3) y sus hidratos.
Un quinto aspecto de la presente invención se refiere a una composición farmacéutica que comprende el co-cristal de (2S) -2- (2-oxo-4-propil-1-pirrolidinil) butanamida y MgCl2, MgSO4, MgBr2, Mg3 (PO4) 2, MgHPO4, Mg (H2PO4) 2, MgCO3, Mg (HCO3) 2 y sus hidratos.
Un sexto aspecto de la presente invención se refiere a un procedimiento para la preparación de una composición farmacéutica, cuyo procedimiento comprende la etapa de proporcionar un co-cristal de 2-[4- (2, 2-difluorovinil) -2ºxopirrolidinil]butanamida y bien MgCl2, MgSO4, MgBr2, Mg3 (PO4) 2, MgHPO4, Mg (H2PO4) 2, MgCO3 o Mg (HCO3) 2 y sus hidratos.
En un modo de realización específico, el API es el diastereómero que está en desarrollo clínico que tiene la DCI brivaracetam, es decir la (2S) -2-oxo-4-n-propil-1-pirrolidinil) butanamida.
En todavía otro modo de realización, el co-cristal es un hidrato del API según la fórmula (I) y bien MgCl2, MgSO4,
MgBr2, Mg3 (PO4) 2, MgHPO4, Mg (H2PO4) 2, MgCO3 o Mg (HCO3) 2 y sus hidratos. Para el API específico (2S) -2-[ (4S) -4- (2, 2-difluorovinil) -2-oxopirrolidinil]butanamida, la estequiometría del co-cristal con MgCl2 puede ser la siguiente:
(2S) -2-[ (4S) -4- (2, 2-difluorovinil) -2-oxopirrolidinil]butanamida x 0, 5 MgCl2 x 2 H2O
Para el API específico [ (2S) -2-[ (4R) -2-oxo-4-n-propil-1-pirrolidinil) butanamida, la estequiometría del co-cristal con MgCl2 puede ser la siguiente: (2S) -2- ( (4R) -2-oxo-4-n-propil-1-pirrolidinil) butanamida x 0, 5 MgCl2 x 2 H2O Los co-cristales de los APIs tienen un punto de fusión significativamente superior que el de los APIs solos. Esto tiene una ventaja importante cuando se formulan los APIs para proporcionar una composición farmacéutica. No es
adecuado formular un API que tenga un punto de fusión bajo. Generalmente, el punto de fusión bajo de un API no complejado hace que sea más difícil elaborar comprimidos con él. Los comprimidos son los más preferidos de las formulaciones de fármacos administrables oralmente.
El punto de fusión de la (2S)... [Seguir leyendo]
Reivindicaciones:
1. Un co-cristal que comprende una pirrolidinona que bien es 2-[4- (2, 2-difluorovinil) -2-oxopirrolidinil]butanamida o bien (2S) -2- (2-oxo-4-n-propil-1-pirrolidinil) butanamida y una sal elegida entre el grupo que consiste en MgCl2, MgSO4, MgBr2, Mg3 (PO4) 2, MgHPO4, Mg (H2PO4) 2, MgCO3, Mg (HCO3) 2, y sus hidratos.
2. Un co-cristal según la reivindicación 1, en el que la sal es MgCl2.
3. Un co-cristal según la reivindicación 2, que es un hidrato.
4. Un co-cristal según cualquiera de las reivindicaciones 1 a 3, en el que la pirrolidinona que tiene la fórmula (I) es la (2S) -2-[ (4S) -4- (2, 2-difluorovinil) -2-oxopirrolidinil]butanamida.
Patentes similares o relacionadas:
 Moléculas difuncionales que contienen PEG para su uso en la inhibición de cataratas y presbicia, del 28 de Agosto de 2019, de THE UNIVERSITY OF MASSACHUSETTS: Una composición oftálmica que comprende una molécula difuncional, en la que la molécula difuncional es**Fórmula**
Moléculas difuncionales que contienen PEG para su uso en la inhibición de cataratas y presbicia, del 28 de Agosto de 2019, de THE UNIVERSITY OF MASSACHUSETTS: Una composición oftálmica que comprende una molécula difuncional, en la que la molécula difuncional es**Fórmula**
Ácido carboxílico de pirrolidona (pca) para uso oftálmico, del 14 de Agosto de 2019, de Laboratori Baldacci S.p.A: Ácido carboxílico de pirrolidona y/o sales farmacéuticamente aceptables del mismo para su uso en el tratamiento de enfermedades y/o trastornos oculares.
Derivados de urea deuterados o marcados isotópicamente o sales farmacológicamente aceptables de los mismos útiles como agonistas de FPRL-1, del 24 de Julio de 2019, de KYORIN PHARMACEUTICAL CO., LTD.: Un compuesto sustituido con deuterio o marcado isotópicamente representado con la fórmula general (I) o una sal farmacológicamente aceptable del mismo o un solvato […]
Combinaciones que comprenden moduladores alostéricos positivos del receptor glutamatérgico metabotrópico de subtipo 2 y su uso, del 10 de Julio de 2019, de JANSSEN PHARMACEUTICA N.V.: Una combinación que comprende (a) un ligando de una proteína de la vesícula sináptica 2a ("SV2A") seleccionado del grupo que consiste en […]
Composiciones farmacéuticas de liberación prolongada de levetiracetam, del 3 de Julio de 2019, de Agenebio, Inc: Una composición farmacéutica de liberación prolongada que comprende: a) 220 mg de levetiracetam; b) 280 mg-350 mg de hidroxipropilmetilcelulosa; […]
Derivado de ácido hidroxámico, del 5 de Junio de 2019, de TAISHO PHARMACEUTICAL CO., LTD: Un compuesto representado por la siguiente fórmula general [1] o una sal farmacéuticamente aceptable del mismo:**Fórmula** en donde R1 representa un grupo alquilo C1-C6, […]
Métodos para reducir partículas de LDL pequeñas y densas, del 9 de Mayo de 2019, de Cymabay Therapeutics, Inc: Un compuesto que es**Fórmula** o una de sus sales, para su uso en un método para disminuir la cantidad de partículas de LDL pequeñas y densas en un ser humano que tiene […]
Derivados de pirrolidinona como inhibidores de MetAP-2, del 12 de Abril de 2019, de MERCK PATENT GMBH: Compuestos seleccionados del grupo.**Fórmula** y sales farmacéuticamente utilizables, tautómeros y estereoisómeros de los mismos, incluyendo mezclas de los mismos en […]