Régimen de dosificación para el tratamiento de una lesión cerebral traumática con progesterona.
Progesterona para uso en tratamiento de lesión cerebral traumática,
donde dicha progesterona se prepara paraadministración a un sujeto humano en al menos un ciclo de terapia, donde dicho ciclo de terapia comprende laadministración de un régimen de dosificación intravenosa de dos niveles terapéuticamente eficaces de progesterona,dicho régimen de dosificación de dos niveles comprende un primer período de tiempo de al menos 1 hora, en la que seadministra al sujeto una dosis elevada de infusión de progesterona por hora de aproximadamente 0,1 mg/kg/hr aaproximadamente 7,1 mg/kg/hr, seguida de un segundo período de tiempo en el que se administra a dicho sujeto unadosis inferior de infusión de progesterona por hora de aproximadamente 0,05 mg/kg/hr a aproximadamente 5 mg/kg/hr.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2006/010797.
Solicitante: EMORY UNIVERSITY.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: Office of Technology Transfer 1599 Clifton Road, NE 4th Floor Atlanta, GA 30322 ESTADOS UNIDOS DE AMERICA.
Inventor/es: Hoffman,Stuart W, Stein,Donald G, Wright,David W, Lowery-North,Douglas W, CUTLER,Sarah,Melissa, KELLERMANN,ARTHUR L.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K31/57 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › sustituidos en posición 17 beta por una cadena con dos átomos de carbono, p. ej. pregnano, progesterona.
- A61P25/00 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › Medicamentos para el tratamiento de trastornos del sistema nervioso.
- A61P25/28 A61P […] › A61P 25/00 Medicamentos para el tratamiento de trastornos del sistema nervioso. › de los problemas neurodegenerativos del sistema nervioso central, p. ej. noótropos, activadores del conocimiento, medicamentos para el tratamiento del Alzheimer o de otras formas de demencia.
PDF original: ES-2392454_T3.pdf
Fragmento de la descripción:
Régimen de dosificación para el tratamiento de una lesión cerebral traumática con progesterona
CAMPO DE LA INVENCIÓN
La invención se refiere a métodos para tratar lesiones cerebrales traumáticas.
ANTECEDENTES DE LA INVENCIÓN
Entre 1, 5 y 2 millones de estadounidenses sufren una lesión cerebral traumática (TCE) cada año (Anónimo, "Traumatic Brain Injur y , " Center for Disease Control and Prevention, National Center for Injur y Prevention and Control, 2003, Vol. 2003) . En EEUU se estima que el TCE es responsable de 50.000 muertes y 100.000 hospitalizaciones anualmente (Anónimo, "Traumatic Brain Injur y , " Center for Disease Control and Prevention, National Center for Injur y Prevention and Control, 2003, Vol. 2003) . Cerca de 80.000 se vuelven discapacitados anualmente, aproximadamente
17.000 de éstos requieren cuidado especializado de por vida (Kraus (1997) "Epidemiology of Head Injur y , " in Head Injur y , ed. Cooper (Williams & Wilkins Co., Baltimore) págs 1-19; Selecki et al. (1982) Australian & New Zealand Journal of Surger y 52 (1) :93-102) . Además de la lesión inicial creada por el traumatismo brusco al cerebro, una fuerza biomecánica excesiva inicia una serie de efectos secundarios deletéreos que puede aumentar espectacularmente el tamaño de la lesión, morbilidad, y mortalidad desde días hasta meses después de la lesión inicial (McIntosh et al. (1996) Lab Invest, 74 (2) :315-42; Stambrook et al. (1990) Can J Surg 33 (2) :115-8) . A pesar de la gravedad del problema, no se ha descubierto un tratamiento farmacológico eficaz para el TCE en seres humanos.
La infusión intravenosa continua (IV) permite un suministro rápido de fármacos y conseguir una concentración de suero de estado estacionario continuo, pero esta vía de administración de la progesterona no está aprobada por la FDA en Estados Unidos. Sólo se han observado tres estudios humanos que implican el uso de progesterona IV en Estados Unidos. En una prueba clínica de fase I inicial aprobada por la FDA (IND 33, 580) , Christen, et al. administraron progesterona IV disuelta en una emulsión de grasa de etanol-Intralípido 20% combinado con doxorubicina en unas 24 horas a 32 pacientes cancerosos sin efectos tóxicos (Christen et al. (1993) Journal of Clinical Oncology 11 (12) :24172426) . En un segundo estudio, Allolio et al. observaron que las concentraciones de suero estable (CSS) de progesterona se podrían conseguir en voluntarios masculinos sanos (Allolio et al. (1995) European Journal of Endocrinology 133 (6) :696-700) . El tercer estudio se hizo después del estudio realizado por Christen et al, pero fue una prueba de fase II que pone a prueba el efecto de coadministración de progesterona en dosis altas en las farmacocinéticas de paclitaxel. El manuscrito no presentaba información detallada de las farmacocinéticas de progesterona.
WO 02/30409 describe un método tratando una lesión del sistema nervioso central, dicho método comprende la administración a un paciente en su necesidad de una cantidad terapéuticamente eficaz de una composición que comprende progesterona.
Goss et al. describe los resultados de un estudio en ratas macho que intentan determinar la dosis de progesterona, efecto de respuesta en el rendimiento conductual y el receptor de expresión GABA-A después de una contusión cortical (Goss et al. (2003) Behavioral effects and anatomic correlates after brain injur y : A progesterona doseresponse study, Pharmacology Biochemistr y and Behaviour 76 (2) :231-241) . Durante el estudio, las ratas macho recibieron inyecciones de 0, 8, 16 o 32 mg/kg de progesterona. Según los autores, los resultados sugieren que dosis bajas y moderadas de progesterona son óptimas para facilitar la recuperación de comportamientos selectos y que el tratamiento de progesterona tras la lesión permite un intervalo de dosis más amplio que el tratamiento de antes de la lesión.
Después de una lesión traumática del sistema nervioso central, una serie de eventos fisiológicos conduce a la pérdida neuronal incluyendo, por ejemplo, una respuesta inmunitaria inflamatoria y excitotoxicidad resultante del impacto inicial que interrumpe los sistemas de receptores de glutamato, acetilcolina, colinérgicos, GABAA, y NMDA. Además, la lesión traumática del SNC es frecuentemente seguida de un edema cerebral y/o de médula espinal que aumenta la reacción en cascada de lesiones y conduce a otra muerte de células secundarias y se incrementa la mortalidad de pacientes. Se necesitan métodos para el tratamiento de lesiones traumáticas del SNC in vivo que sean apropiados para proveer un soporte trófico subsecuente para continuar con el tejido del sistema central restante, y mejorar así la recuperación y reparación funcional, bajo la reacción en cascada psicológica compleja de eventos que siguen la agresión inicial.
RESUMEN DE LA INVENCIÓN
Éste es un método para tratar una lesión cerebral traumática en un sujeto humano. El método comprende la administración al sujeto que lo necesite de al menos un ciclo de terapia, donde dicho ciclo comprende la administración de un régimen de dosificación intravenosa de dos niveles terapéuticamente efectivos de progesterona. El régimen de dosificación de dos niveles comprende un primer periodo de tiempo donde se administra al sujeto una dosis más alta de 2 15
progesterona por hora, seguida de un segundo periodo de tiempo donde se administra al sujeto una dosis más baja de progesterona por hora. El primer periodo de tiempo comprende una dosis por hora de progesterona de aproximadamente 0.1 mg/kg a aproximadamente 7.1 mg/kg durante al menos 1 hora o éste comprende una inyección en bolo. El segundo período de tiempo comprende una dosis por hora de progesterona de aproximadamente 0.05 mg/kg a aproximadamente 5 mg/kg. En otros métodos, un tercer período de tiempo que comprende un protocolo de administración gradual se añade al régimen de dosificación de progesterona.
BREVE DESCRIPCIÓN DE LOS DIBUJOS
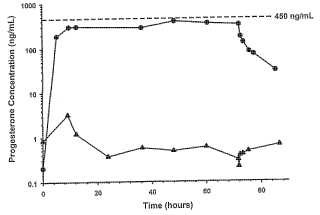
La figura 1 muestra que se pueden obtener rápidamente concentraciones estables de progesterona utilizando infusiones intravenosas continuas. Los círculos cerrados representan el perfil concentración-tiempo del suero para un paciente que recibe progesterona. Los triángulos sólidos representan el perfil concentración-tiempo del suero para un paciente que recibe una infusión de placebo. Las concentraciones de progesterona para pacientes que reciben una infusión de placebo se mantuvieron constantes a lo largo del periodo de estudio. Las concentraciones CSS en pacientes que reciben progesterona se consiguen rápidamente y, una vez conseguidas, son estables a lo largo del periodo de infusión. La figura 2 muestra que existe una correlación significativa entre CSS previstos y medidos. Los CSS fueron previstos como proporción del índice de infusión y de CL. Los valores previstos fueron comparados con los CSS medidos en cada paciente por trazado de cada par de valores en la línea de identidad. El coeficiente de correlación de Spearman por rangos para esta relación fue 0.946 (p<0.001) . La figura 3 muestra el análisis de Bland-Altman de la correlación entre los CSS previstos y medidos. Puesto que un gráfico de CSS previstos versus medidos a menudo no revela una sobre o infra estimación (diagonal) sistemática, se llevó a cabo un análisis Bland-Altman. Los promedios de los valores previstos y medidos (abscisa) se representan comparados con la diferencia relativa de los dos valores (ordenada) . La línea continua es el valor medio para la diferencia relativa (-0.8±12.2%; media±SD) y las líneas de puntos representan el 95% de los intervalos seguros para los datos. Este gráfico demuestra claramente que no hay diagonal significativa asociada a este método de predicción. La figura 4 muestra que los valores CSS son considerablemente inferiores a los previstos basados en parámetros farmacocinéticos indicados previamente. Los CSS medidos en los 21 hombres (círculos sólidos) y 11 mujeres (triángulos sólidos) se han representado individualmente. Las líneas continuas y de puntos representan nuestras concentraciones de destino originales de 450±100 ng/mL. Estos datos demuestran claramente que en pacientes con TCE, los valores CSS son significativamente inferiores a los previstos usando los parámetros farmacocinéticos indicados previamente. La figura 5 provee un esquema del protocolo de registro para la selección del paciente para el estudio de TCE.
DESCRIPCIÓN DETALLADA DE LA INVENCIÓN
... [Seguir leyendo]
Reivindicaciones:
1. Progesterona para uso en tratamiento de lesión cerebral traumática, donde dicha progesterona se prepara para administración a un sujeto humano en al menos un ciclo de terapia, donde dicho ciclo de terapia comprende la administración de un régimen de dosificación intravenosa de dos niveles terapéuticamente eficaces de progesterona, dicho régimen de dosificación de dos niveles comprende un primer período de tiempo de al menos 1 hora, en la que se administra al sujeto una dosis elevada de infusión de progesterona por hora de aproximadamente 0, 1 mg/kg/hr a aproximadamente 7, 1 mg/kg/hr, seguida de un segundo período de tiempo en el que se administra a dicho sujeto una dosis inferior de infusión de progesterona por hora de aproximadamente 0, 05 mg/kg/hr a aproximadamente 5 mg/kg/hr.
2. Progesterona para uso según la reivindicación 1 donde el primer período de tiempo comprende una dosis de infusión de progesterona de aproximadamente 0, 71 mg/kg/hr.
3. Progesterona para uso en tratamiento de lesión cerebral traumática, dicha progesterona se prepara para la administración a un sujeto humano en al menos un ciclo de terapia, donde dicho ciclo de terapia comprende la administración de un régimen de dosificación intravenosa de dos niveles terapéuticamente eficaces de progesterona, dicho régimen de dosificación de dos niveles comprende un primer período de tiempo, en el que se administra al sujeto una dosis elevada de infusión de progesterona por hora, seguida de un segundo período de tiempo, en el que se administra a dicho sujeto una dosis inferior de infusión de progesterona por hora de aproximadamente 0, 05 mg/kg/hr a aproximadamente 5 mg/kg/hr, y el primer periodo comprende una inyección en bolo.
4. Progesterona para uso según la reivindicación 1 o 2, donde el segundo período de tiempo comprende una dosis de infusión de aproximadamente 0, 5 mg/kg/hr.
5. Progesterona para uso según cualquiera de las reivindicaciones precedentes, donde el segundo período de tiempo comprende un periodo de aproximadamente 24 horas hasta aproximadamente 120 horas.
6. Progesterona para uso según la reivindicación 5, donde el segundo período de tiempo comprende un periodo de aproximadamente 71 horas.
7. Progesterona para uso según cualquiera de las reivindicaciones precedentes, donde el primer período de tiempo comprende una dosis de infusión de progesterona de aproximadamente 0, 71 mg/kg/hr, el segundo período de tiempo comprende una dosis de infusión de aproximadamente 0, 5 mg/kg/hr, el primer período de tiempo comprende aproximadamente 1 hora, y el segundo período de tiempo comprende un periodo de aproximadamente 71 horas.
8. Progesterona para uso según cualquiera de las reivindicaciones precedentes, donde el régimen de dosificación intravenosa de dos niveles de progesterona produce un nivel sérico de progesterona en dicho sujeto de aproximadamente 100 ng/ml a aproximadamente 2000 ng/ml.
9. Progesterona para uso según la reivindicación 8, donde el nivel sérico de progesterona es de aproximadamente 200 ng/ml a aproximadamente 750 ng/ml.
10. Progesterona para uso según la reivindicación 9, donde el nivel sérico de progesterona es de aproximadamente 350 ng/ml a aproximadamente 450 ng/ml.
11. Progesterona para uso según cualquiera de las reivindicaciones precedentes, comprende además un tercer período de tiempo, donde dicho tercer período de tiempo comprende una administración gradual de progesterona al sujeto.
12. Progesterona para uso según cualquiera de las reivindicaciones precedentes, donde el primer y el segundo período de tiempo son continuos.
13. Progesterona para uso según cualquiera de las reivindicaciones de 1 a 11, donde el primer y el segundo período de tiempo son discontinuos.
14. Uso de progesterona en la preparación de un medicamento para el tratamiento de una lesión cerebral traumática en un sujeto humano, donde dicho medicamento se prepara para la administración a un sujeto humano en al menos un ciclo de terapia, dicho ciclo de terapia comprendiendo la administración de un régimen de dosificación intravenosa de dos niveles terapéuticamente eficaces de progesterona, dicho régimen de dosificación de dos niveles comprende un primer período de tiempo de al menos 1 hora donde se administra al sujeto una dosis de infusión de progesterona elevada por hora de aproximadamente 0, 1 mg/kg/hr a aproximadamente 7, 1 mg/kg/hr, seguido de un segundo período de tiempo, donde se administra a dicho sujeto una dosis inferior de infusión de progesterona por hora de aproximadamente 0, 05 mg/kg/hr a aproximadamente 5 mg/kg/hr.
15. Uso según la reivindicación 14, donde el primer período de tiempo comprende una dosis de infusión de progesterona de aproximadamente 0, 71 mg/kg/hr.
16. Uso de progesterona en la preparación de un medicamento destinado al tratamiento de lesión cerebral traumática en un sujeto humano, dicha progesterona se prepara para la administración a un sujeto humano en al menos un ciclo de terapia, donde dicho ciclo de terapia comprende la administración de un régimen de dosificación intravenosa de dos niveles terapéuticamente eficaces de progesterona, dicho régimen de dosificación de dos niveles comprende un primer período de tiempo, en el que se administra al sujeto una dosis elevada de infusión de progesterona por hora, seguida de
un segundo período de tiempo, en el que se administra a dicho sujeto una dosis inferior de infusión de progesterona por hora de aproximadamente 0, 05 mg/kg/hr a aproximadamente 5 mg/kg/hr, y el primer periodo comprende una inyección en bolo.
17. Uso según la reivindicación 14 o 16, donde el segundo período de tiempo comprende una dosis de infusión de 15 aproximadamente 0, 5 mg/kg/hr.
18. Uso según cualquiera de las reivindicaciones de 15 a 17, donde el segundo período de tiempo comprende un periodo de aproximadamente 24 horas a aproximadamente 120 horas.
19. Uso según la reivindicación 18, donde el segundo período de tiempo comprende un periodo de aproximadamente 71 horas.
20. Uso según cualquiera de las reivindicaciones de 14 a 19, donde el primer período de tiempo comprende una dosis de infusión de progesterona de aproximadamente 0, 71 mg/kg/hr, el segundo período de tiempo comprende una dosis de
infusión de aproximadamente 0, 5 mg/kg/hr, el primer período de tiempo comprende aproximadamente 1 hora, y el segundo período de tiempo comprende un periodo de aproximadamente 71 horas.
21. Uso según cualquiera de las reivindicaciones de 14 a 20, donde el régimen de dosificación intravenosa de dos
niveles de progesterona produce un nivel sérico de progesterona en dicho sujeto de aproximadamente 100 ng/ml a 30 aproximadamente 2000 ng/ml.
22. Uso según la reivindicación 21, donde el nivel sérico de progesterona es de aproximadamente 200 ng/ml a aproximadamente 750 ng/ml.
23. Uso según la reivindicación 22, donde el nivel sérico de progesterona es de aproximadamente 350 ng/ml a aproximadamente 450 ng/ml.
24. Uso según cualquiera de las reivindicaciones de 14 a 23, que comprende además un tercer período de tiempo,
donde dicho tercer período de tiempo comprende una administración gradual de progesterona al sujeto. 40
25. Uso según cualquiera de las reivindicaciones de 14 a 24, donde el primer y segundo período de tiempo son continuos.
26. Uso según cualquiera de las reivindicaciones de 14 a 24, donde el primer y segundo período de tiempo son 45 discontinuos.
Patentes similares o relacionadas:
Preparación sólida que contiene colorante, del 29 de Julio de 2020, de DAIICHI SANKYO COMPANY, LIMITED: Preparación farmacéutica sólida que comprende monobencenosulfonato de ácido [(1R,5S,6S)-6-(aminometil)-3- etilbiciclo[3.2.0]hept-3-en-6-il]acético […]
Derivados de 8-amino-2-oxo-1,3-diazaespiro-[4.5]-decano, del 29 de Julio de 2020, de GRUNENTHAL GMBH: Un compuesto según la fórmula general (I) **(Ver fórmula) donde R1 y R2 significan independientemente -H; -alquilo C1-C6, lineal o ramificado, […]
Derivados de bencimidazol como inhibidores Nav 1.7 (subunidad alfa del canal de sodio, dependiente del voltaje, tipo IX (SCN9A)) para tratar el dolor, la disuria y la esclerosis múltiple, del 22 de Julio de 2020, de Sumitomo Dainippon Pharma Co., Ltd: Un compuesto de fórmula (I): **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, donde R1a, R1b, R1c, y R1d son independientemente hidrógeno, […]
Derivado de 5-etiol-4-metil-pirazol-3-carboxamida que tiene actividad como agonista de TAAR, del 15 de Julio de 2020, de F. HOFFMANN-LA ROCHE AG: Un compuesto de fórmula I: **(Ver fórmula)** que es 5-etil-4-metil-N-[4-[(2S) morfolin-2-il]fenil]-1H-pirazol-3-carboxamida, o una sal de adición de ácido farmacéuticamente […]
Nuevos moduladores de receptores de fosfato de esfingosina, del 15 de Julio de 2020, de THE SCRIPPS RESEARCH INSTITUTE: Una composicion farmaceutica que comprende un compuesto de formula 265: **(Ver fórmula)** o una sal, estereoisomero, hidrato o solvato farmaceuticamente aceptable […]
Composición que comprende cinamaldehído y cinc, del 8 de Julio de 2020, de SOCIETE DES PRODUITS NESTLE S.A.: Composición que comprende cinamaldehído y cinc para la utilización en la mejora de uno o más de rendimiento cognitivo, cognición, humor o memoria en un […]
Síntesis y formas de sal novedosas de (R)-5-((E)-2-pirrolidin-3-ilvinil)pirimidina, del 1 de Julio de 2020, de Oyster Point Pharma, Inc: Un procedimiento para la fabricación de (R)-5-((E)-2-pirrolidin-3-ilvinil)pirimidina que comprende: (a) tratar el compuesto 1 con cloruro de metanosulfonilo para […]
Derivado de amina cíclica y uso farmacéutico del mismo, del 1 de Julio de 2020, de TORAY INDUSTRIES, INC.: Un derivado de amina cíclica representado por la siguiente fórmula general (I): **(Ver fórmula)** donde R1 representa un grupo alquiloxi que tiene de 1 a 3 átomos […]