Derivados de 3- pirrolo-ciclohexilen-2-dihidro-indolinona y usos de los mismos.
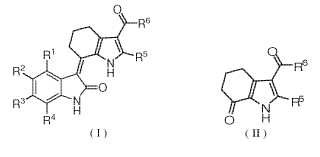
Un compuesto de Fórmula (I) o una sal farmacéuticamente aceptable del mismo:
en la que:
R1 se selecciona entre el grupo que consiste en hidrógeno, halo, alquilo, cicloalquilo, heteroalicíclico, hidroxi, alcoxi,
-C(O)R7, -NR8R9, -(CH2)nR10 y -C(O)NR11R12;
R2 se selecciona entre el grupo que consiste en hidrógeno, halo, alquilo, haloalquilo, hidroxi, alcoxi, haloalcoxi,
nitro, ciano, -NR8R9, -NR8C(O)R9, -C(O)R7, -C(O)NR11R1; -S(O)2NR8R9 y -SO2R13
R3 se selecciona entre el grupo que consiste en hidrógeno, halo, alquilo, haloalquilo, hidroxi, alcoxi, -C(O)R7, -
NR8R9, -NR8S(O)2R9, -S(O)2NR8R9, -NR8C(O)R9, -NR8C(O)OR9 y -SO2R13 ; R4 se selecciona entre el grupo que consiste en hidrógeno, halo, alquilo, hidroxi, alcoxi y -NR8R9;
R5 se selecciona entre el grupo que consiste en hidrógeno, alquilo y -C(O)R14;
R6 se selecciona entre el grupo que consiste en hidroxi, alcoxi, ariloxi, -N(R15)(CH2)rR16, -NR8R9 y -N(R17)-CH(R18)-
CR19(OH)-CH(R20)Z;
R7 se selecciona entre el grupo que consiste en hidrógeno, hidroxi, alcoxi y ariloxi;
cada uno de R8 y R9 se selecciona independientemente entre el grupo que consiste en hidrógeno, alquilo, cicloalquilo, arilo y heteroarilo;
o R8 y R9 junto con los átomos a los que están unidos pueden formar un anillo heterocíclico;
R10 se selecciona entre el grupo que consiste en hidroxi, -C(O)R7, -NR8R9 y -C(O)NR8R9;
cada uno de R11 y R12 se selecciona independientemente entre el grupo que consiste en hidrógeno, alquilo y arilo;
o R11 y R12 junto con el átomo de nitrógeno al que están unidos pueden formar un anillo heterocíclico;
R13 se selecciona entre el grupo que consiste en alquilo, arilo, arilalquilo, heteroarilo y heteroarilalquilo;
R14 se selecciona entre el grupo que consiste en hidroxi, alcoxi, ariloxi y -NR8R9;
R15 se selecciona entre el grupo que consiste en hidrógeno y alquilo;
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/CN2007/071161.
Solicitante: JIANGSU SIMCERE PHARMACEUTICAL R&D CO., LTD.
Nacionalidad solicitante: China.
Dirección: NO. 12 HUANYUAN ROAD NANJING JIANGSU 210042 CHINA.
Inventor/es: TANG,Feng, SHEN,Han, JIN,Qiu, DING,Lei, YANG,Jie, YIN,Xiaojin, LU,Shiyue.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K31/404 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › Indoles, p. ej. pindolol.
- A61K31/405 A61K 31/00 […] › Acidos indol-alcoilcarboxílicos; Sus derivados, p. ej. triptófano,indometacina.
- A61P29/00 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › Agentes analgésicos, antipiréticos o antiinflamatorios que no actúan sobre el sistema nervioso central, p. ej. agentes antirreumáticos; Antiinflamatorios no esteroideos (AINEs).
- A61P3/10 A61P […] › A61P 3/00 Medicamentos para el tratamiento de trastornos del metabolismo (de la sangre o de fluido extracelular A61P 7/00). › para la hiperglucemia, p.ej. antidiabéticos.
- A61P35/00 A61P […] › Agentes antineoplásicos.
- A61P37/00 A61P […] › Medicamentos para el tratamiento de problemas inmunológicos o alérgicos.
- A61P7/00 A61P […] › Medicamentos para el tratamiento de trastornos de la sangre o del fluido extracelular.
- A61P9/00 A61P […] › Medicamentos para el tratamiento de trastornos en el aparato cardiovascular.
- C07D403/04 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07D COMPUESTOS HETEROCICLICOS (Compuestos macromoleculares C08). › C07D 403/00 Compuestos heterocíclicos que contienen dos o más heterociclos, que tienen átomos de nitrógeno como únicos heteroátomos del ciclo, no previstos por el grupo C07D 401/00. › unidos directamente por un enlace entre dos miembros cíclicos.
PDF original: ES-2383084_T3.pdf
Fragmento de la descripción:
Derivados de 3-pirrolo[b]ciclohexilen-2-dihidroindolinona y usos de los mismos.
Campo de la Invención La presente invención se refiere a derivados de 3-pirrolo[b]ciclohexilen-2-dihidroindolinona y usos de los mismos. La presente invención también se refiere al método para preparar los compuestos anteriores y los intermedios de los mismos.
Antecedentes de la Invención Lo siguiente se ofrece como información de antecedentes solamente y no se admite que sea técnica anterior a la presente invención.
En la actualidad, se han intentado identificar muchos derivados de 2-dihidroindolinona como inhibidores de proteína quinasa, que se usan ampliamente en el tratamiento de una diversidad de enfermedades asociadas con actividad quinasa anómala, tales como cáncer, soriasis, hepatocirrosis, diabetes, angiogénesis, enfermedad oftalmológica, artritis reumatoide y otros trastornos inflamatorios, enfermedad inmune, enfermedad cardioavascular, por ejemplo aterosclerosis y una diversidad de enfermedades renales. De estos, muchos derivados de indirubina (documento PCT WO2001037819, documento PCT WO2002092079) , derivados de 3-metilenpirrol-2-dihidroindolinona (documentos US6642251, PCT WO2001060814, PCT WO2003035009, PCT WO2005053686) , derivados de 3pirrolo[b]ciclopentilen-2-dihidroindolinona (documento PCT WO2005016875) y otros derivados de 2dihidroindolinona (documento PCT WO 2000012084) etc, se han descrito todos como los inhibidores de quinasa para tratar cáncer.
Las células de mamíferos tienen mecanismos moleculares similares para regular la proliferación, diferenciación y muerte celular en el ciclo celular completo. De estos, la fosforilación de proteínas es un mecanismo principal para transducción de señal intracelular o transmembrana, con la función de regulación del ciclo celular, mientras que la fosforilación se regula por proteínas quinasas (PK) y proteínas fosfatasas. Las proteínas quinasas son la familia más grande conocida de enzimas en seres humanos, con un dominio catalítico conservado y diversos modos de regulación. Las proteínas quinasas son enzimas que catalizan la transferencia del grupo fosforilo terminal (y) de ATP a restos aminoacídicos específicos de sustrato. De acuerdo con la especificidad de estos restos aminoacídicos, estas quinasas se dividen en cuatro tipos, de las que los dos tipos principales son serina/treonina quinasas (STK) y proteína tirosina quinasas (PTK) . En eucariotas, hay segregación física y distancia entre los receptores de superficie celular y la transcripción nuclear. Las señales extracelulares afectan a las cascadas de algunas proteínas quinasas con fosforilación multietapa y finalmente alteran la actividad de los factores de transcripción para activar o bloquear la transcripción génica. Las proteínas tirosina quinasas y proteínas serina/treonina quinasas desempeñan un papel importante en el proceso de transducción de señal normal y su expresión aberrante dará como resultado una amplia serie de trastornos y enfermedades tales como cáncer, arteriosclerosis, psoriasis, respuestas inflamatorias y así sucesivamente. Por lo tanto, es una nueva estrategia de terapia regular la actividad quinasa y restaurar el equilibrio fisiológico.
La familia de proteína tirosina quinasas, que consiste en receptores transmembrana (tirosina quinasas receptoras, RTK) y formas citoplásmicas (tirosina quinasas no receptoras, CTK) , está implicada en la transducción de señal celular. El complemento de proteína quinasa del genoma humano (quinoma) consiste en 30 familias de tirosina quinasa que contienen aproximadamente 90 proteínas tirosina quinasas diferentes (PTK) , de las que 58 miembros son tirosina quinasas receptoras. Para un análisis más completo de las tirosina quinasas, véase Manning G, Science, 2002, 298: 1912 que se incorpora por referencia, incluyendo cualquier dibujo, como si se expusiera completamente en la presente memoria. La tirosina quinasa receptora es una clase de proteína transmembrana con región citoplásmica y una parte extracelular que está compuesta por un dominio proteico muy grande que se une a ligandos extracelulares por ejemplo un polipéptido soluble o unido a membrana, incluyendo insulina y una diversidad de factores de crecimiento. Una parte citoplásmica contiene el dominio catalítico de tirosina quinasa con sitio de autofosforilación, cuya actividad catalítica intrínseca se activa tras la unión al ligando. Las tirosina quinasas receptoras incluyen EGFR (receptor de crecimiento epidérmico) , VEGFR (receptor de factor de crecimiento endotelial vascular) , PDGFR (receptor de factor de crecimiento derivado de plaquetas) , FGFR (receptor del factor de crecimiento de fibroblastos) y así sucesivamente. Las cascadas de señalización corriente abajo más importantes activadas por RTK incluyen la ruta ERK/MAPK de Ras extracelular, la PI-3' quinasa AKT y la ruta de JAK/STAT. Las PTK proporcionan señales de comunicación que unen todas estas rutas conduciendo en última instancia a la regulación de la transcripción génica. También pueden utilizarse cascadas adicionales. A través de un mecanismo regulador diferente, las tirosina quinasas no receptoras (CTK) participan en respuestas a señales extracelulares asociándose físicamente con receptores transmembrana (Grosios k, et al, Drugs Fut, 2003, 28: 679) .
Estos restos de tirosina fosforilados sirven como sitios de acoplamiento para dominios de unión a fosfotirosina (por ejemplo, dominios de homología de Src 2 y 3 [SH2 y SH3] y de unión a fosfotirosina [PT-3]) hallados en varias proteínas de señalización intracelular (por ejemplo, Shc, Grb2, Src, Cbl, fosfolipasa Cg y fosfoinositol-3' [PI-3' quinasa]) . El ensamblaje de complejos activados en la membrana inicia varias cascadas que son la clave para la señalización corriente abajo y la respuesta biológica. La formación de homo y heterodímeros también es posible. Los receptores sin actividad catalítica pueden acoplarse a PTK no receptoras mediante asociación no covalente con el dominio citoplásmico de una subunidad receptora, formando de este modo receptores "binarios". Las cascadas de señalización corriente abajo más importantes activadas por RTK incluyen la ruta de quinasa activada por mitógeno (MAP) -quinasa regulada por Ras extracelular (ERK) , la PI-3' quinasa-AKT y la ruta de JAK/STAT. Las PTK proporcionan señales de comunicación que unen todas estas rutas conduciendo en última instancia a la regulación de la transcripción génica. Pueden utilizarse también cascadas adicionales. Por ejemplo, la InsR utiliza el sistema de señalización de adenilil ciclasa que, a su vez, activa proteína quinasas específicas de serina-treonina dependientes de AMPc. (Grosios k, et al, Drugs Fut, 2003, 28: 679) .
Las tirosina quinasas no receptoras (CTK) participan en respuesta a señales extracelulares asociándose físicamente con receptores transmembrana, tales como hormona, citocina y receptores del factor de crecimiento. Se activan después cuando estos receptores se unen por ligandos extracelulares o componentes de adhesión celular en fases particulares del ciclo celular.
En células normales, las RTK activadas se internalizan rápidamente lejos de la superficie celular y se someten a modificaciones que inhiben su actividad enzimática. Esto asegura que la activación de las cascadas de señal es solamente transitoria y la célula vuelve a su estado no estimulado oportunamente. Sin embargo, una diversidad de alteraciones estructurales que varían de sustituciones de aminoácido sencillo a grandes deleciones o desregulación de las señales inhibidoras y mecanismos de autocontrol, pueden bloquear las quinasas en la forma activada en la que el dominio quinasa está siempre activo. Se ha mostrado que varias enfermedades se deben a mutaciones que activan o conducen a expresión errónea/sobreexpresión de PTK. Durante la caracterización molecular de tumores malignos, aproximadamente la mitad de todas las PTK conocidas tales como EGF, ErbB2, Ret, Kit, Src, Abl, PDGFR, VEGF1/2/3, FGFR1/2/3, etc, se han hallado en formas mutadas o sobreexpresadas incluyendo casos esporádicos. Los estudios clínicos también muestran que la sobreexpresión o trastornos de PTK son de valor de referencia importante para el pronóstico de pacientes con cáncer y predicción de síntomas (Madhusudan S, et al, Clin Biochem, 2004, 37: 618) . En resumen, las tirosina quinasas son muy importantes para la autorregulación fisiológica y la mutación/reordenamiento de genes puede conducir al trastorno o sobreexpresión de PTK, después dar como resultado la aparición de enfermedades, de modo que el agonista o antagonista de PTK puede usarse en el tratamiento.
Independientemente... [Seguir leyendo]
Reivindicaciones:
1. Un compuesto de Fórmula (I) o una sal farmacéuticamente aceptable del mismo:
en la que:
R1 se selecciona entre el grupo que consiste en hidrógeno, halo, alquilo, cicloalquilo, heteroalicíclico, hidroxi, alcoxi, -C (O) R7, -NR8R9, - (CH2) nR10 y -C (O) NR11R12; R2 se selecciona entre el grupo que consiste en hidrógeno, halo, alquilo, haloalquilo, hidroxi, alcoxi, haloalcoxi, nitro, ciano, -NR8R9, -NR8C (O) R9, -C (O) R7, -C (O) NR11R12ᇬ-S (O) 2NR8R9 y -SO2R13᧷
R3 se selecciona entre el grupo que consiste en hidrógeno, halo, alquilo, haloalquilo, hidroxi, alcoxi, -C (O) R7, 10 NR8R9, -NR8S (O) 2R9, -S (O) 2NR8R9, -NR8C (O) R9, -NR8C (O) OR9 y -SO2R13᧷
R4 se selecciona entre el grupo que consiste en hidrógeno, halo, alquilo, hidroxi, alcoxi y -NR8R9; R5 se selecciona entre el grupo que consiste en hidrógeno, alquilo y -C (O) R14; R6 se selecciona entre el grupo que consiste en hidroxi, alcoxi, ariloxi, -N (R15) (CH2) rR16, -NR8R9 y -N (R17) -CH (R18)
CR19 (OH) -CH (R20) Z;
R7 se selecciona entre el grupo que consiste en hidrógeno, hidroxi, alcoxi y ariloxi; cada uno de R8 y R9 se selecciona independientemente entre el grupo que consiste en hidrógeno, alquilo, cicloalquilo, arilo y heteroarilo;
o R8 y R9 junto con los átomos a los que están unidos pueden formar un anillo heterocíclico;
R10 se selecciona entre el grupo que consiste en hidroxi, -C (O) R7, -NR8R9 y -C (O) NR8R9; 20 cada uno de R11 y R12 se selecciona independientemente entre el grupo que consiste en hidrógeno, alquilo y arilo;
o R11 y R12 junto con el átomo de nitrógeno al que están unidos pueden formar un anillo heterocíclico; R13 se selecciona entre el grupo que consiste en alquilo, arilo, arilalquilo, heteroarilo y heteroarilalquilo; R14 se selecciona entre el grupo que consiste en hidroxi, alcoxi, ariloxi y -NR8R9; R15 se selecciona entre el grupo que consiste en hidrógeno y alquilo;
R16
se selecciona entre el grupo que consiste en hidroxi, -NR8R9, -C (O) R7, arilo, heteroarilo, -N+ (O-) R8R9, N (OH) R8 y -NHC (O) Ra, en la que Ra se selecciona entre el grupo que consiste en alquilo sin sustituir, haloalquilo y arilalquilo;
cada uno de R17, R18, R19 y R20 se selecciona independientemente entre el grupo que consiste en hidrógeno y alquilo;
Z se selecciona entre el grupo que consiste en arilo, heteroarilo y -NR8R9;
cada uno de n y r es independientemente un número entero de 1 a 4, 2. El compuesto o una sal farmacéuticamente aceptable de la reivindicación 1, en el que:
R1 se selecciona entre el grupo que consiste en hidrógeno, halo, alquilo, cicloalquilo, heteroalicíclico, hidroxi, alcoxi, -C (O) R7, -NR8R9, - (CH2) nR10 and -C (O) NR11R12; R2 se selecciona entre el grupo que consiste en hidrógeno, halo, alquilo, trihalometilo, hidroxi, alcoxi, trihalometoxi, nitro, ciano, -NR8R9, -NR8C (O) R9, -C (O) R7, -C (O) NR11R12, -S (O) 2NR8R9 y -SO2R13;
R3 se selecciona entre el grupo que consiste en hidrógeno, halo, alquilo, trihalometilo, hidroxi, alcoxi, -C (O) R7, -NR8R9, -NR8S (O) 2R9, -S (O) 2NR8R9, -NR8C (O) R9, -NR8C (O) OR9 y -SO2R13; R4 se selecciona entre el grupo que consiste en hidrógeno, halo, alquilo, hidroxi, alcoxi y -NR8R9; R5 se selecciona entre el grupo que consiste en hidrógeno, alquilo y -C (O) R14; R6 se selecciona entre el grupo que consiste en hidroxi, alcoxi, -NR8R9, -N (R15) (CH2) rR16 y -NHCH (R18) -CR19 (OH)
CH (R20) Z; R7 se selecciona entre el grupo que consiste en hidrógeno, hidroxi, alcoxi y ariloxi; cada uno de R8 y R9 se selecciona independientemente entre el grupo que consiste en hidrógeno, alquilo, cicloalquilo, arilo y heteroarilo;
Z se selecciona entre el grupo que consiste en arilo, heteroarilo y -NR8R9; n es un número entero de1 a 4; r es un número entero de 1 a 3. 3. El compuesto o una sal farmacéuticamente aceptable de la reivindicación 1, en el que: cada uno de R1, R3 y R4 se selecciona independientemente entre el grupo que consiste en hidrógeno, halo y alquilo. R2 se selecciona entre el grupo que consiste en hidrógeno, halo, alquilo, alcoxi, trihalometoxi, nitro, -NR8C (O) R9, C (O) R7, -S (O) 2NR8R9 y -C (O) NR11R12; R5 es metilo; R6 se selecciona entre el grupo que consiste en hidroxi, alcoxi, -NR8R9, -N (R15) (CH2) rR16 y -NHCH2CH (OH) CH2-NR8R9; R7 se selecciona entre el grupo que consiste en hidroxi, alcoxi y ariloxi; cada uno de R8 y R9 se selecciona independientemente entre el grupo que consiste en hidrógeno, alquilo, cicloalquilo, arilo y heteroarilo; 15 o R8 y R9 junto con los átomos a los que están unidos pueden formar un anillo heterocíclico; cada uno de R11 y R12 se selecciona independientemente entre el grupo que consiste en hidrógeno, alquilo y arilo; o R11 y R12 junto con el átomo de nitrógeno al que están unidos pueden formar un anillo heteroalicíclico; R15 se selecciona entre el grupo que consiste en hidrógeno y alquilo; R16 se selecciona entre el grupo que consiste en hidroxi, arilo, heteroarilo y -NR8R9; r es un número entero de 1 a 3. 4. Un procedimiento para preparar el compuesto de Fórmula (I) , en el que: en condiciones de ácido de Lewis, el compuesto de Fórmula (III) y el compuesto de Fórmula (II) se hacen reaccionar en un disolvente no protónico durante 1 a 20 horas a una temperatura de reacción de entre 50 ºC y 150 ºC de acuerdo con la siguiente ecuación de reacción: En la que las definiciones de R1, R2, R3, R4, R5 y R6 son como se han descrito en la reivindicación 1. 5. El procedimiento de la reivindicación 4, en el que dicho ácido de Lewis es TiCl4. 6. El procedimiento de la reivindicación 4, en el que dicho disolvente no protónico es un disolvente protefílico no protónico o disolvente inerte, en el que dicho disolvente protofílico no protónico se selecciona entre el grupo que consiste en N, N-dimetilformamida, acetona, acetonitrilo, dimetilsulfóxido y piridina, y en el que; dicho disolvente inerte se selecciona entre el grupo que consiste en pentano, hexano, ciclonexano, benceno y 5 tolueno; 7. El procedimiento de la reivindicación 6, en el que dicho disolvente no protónico es piridina. 8. El procedimiento de la reivindicación 4, en que dicha temperatura de reacción está entre 100 ºC y 110 ºC y el tiempo de reacción es de 8 a 10 horas. 9. Uso de un compuesto o una sal farmacéuticamente aceptable de una cualquiera de las reivindicaciones 1 a 3 para la fabricación de un medicamento para tratar un trastorno relacionado con proteína quinasa en un organismo, seleccionándose dicho trastorno relacionado con proteína quinasa del grupo que consiste en carcinoma de células escamosas, astrocitoma, sarcoma de Kaposi glioblastoma, cáncer de pulmón, cáncer de vejiga, cáncer de cabeza y cuello, melanoma, cáncer de ovario, cáncer de próstata, cáncer de mama, glioma, cáncer colorrectal, cáncer hepático, cáncer renal, cáncer genitourinario, cáncer pancreático y cáncer gastrointestinal, diabetes, un trastorno de hiperproliferación, angiogénesis, un trastorno inflamatorio, un trastorno inmunológico y un trastorno cardiovascular. 10. El uso de la reivindicación 9, en el que dicho organismo es un mamífero o un ser humano. 11. Una composición farmacéutica para tratar un trastorno relacionado con proteína quinasa en un organismo, que comprende un compuesto o sal farmacéuticamente aceptable de una cualquiera de las reivindicaciones 1 a 3 y un 20 vehículo o excipiente farmacéuticamente aceptable. 12. Un intermedio de Fórmula (II) : en la que: R5 se selecciona entre el grupo que consiste en hidrógeno, alquilo y -C (O) R14; R6 se selecciona entre el grupo que consiste en hidroxi, alcoxi, -N (R15) (CH2) rR16, -NR8R9 y -NHCH (R18) -CR19 (OH) CH (R20) Z; cada uno de R8 y R9 se selecciona independientemente entre el grupo que consiste en hidrógeno, alquilo, cicloalquilo, arilo y heteroarilo; o R8 y R9 junto con los átomos a los que están unidos pueden formar un anillo heterocíclico; 30 R14 se selecciona entre el grupo que consiste en hidroxi, alcoxi, ariloxi y -NR8R9; R15 se selecciona entre el grupo que consiste en hidrógeno y alquilo; R16 se selecciona entre el grupo que consiste en hidroxi, -NR8R9 y heteroarilo; cada uno de R18, R19 y R20 se selecciona independientemente entre el grupo que consiste en hidrógeno y alquilo; Z se selecciona entre el grupo que consiste en arilo, heteroarilo y -NR8R9; y r es un número entero 2 ó 3, o R8 y R9 junto con los átomos a los que están unidos pueden formar un anillo heterocíclico; R10 se selecciona entre el grupo que consiste en hidroxi, -C (O) R7, -NR8R9 y -C (O) NR8R9; cada uno de R11 y R12 se selecciona independientemente entre el grupo que consiste en hidrógeno, alquilo y arilo;
o R11 y R12 junto con el átomo de nitrógeno al que están unidos pueden formar un anillo heterocíclico; R13 se selecciona entre el grupo que consiste en alquilo, arilo, arilalquilo, heteroarilo y heteroarilalquilo; R14 se selecciona entre el grupo que consiste en hidroxi, alcoxi, ariloxi y -NR8R9; R15 se selecciona entre el grupo que consiste en hidrógeno y alquilo; R16 se selecciona entre el grupo que consiste en hidroxi, arilo, heteroarilo y -NR8R9; cada uno de R18, R19 y R20 se selecciona independientemente entre el grupo que consiste en hidrógeno y alquilo;
Patentes similares o relacionadas:
 Composiciones y métodos para el tratamiento de trastornos de células plasmáticas y trastornos prolinfocíticos de células b, del 29 de Julio de 2020, de Knopp Biosciences LLC: Una composición que comprende una cantidad terapéuticamente eficaz de dexpramipexol para su uso en el tratamiento de un trastorno de células B caracterizado por niveles elevados […]
Composiciones y métodos para el tratamiento de trastornos de células plasmáticas y trastornos prolinfocíticos de células b, del 29 de Julio de 2020, de Knopp Biosciences LLC: Una composición que comprende una cantidad terapéuticamente eficaz de dexpramipexol para su uso en el tratamiento de un trastorno de células B caracterizado por niveles elevados […]
Derivados de piperidina 1,4 sustituidos, del 29 de Julio de 2020, de 89Bio Ltd: Un compuesto de acuerdo con la Fórmula I: **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, en donde: A se selecciona de […]
Profármacos de gemcitabina, del 29 de Julio de 2020, de NuCana plc: Una formulación farmacéutica que comprende gemcitabina-[fenil-benzoxi-L-alaninil)]-(S)-fosfato 3: **(Ver fórmula)** o una sal o solvato […]
Formas cristalinas de 6-((6,7-dimetoxiquinazolin-4-il)oxi)-N,2-dimetilbenzofuran-3-carboxamida, del 29 de Julio de 2020, de Hutchison Medipharma Limited: Forma I de 6-((6,7-dimetoxiquinazolin-4-il)oxi)-N,2-dimetilbenzofuran-3-carboxamida, en donde el difractograma de rayos X de polvo de la Forma […]
Compuestos y procedimientos de uso, del 29 de Julio de 2020, de Medivation Technologies LLC: Un compuesto de fórmula (Aa-1): **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, en la que: A representa H, halógeno, amino, […]
Complejos de agentes terapéuticos de base vírica y poli(beta-amino-ésteres) modificados, del 29 de Julio de 2020, de Sagetis Biotech, SL: Un complejo de un agente terapéutico de base vírica con un polímero de fórmula I: **(Ver fórmula)** donde cada L1 y L2 están seleccionados […]
Compuestos de alquinilbenceno heterocíclicos, y composiciones médicas y usos de los mismos, del 29 de Julio de 2020, de Guangzhou Healthquest Pharma Co., Ltd: Un compuesto de alquinilbenceno heterocíclico que tiene la fórmula (I) y una sal farmacéuticamente aceptable, o estereoisómero del mismo, **(Ver […]
Régimen de terapia y métodos para sensibilizar células de cáncer tratadas con una terapia epigenética frente a inhibidores de PARP en múltiples cánceres, del 22 de Julio de 2020, de THE JOHNS HOPKINS UNIVERSITY: Una combinación que comprende un agente desmetilante del ADN y un inhibidor de poli ADP ribosa polimerasa (PARP) para su uso en el tratamiento del cáncer, en […]