Derivado polimérico de docetaxel, método de preparación del mismo y sus usos.
Un derivado polimérico de docetaxel proporcionado por un enlace éster entre al menos un grupo hidroxilo dedocetaxel y un grupo carboxilo en una cadena lateral de ácido aspártico de un copolímero de bloques quecomprende polietilenglicol y ácido poliaspártico,
en donde (i) la relación del número de moléculas enlazadas dedocetaxel con respecto al número total de unidades de repetición de ácido aspártico por molécula del copolímero debloques es de 28% o más, y/o (ii) el número de moléculas enlazadas de docetaxel por molécula del copolímero debloques es 11 o más.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/JP2009/059633.
Solicitante: NANOCARRIER CO., LTD.
Nacionalidad solicitante: Japón.
Dirección: 4-19, Kashiwa-no-ha 5-chome Kashiwa-shi, Chiba 277-0882 JAPON.
Inventor/es: KATO, YASUKI, SAITO, HIROYUKI, HARADA,Mitsunori.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K31/337 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › que tienen ciclos de cuatro eslabones, p. ej. taxol.
- A61K47/34 A61K […] › A61K 47/00 Preparaciones medicinales caracterizadas por los ingredientes no activos utilizados, p. ej. portadores o aditivos inertes; Agentes de direccionamiento o agentes modificadores enlazados químicamente al ingrediente activo. › Compuestos macromoleculares obtenidos por reacciones distintas a aquellas en las que intervienen solamente enlaces insaturados carbono-carbono, p. ej. poliésteres, poly(amino ácidos), polisiloxanos, polifosfacinas, copolímeros de polialquilenglicol o poloxámeros (A61K 47/10 tiene prioridad).
- A61K47/48
- A61P35/00 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › Agentes antineoplásicos.
- C08G69/40 QUIMICA; METALURGIA. › C08 COMPUESTOS MACROMOLECULARES ORGANICOS; SU PREPARACION O PRODUCCION QUIMICA; COMPOSICIONES BASADAS EN COMPUESTOS MACROMOLECULARES. › C08G COMPUESTOS MACROMOLECULARES OBTENIDOS POR REACCIONES DISTINTAS A AQUELLAS EN LAS QUE INTERVIENEN SOLAMENTE ENLACES INSATURADOS CARBONO - CARBONO (procesos de fermentación o procesos que utilizan enzimas para sintetizar un compuesto dado o una composición dada o para la separación de isómeros ópticos a partir de una mezcla racémica C12P). › C08G 69/00 Compuestos macromoleculares obtenidos por reacciones que forman un enlace amidocarboxílico en la cadena principal de la macromolécula (polihidrazidas C08G 73/08; poliamido-ácidos C08G 73/10; poliamida-imidas C08G 73/14). › Poliamidas que contienen oxígeno en la forma de grupos éter (C08G 69/12, C08G 69/32 tienen prioridad).
- C08G81/00 C08G […] › Compuestos macromoleculares obtenidos por interreacción de polímeros en ausencia de monómeros, p. ej. polímeros en bloque (que implican solamente las reacciones enlace carbono-carbono insaturado C08F 299/00).
PDF original: ES-2396134_T3.pdf
Fragmento de la descripción:
Derivado polimérico de docetaxel, método de preparación del mismo y sus usos. Campo de la técnica La presente invención se refiere a un derivado polimérico de docetaxel, así como a un método de preparación del
derivado y usos del derivado.
Antecedentes El docetaxel es un agente anticancerígeno a base de taxano semisintetizado a partir de un extracto de agujas de Taxus baccata. Promueve la polimerización tubular para formar micro túbulos estables y previene la depolimerización de éstos. También forma fascículos de micro túbulos morfológicamente anormales en las células.
Se conoce que detiene la mitosis a través de estos efectos.
En general, los agentes anticancerígenos a base de taxano son poco solubles en agua, y por tanto requieren el uso de solventes orgánicos especiales para su administración a humanos. Para superar el problema de tal baja solubilidad en agua, se han desarrollado métodos para mejorar la solubilidad en agua de un agente anticancerígeno a base de taxano encapsulándolo en un copolímero de bloques que tenga un segmento hidrófilo y un segmento hidrófobo para formar micelas poliméricas a través de su interacción hidrófoba (Documentos de patentes 1 y 2)
El documento de patente 3 divulga que la solubilidad en agua de hidrocloruro de doxorubicina se puede mejorar enlazando a éste con un copolímero de bloques que incluya polietilenglicol y ácido poliaspártico vía un enlace amida.
El documento de patente 4 divulga un derivado polimérico del SN-38 en el cual el grupo hidroxil fenólico del SN-38 20 se enlaza con un copolímero de bloques que tiene polietilenglicol y ácido poliglutámico vía un enlace éster.
El documento de patente 5 divulga un derivado polimérico de un taxano como es docetaxel, en el cual el grupo hidroxilo alcohólico de taxano se enlaza con un copolímero de bloques que incluye polietilenglicol y ácido poliaspártico.
Referencias del estado de la técnica.
Documentos de patentes. Documento de patente 1: EP1127570 A Documento de patente 2: WO2004/082718 Documento de patente 3: JP02-300133 A Documento de patente 4: WO2004/039869
Documento de patente 5: WO2007/111211
Descripción de la invención
Problemas a resolver mediante la invención Sin embargo, a pesar de la existencia de los documentos del estado de la técnica antes mencionados, todavía existe la necesidad en un derivado de docetaxel de efectos colaterales reducidos y eficacia incrementada.
En vista de los problemas anteriores, la presente invención se llevó a cabo para reducir aún más los efectos colaterales del docetaxel y mejorar su eficacia.
Medios para resolver los problemas Los solicitantes de la presente invención esperaban que una formulación de liberación sostenida, una forma de dosificación que regule la cantidad en que se libere el medicamento después de su administración, pudiera ser
efectivo en términos de reducción de los efectos colaterales, debido a que un incremento repentino de la concentración del medicamento liberado inmediatamente después de la administración de un agente anticancerígeno podría provocar la aparición de efectos colaterales. Los solicitantes de la presente invención también consideraron que tal forma de dosificación pudiera prolongar la duración de la acción de un taxano como es docetaxel sobre células tumorales mejorando por tanto la eficacia de éste.
Además, después de esfuerzos intensivos y extensivos para desarrollar un agente anticancerígeno con efectos colaterales reducidos y eficacia incrementada, los solicitantes de la presente invención han encontrado que la velocidad de liberación del docetaxel a partir de un derivado polimérico de docetaxel se puede controlar ajustando la relación y/o el número de moléculas de docetaxel enlazadas con un copolímero de bloques y han logrado obtener un derivado polimérico novedoso de docetaxel que encapsula un alto contenido de docetaxel para completar, con esto la presente invención.
Los objetos de la invención se ilustran a continuación:
(1) un método de preparación de un derivado polimérico de docetaxel proporcionado por un enlace éster entre al menos un grupo hidroxilo de docetaxel y un grupo carboxilo de una cadena lateral de ácido aspártico de un copolímero de bloques que tiene polietilenglicol y ácido poliaspártico. El método incluye un paso de ajuste de la relación y/o el número de moléculas de docetaxel enlazadas al copolímero de bloques para controlar así la velocidad de liberación de docetaxel del derivado polimérico de docetaxel resultante;
(2) el método según (1) , en donde el ajuste incluye (i) el ajuste a 28% o más de la relación del número de moléculas de docetaxel enlazadas con respecto al número total de unidades de repetición de ácido aspártico por molécula del copolímero de bloques, y/o (ii) el ajuste a 29%, o menos, del número de moléculas de docetaxel enlazadas por molécula del copolímero de bloques a 11 o más, para controlar así la velocidad de liberación de docetaxel a partir del derivado polimérico de docetaxel resultante en un tampón de fosfato de sodio 0, 1 M, pH 7, 4, a 37ºC en 24 horas;
(3) un derivado polimérico de docetaxel proporcionado por un enlace éster entre al menos un grupo hidroxilo de docetaxel y un grupo carboxilo de ácido aspártico de una cadena lateral de un copolímero de bloques que tenga polietilenglicol y ácido poliaspártico, en donde (i) la relación del número de moléculas enlazadas de docetaxel con respecto al número total de unidades de repetición de ácido aspártico por molécula del copolímero de bloques sea de 28% o más, y/o (ii) el número de moléculas enlazadas de docetaxel por molécula del copolímero de bloques sea 11 o más;
(4) el derivado polimérico de docetaxel según (3) , en donde la velocidad de liberación de docetaxel en un tampón de fosfato de sodio 0, 1 M, pH 7, 4 a 37ºC en 24 horas sea 29% o menos;
(5) El derivado polimérico de docetaxel según (3) o (4) , representado por la fórmula (I) :
Donde R1 es un átomo de hidrógeno o un grupo alquilo C1-C6, L1 es un grupo ligante, R es un átomo de hidrógeno o una molécula de docetaxel de la que al menos un grupo hidroxilo de docetaxel forma el enlace éster, n es un número entero de 40 a 450, y m+x es un número entero de 35 a 60, siempre que de 0% a 90% de m+x sea x, y que cuando x sea superior a 0, las unidades de (COHNH) y unidades de (COCH2CHNH) estén presentes al azar; y
(6) un agente anticancerígeno que comprende el derivado polimérico de docetaxel según (3) a (5)
Según la presente invención, se puede proporcionar un derivado polimérico de docetaxel que tenga un efecto colateral reducido y una excelente eficacia como medicamento.
Breve descripción de las figuras
La Figura 1 es un gráfico que muestra los resultados de un ensayo de liberación de medicamento de derivados poliméricos de docetaxel. Los círculos negros indican el porcentaje de docetaxel liberado a partir de un derivado polimérico de docetaxel en el cual 14 moléculas de docetaxel están enlazadas por molécula del polímero (14DTX: Ejemplo 1) . Los cuadrados blancos indican el porcentaje de docetaxel liberado a partir de un derivado polimérico de docetaxel en el cual 12 moléculas de docetaxel están enlazadas por molécula del polímero (12DTX: Ejemplo 2) . Los triángulos negros indican el porcentaje de docetaxel liberado a partir de un derivado polimérico de docetaxel en el cual 5 moléculas de docetaxel están enlazadas por molécula del polímero (5DTX: Ejemplo Comparativo 1) .
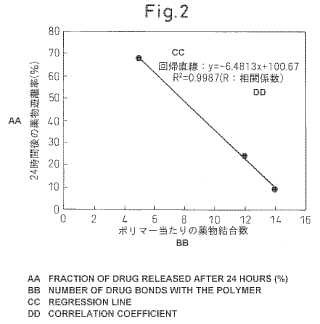
La Figura 2 es la representación de las relaciones de liberación del medicamento en 24 horas después de comenzado el experimento respecto a la cantidad de docetaxel enlazado con el polímero, basándose en los resultados del ensayo de liberación del medicamento mostrados en la Figura 1. Se determinó una línea de regresión a partir de los tres puntos.
La Figura 3 es un gráfico que muestra los resultados de un estudio farmacocinético en el cual se administró a ratones el derivado polimérico de docetaxel (PEG-pAsp-14DTX) del Ejemplo 1 o una solución de docetaxel. Los círculos negros indican las concentraciones de docetaxel total en el plasma al administrar 50 mg/kg de PEG-pAsp14DTX. Los cuadrados blancos indican las concentraciones de docetaxel liberadas a partir de PEG-pAsp-14DTX.
Los triángulos negros indican las concentraciones de docetaxel en el plasma al administrar 10 mg/kg de docetaxel disueltos en 10% de sacarosa. Cada punto representa el promedio de tres ejemplos y cada barra representa una desviación estándar.
La Figura 4 es un gráfico... [Seguir leyendo]
Reivindicaciones:
1. Un derivado polimérico de docetaxel proporcionado por un enlace éster entre al menos un grupo hidroxilo de docetaxel y un grupo carboxilo en una cadena lateral de ácido aspártico de un copolímero de bloques que comprende polietilenglicol y ácido poliaspártico, en donde (i) la relación del número de moléculas enlazadas de docetaxel con respecto al número total de unidades de repetición de ácido aspártico por molécula del copolímero de bloques es de 28% o más, y/o (ii) el número de moléculas enlazadas de docetaxel por molécula del copolímero de bloques es 11 o más.
2. El derivado polimérico de docetaxel según la reivindicación 1, en donde la velocidad de liberación de docetaxel en un tampón de fosfato de sodio 0, 1 M, pH 7, 4, a 37ºC en 24 horas es 29% o menos.
3. El derivado polimérico de docetaxel según la reivindicación 1, representado por la fórmula (I) :
donde R1 es un átomo de hidrógeno o un grupo alquilo C1-C6, L1 es un grupo ligante, R, es un átomo de hidrógeno o una molécula de docetaxel de la cual al menos un grupo hidroxilo forma el enlace éster, n es un número entero de 40 a 450, y m+x es un número entero de 35 a 60, siempre que de 0% a 90% de m+x sea x, y que cuando x sea superior a 0, estén presentes al azar unidades de (COCHNH) y unidades de (COCH2CHNH) .
en donde (i) la relación del número de grupos R que corresponden a moléculas de docetaxel con respecto a m+x se ha ajustado a 28% o más, y/o, (ii) el número de grupos R que corresponden a moléculas de docetaxel se ha ajustado a 11 o más.
4. El derivado polimérico de docetaxel según la reivindicación 1, representado por la fórmula (I) :
donde R1 es un átomo de hidrógeno o un grupo alquilo C1-C6, L1 es un grupo ligante, R es un átomo de hidrógeno o una molécula de docetaxel de la cual al menos un grupo hidroxilo forma el enlace éster, n es un número entero de 40 a 450, y m+x es un número entero de 35 a 60, siempre que de 0% a 90% de m+x sea x, y que cuando x sea superior a 0, estén presentes al azar unidades de (COCHNH) y unidades de (COCH2CHNH) .
en donde (i) la relación del número de grupos R que corresponden a moléculas de docetaxel con respecto a m+x se ha ajustado a 28% o más, y/o (ii) el número de grupos R que corresponden a moléculas de docetaxel se ha ajustado a 11 o más, en donde la velocidad de liberación de docetaxel en un tampón de fosfato de sodio 0, 1 M, pH 7, 4, a 37ºC en 24 horas se ha inhibido a 29% o menos.
5. El derivado polimérico de docetaxel según la reivindicación 1, representado por la fórmula (I) : 5 superior a 0, estén presentes al azar unidades de (COCHNH) y unidades de (COCH2CHNH) .
en donde (i) la relación del número de grupos R correspondientes a moléculas de docetaxel con respecto a m+x se ha ajustado a 28% o más, y/o (ii) el número de grupos R correspondientes a moléculas de docetaxel se ha ajustado a 11 o más, en donde la velocidad de liberación de docetaxel en un tampón de fosfato de sodio 0, 1 M, pH 7, 4, a 37ºC en 24 horas se ha inhibido a 29% o menos, y
en donde cuando el derivado polimérico de docetaxel se formula en la forma de una micela polimérica con una capa externa hecha de un polímero soluble en agua que tiene un diámetro de partícula de 200 nm o menor y se administra de forma intravenosa a un animal, la micela presenta efectos anti tumorales a la vez que previene la pérdida de peso corporal del animal después de la administración.
6. Un agente anticancerígeno que comprende el derivado polimérico de docetaxel según una cualquiera de las 15 reivindicaciones 1 a 5.
VELOCIDAD DE LIBERACIÓN
VELOCIDAD DE LIBERACIÓN
DEL MEDICAMENTO (%)
DEL MEDICAMENTO (%)
Fig. 1
Tiempo (h)
Fig. 2
NÚMERO DE MOLÉCULAS DEL MEDICAMENTO VINCULADAS AL POLÍMERO 1/4
VOLUMEN RELATIVO DEL TUMOR
CONCENTRACIÓN DTX (μO/ml)
(% DEL VOLUMEN ORIGINAL)
Fig. 3
TIEMPO DESPUÉS DE LA ADMINISTRACIÓN (h)
Fig. 4
TIEMPO (DÍAS) 2/4
CAMBIOS EN EL PESO CORPORAL
VOLUMEN RELATIVO DEL TUMOR
(% DEL PESO CORPORAR ORIGINARL)
(% DEL VOLUMEN ORIGINAL)
Fig. 5
TIEMPO (DÍAS) 2/4
Fig. 6
TIEMPO EN DIAS 3/4
CAMBIOS EN PESO CORPORAL (% DEL PESO CORPORAR ORIGINARL) CAMBIOS EN PESO CORPORAL (% DEL PESO CORPORAR ORIGINARL)
Fig. 7
TIEMPO (DÍAS)
Fig. 8
TIEMPO DESPUÉS DE LA ADMINISTRACIÓN (DÍAS)
Patentes similares o relacionadas:
Compuestos de alquinilbenceno heterocíclicos, y composiciones médicas y usos de los mismos, del 29 de Julio de 2020, de Guangzhou Healthquest Pharma Co., Ltd: Un compuesto de alquinilbenceno heterocíclico que tiene la fórmula (I) y una sal farmacéuticamente aceptable, o estereoisómero del mismo, **(Ver […]
 Composiciones y métodos para el tratamiento de trastornos de células plasmáticas y trastornos prolinfocíticos de células b, del 29 de Julio de 2020, de Knopp Biosciences LLC: Una composición que comprende una cantidad terapéuticamente eficaz de dexpramipexol para su uso en el tratamiento de un trastorno de células B caracterizado por niveles elevados […]
Composiciones y métodos para el tratamiento de trastornos de células plasmáticas y trastornos prolinfocíticos de células b, del 29 de Julio de 2020, de Knopp Biosciences LLC: Una composición que comprende una cantidad terapéuticamente eficaz de dexpramipexol para su uso en el tratamiento de un trastorno de células B caracterizado por niveles elevados […]
Derivados de piperidina 1,4 sustituidos, del 29 de Julio de 2020, de 89Bio Ltd: Un compuesto de acuerdo con la Fórmula I: **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, en donde: A se selecciona de […]
Profármacos de gemcitabina, del 29 de Julio de 2020, de NuCana plc: Una formulación farmacéutica que comprende gemcitabina-[fenil-benzoxi-L-alaninil)]-(S)-fosfato 3: **(Ver fórmula)** o una sal o solvato […]
Formas cristalinas de 6-((6,7-dimetoxiquinazolin-4-il)oxi)-N,2-dimetilbenzofuran-3-carboxamida, del 29 de Julio de 2020, de Hutchison Medipharma Limited: Forma I de 6-((6,7-dimetoxiquinazolin-4-il)oxi)-N,2-dimetilbenzofuran-3-carboxamida, en donde el difractograma de rayos X de polvo de la Forma […]
Compuestos y procedimientos de uso, del 29 de Julio de 2020, de Medivation Technologies LLC: Un compuesto de fórmula (Aa-1): **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, en la que: A representa H, halógeno, amino, […]
Complejos de agentes terapéuticos de base vírica y poli(beta-amino-ésteres) modificados, del 29 de Julio de 2020, de Sagetis Biotech, SL: Un complejo de un agente terapéutico de base vírica con un polímero de fórmula I: **(Ver fórmula)** donde cada L1 y L2 están seleccionados […]
Régimen de terapia y métodos para sensibilizar células de cáncer tratadas con una terapia epigenética frente a inhibidores de PARP en múltiples cánceres, del 22 de Julio de 2020, de THE JOHNS HOPKINS UNIVERSITY: Una combinación que comprende un agente desmetilante del ADN y un inhibidor de poli ADP ribosa polimerasa (PARP) para su uso en el tratamiento del cáncer, en […]