SAL CRISTALINA DE CLORHIDRATO DE MALEATO DE S-[2(1-IMINOETIL)ETIL]-2-METIL-L-CISTEINA.
Clorhidrato de maleato de S-[2-[(1-iminoetil)amino]etil]-2-metil-L-cisteína
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/IB2004/000678.
Solicitante: PHARMACIA CORPORATION.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 100 ROUTE 206 NORTH PEAPACK, NJ 07977 ESTADOS UNIDOS DE AMERICA.
Inventor/es: BROSTROM, LYLE, R., ZIA,VAHID, SHEIKH,Ahmad, CZYZEWSKI,Ann,M.
Fecha de Publicación: .
Fecha Solicitud PCT: 4 de Marzo de 2004.
Clasificación Internacional de Patentes:
- C07C319/28 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07C COMPUESTOS ACICLICOS O CARBOCICLICOS (compuestos macromoleculares C08; producción de compuestos orgánicos por electrolisiso electroforesis C25B 3/00, C25B 7/00). › C07C 319/00 Preparación de tioles, de sulfuros, de hidropolisulfuros o de polisulfuros. › Separación; Purificación.
- C07C323/59 C07C […] › C07C 323/00 Tioles, sulfuros, hidropolisulfuros o polisulfuros sustituidos por halógenos, átomos de oxígeno o de nitrógeno o por átomos de azufre que no forman parte de grupos tio. › con grupos amino acilados unidos a la estructura carbonada.
Clasificación PCT:
- A61K31/198 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › Alfa-amino-ácidos, p. ej. alanina, ácido etilendiamino tetraacético (EDTA) (betaína A61K 31/205; prolina A61K 31/401; triptófano A61K 31/405; histidina A61K 31/4172; péptidos no degradados en aminoácidos individuales A61K 38/00).
- A61P29/00 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › Agentes analgésicos, antipiréticos o antiinflamatorios que no actúan sobre el sistema nervioso central, p. ej. agentes antirreumáticos; Antiinflamatorios no esteroideos (AINEs).
- C07C319/28 C07C 319/00 […] › Separación; Purificación.
- C07C323/59 C07C 323/00 […] › con grupos amino acilados unidos a la estructura carbonada.
Clasificación antigua:
- A61K31/198 A61K 31/00 […] › Alfa-amino-ácidos, p. ej. alanina, ácido etilendiamino tetraacético (EDTA) (betaína A61K 31/205; prolina A61K 31/401; triptófano A61K 31/405; histidina A61K 31/4172; péptidos no degradados en aminoácidos individuales A61K 38/00).
- A61P29/00 A61P […] › Agentes analgésicos, antipiréticos o antiinflamatorios que no actúan sobre el sistema nervioso central, p. ej. agentes antirreumáticos; Antiinflamatorios no esteroideos (AINEs).
- C07C319/28 C07C 319/00 […] › Separación; Purificación.
- C07C323/59 C07C 323/00 […] › con grupos amino acilados unidos a la estructura carbonada.
Países PCT: Austria, Bélgica, Suiza, Alemania, Dinamarca, España, Francia, Reino Unido, Grecia, Italia, Liechtensein, Luxemburgo, Países Bajos, Suecia, Mónaco, Portugal, Irlanda, Eslovenia, Finlandia, Rumania, Chipre, Lituania, Letonia, Ex República Yugoslava de Macedonia, Albania.
PDF original: ES-2363001_T3.pdf
Fragmento de la descripción:
Campo de la invención
La presente invención comprende un nuevo compuesto útil en el tratamiento de enfermedades, y más particularmente a una nueva sal de S-[2-[(1-iminoetil)amino]etil]-2-metil-L-cisteína, y aún más particularmente a un nuevo clorhidrato cristalino de maleato de S-[2-[(1-iminoetil)amino]etil]-2-metil-L-cisteína, y a composiciones farmacéuticas de los mismos para el tratamiento de afecciones que implican una expresión inapropiada de óxido nítrico a partir de la isoforma inducible de la óxido nítrico sintasa.
La S-[2-[(1-iminoetil)amino]etil]-2-metil-L-cisteína se describe y reivindica en la Patente de Estados Unidos de cesión común con número 6.403.830.
Antecedentes de la invención
El óxido nítrico (NO) es un radical libre gaseoso bioactivo, producido por una cualquiera de las diversas isoformas de la enzima óxido nítrico sintasa (NOS). La actividad fisiológica de lo que posteriormente se identificó como NO se descubrió inicialmente a principios de los años 80 cuando se encontró que la relajación vascular provocada por acetil colina era dependiente de la presencia del endotelio vascular. El factor derivado del endotelio, denominado entonces factor de relajación derivado del endotelio (EDRF), que media dicha relajación vascular, se sabe ahora que es NO que se genera en el endotelio vascular por una isoforma de NOS. La actividad de NO como vasodilatador se ha conocido desde hace más de 100 años. Además, el NO es la especie activa derivada de los nitrovasodilatadores conocidos incluyendo amilnitrito y gliceriltrinitrato. El óxido nítrico es también un estimulante endógeno de guanilato ciclasa soluble (GMPc) y, de esta manera, estimula la producción de GMPc. Cuando NOS se inhibe por Nmonometilarginina (L-NMMA), la formación de GMPc se evita completamente. Además de la relajación dependiente del endotelio, se sabe que el NO está implicado en numerosas acciones biológicas incluyendo citotoxicidad de las células fagocíticas y la comunicación de célula a célula en el sistema nervioso central.
La identificación de EDRF como NO coincide con el descubrimiento de una ruta bioquímica mediante la cual el NO se sintetiza a partir del aminoácido L-arginina por la enzima NO sintasa. Hay al menos tres tipos de NO sintasa como sigue:
(i) una enzima constitutiva dependiente de Ca++/calmodulina, localizada en el cerebro, que libera NO como respuesta al receptor o estimulación física;
(ii) una enzima independiente de Ca++, una proteína de 130 kD que se induce después de la activación del músculo liso vascular, macrófagos, células endoteliales y un número de otras células por endotoxinas y citoquinasa; y
(iii) una enzima constitutiva, dependiente de Ca++/calmodulina, localizada en el endotelio, que libera NO como respuesta al receptor o estimulación física.
Una vez expresada, el óxido nítrico sintasa inducible (en lo sucesivo en el presente documento “iNOS”) genera NO continuamente durante largos periodos. Los estudios clínicos han demostrado que la producción de NO y la expresión de iNOS aumentan en una diversidad de enfermedades inflamatorias crónicas, tales como artritis reumatoide y osteoartritis (véase, por ejemplo, McInnes I. B. y col., J. Exp. Med. 184: 1519 (1996)), enfermedad inflamatoria del intestino (véase, por ejemplo, Lundberg J. O. N. y col., Lancet 344: 1673, (1994)), y asma (véase por ejemplo, Hamid, Q. y col., Lancet 342: 1510 (1993)), e iNOS está implicada como un factor patológico principal en estas enfermedades inflamatorias crónicas.
De esta manera, la inhibición de la producción excesiva de NO por iNOS es probable que sea antiinflamatoria. Sin embargo, puesto que la producción de NO a partir de eNOS y nNOS está implicada en la fisiología normal, sería deseable que cualquier inhibidor de NOS que se use para tratar la inflamación sea selectivo para iNOS, de manera que la modulación fisiológica normal de la presión sanguínea por el NO generado por eNOS y la transmisión neuronal no adrenérgica y no colinérgica por el NO generado por nNOS permanezcan sin afectar.
Con todos los compuestos farmacéuticos y composiciones, la estabilidad química y física de un compuesto farmacéutico es importante en el desarrollo comercial de esta sustancia farmacéutica. Dicha estabilidad incluye la estabilidad en condiciones ambiente, especialmente en condiciones de humedad y almacenamiento. La estabilidad elevada en diferentes condiciones de almacenamiento es necesaria para predecir las diferentes condiciones de almacenamiento posibles durante la vida útil de un producto comercial. Un fármaco estable evita el uso de condiciones de almacenamiento especiales así como una restitución de inventario frecuente. Un compuesto farmacéutico debe ser estable también durante el procedimiento de fabricación, que a menudo requiere la molienda del fármaco para conseguir un material farmacéutico con un tamaño de partícula y área superficial uniforme. Los materiales inestables a menudo experimentan cambios polimórficos. Por lo tanto, cualquier modificación de una sustancia farmacéutica que potencie su perfil de estabilidad proporciona un beneficio significativo respecto a las sustancias menos estables.
Se han descrito diversos inhibidores de iNOS, tales como por ejemplo, S-[2-[(1-iminoetil)amino]etil]-2-metil-Lcisteína, que se describe y reivindica en la Patente de Estados Unidos de cesión común 6.403.830. Este compuesto, sin embargo, es un sólido amorfo. Sería deseable, por lo tanto, proporcionar una forma sólida cristalina de un inhibidor de iNOS tal como S-[2-[(1-iminoetil)amino]etil]-2-metil-L-cisteína.
Breve descripción de los dibujos
La Figura 1 muestra un patrón de difracción de rayos X de polvo de clorhidrato cristalino de maleato de S-[2-[(1iminoetil)amino]etil]-2-metil-L-cisteína obtenido a partir del Ejemplo 9 (patrón superior) y el Ejemplo 20 (patrón inferior);
La Figura 2 es un gráfico de un estudio de calorimetría de barrido diferencial de una muestra (Ejemplo 11) de clorhidrato cristalino de maleato de S-[2-[(1-iminoetil)amino]etil]-2-metil-L-cisteína;
La Figura 3 es una representación termogravimétrica de una muestra (Ejemplo 11) de clorhidrato cristalino de maleato de S-[2-[(1-iminoetil)amino]etil]-2-metil-L-cisteína;
La Figura 4 es una representación de un estudio de absorción de humedad de una muestra (Ejemplo 10) de clorhidrato cristalino de maleato de S-[2-[(1-iminoetil)amino]etil]-2-metil-L-cisteína;
La Figura 5 muestra un espectro Raman de clorhidrato cristalino de maleato de S-[2-[(1-iminoetil)amino]etil]-2-metilL-cisteína obtenido a partir de una muestra del Ejemplo 20;
La Figura 6 es una fotomicrografía del clorhidrato cristalino de maleato de S-[2-[(1-iminoetil)amino]etil]-2-metil-Lcisteína del Ejemplo 9;
La Figura 7 son dos dibujos SEM de los aglomerados envasados aleatoriamente de clorhidrato cristalino de maleato de S-[2-[(1-iminoetil)amino]etil]-2-metil-L-cisteína obtenidos del Ejemplo 9, la Figura 7A muestra la forma generalmente aleatoria de los aglomerados, mientras que la Figura 7B muestra el empaquetado aleatorio de los cristales dentro de los aglomerados;
La Figura 8 muestra diversos dibujos SEM de los aglomerados empaquetados ordenadamente de clorhidrato cristalino de maleato de S-[2-[(1-iminoetil)amino]etil]-2-metil-L-cisteína preparado por un procedimiento de cristalización QESD con siembra y obtenido a partir del Ejemplo 20;
La Figura 9 muestra dos dibujos SEM de aglomerados empaquetados ordenadamente de clorhidrato cristalino de maleato de S-[2-[(1-iminoetil)amino]etil]-2-metil-L-cisteína preparado por un procedimiento de cristalización QESD con siembra in situ y obtenido a partir del Ejemplo 23, la Figura 9A muestra la forma generalmente cilíndrica mientras que la Figura 9B muestra los cristales generalmente ordenados;
La Figura 10 es un diagrama x-T conceptual para un sistema ternario que presenta comportamiento LLPS para una cantidad fija de anti-disolvente;
La Figura 11 es un diagrama que muestra las superficies coexistentes a temperatura constante para un sistema ternario.
La Figura 12 muestra un gráfico de la distribución del tamaño de partícula de aglomerados empaquetados ordenadamente de cristales de clorhidrato de maleato de S-[2-[(1-iminoetil)amino]etil]-2-metil-L-cisteína;
La Figura 13 es un gráfico que representa la dureza del comprimido como una función de la fuerza de compresión;
... [Seguir leyendo]
Reivindicaciones:
1. Clorhidrato de maleato de S-[2-[(1-iminoetil)amino]etil]-2-metil-L-cisteína.
2. Una forma cristalina de la sal de la reivindicación 1.
3. Una composición farmacéutica que comprende la sal de la reivindicación 1 o la forma cristalina de la 5 reivindicación 2, junto con un vehículo farmacéuticamente aceptable.
4. La sal de la reivindicación 1, la forma cristalina de la reivindicación 2 o la composición farmacéutica de la reivindicación 3 para su uso en el tratamiento de una afección en la que forma parte una producción de NO patológicamente alta.
5. La sal de la reivindicación 1, la forma cristalina de la reivindicación 2 o la composición farmacéutica de la
10 reivindicación 3, para su uso en el tratamiento de artritis reumatoide, osteoartritis, artritis gotosa, artritis juvenil, artritis séptica, espondiloartritis, artritis reumática aguda, artritis enteropática, artritis neuropática y artritis piogénica.
Patentes similares o relacionadas:
Moléculas que tienen utilidad plaguicida e intermediarios, composiciones y procesos, relacionados con ellas, del 22 de Mayo de 2019, de DOW AGROSCIENCES LLC: Una molécula que tiene la siguiente fórmula**Fórmula** en donde: (A) R1 se selecciona del grupo que consiste en H, F, Cl, Br, I, CN, NH2, NO2, alquilo(C1-C4), cicloalquilo(C3-C6), […]
Procedimiento para despigmentar materiales queratínicos usando nuevos compuestos basados en resorcinol, del 5 de Diciembre de 2018, de L'OREAL: Compuestos de fórmula (I):**Fórmula** en la que: * R indica un átomo de hidrógeno; * Y indica un radical elegido de OR' y NAR"; * R' indica […]
 Compuestos de isoprenilo y métodos de los mismos, del 8 de Julio de 2015, de SIGNUM BIOSCIENCES, INC: Compuesto de fórmula: **Fórmula**
o una sal farmacéuticamente aceptable del mismo.
Compuestos de isoprenilo y métodos de los mismos, del 8 de Julio de 2015, de SIGNUM BIOSCIENCES, INC: Compuesto de fórmula: **Fórmula**
o una sal farmacéuticamente aceptable del mismo.
Compuestos para el tratamiento de trastornos metabólicos, del 9 de Octubre de 2013, de WELLSTAT THERAPEUTICS CORPORATION: Un agente biológicamente activo, en donde el agente es un compuesto de la fórmula:**Fórmula** en donde n es 1 ó 2; q es 0 ó 1; t es 0 ó 1; R5 es alquilo que […]
Polímeros solubles en agua ramificados y sus conjugados, del 26 de Agosto de 2013, de BioGeneriX GmbH: Un péptido que tiene la fórmula:**Fórmula** en la que PSA es un polímero soluble en agua y R14 es un miembro seleccionado entre OH, grupos […]
Proceso para preparación de aminoácidos utilizando la reacción de amidocarbonilación, del 14 de Agosto de 2013, de EVONIK DEGUSSA GMBH: Proceso para producir un aminoácido que comprende los pasos de reacción siguientes: a) reacción de un aldehído con una amida y monóxido […]
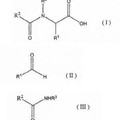 Método para producir un N-acilaminoácido, del 25 de Abril de 2013, de SUMITOMO CHEMICAL COMPANY, LIMITED: Se proporciona un método para producir un N-acilaminoácido de fórmula (I):
****IMAGEN-01****
en la que R1, R2 y R3 son iguales o diferentes y cada uno representa […]
Método para producir un N-acilaminoácido, del 25 de Abril de 2013, de SUMITOMO CHEMICAL COMPANY, LIMITED: Se proporciona un método para producir un N-acilaminoácido de fórmula (I):
****IMAGEN-01****
en la que R1, R2 y R3 son iguales o diferentes y cada uno representa […]
DERIVADOS DE ÁCIDO 4 O 5-AMINOSALICÍLICO, del 21 de Noviembre de 2011, de Antibe Therapeutics Inc: Un compuesto de fórmula general: **Fórmula** A ¿ L ¿ R (I) en la que A es en la que ¿N= se encuentra bien en la posición 4 ó 5, en la que ¿NH se encuentra bien en la posición […]