PREMEZCLA ALIMENTARIA MEDICAMENTOSA QUE COMPRENDE HIDROCLORURO DE CLORTETRACICLINA.
Premezcla alimentaria medicamentosa, que comprende: 15% en peso a 65% en peso de un hidrocloruro de clortetraciclina farmacéuticamente aceptable,
20% en peso a 85% en peso de un portador, y 0,1% en peso a 10% en peso de un ligante, en la que todas las cantidades se basan en el peso total de la premezcla alimentaria medicamentosa
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2007/004221.
Solicitante: Alpharma, LLC.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 400 Crossing Boulevard Bridgewater, NJ 08807.
Inventor/es: HOLMES, STEVEN, CORNEZ,Robert, VAN MALCOT,Dirk.
Fecha de Publicación: .
Fecha Solicitud PCT: 16 de Febrero de 2007.
Clasificación Internacional de Patentes:
- A61K9/16H2
- A61K9/16H6F
Clasificación PCT:
- A61K31/065 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › Alcoholes acíclicos difenil-sustituidos.
- A61K9/16 A61K […] › A61K 9/00 Preparaciones medicinales caracterizadas por un aspecto particular. › Aglomerados; Granulados; Microbolitas.
Países PCT: Austria, Bélgica, Suiza, Alemania, Dinamarca, España, Francia, Reino Unido, Grecia, Italia, Liechtensein, Luxemburgo, Países Bajos, Suecia, Mónaco, Portugal, Irlanda, Eslovenia, Finlandia, Rumania, Chipre, Lituania, Letonia, Ex República Yugoslava de Macedonia, Albania.
PDF original: ES-2356395_T3.pdf
Fragmento de la descripción:
ANTECEDENTES
Los antibióticos, tales como las tetraciclinas, se utilizan como estimulantes del crecimiento y estimulantes de la eficiencia de alimentación en animales tales como aves de corral y ganado, y para el control terapéutico y profiláctico de enfermedades en animales tales como aves de corral y ganado, peces, animales domésticos, y similares. Dichos 5 antibióticos se formulan típicamente en una premezcla alimentaria animal medicamentosa o en un suplemento alimentario animal que contiene el antibiótico y un portador o diluyente comestible. Dichas premezclas o suplementos alimentarios animales pueden mezclarse a continuación con una cantidad suficiente de un producto alimenticio animal apropiado (por ejemplo para vacas, aves de corral, peces, animales domésticos y/o otros animales), proporcionando una formulación alimentaria animal final que presenta el nivel deseado de antibiótico en el alimento. 10
Las premezclas alimentarias animales que contienen clortetraciclina típicas de la técnica anterior se preparan mediante la fermentación y la deshidratación normales de la harina de micelio, que se añade directamente a la premezcla alimentaria. El Streptomyces aureofaciens es un organismo microbiano fuente para la clortetraciclina. Bajo procedimientos normales de fermentación y deshidratación, se han producido premezclas alimentarias que comprenden aproximadamente 20% en peso o menos de clortetraciclina. La patente US nº 6.844.006 describe premezclas 15 alimentarias animales que contienen más de 35% en peso de clortetraciclina producidas utilizando un nuevo procedimiento de fermentación en el que también se añade directamente clortetraciclina procedente de un producto de fermentación.
Otro problema con las premezclas alimentarias animales con tetraciclina (por ejemplo clortetraciclina) anteriores consiste en la estabilidad de la tetraciclina en estas premezclas. Debido a que las tetraciclinas son solubles en agua, 20 existe un problema intrínseco de estabilidad en los alimentos acabados que contienen humedades de 10% o superiores. La mayor actividad de agua (presión de vapor relativa) del pienso en comparación con la tetraciclina conduce a un incremento inevitable de la humedad de la mayoría de formulaciones.
La patente US nº 6.773.717 B1 da a conocer composiciones alimentarias animales que contienen clortetraciclina y procedimientos para la preparación de las mismas. La composición puede ser producida en forma de 25 gránulos y puede contener ligantes y portadores. Sin embargo, enseña la provisión de composiciones alimentarias animales que comprenden clortetraciclina en la forma de base libre con el fin de mejorar su estabilidad.
El documento US nº 2.962.378 A da a conocer la suplementación de una dieta con hidrocloruro de clortetraciclina.
El documento US nº 3.531.568 A da a conocer una composición potable que comprende una combinación de 30 un antibiótico tetraciclina, particularmente hidrocloruro de clortetraciclina, con iones sulfato para potenciar la absorción del antibiótico.
De esta manera, sigue existiendo una necesidad de premezclas alimentarias animales alternativas que comprendan las tetraciclinas.
BREVE SUMARIO 35
Las desventajas descritas anteriormente y otras resultan aliviadas mediante una composición de premezcla alimentaria medicamentosa que comprende entre 15% en peso y 65% en peso de un hidrocloruro de clortetraciclina farmacéuticamente aceptable, entre 20% en peso y 85% en peso de un portador, y entre 0,1% en peso y 10% en peso de un ligante, en la que todas las cantidades se basan en el peso total de la premezcla alimentaria medicamentosa. También se encuentra comprendida una composición alimentaria animal que comprende una cantidad efectiva de la 40 premezcla alimentaria medicamentosa.
En una forma de realización, se encuentra comprendida la utilización de un hidrocloruro de clortetraciclina en la preparación de un medicamento destinado al tratamiento de las infecciones microbianas en animales. El medicamento comprende entre 15% en peso y 65% en peso de un hidrocloruro de clortetraciclina farmacéuticamente aceptable, entre 20% en peso y 85% en peso de un portador, y entre 0,1% en peso y 10% en peso de un ligante, en la que todas las 45 cantidades se basan en el peso total del medicamento.
En otra forma de realización, un procedimiento para preparar una premezcla alimentaria medicamentosa que comprende formar una mezcla que comprende entre 15% en peso y 65% en peso de un hidrocloruro de clortetraciclina farmacéuticamente aceptable, entre 20% en peso y 85% en peso de un portador, entre 0,1% en peso y 10% en peso de un ligante, en la que todas las cantidades se basan en el peso total de la premezcla alimentaria medicamentosa, y 50 granular la mezcla para formar un granulado.
Todavía en otra forma de realización, una premezcla alimentaria medicamentosa comprende entre 15% en peso y 65% en peso de un hidrocloruro de tetraciclina farmacéuticamente aceptable, entre 20% en peso y 85% en peso de un portador, y entre 0,1% en peso y 10% en peso de un ligante, en la que todas las cantidades se basan en el peso
total del suplemento alimentario animal, y en la que la premezcla alimentaria animal se encuentra en forma de un granulado y presenta un pH de entre 3 y 4.
Las características descritas anteriormente y otras serán apreciadas y resultarán evidentes por el experto en la materia a partir de la descripción detallada siguiente y de la reivindicaciones adjuntas.
BREVE DESCRIPCIÓN DE LOS DIBUJOS 5
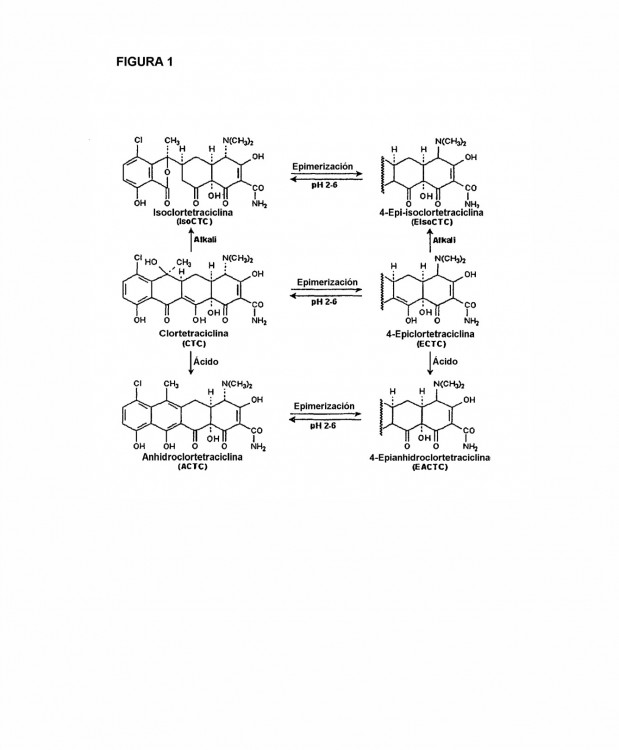
La figura 1 representa las vías de degradación de la clortetraciclina.
DESCRIPCIÓN DETALLADA
Se dan a conocer en la presente memoria premezclas alimentarias medicamentosas que comprenden tetraciclina farmacéuticamente aceptable (por ejemplo hidrocloruro de clortetraciclina), un ligante y un portador. La expresión "premezcla alimentaria medicamentosa" se refiere a una composición que resulta adecuada para la 10 incorporación en la dieta de un animal mediante la incorporación en el alimento y/o agua del animal. En una forma de realización, la premezcla alimentaria medicamentosa se encuentra en la forma de un granulado. Las premezclas alimentarias medicamentosas también se denominan composiciones de "suplemento" alimentario y composiciones de "aditivo alimentario".
Tal como se utiliza en la presente memoria, el término "tetraciclina" incluye tetraciclina, clortetraciclina, 15 oxitetraciclina, doxiciclina, demeclociclina, limeciclina, meclociclina, metaciclina, minociclina, rolitetraciclina y combinaciones que comprenden una o más de las tetraciclinas mencionadas anteriormente. Se encuentran comprendidos en el término tetraciclina las sales, ésteres, éteres, isómeros, mezclas de isómeros, complejos o derivados del compuesto libre y las combinaciones que comprenden una o más de las tetraciclinas mencionadas anteriormente. En una forma de realización, la tetraciclina es el hidrocloruro de clortetraciclina. 20
Debido a que el hidrocloruro de clortetraciclina es el estándar de referencia para los materiales de grado alimentario de clortetraciclina, todas las concentraciones y porcentajes de clortetraciclina indicados en la presente memoria, a menos que se indique lo contrario, se calculan como el equivalente hidrocloruro, con independencia de la forma presente (por ejemplo la base libre, complejos o sales aparte del hidrocloruro, etc.).
La directiva 2001/82EC del Parlamento Europeo y del Consejo, de 6 de noviembre de 2001, por la que se 25 establece el código comunitario sobre los productos medicinales veterinarios - anexo 1.C, describe el control de las materias primas. En particular la sección 1.1 se refiere a las materias primas comprendidas en las farmacopeas, que establece en parte "Los monográficos de la Farmacopea europea (EP) resultarán aplicables a todas las sustancias que aparecen en la misma". La expresión "farmacéuticamente aceptable" tal como se utiliza en la presente memoria se refiere a una tetraciclina (por ejemplo hidrocloruro de clortetraciclina) tal como se encuentra comprendida en la 30 Farmacopea europea, por ejemplo la quinta edición de la Farmacopea europea. En una forma de realización, el hidrocloruro de clortetraciclina farmacéuticamente aceptable comprende un mínimo de 89,5% en peso de hidrocloruro de clortetraciclina anhidra y un máximo de 8% en peso de tetraciclina anhidra, con un 94% a 102% en peso de suma de hidrocloruro de clortetraciclina anhidra e hidrocloruro de tetraciclina... [Seguir leyendo]
Reivindicaciones:
1. Premezcla alimentaria medicamentosa, que comprende:
15% en peso a 65% en peso de un hidrocloruro de clortetraciclina farmacéuticamente aceptable,
20% en peso a 85% en peso de un portador, y
0,1% en peso a 10% en peso de un ligante, 5
en la que todas las cantidades se basan en el peso total de la premezcla alimentaria medicamentosa.
2. Premezcla alimentaria medicamentosa según la reivindicación 1, en la que el ligante comprende la carboximetilcelulosa sódica.
3. Premezcla alimentaria medicamentosa según la reivindicación 1, en la que el portador comprende sulfato de calcio. 10
4. Premezcla alimentaria medicamentosa según la reivindicación 1, que presenta un pH de 3 a 4.
5. Premezcla alimentaria medicamentosa según la reivindicación 1, que comprende 20% en peso a 65% en peso del hidrocloruro de clortetraciclina farmacéuticamente aceptable.
6. Premezcla alimentaria medicamentosa según la reivindicación 1, en la que el hidrocloruro de clortetraciclina farmacéuticamente aceptable comprende un mínimo de 89,5% en peso de hidrocloruro de clortetracicina 15 anhidra y un máximo de 8% en peso de tetraciclina anhidra, con un 94,5% a 102% en peso de hidrocloruro de clortetraciclina anhidra más hidrocloruro de tetraciclina anhidra.
7. Premezcla alimentaria medicamentosa según la reivindicación 1, en forma de una composición multiparticulada.
8. Premezcla alimentaria medicamentosa según la reivindicación 7, en la que la composición multiparticulada 20 es un granulado.
9. Utilización de un hidrocloruro de clortetraciclina en la preparación de un medicamento destinado al tratamiento de infecciones microbianas en animales, en la que el medicamento comprende:
20% en peso a 65% en peso de un hidrocloruro de clortetraciclina farmacéuticamente aceptable,
20% en peso a 85% en peso de un portador, y 25
0,1% en peso a 10% en peso de un ligante,
en la que todas las cantidades se basan en el peso total del medicamento.
10. Utilización según la reivindicación 9, en la que el medicamento se administra como pienso o por medio de agua para beber.
11. Utilización según la reivindicación 9, en la que el portador comprende el sulfato de calcio. 30
12. Utilización según la reivindicación 9, en la que la premezcla alimentaria medicamentosa presenta un pH de 3 a 4.
13. Composición alimentaria animal que comprende:
un producto alimenticio animal, y
una cantidad efectiva de una premezcla alimentaria medicamentosa que comprende: 35
15% en peso a 65% en peso de un hidrocloruro de clortetraciclna farmacéuticamente aceptable,
20% en peso a 85% en peso de un portador, y
0,1% en peso a 10% en peso de un ligante,
en la que todas las cantidades se basan en el peso total de la premezcla alimentaria medicamentosa.
14. Composición alimentaria animal según la reivindicación 13, en la que el portador comprende el sulfato de 40 calcio.
15. Composición alimentaria animal según la reivindicación 13, en la que la premezcla alimentaria medicamentosa presenta un pH de 3 a 4.
Patentes similares o relacionadas:
FORMA FARMACÉUTICA HINCHABLE QUE COMPRENDE GOMA GELLAN, del 22 de Diciembre de 2011, de Egalet Ltd: Forma farmacéutica en forma particulada para la administración oral de uno o más principios activos, comprendiendo la forma farmacéutica un vehículo en forma particulada que […]
FORMULACIÓN DE LIBERACIÓN LENTA BASADA EN UNA ASOCIACIÓN DE GLUCÓGENO Y ALGINATO, del 7 de Diciembre de 2011, de AZIENDE CHIMICHE RIUNITE ANGELINI FRANCESCO A.C.R.A.F. S.P.A.: Formulación farmacéutica que comprende por lo menos un principio activo disperso en una matriz que comprende por lo menos un excipiente de […]
FORMULACIONES SÓLIDAS DE OSPEMIFENO, del 19 de Septiembre de 2011, de HORMOS MEDICAL LTD.: Una formulación sólida de un fármaco, que comprende granulados que contienen 30 a 90 mg de ospemifeno o una de sus sales farmacéuticamente aceptables en combinación con una […]
COMPOSICIONES Y MÉTODOS PARA REDUCCIÓN DEL OXALATO, del 14 de Julio de 2011, de OXTHERA, INC: Una composición que comprende partículas que contienen una o más enzimas degradantes del oxalato incrustadas en un primer material polímero, en donde la enzima incrustada […]
NUEVA FORMA DE SUPOSITORIO QUE COMPRENDE UN COMPUESTO ACTIVO ÁCIDO-LÁBIL, del 5 de Julio de 2011, de NYCOMED GMBH: Un supositorio para compuestos activos ácido-lábiles, en donde el compuesto ácido-lábil es un inhibidor de la bomba de protones ácido-lábil, una sal […]
COMPOSICIÓN SÓLIDA QUE CONTIENE ESPORAS DE BACTERIAS NO PATÓGENAS DEL GÉNERO BACILLUS, del 7 de Abril de 2011, de SANOFI-AVENTIS S.P.A: Composición sólida de esporas de bacterias no patogénicas del género Bacillus adsorbidas sobre una matriz formada: - por al menos un compuesto adsorbente […]
COMPOSICIÓN FARMACÉUTICA QUE COMPRENDE LOS DERIVADOS DE 2,3-DIHIDRO-6-NITROIMIDAZO[2,1-B]OXAZOL, del 28 de Marzo de 2011, de OTSUKA PHARMACEUTICAL CO., LTD.: Composición farmacéutica que comprende: (I) por lo menos un compuesto oxazol seleccionado de entre el grupo constituido por compuestos de 2,3-dihidro-6-nitroimidazo[2,1-b]oxazol […]
MICROPARTÍCULAS MARCADAS RADIACTIVAMENTE, PROCEDIMIENTO PARA SU FABRICACIÓN Y UTILIZACIÓN DE LAS MISMAS, del 5 de Diciembre de 2011, de BOEHRINGER INGELHEIM INTERNATIONAL GMBH: Procedimiento para la fabricación de micropartículas marcadas radiactivamente con el isótopo de tecnecio Tc 99m (Tc*) de un tamaño medio de partícula de 0,5 […]